重芳烃轻质化催化剂n(Ni)/n(Ni+Mo)的优化与分析
刘 航,臧甲忠,范景新,郭春垒,靳凤英,赵训志
(1.中海油天津化工研究设计院有限公司,天津300131;2.天津市炼化催化技术工程中心)
重芳烃是指C9及以上的芳烃,其来源有两个方面:1)石油化工副产,如催化重整装置及乙烯裂解装置副产的C9+重芳烃,其是重芳烃的主要来源[1];2)煤化工副产,如煤高温炼焦副产的芳烃-煤焦油组分。近年来中国特大型炼厂陆续建成,芳烃联合装置和乙烯裂解装置迅速扩能,重芳烃的产能迅速增加,如何对其进行高值化利用成为炼厂亟待解决的问题[2]。
重芳烃根据其来源目前的利用途径主要有两种:1)对于重整重芳烃,先分离再利用,重整重芳烃中的偏三甲苯、均三甲苯、连三甲苯、均四甲苯是精细化工的原料,其余组分部分用来生产溶剂油;2)对于裂解重芳烃,主要用来生产石油树脂,少部分经切割馏分生产高沸点溶剂油[3]。重芳烃的这两种利用途径,利用率均较低。近年来开发的重芳烃轻质化工艺是目前提高重芳烃利用率最优的解决方案,按工艺特点分为以下几种[4]:1)热脱烷基,代表工艺为HAD工艺[5];2)催化加氢脱烷基,代表工艺为Detol工艺[6]和ZEOLYST/SK工艺[7];3)烷基转移,代表工艺为TAC9[8]和Trans-Plus工艺[9]。上述几种工艺的缺点是原料适应范围窄,仅能处理C9~C10的重芳烃,C10+重芳烃的转化率很低。
为解决上述问题,开发一种选择性地将稠环芳烃的芳环加氢饱和开环,保留一个芳环,以最大限度地生产C6~C9轻质芳烃的重芳烃轻质化催化剂是十分有必要的。鉴于此,轻质化催化剂需同时具备加氢活性和裂解活性,金属改性的分子筛催化剂是轻质化催化剂的研究方向,其中金属的作用是修饰沸石分子筛的酸性,使其能够具备双功能催化作用。由于重芳烃中稠环芳烃含量较高、馏程较重,因此制备出兼具高活性和高稳定性的轻质化催化剂是目前的难点。笔者制备了不同n(Ni)/n(Ni+Mo)的催化剂,结合表征及评价数据阐明了n(Ni)/n(Ni+Mo)对催化剂性能的影响,优化了催化剂的加氢活性和稳定性。
1 实验部分
1.1 原料和试剂
试剂:七钼酸铵[(NH4)6·Mo7O24·4H2O]、硝酸镍[Ni(NO3)2·6H2O],均为分析纯。
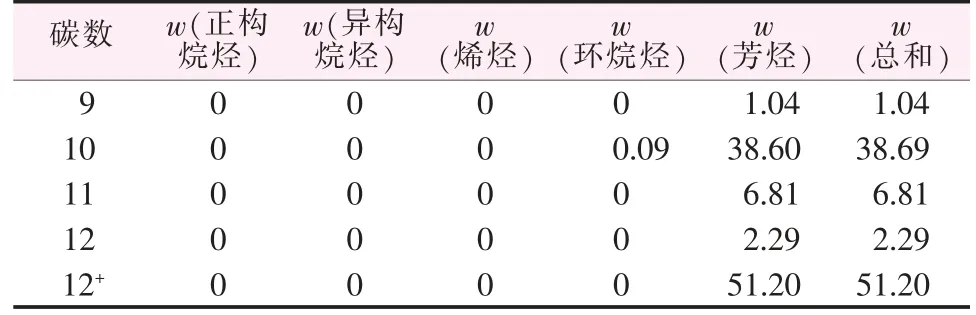
表1 重整重芳烃的PONA组成Table 1 PONA composition of reformed heavy aromatic hydrocarbon %
1.2 催化剂的制备
以成型后的三叶草型β分子筛为载体,采用等体积浸渍法分步浸渍Ni和Mo,浸渍后的催化剂在室温静置6 h,之后转移至120℃烘箱中干燥4 h,最后于500℃焙烧4 h,制得n(Ni)/n(Ni+Mo)等于基准的催化剂。按照上述制备方法,在保持总金属负载量(物质的量)不变的情况下提高n(Ni)/n(Ni+Mo)的比例,分别得到n(Ni)/n(Ni+Mo)等于基准+0.2、基准+0.3、基准+0.4的催化剂。
1.3 催化剂的表征
XRD表征采用D/max-2500PC型X射线衍射仪,操作条件:CuKα为标准光源,管电压为40 kV,管电流为40 mA,扫描速率为2(°)/min,5~35°扫描。比表面积(BET)表征采用ASAP2420型全自动比表面积孔隙分析仪,操作条件:样品在压力为1.999 Pa真空条件下在300℃净化脱气处理5 h,然后在-196℃用N2进行静态吸附分析,比表面积由BET方程计算得出,孔径及孔径分布由BJH法计算,孔容由BJH吸附孔容累计曲线得到。TG-DTG分析采用TGA/DSC 1专业型热重差热同步分析仪,操作条件:称取10 mg失活剂样品,以80 mL/min的流速通空气,以10℃/min的速率升温至900℃。NH3-TPD、H2-TPR和H2-TPD表征均采用AutoChemⅡ2920型全自动化学吸附仪。NH3-TPD操作条件:使用He吹扫样品(30 mL/min),升温至400℃并保持1 h,待温度降至200℃,吸附NH3(10 mL/min)0.5 h,切换He吹扫(40 mL/min),程序升温脱附,以10℃/min的升温速率升温至650℃,记录谱图出峰情况得到NH3吸附-脱附温度曲线,根据脱附峰的温度比较样品酸中心的强弱,由峰面积得到样品中不同强度酸中心的酸量。H2-TPR操作条件:0.05 g样品在100℃用N2预处理1 h(27 mL/min),然后冷却至室温,在40 mL/min的H2/Ar混合气氛下(H2体积分数为10%)由室温以7℃/min程序升温至950℃进行测试。H2-TPD操作条件:载气为高纯Ar气,流速为40 mL/min,升温速率为20℃/min,采用热导池检测器(TCD)检测,脱附前先用氢脉冲进样至催化剂吸氢饱和。
1.4 催化剂的评价
将制得的催化剂破碎得到粒径为500~850μm的颗粒。取10 g催化剂颗粒装入30 mL固定床反应器内,在500℃通入氢气还原2 h,之后降温至370℃准备进料。以C+10重芳烃为原料,在热点温度为405℃、压力为5 MPa、空速(MHSV)=1.5 h-1、V(H2)∶V(油)=1 000∶1条件下评价催化剂的轻质化性能。每隔24 h取一次液相产物,并采用气相色谱仪进行分析。反应相同的时间后将催化剂卸出,在120℃烘干12 h,送TG分析。最后计算芳烃转化率和C6~C9轻质芳烃收率,计算公式:

2 结果与讨论
2.1 XRD表征
β分子筛及4种催化剂的XRD谱图见图1。由图1看出,β分子筛在2θ为7.8°和22.5°处出现了归属于β分子筛特征结构的衍射峰[10];与β分子筛XRD谱图相比,金属改性的4种催化剂XRD谱图无明显变化,且未出现Ni和Mo物种的衍射峰,说明负载金属并没有破坏β分子筛的晶体结构,催化剂拓扑结构保持完好,同时Ni和Mo物种高度分散在β分子筛载体上[10]。

图1 载体及催化剂的XRD谱图Fig.1 XRD patterns of carrier and catalysts
2.2 比表面积(BET)分析
载体及催化剂的比表面积见2。由表2看出,与β载体相比,负载Ni、Mo催化剂的比表面积和孔容均有一定程度的降低,表明金属负载过程中部分孔被堵塞;对比4种催化剂,不同金属负载量催化剂的比表面积和孔容相近,表明Ni、Mo对催化剂的孔结构影响较小。

表2 载体及催化剂的比表面积Table 2 BET of the support and catalysts
2.3 NH3-TPD表征
作为一种双功能催化剂,重芳烃轻质化催化剂的酸性质尤为重要,其最主要的作用是提供裂化活性中心,同时还可以与加氢活性中心相互作用,优化催化剂的加氢裂化活性。一般把NH3在酸性中心上的脱附温度分为3个部分,即20~200℃、200~350℃和350~600℃,分别对应催化剂上的弱酸、中强酸和强酸酸性位[11]。4种催化剂的NH3-TPD表征数据和曲线见表3及图2。由表3及图2看出,4种催化剂均只有一个NH3脱附峰,脱附峰温度均在310℃附近,归属于中强酸;随着n(Ni)/n(Ni+Mo)增加,催化剂脱附峰温度先降低后升高,脱附峰温度代表催化剂的酸强度,即酸强度先减弱后增强;由NH3-TPD脱附曲线可计算得到每个催化剂的酸量,从表3计算结果来看4种催化剂的酸量相近,这是由于催化剂制备过程中总金属负载量保持不变,由负载金属引进的酸量是相近的,因此催化剂的酸量也相近。

表3 4种催化剂的NH3-TPD表征数据Table 3 NH3-TPD data of the four catalysts
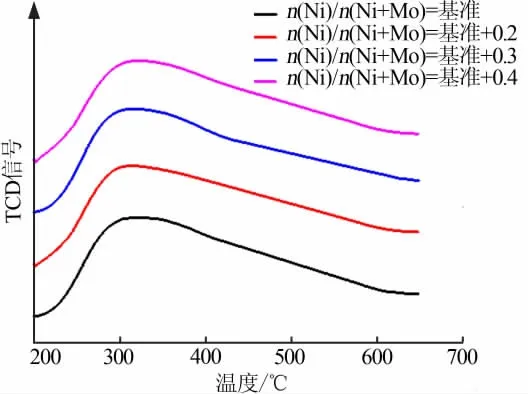
图2 4种催化剂的NH3-TPD曲线Fig.2 NH3-TPD curves of the four catalysts
2.4 H2-TPR表征
催化剂的H2-TPR分析表征了活性金属与载体之间相互作用的强弱,也能够有效地表征活性金属被还原的难易程度。图3为4种催化剂的H2-TPR曲线。由图3看出,4种催化剂均仅出现一个还原峰,该还原峰归属于八面体配位的钼物种的还原[12],即Mo6+→Mo4+,该物种是形成高加氢活性中心的前驱体[13-17];还原峰温度表征了活性金属被还原的难易程度,4种催化剂还原峰对应的还原温度不同,由高到低的顺序依次为n(Ni)/n(Ni+Mo)等于基准、基准+0.4、基准+0.3、基准+0.2,即随着n(Ni)/n(Ni+Mo)增加,还原温度先降低后升高,在n(Ni)/n(Ni+Mo)等于基准+0.2时对应的还原温度最低,这表明该催化剂上的八面体配位的钼物种与载体之间的相互作用最弱,最容易被还原,由于Ni具有促进八面体配位的Mo物种还原的作用,因此在该比例下Ni对八面体配位的Mo物种的还原促进作用最明显;4种催化剂均未出现明显的Ni物种还原峰,其主要原因是Ni物种的低温还原峰与Mo物种的还原峰重叠[18-19]。
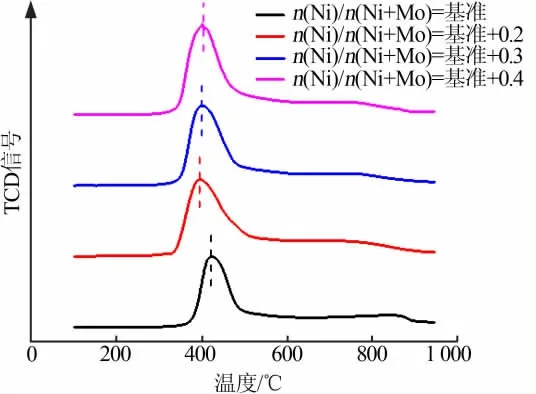
图3 4种催化剂的H2-TPR曲线Fig.3 H2-TPR curves of the four catalysts
2.5 H2-TPD表征
催化剂的H2-TPD分析表征了催化剂上的活性金属吸附H2能力的强弱。图4为4种催化剂的H2-TPD曲线。由图4看出,4种催化剂均可观察到位于400~700℃的H2脱附峰,且脱附峰对应的脱附温度相近,该脱附峰可归属于催化剂上活性金属对H2的强化学吸附[20]。采用高斯函数拟合对4种催化剂的H2脱附量进行计算,其由高到低的顺序依次为n(Ni)/n(Ni+Mo)等于基准+0.2、基准+0.3、基准+0.4、基准,即随n(Ni)/n(Ni+Mo)增加,H2脱附量先增加后降低,在n(Ni)/n(Ni+Mo)等于基准+0.2时H2脱附量最大,表明此时催化剂吸附H2的能力最强,催化剂上吸附氢的活性位点最多。
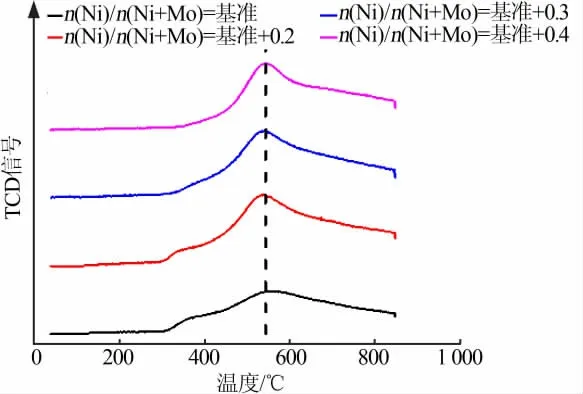
图4 4种催化剂的H2-TPD曲线Fig.4 H2-TPD curves of the four catalysts
2.6 催化剂评价
4种催化剂的评价数据见图5。由C+10转化率看出,4种催化剂初活性相近,C+10转化率均保持在95%左右;进入稳定期后,4种催化剂的性能呈现如下规律,即随着n(Ni)/n(Ni+Mo)增加,C+10转化率先升高后降低,在n(Ni)/n(Ni+Mo)为基准+0.2时催化剂具有最高的活性,且此时催化剂也体现出优异的稳定性,在稳定期内其C+10转化率始终保持在85%左右,出现平台期,而另外3种催化剂C+10转化率迅速下降,未出现稳定的平台期;4种催化剂的C6~C9芳烃收率相近,但是n(Ni)/n(Ni+Mo)等于基准+0.2催化剂的C6~C9芳烃收率随着评价时间的延长稳定性较好,说明n(Ni)/n(Ni+Mo)等于基准+0.2的催化剂同时具有较高的催化活性和稳定性。结合催化剂的H2-TPD结果,n(Ni)/n(Ni+Mo)等于基准+0.2的催化剂具有最强的吸附H2的能力,使其保持了较高的活性。而其稳定性的差别可结合下述TG-DTG分析进行对比。
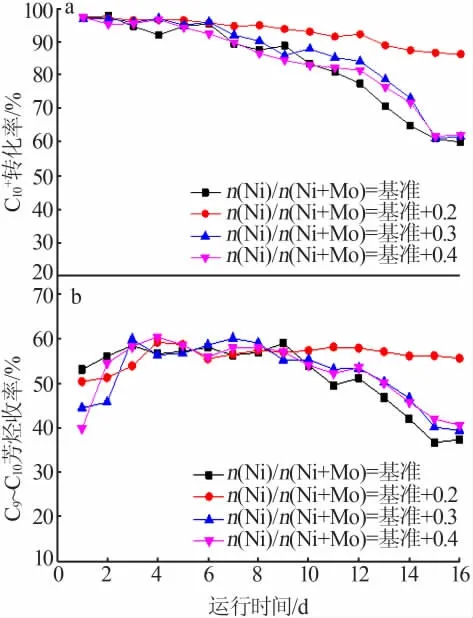
图5 4种催化剂C+10转化率(a)及C6~C9芳烃收率(b)对比Fig.5 Comparison of C+10 heavy aromatics conversion rate(a)and yield of C6~C9 aromatics(b)of four catalysts
采用TG-DTG分析表征了失活剂积炭量及烧炭峰温度,结果见图6。由图6看出,随着温度的升高,4种评价后催化剂的TG曲线逐渐下降,说明其处于逐渐质量损失状态;由DTG曲线看到,4种评价后的催化剂均存在3个质量损失峰,一般认为<150℃的峰对应的是催化剂上的水分或者低沸点组分的脱除,150~300℃的峰对应的是催化剂上软积炭的脱除,300~700℃的峰对应的是硬积炭的脱除[21]。4种催化剂的最大质量损失速率均为500℃,说明积炭主要集中在此范围内,且均为硬积炭,软积炭量极少;通过TG曲线计算得到硬积炭的积炭量由高到低的顺序依次为n(Ni)/n(Ni+Mo)等于基准、基准+0.4、基准+0.3、基准+0.2,即随n(Ni)/n(Ni+Mo)增大,评价后的催化剂硬积炭量先降低后升高,n(Ni)/n(Ni+Mo)等于基准+0.2对应的催化剂的硬积炭量最低,说明此比例时的催化剂明显抑制了催化剂在反应过程中的硬积炭。结合催化剂的H2-TPD表征结果,分析原因如下:由于n(Ni)/n(Ni+Mo)等于基准+0.2对应催化剂的H2吸附量最大,被吸附的H2在还原后的金属表面解离为原子H,然后原子H沿金属表面溢流至邻近的金属表面上,H2的吸附量越大金属表面的溢流氢越多,在反应过程中溢流氢的主要作用是提高催化剂的消碳能力,即沉积在加氢活性中心表面的积炭前驱体被溢流氢及时消除,保护催化剂的加氢活性中心不被积炭覆盖,有助于催化剂在较高的活性下保持稳定[22]。
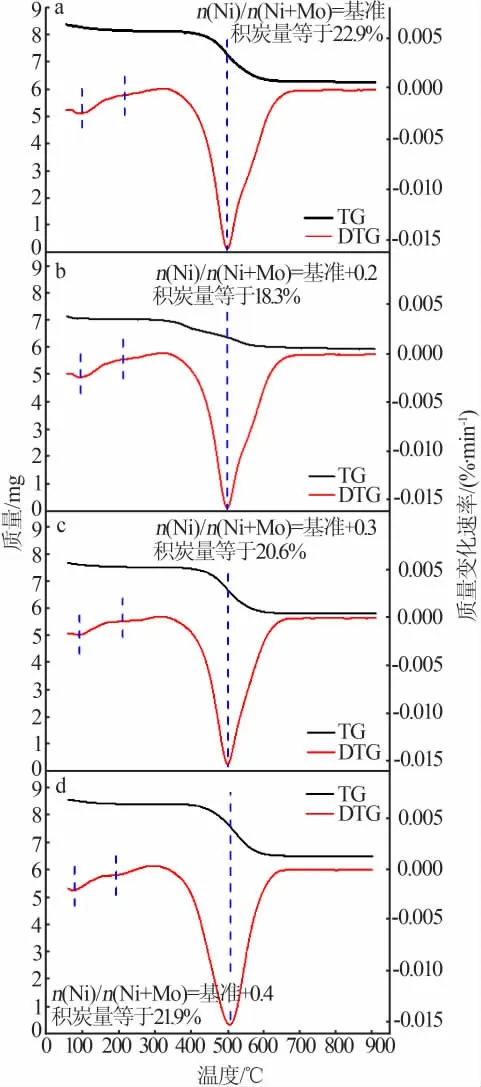
图6 4种催化剂的TG-DTG曲线Fig.6 TG-DTG curves of the four catalysts
3 结论
1)n(Ni)/n(Ni+Mo)显著影响催化剂上活性金属被还原的难易程度、吸附H2能力的强弱及反应过程积炭量的多少。在考察范围内,n(Ni)/n(Ni+Mo)等于基准+0.2的催化剂活性金属最易被还原,具有最强的吸附H2能力,且对应的评价后催化剂的积炭量最低。
2)影响重芳烃轻质化催化剂活性和稳定性的关键因素是催化剂H2吸附量的多少,H2吸附量越多金属表面的溢流氢越多,积炭前驱体被溢流氢及时消除,从而保护了催化剂的加氢活性中心不被积炭覆盖,有助于催化剂在较高的活性下保持稳定,因此n(Ni)/n(Ni+Mo)等于基准+0.2的催化剂具有最高的催化活性和稳定性。

