中医方药对阿尔茨海默病NF-κB信号通路调控的研究进展
彭 超,张 艳,米彩云,王虎平
(甘肃中医药大学,兰州 730000)
阿尔茨海默病是一种以记忆和认知能力逐渐丧失、运动能力减退等为主要临床表现的神经退行性疾病[1,2]。据相关报告预估,全世界患病人数将于2050年达到1.315亿[3]。随着我国老年化进程的加快,2020年我国患病人数将达到1450万,并以每10年500万的数量递增[4],将造成严重的社会医疗和经济负担。
AD的主要病理特征包括β-淀粉样蛋白(β-amyloid,Aβ)在神经元细胞间形成的聚集体和高磷酸化Tau(microtubule-associated protein,Tau )蛋白在神经细胞内形成的纤维缠结,以及突触和神经元的丢失[5],其发病机制复杂,常由Aβ沉积、Tau蛋白异常磷酸化、神经元凋亡、自由基损伤、免疫异常、基因突变、胆碱能损伤、金属离子代谢紊乱、内分泌失调等多种因素诱发[6,7]。目前的临床治疗多以乙酰胆碱酯抑制剂(acetylcholinesterase inhibtor,AChEI)和谷氨酸受体拮抗剂(美金刚)等为主[8],但对于AD进程无法起到抑制效果,并带来严重的副作用。因此,深入探寻AD的病因病机、治则治法和靶向新药刻不容缓。
近年研究表明,NF-κB信号通路与AD患者脑内Aβ的形成以及神经炎症和氧化应激反应等有着密切关系。而中药单体和复方已被证明具有降低Aβ的沉积[9],减轻神经炎症反应[10],保护AD患者脑内突触和神经元细胞[11]等多重作用。因此,深入探究中医方药如何调控NF-κB信号通路防治AD已成为研究热点。
1 NF-κB信号通路在AD中的角色
NF-κb是正常大脑中的多种神经元基因靶点,参与很多生物学效应,包括细胞生长、神经传递、氧化还原信号、免疫炎症和基因调控等[12],它在突触可塑性以及大脑学习和记忆中也起着重要作用[13,14]。在AD脑内弥漫性β-淀粉样斑块附近的神经元核内,NF-κB免疫反应性增强。Aβ肽是老年斑块的主要成分,具有刺激NF-κB活性的作用,而NF-κB抑制剂能减少β淀粉样蛋白前体(β-amyloid precursor,β-APP)的生成以及β-位点APP裂解酶1(beta-site app-cleaving enzyme1,BACE-1)的产生[15],这表明β-APP和BACE-1可能是NF-κB的基因靶标。β-APP通过2种分泌酶活性进行蛋白水解,产生致病性Aβ。N端的裂解是由BACE介导,而c端的膜内裂解是由早老素(presenilin,PS)γ-分泌酶复合物介导,此过程中NF-κB信号通路的激活是其重要原因[16]。此外,致病性Aβ的聚集体能引起神经元细胞的氧化应激和炎症反应的增强,使其活性氧簇(reactive oxygen species,ROS)、炎症因子TNF-α(tumor necrosis factorα,TNF-α)、IL-1β(interleukin-1β,IL-1β)、IL-6等大量释放。一些促氧化基因包括环氧化酶-2(cyclooxygenase-2,COX2)、诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)和几种脂氧合酶的表达也增加,而ROS通过上游激酶或磷酸酶直接或间接影响NF-κB亚基或是其抑制蛋白(Iκb),对一些生物分子进行破坏,从而使神经元损伤、突触功能障碍等[17],且这些细胞因子反过来可以作用于神经元和星形胶质细胞,诱导更多细胞因子和趋化因子的表达,导致炎症循环[18],这些炎症反应、氧化应激、突触功能障碍、神经元的丢失等加重了AD的进程[19],而NF-κB信号通路在其中扮演了重要角色。
2 中医方药对AD NF-κB信号通路调控的研究
2.1 中医复方对AD NF-κB信号通路调控的研究 (表1)

表1 中医复方对AD的NF-κB信号通路调控研究
在中医复方干预AD的实验研究中发现,七福饮可调控AGEs(advanced glycation end products,AGEs)/RAGE(advanced glycation end product receptor,RAGE)/NF-κB通路,降低模型大鼠海马内AGEs、下调皮层和海马中其受体RAGE和NF-κB的表达,降低IL-1β水平而减轻神经炎症[20];黄连解毒汤(HJD)可提高AD模型大鼠脑内超氧化物歧化酶(superoxide dismutase,SOD)活性,降低丙二醛(malondialdehyde,MDA)含量,抑制IκB/NF-κB信号通路活化,改善脑内氧化应激以及炎症状态[21];苓桂术甘汤可以降低AD模型大鼠脑内海马与皮质区的3种主要细胞因子(IL-1β、IL-6与TNF-α)的表达,抑制NF-κB信号通路[22];中成药天芪益智颗粒能抑制AD模型大鼠脑内p38/NF-κB信号通路激活,降低促炎因子COX-2、iNOS的表达,减轻AD大鼠神经炎性反应[23]。此外临床实验研究也发现,中药复方薯蓣丸浓缩汤剂能降低AD患者外周血中IL-1β、NF-κB以及血清中微小核糖核酸-146a(miR-146a)、miR-107、miR-29a、miR-29b、miR-181c、miR-125b、miR-342-3p的表达,降低炎症反应改善患者生活质量[24,25]。可见,部分中医复方可以通过调控NF-κB信号通路,进而减轻炎症反应和氧化应激状态,实现对AD的防治作用。
刘学凤[26]等根据全国名老中医王灿晖经验,使用改良三甲散的含药脑脊液处理AD模型细胞,发现其有效降低NF-κB的表达;此外改良三甲散还能改善AD模型大鼠学习记忆能力,降低Aβ表达,促进神经生长因子NGF(nerve growth factor,NGF)的表达[27];李玲[28]等使用何明大经验方脑灵汤灌胃干预AD大鼠模型,发现脑灵汤能有效降低NF-κB和增强IκB的表达,改善AD大鼠学习记忆能力。由此可知,中医复方具有改善学习记忆能力、减轻Aβ沉积并改善AD症状的作用。
费洪新等[29]使用补阳还五汤治疗AD小鼠模型发现,补阳还五汤能维持AD小鼠神经元细胞的形态,且明显降低NF-κB p65蛋白水平;刘斌[30]也发现,补阳还五汤对APP/PS1双转基因小鼠大脑中NF-κB p65蛋白有明显的抑制作用,且减弱低密度脂蛋白受体相关蛋白LRP (low density lipoprotein receptor related protein,LRP)的表达,改善海马组织血管内皮细胞的形态。因此,中医方药通过NF-κB信号通路,达到保护神经元细胞的作用被证实。
2.2 单味中药及其提取物对AD NF-κB信号通路调控的研究(表2)
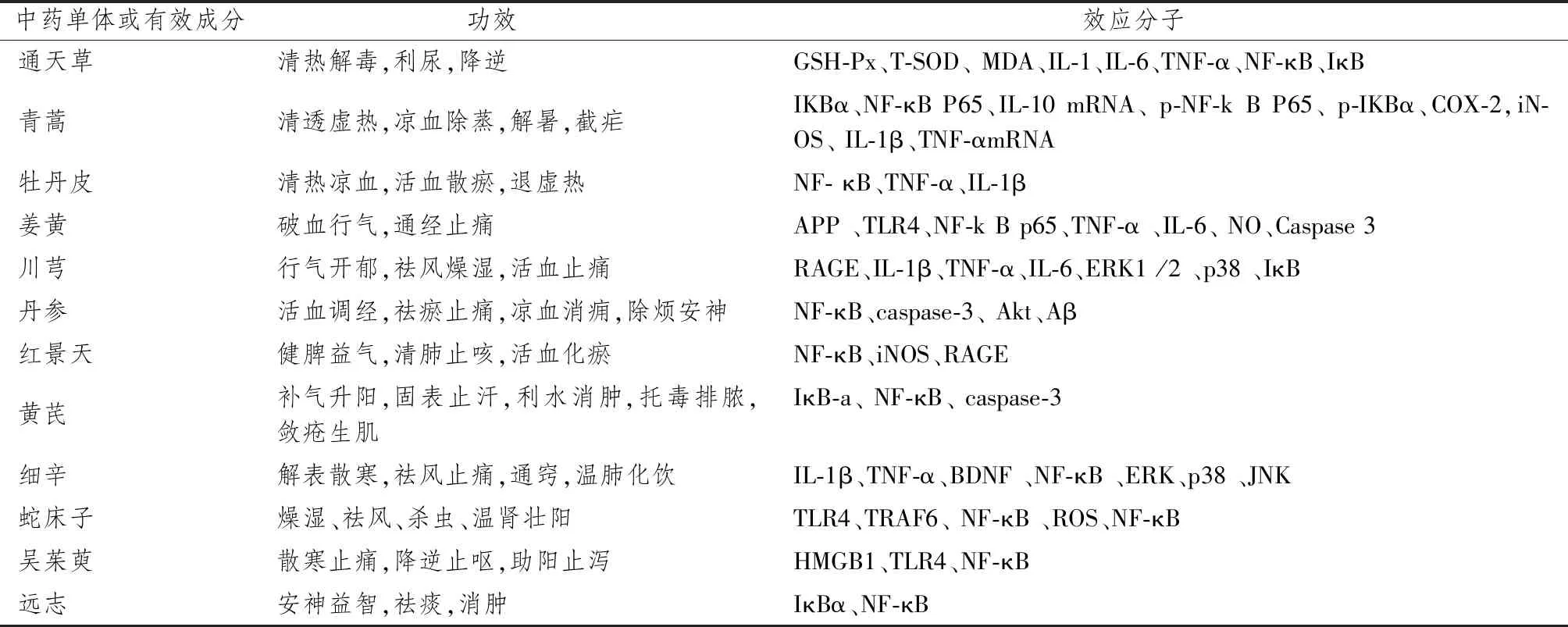
表2 单味中药及其提取物对AD NF-κB信号通路调控的研究
2.2.1 清热类药物 荸荠又名通天草,具有清热解毒、利尿、降逆的功效。通天草提取物能抑制AD模型大鼠脑内NF-κB/IκB通路的表达,诱导谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)和T-SOD活性,抑制MDA生成和炎症因子IL-1、IL-6和TNF-α的分泌[31],保护AD模型大鼠的神经元细胞,降低血液和脑组织免疫炎性,抑制脑内氧化应激反应[32,33]。
青蒿具有清透虚热、凉血除蒸、解暑截疟等功效,其所含的青蒿素和青蒿琥酯相继被证实能保护神经元细胞,改善AD大鼠学习记忆能力[34,35]。王海英等[36]通过建立AD细胞模型,发现青蒿素能使细胞内IKBα、NF-κB P65蛋白以及抑炎因子IL-10 mRNA的表达升高,COX-2、iNOS、IL-1β、TNF-αmRNA的表达降低;郑云秋等[37]也发现,青蒿素能显著提高脂多糖活化小胶质细胞中NF-κB、IKBα的表达,降低iNOS、COX-2的表达,说明青蒿素能调控NF-κB信号通路,减轻炎症反应。
牡丹皮具有清热凉血、活血散瘀、退虚热的功效。丹皮酚为牡丹皮的主要活性成分,在治疗AD模型大鼠的实验研究中发现,丹皮酚可下调脑组织中NF-κB、TNF-α和IL-1β等表达,从而减轻神经炎症反应,达到保护神经元的作用[38]。
2.2.2 活血类药物 郁金又名姜黄,具有破血、行气、通经、止痛之功效,其所含姜黄素具有减轻Aβ聚集、抗金属螯合以及促进损伤神经修复等功能[39]。李凡[40]用姜黄素腹腔注射治疗AD模型大鼠,结果显示与模型组比较,治疗组APP、TLR4、NF-κB p65、TNF-α、IL-6、NO含量和含半胱氨酸的天冬氨酸蛋白水解酶(cysteinyl aspartate specific proteinase,Caspase)3活性均明显降低,因此姜黄素对AD大鼠的认知功能保护机制,可能是通过干预TLR4/NF-κB信号通路实现的。
川芎具有行气开郁、祛风燥湿、活血止痛等功效。川芎提取物川芎嗪被证实能显著降低AD模型大鼠中RAGE基因表达,抑制ERK1/2(extracellular regulated protein kinases,ERK)、p38、IκB的磷酸化,降低IL-1β、TNF-α、IL-6等炎性因子水平,从而改善AD大鼠脑内炎症[41]。
丹参具有活血调经、祛瘀止痛、凉血消痈、除烦安神的功效。丹参提取物丹参酮ⅡA(TanⅡA)能降低AD模型大鼠脑中NF-κB与caspase-3的表达水平,上调Akt蛋白表达,减少Aβ的生成,起到神经保护作用[42]。
2.2.3 补益类药物 红景天具有健脾益气、清肺止咳、活血化瘀之功效。在治疗AD中,红景天有很好的神经营养和神经保护、改善认知能力下降等多种神经生物学作用[43]。实验研究发现,红景天苷能降低海马组织中NF-κB、iNOS及RAGE的表达,通过抗氧化达到治疗AD的作用[44]。
黄芪具有补气升阳、固表止汗、利水消肿、托毒排脓、敛疮生肌的功效。高立威[45]使用黄芪提取物对AD模型大鼠干预治疗,发现黄芪提取物能提高AD大鼠海马区IkBα的含量;单铁强[46]也同样证明,黄芪提取物能提高IκBa的表达,减少游离NF-κB含量,并抑制caspase-3的表达,从而抑制神经细胞的凋亡。
2.2.4 祛风散寒温阳类药物 细辛具有解表散寒、祛风止痛、通窍、温肺化饮的功效。在实验研究中,细辛及其提取物也被证实具有改善AD大鼠的认知缺陷、记忆障碍和突出可塑性等作用[47,48]。何潆[49]使用β-细辛醚干预Aβ1-42诱导的星形胶质细胞活化所致PC12细胞损伤,结果显示β-细辛醚能有效抑制NF-κB的活性,降低IL-1β、TNF-α减轻PC12细胞损伤。
蛇床子具有燥湿、祛风、杀虫、温肾壮阳之功。利用蛇床子素腹腔注射干预AD模型大鼠,结果显示蛇床子素能明显抑制TLR4、TRAF6和NF-κB的表达[50]。Liao等[51]也证明,蛇床子素能够抑制LPS刺激大鼠脑内NF-κB的活化和ROS的释放,从而减轻炎症和氧化应激反应,达到改善大鼠学习记忆能力的作用。
吴茱萸具有散寒止痛、降逆止呕、助阳止泻的功效。孙文蕾[52]利用吴茱萸碱治疗AD模型大鼠发现,吴茱萸碱能下调HMGB1(high mobility group protein,HMGB1)、TLR4及NF-κB蛋白表达,从而抑制HMGB1/TLR4/NF-κB信号通路,改善AD大鼠的学习记忆能力。
2.2.5 其他类药物 远志具有安神益智、祛痰、消肿的功效,其所含的远志皂苷也被证实在AD中具有促进神经干细胞增殖、减轻Aβ损伤、抗氧化、减轻tau蛋白过度磷酸化、保护神经胆碱能系统的作用[53]。黄作义[54]用远志干预AD模型大鼠,发现远志能够通过抑制IκBa降解而减轻AD症状。
3 总结与展望
综上所述,中医方药通过调节NF-κB信号通路达到以下可能机制:一是改善脑内炎症,减轻Aβ沉积及相关蛋白的表达,发挥抗氧化抗炎症的作用;二是通过抑制Aβ神经毒性保护神经元,并促进已损伤神经元的修复;三是促进神经干细胞增殖达到抗凋亡的效用,改善学习记忆和认知功能。从临床选方用药分析,中医方药治疗AD多以填精益髓、补益气血、调补五脏加以化痰逐瘀祛邪之法防治AD,如改良三甲散、七福饮、姜黄、红景天、黄芪等,并根据辨证配伍以清热类药物如青蒿、通天草、丹皮,或配以祛风散寒温阳类药物如红景天、蛇床子、吴茱萸等,以兹疗效。
因此,基于NF-κB信号通路,运用中医药治疗AD已成为可行的思路方法,其视角在中医理论及现代分子生物学的集合下更为宽广,且包容性更丰富,操作性更强。但其深入机制和以该通路为靶标的具体治疗策略以及临床实践价值,仍需诸位同仁共同探讨,相信未来中医药于AD的治疗应用,可绽中医之光,以救苍黎之患。

