病耻感与首发卒中患者卒中后抑郁的相关性研究
胡瑞丹 ,周宏珍 *,刘志红 ,侯佳坤 ,刘杨杨 ,白雪洁 ,李牧玲
卒中后抑郁(post-stroke depression,PSD)是卒中幸存者最常见的精神障碍,约1/3的患者会在卒中后某个时间点发生PSD[1]。PSD患者可出现情绪低落、兴趣缺乏及睡眠、食欲紊乱等躯体症状,甚至出现焦虑、自罪自责、自杀等心理症状,增加疾病的复发率和死亡率[2]。与此同时,80%的患者在卒中急性期、康复期可能因躯体障碍遭遇来自家人、朋友的歧视,经历中等水平的病耻感[3-5]。病耻感指患者因疾病原因怀疑自身价值和在社会群体中产生刻板印象的羞耻表现[6]。已有研究表明病耻感和抑郁存在正相关关系,但尚未深入阐释两者的联系和作用机制[3-5]。鉴于目前PSD的病理生理学机制仍不清晰,而心理-社会因素可能是PSD的重要发病机制之一[7],本研究对首发卒中患者的抑郁和病耻感进行随访调查,以期通过明确两者的关系和影响机制而促进PSD的识别和干预。
1 对象与方法
1.1 研究对象 采用横断面调查研究设计和便利抽样的方法,选取2019年7—12月就诊于南方医科大学南方医院、广东三九脑科医院神经内科和神经外科的首发卒中患者299例。纳入标准:年龄≥18岁;符合《中国各类主要脑血管病诊断要点2019》[8]中卒中的诊断标准,并经CT或MRI检查确诊;7 d≤距首次确诊卒中时间≤1个月;意识清晰,生命体征平稳;有阅读、沟通和理解能力;自愿参加本研究。排除标准:既往有抑郁、精神分裂症或其他精神疾病史;伴有其他中枢神经系统疾病、恶性肿瘤等严重合并症或明显并发症;伴有意识障碍、认知功能损伤、痴呆、运动型失语、感觉性失语、耳聋。本研究经南方医科大学南方医院伦理委员会审查批准(批准号:NFEC-2018-054)。
1.3 资料收集
1.3.1 一般临床资料 包括人口学资料(性别、年龄、受教育程度、婚姻状态、工作情况、家庭人均月收入、居住类型、照顾类型)和卒中病史资料(卒中类型、卒中部位、卒中家族史、精神疾病家族史、高脂血症、高血压、糖尿病)。
1.3.2 结局指标 以患者首次发病时间为准,采取在患者住院期间调查或出院后电话随访的方式评估患者卒中后1个月时病耻感、抑郁和神经功能恢复情况。
1.3.2.1 卒中病耻感量表(Stroke Stigma Scale,SSS)SSS由ZHU等[9]研发的卒中患者病耻感测量专用量表,包括躯体障碍(physical impairment)、社会交往(social isolation)、受歧视经历(discrimination experience)和自我感受(internalized stigma)4个维度,共16个条目。各条目采用Likert 5级评分法(1~5分),依次为“从不”“偶尔”“有时”“经常”“总是”,部分条目为反向计分,总分为16~80分,总分越高表示患者的病耻感越高。量表内容效度为0.989,Cronbach'sα系数为0.916,重测信度为0.924,具有较好的信效度,可作为卒中患者病耻感的评价工具。
1.3.2.2 9条目患者健康量表(Patient Health Questionnaire,PHQ-9)PHQ-9基于美国《精神障碍与统计手册(第4版)》[10]制订,被广泛应用于基层卫生中心抑郁症的筛查工作,在一般人群和不同的患病人群中显示良好的心理学特性,适合护士在内的非精神医学专业人士使用[11]。2013年郑婷等[12]将PHQ-9引进国内,并证实该量表在PSD患者信效度良好,其中Cronbach'sα系数为0.838 3,条目与总分的相关系数为0.533~0.777,各条目间的相关系数为0.183~0.599;效标效度为0.599。PHQ-9主要调查患者在过去的两周出现相应情况的频率,共9个条目,每个条目的分值如下:0分=“一点没有”,1分=“有几天”,2分=“超过一周”,3分=“几乎每天都是”。该量表总分为0~27分,其中,0~4分为无抑郁;5~9分为有抑郁症状;10~14分为明显抑郁症状;≥15分为重度抑郁。本研究将存在抑郁症状者纳入PSD组,余纳入非PSD组。
1.3.2.3 改良Rankin量表(Modified Rankin Scale,mRS)mRS用于评估卒中患者神经功能恢复情况,共6个条目,并将患者的神经功能恢复程度分为6级(0~5分);0分表示无症状;1分表示没有明显的残疾,能够完成自己的工作;2分表示轻度残疾,但可以照顾自己;3分表示中度残疾,需要一些帮助;4分表示中重度残疾,在没有别人帮助的情况下不能独自行走和照顾自己;5分表示重度残疾,卧床,大小便失禁,需要长期的护理和照顾。
1.4 统计学方法 使用EpiData Version 3.1软件进行双人独立录入,采用SPSS 19.0软件进行统计学分析。非正态分布的计量资料以M(P25,P75)表示,组间比较采用非参数检验;计数资料以相对数表示,组间比较采用χ2检验;相关性分析采用Spearman秩相关分析;采用多因素Logistic回归分析探究首发卒中患者PSD的影响因素。以P<0.05为差异有统计学意义。
2 结果
2.1 首发卒中患者抑郁发生情况 共纳入299例首发卒中患者,完整随访221例,脱落78例(包含由于病情加重无法配合调查6例,退出调查25例,失联42例,资料收集不全5例)。根据PHQ-9评分,无抑郁156例(70.6%),有抑郁症状57例(25.8%),明显抑郁症状7例(3.2%),重度抑郁1例(0.4%)。最终进入PSD组65例,非PSD组156例。
2.2 PSD组和非PSD组一般临床资料比较 PSD组和非PSD组性别、年龄、受教育程度、婚姻状态、工作情况、家庭人均月收入、居住类型、卒中类型、卒中部位、卒中家族史、精神疾病家族史及高脂血症、高血压、糖尿病发生率比较,差异均无统计学意义(P>0.05);两组照顾类型比较,差异有统计学意义(P<0.05,见表1)。
2.3 PSD组和非PSD组SSS总分及各维度评分、PHQ-9评分、mRS评分比较 PSD组SSS总分及躯体障碍、社会交往、受歧视经历、自我感受、PHQ-9、mRS评分均高于非PSD组,差异有统计学意义(P<0.05,见表2)。
2.4 相关性分析 PHQ-9评分与SSS总分及躯体障碍、社会交往、受歧视经历、自我感受、mRS评分呈正相关(P<0.05);mRS评分与SSS总分及躯体障碍、社会交往、受歧视经历、自我感受评分呈正相关(P<0.05,见表3)。
2.5 多因素Logistic回归分析 以出现PSD为因变量(赋值:是=2,否=1),以单因素分析中P<0.1的指标为自变量〔照顾类型(赋值:自己照顾自己=1,直系亲属照顾=2)、SSS总分(赋值:实测值)、mRS评分(赋值:实测值)〕,考虑包括性别(赋值:男=1,女=2)、年龄、卒中部位(赋值:左半大脑=1,右半大脑=2,小脑=3,脑干=4,混合/多发部位=5)在内的混杂因素同时纳入作为自变量进行多因素Logistic回归分析,结果显示,SSS总分是首发卒中患者发生PSD的影响因素(P<0.05,见表4)。
2.6 PSD组和非PSD组SSS评价情况 PSD组和非PSD组SSS评价情况见表5。
3 讨论
3.1 重视卒中患者早期PSD的评估 卒中是我国成年人病死、致残的首位病因,目前我国≥40岁居民卒中现患例数为1 242万,其中75%的卒中幸存者出院后要长期适应不同程度的功能障碍[13]。卒中后生活能力差、负性生活事件、社会支持不良、合并多种疾病及神经质人格特征等均可能促使PSD的发生[7]。早期卒中患者的治疗以稳定病情为主,但部分患者伴有失语症状,使得PSD的识别较困难,因此要警惕PSD的发生[14]。本研究中首发卒中患者PSD发生率为29.4%,与既往研究结果[15]相似。PSD和非PSD患者性别、年龄、卒中部位间无差异,相关Meta分析[16]结果指出女性、年龄<70岁、卒中部位为左大脑半球与PSD的发生密切相关,但仍存在争议,需进一步研究。

表1 PSD组和非PSD组一般临床资料比较〔n(%)〕Table 1 Comparison of general and clinical characteristics between PSD group and non-PSD group
3.2 病耻感和PSD的关系 卒中后遗症是卒中患者产生负性情绪的基础,也是PSD[17]和病耻感[18-19]的危险因素。身体残疾和功能依赖降低了患者的日常生活自理能力和社会交往能力,给患者的身心带来负面的影响;而大众对卒中的不正确认识、对残疾患者的污名化可进一步降低患者的自我评价,导致患者出现社会孤立,造成抑郁[20]。一项针对大众对卒中患者症状的归因调查显示,年轻卒中患者出现的疲劳、抑郁症状被视为懒惰[21]。伴有卒中后遗症的患者因被视为不具有最佳工作能力而丢失工作[22]。部分患者家属因受到社会文化观念的影响而不愿意带伴有卒中残疾的患者外出[23]。本研究多因素Logistic回归分析结果显示,SSS总分是首发卒中患者发生PSD的独立危险因素。削弱社会支持水平、加深自我的负性评价可能是病耻感对首发卒中患者发生PSD的作用机制。

表2 PSD组和非PSD组SSS总分及各维度评分、PHQ-9评分、mRS评分比较〔M(P25,P75),分〕Table 2 Comparisons of SSS Scale score an score of each dimension,PHQ and mRS scores between PSD group and non-PSD group

表3 首发卒中患者SSS总分及各维度评分、PHQ-9和mRS评分的相关性分析(rs值)Table 3 Correlations of stroke stigma scale and scores of each dimension,PHQ-9 and mRS score among patients with initial stroke
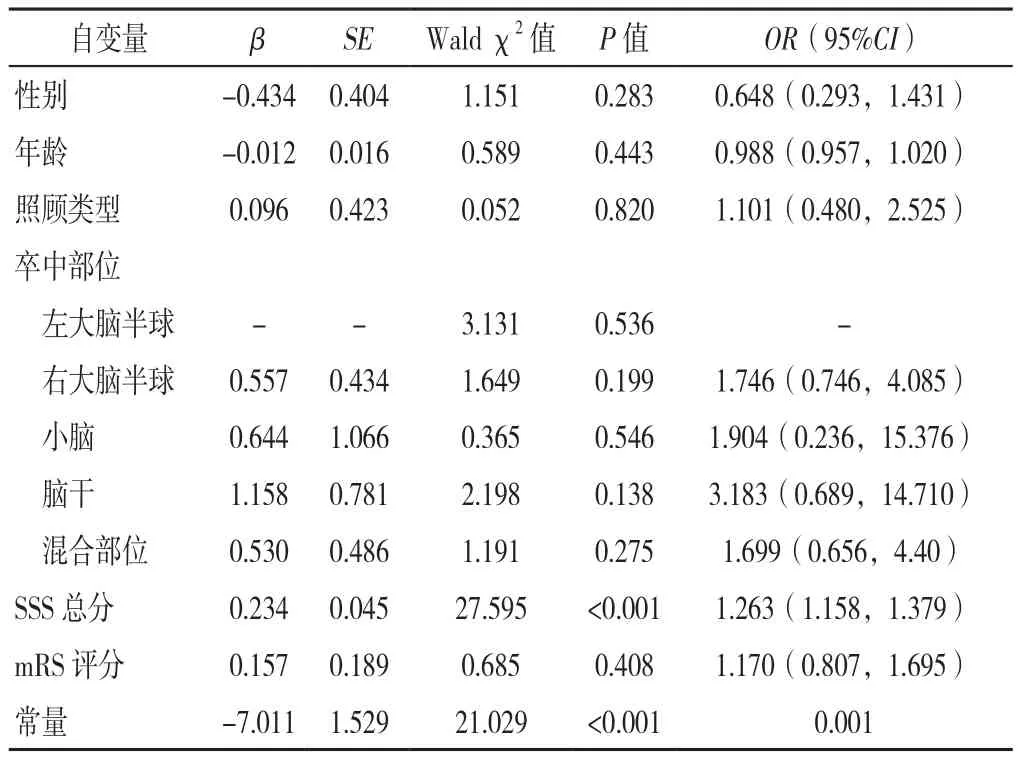
表4 首发卒中患者发生PSD影响因素的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis of influencing factors of post-stroke depression among patients with initial stroke
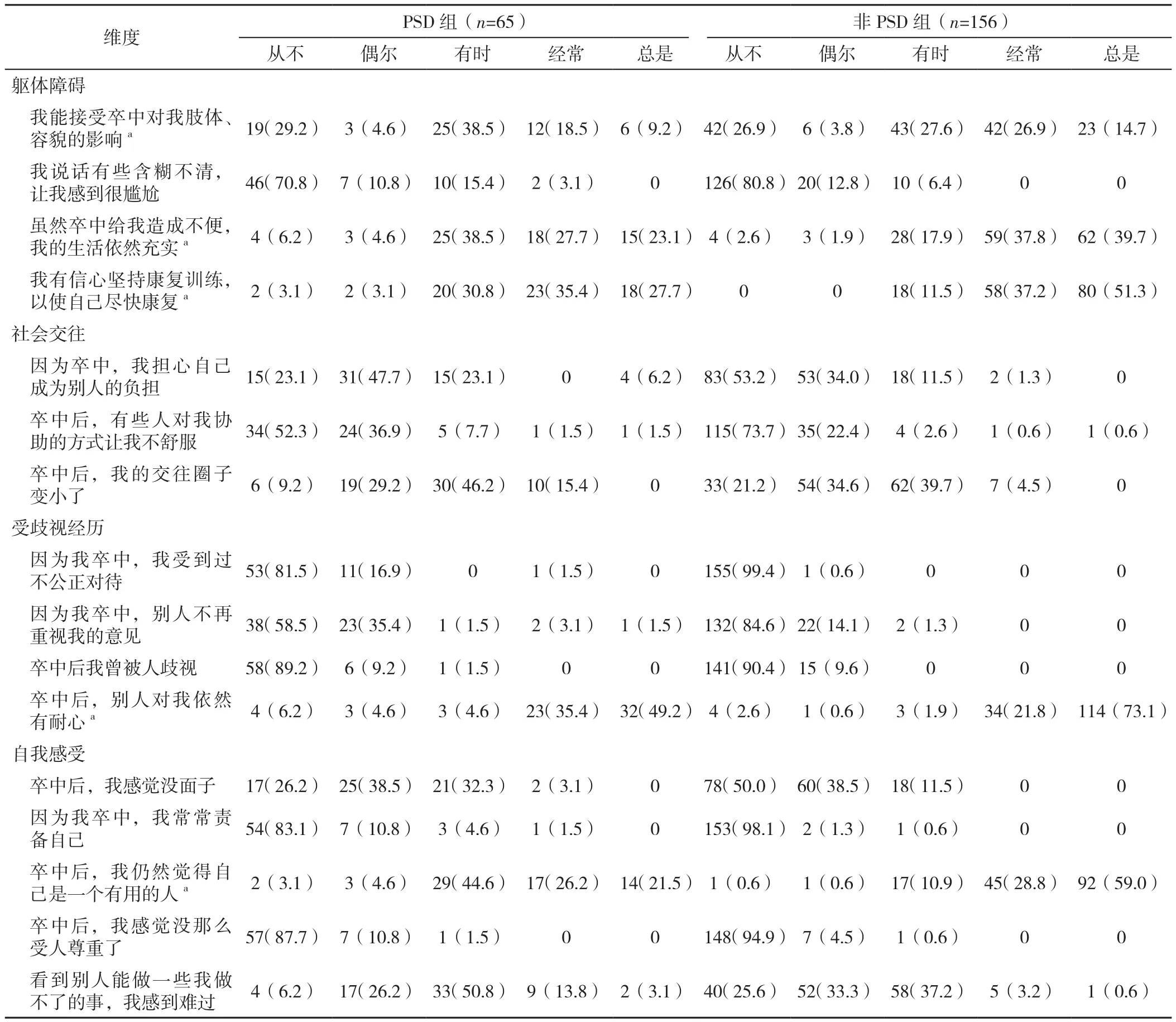
表5 PSD组和非PSD组SSS评价情况分析〔n(%)〕Table 5 Analysis of SSS evaluation in the PSD group and non-PSD group
CORRIGAN等[24]采用心理认知模型解释病耻感的影响,并指出存在病耻感的患者在污名化过程中出现了认知、情绪和行为的变化,如内化歧视经历,接受刻板印象,产生低自尊、自我效能感降低等消极情绪和社会孤立、治疗依从性差等行为。本研究中接近40%的PSD患者表示“因为卒中,别人不再重视我的意见”,经历了不同程度的不公正对待和歧视,交往圈子变小。来自家人、朋友等对卒中的歧视和误解加深了卒中患者的病耻感,使患者因此而产生回避社交的行为[19]。近30%的PSD患者表示“从不接受卒中对肢体、容貌的影响”并出现悲伤的情绪,使康复训练信心和积极性受到影响;因此与非PSD患者相比,PSD患者具有更高的残疾程度。
卒中患者是社交受限的高危人群[22]。良好的社会支持水平和认知、心理状态有助于患者采取积极的方式应对卒中带来的身体和生活改变。据统计中国目前仍有30%的农村卒中患者参与社会活动受限,并缺乏有意义的休闲活动[25];病耻感等不良心理因素使患者身心遭受二次打击,导致卒中后适应不良。病耻感对卒中患者自我认知和心理-社会方面的影响可能引发PSD,应当引起人们的重视。
综上,本研究结果显示病耻感是首发卒中患者发生PSD的独立危险因素,早期的病耻感对PSD的发生具有一定的预测价值;本研究结果有望为病耻感的干预和PSD的防治提供新的理论依据,促进PSD的早期识别。但本研究仅评估了首发卒中患者发病后1个月时PSD发生情况,今后可通过延长随访时间而观察两者的动态变化。
本研究价值:
本研究根据卒中病耻感量表总分及各维度评分结果分析病耻感对卒中后抑郁(PSD)患者自尊、情绪和行为的影响表现,今后可使用自尊、自我效能感、社会支持专用量表进行相关路径分析,以进一步验证病耻感对PSD的作用机制。
作者贡献:胡瑞丹、周宏珍进行文章的构思与设计;胡瑞丹、刘志红、侯佳坤、刘杨杨、白雪洁、李牧玲进行研究的实施与可行性分析;胡瑞丹、侯佳坤、刘杨杨进行数据收集与整理、统计学处理;胡瑞丹撰写论文;周宏珍进行论文的修订,对文章整体负责,监督管理。
本文无利益冲突。

