实时直接分析-高分辨质谱法快速筛查乳粉中抗生素残留
杨 帆,张璐琪,张鸿伟,纪仁春,张晓梅,许 辉,王凤美,王妍婷,宫小明,徐 杰
(1.中国海洋大学食品科学与工程学院,山东 青岛 266003;2.青岛海关技术中心,山东 青岛 266002;3. 西双版纳海关综合技术中心,云南 景洪 666100;4.潍坊海关技术中心,山东 潍坊 261041)
兽药被广泛用于动物疾病的预防和治疗、促进动物生长等方面,其种类繁多,抗生素是兽药残留分析中最常见的残留类别[1]。乳粉中含有大量对人体生长发育有重要作用的营养元素,是生活中常见的食品,婴幼儿、儿童和老人是乳粉的主要受众群体。乳粉中抗生素残留一直是食品安全关注的重点,长期食用含有抗生素残留的乳粉会使人体内产生耐药菌株[2],降低机体免疫力[3-4],给消费者带来健康隐患。在乳粉抗生素残留分析中,磺胺类、喹诺酮类及大环内酯类药物类属高频次检测项目[5],建立这些药物残留的快速筛查分析方法有利于提高日常筛查分析通量,增进风险监测效能,完善乳粉产品质量安全控制的技术支持体系。
实时直接分析(direct analysis in real time, DART)是一种新型的敞开式常压原位电离技术,可在大气压和开放式实验环境中,不改变被分析物本身性质的前提下,直接完成对样品的离子化以及进样分析[6-8]。该技术的优点在于大幅简化样品制备过程,使无样品制备而直接分析成为可能。DART已经被成功应用于药物研发与监管[9-10]、环境监测[11]、化妆品监测[12-13]、食品分析[14-15]、复杂样品分析及法证科学等领域[16-17]。在食品分析领域,Al-Balaa等[18]利用实时直接分析-飞行时间质谱(DART-TOF MS)快速定性和半定量分析干鸡蛋和鸡蛋面食中胆固醇;Farre等[19]利用实时直接分析-高分辨质谱(DART-HRMS)法实现了苹果、梨、柠檬果皮上的氧化剂、杀菌剂以及糖类物质残留的定性定量分析;李伟丽等[20]利用直接分析质谱(DART-MS/MS)法快速检测辣椒及其制品中的辣椒素类物质,并进行了方法学验证。在化学危害物残留分析领域,齐春艳等[21]利用实时直接分析-四极杆-离子回旋轨道阱质谱(DART-Q-Orbitrap MS)法检测了南美白对虾中15种磺胺类药物;Vaclavik等[22]利用实时直接分析-飞行时间质谱法检测了奶粉、炼乳、乳酪等奶制品中三聚氰胺和氰尿酸;Zhang等[23]利用实时直接分析-四极杆-飞行时间质谱(DART-Q-TOF MS/MS)法实现了对奶粉中双氰胺的定性定量分析。
本实验拟将DART离子源与四极杆-离子回旋轨道阱高分辨质谱仪(DART-Q-Orbitrap HRMS)联用,快速筛查乳粉中磺胺类、喹诺酮类和大环内酯类等16种常见抗生素的残留,并对分析条件进行优化,希望建立相关药物残留的筛查方法。
1 实验部分
1.1 主要仪器与装置
DART实时直接分析离子源:美国IonSense公司产品;Q-Exactive Orbitrap高分辨质谱仪:美国Thermo Scientific公司产品,配有Xcalibur1.2工作站;CR22G Ⅱ高速冷冻离心机:日本日立公司产品;Mettler PL202-L型电子分析天平:瑞士美特勒-托利多公司产品;Turbo Vap®LV型高通量水浴氮吹浓缩仪:美国Caliper公司产品;MMV-1000W站立式振荡器:日本EYELA公司产品;MS3型涡旋混匀器:美国IKA公司产品;KQ-100E台式超声波仪:昆山市超声仪器有限公司产品;Captiva ND lipids固相萃取柱、EMR-Lipid净化管:美国Agilent公司产品。
1.2 主要材料与试剂
乙腈(质谱纯):美国Fisher Scientific公司产品;甲酸(质谱纯):美国Fluka公司产品。
磺胺嘧啶、磺胺-5-(对)甲氧嘧啶、磺胺二甲氧嘧啶、磺胺甲基嘧啶、磺胺吡啶、甲氨苄啶(纯度≥99.0%):德国Dr.Ehrenstorfer公司产品;磺胺二甲嘧啶(纯度≥98.0%):美国Sigma Aldrich公司产品;丹诺沙星、西诺沙星、双氟沙星、司帕沙星、萘啶酸、氟甲喹、奥比沙星(纯度≥98.0%)、替米考星、交沙霉素(纯度≥80.0%):中国First Standard公司产品。
1.3 实验条件
1.3.1DART离子源条件 正离子模式,载气为氦气,选择QuickStrip (QS)样品卡模块进样,进样速度1 mm/s,离子化温度400 ℃。
1.3.2质谱条件 采集方式:Full MS-ddMS2(正离子模式扫描),其中Full MS母离子扫描质谱分辨率设定为70 000,子离子质谱依赖性扫描分辨率设定为17 500(3级碰撞能量分别设定20、40、60 eV);喷雾电压3.0 kV;毛细管温度350 ℃;鞘气流速30 L/min;辅助气流速3.3 L/min;反吹气流量0;质量扫描范围m/z100~500。
1.4 标准储备液与混合标准工作液的配制
标准储备液(1 g/L)的配制:分别称取10 mg(精确到0.1 mg)标准品于10 mL容量瓶中,用乙腈溶解并定容,-20 ℃可保存6个月。
混合标准工作溶液(1 mg/L)的配制:分别移取10 μL相应标准储备液于10 mL容量瓶中,用50%乙腈-水溶液定容,-20 ℃可保存1个月。
1.5 实验方法
称取(2.00±0.02) g乳粉于50 mL离心管中,用4 mL水溶解,混匀,加入12 mL乙腈,涡旋振荡10 min,以10 000 r/min离心10 min,取4 mL上清液,过Captiva ND lipids固相萃取柱,收集滤出液,40 ℃下氮吹至近干,准确加入2 mL 0.3%甲酸-5%乙腈-水溶液复溶残渣,涡旋并超声5 min,过0.22 μm滤膜,作为待测液备用。
吸取4 μL待测液,将其滴至QS样品卡的金属筛网进样点处,放置在通风橱中使其蒸发至近干,然后将其固定在DART离子源和Q-Exactive Orbitrap高分辨质谱仪之间的滑动轨道上进行检测。
2 结果与讨论
2.1 载气类型和进样模块的选择
高纯度的氮气和氦气是DART离子源最常用的载气,氦气由于其激发态离子能量比氮气高且灵敏度高,因此能电离的化合物较多。由于氦气可电离大分子质量化合物,且副反应较小,可用于相对较大的大分子质量抗生素的检测[24],因此本实验选择氦气作为载气。但由于氦气和氮气相比价格昂贵,故在样品分析前后和实验准备期间选择氮气作为辅助气体。
本实验尝试了用Dip-It玻棒模块进样,但出现了挂在玻棒上的样品液滴不稳定,导致质谱峰响应低且出现拖尾现象,因此选用QS样品卡模块进样。
2.2 载气温度的选择
对于DART离子源,温度对其敏感度的影响很大。本实验分别考察了300、350、400 ℃下氦气的离子化效果,并与扣除空气背景后的质谱图进行对比,结果示于图1。可见,离子化温度过低,会减少离子进入质谱仪的数量;离子化温度越高,离子化效果越好,背景干扰越小,灵敏度越高。实验还验证了450 ℃的离子化效果,发现出峰率和响应较低,离子化效果不理想,这是由于温度过高容易使残留药物分子分解,液体样品挥发过快而导致目标物在进样模块网格中扩散。因此,本实验选择400 ℃作为载气温度。
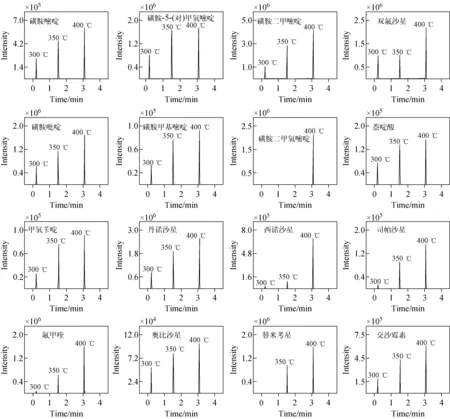
图1 在300、350、400 ℃温度下,各目标分析物的离子化效果对比图Fig.1 Ionization effect of the analytes in DART ion source at the temperature of 300, 350, 400 ℃
2.3 进样速度的选择
QS样品卡的移动速度对DART离子源灵敏度的影响较大,本实验分别考察进样速度为0.4、0.6、0.8、1.0、1.5 mm/s时的离子化效果。经分析可知,进样速度过慢时,质谱峰会有峰型拖尾、出现双峰或三峰的情况;进样速度过快时,离子进入质谱的数量减少,从而导致响应过低甚至无响应。因此本实验选择1.0 mm/s的速度进样。
需要指出的是,采用DART-Q-Orbitrap HRMS分析时经常出现双峰现象,使用优化的进样速度和载气温度,点样时把握好液滴在样品卡上的位置和液滴大小,控制液滴干燥程度不要过干,可以有效地避免双峰、拖尾及影响目标分析物响应等现象。
2.4 方法验证
2.4.1定性分析指标 本研究以目标分析物的准分子离子峰作为筛查定性离子,采用准分子离子和高分辨碎片离子库匹配的方式进行准确定性,具体如下:1) 准分子离子峰的质量准确度≤5×10-6;2) 具有与准分子离子峰相似的同位素分布;3) 与标准品谱库相比存在2个质量准确度≤5×10-6的特征碎片离子[25-26]。本实验对空白样品进行添加(100 μg/kg),使用DART-Q-Orbitrap HRMS系统进行正离子一级质谱全扫描,检测得到了16种目标分析物的准分子离子峰质量数与理论值,以及主要特征碎片离子,列于表1。可知,相对误差均在5×10-6以下,特征碎片离子与实验室利用标准溶液自建的数据库匹配较好,可以实现相关残留物质的准确定性分析。
2.4.2筛查限浓度水平和回收率 选取20个空白乳粉样品,每个样品各称取4份,1份作为空白样品,另3份作为加标样品,加标水平分别为10、50、100 μg/kg,每个样品均进行平行测定,各分析目标物前体离子在空白样品中响应的最大值不小于加标样品中响应的最小值时为假阴性。在100 μg/kg浓度水平下,除双氟沙星和替米考星外,其余所有分析物的假阴性率均为零,双氟沙星和替米考星在20次测定中各有1次出现了提取前体离子窗口无响应的情况,推测这两种分析物对点样要求较高,液滴过干会影响其响应,将添加回收样品重新点样后响应正常,因此实验要控制样滴在样品卡上的干燥情况,结果列于表2。根据欧盟关于筛查方法在筛查限浓度水平下假阴性率的要求[27],本实验各目标分析物在100 μg/kg浓度下的假阴性率均≤5%,故将本方法的筛查限浓度水平确定为100 μg/kg。鉴于高分辨质谱无法使用信噪比推算分析物的方法检出限(LOD),因此,各分析物的检出限按照加标水平提取离子的响应情况(在相应加标水平的所有样品中有明显且稳定的响应)进行标示,结果列于表3。
按1.5节方法对乳粉空白基质进行前处理,获得基质空白提取液,制备相当于样品分析物水平为20、50、100、150、200 μg/kg的标准溶液,并进行6个重复样品的添加回收实验,使用制备的基质标准曲线进行定量分析,标准曲线决定系数r2为0.992 1~0.998 8,各分析目标物的回收率在72.5%~106.7%之间,典型的离子流图示于图2。
需要指出的是,回收率不是筛查方法必须考察的指标,回收率的引入可作为后续确证定量分析浓度范围的参考。
2.5 实际样品检测
使用本方法快速筛查193份市售乳粉产品中16种常见抗生素,结果筛查出1例甲氧苄啶阳性样品,其一级全扫描离子流图和二级质谱图分别示于图3和图4。
由图3可见,在DART-Q-Orbitrap HRMS一级质谱正离子全扫描模式下,发现存在m/z291.145[M+H]+准分子离子峰,其质谱依赖性二级质谱子离子扫描得到了m/z123.066、261.097特征碎片离子,对照已建立的甲氧苄啶二级高分辨质谱信息库,确定样品中含有甲氧苄啶。


表2 16种目标分析物残留筛查测定假阴性率Table 2 False negative rates of 16 analytes with optimized method

表3 16种目标分析物在筛查限浓度水平下的平均回收率及检出限Table 3 Average recoveries of 16 analytes at the level of screening concentration and limits of detection

图2 空白加标回收乳粉样品中16种目标分析物残留的提取离子流图Fig.2 Extracted ion chromatograms of 16 analytes residues in the spiked milk powder samples

图3 市售51号乳粉样品中目标化合物的检测结果Fig.3 Analysis result of No.51 milk powder sample
3 结论
本研究建立了敞开式常压离子化技术-实时直接分析离子源结合四极杆-回旋轨道阱高分辨质谱法快速筛查乳粉样品中16种常见抗生素残留。通过优化DART离子源参数,借助Q-Orbitrap质谱仪高分辨率及Full MS-ddMS2数据采集方法,使用高通量通用性前处理有效地控制乳粉样品的基质影响,实现乳粉中16种常见抗生素残留的快速有效筛查。
通过验证实验确定了方法的筛查限浓度水平、假阴性率等关键指标,并使用基质标准曲线考察方法在筛查限浓度水平的回收率,方法指标满足筛查分析要求,实际样品检测结果表明,该方法可有效完成乳粉中相关残留的风险监测分析。虽然该方法存在筛查限浓度水平相对较高的情况,但对于相关抗生素高水平风险残留有实际的筛查意义和效果,且其前处理简单、定性分析准确、假阴性率低,可为风险监测实验室和相关行业机构提供一种快速可靠的筛查分析技术。

图4 51号乳粉样品(a)和甲氧苄啶标准品(b)的二级质谱图Fig.4 Mass spectra of No.51 milk powder sample (a) and trimethoprim standard (b)

