羧甲基魔芋葡甘露聚糖对豌豆蛋白水分散液的稳定性作用
陶 冉,李瑞琪,郭亚龙,韦 越,张洪斌
(上海交通大学化学化工学院,上海 200240)
除传统意义上的中性蛋白饮料(如牛奶)外,酸性蛋白饮料由于营养丰富、口感独特,逐渐在蛋白饮料消费市场占据重要地位。相比于市场上长期大量存在的动物蛋白(主要为酪蛋白)饮料,近年来,消费者对中性与酸性植物蛋白饮料的需求不断增加[1-2]。豌豆蛋白作为一种植物来源的天然可持续性蛋白质,不仅价格低、营养价值高、致敏性低,还具有降低胆固醇、血压等独特生理活性[3-4],是代替动物蛋白用于食品配方的可靠原料之一,无疑在蛋白饮料行业具有更强的应用前景[5-7]。然而,豌豆蛋白因表面疏水性强且电荷量低,导致其在水中的溶解度低、物理稳定性差[8-9]。尤其在酸性条件下,当体系pH值接近蛋白质等电点时,豌豆蛋白易发生聚集,使体系稳定性进一步大幅降低[9],因此豌豆蛋白在酸性蛋白饮料中的应用受到很大限制。如何控制豌豆蛋白在中性特别是酸性条件下的稳定分散,是豌豆蛋白饮料发展的主要瓶颈问题。
一些天然生物大分子多糖作为增稠剂、乳化剂、胶凝剂和稳定剂等,已广泛应用于食品工业中[10-12]。通过多糖与蛋白质相互作用,可以阻止或减缓蛋白质的聚集和沉降,提高蛋白分散液的物理稳定性[11,13-14]。多糖对蛋白分散液体系的稳定主要有2 种作用机制:一是在酸性条件下,聚阴离子多糖,如果胶[10,15-16]、羧甲基纤维素(carboxymethyl cellulose,CMC)[17-19]或大豆可溶性多糖[20],可与带正电荷的蛋白颗粒形成静电复合物,通过静电排斥和空间位阻保持蛋白质分散液的稳定性[9]。这些多糖与酪蛋白胶束发生静电吸附,在蛋白胶束表面形成了刷状或环状吸附结构,从而阻止了蛋白胶束的酸诱导聚集使体系稳定。二是,添加的多糖在体系中形成高分子物理缠结网络,增加了连续相的黏度,从而阻碍和迟滞了蛋白颗粒的聚集和沉降[21]。而对于添加了聚阴离子多糖的酸性乳体系,上述2 种稳定作用均会存在。作为多相多组分复杂体系的多糖-蛋白分散液,其稳定性与诸多因素有关,除加工工艺的影响外[19],多糖稳定剂本身的结构和性能是稳定体系的主导因素,特别是多糖分子参数(如分子质量及取代度和取代分布)对体系物理稳定性起着决定性作用[17-18,22]。
在乳液制品研究领域,对高性能稳定剂的需求和对稳定剂不同稳定机理的阐明一直处于不断发展中。近期对魔芋葡甘露聚糖(konjac glucomannan,KGM)、CMC和玉米纤维胶以及羧甲基改性的玉米纤维胶(carboxymethylated corn fiber gum,CMCFG)提高豌豆蛋白分散液(pea protein dispersion,PPD)稳定性的能力进行比较研究发现,KGM的添加可通过增黏作用实现PPD在中性和酸性(pH 3.5)条件下的物理稳定,羧甲基化的CMC和CMCFG则通过与豌豆蛋白的静电吸附促成了体系的稳定[21]。目前,对高浓度、高分子质量和高取代度的多糖有利于乳状液稳定逐渐形成了共识,但稳定剂分子的分子质量和取代度同时变化时如何影响乳状液的行为尚不清晰。
KGM具有天然的生物相容性、生物可降解性、增稠性、胶凝性和成膜性等,同时作为优良的膳食纤维和食品原料,还具有降低血液胆固醇和血糖含量以及促进肠道消化和特异免疫功能的特性,已被广泛用于食品、化工和生物医药等诸多领域[12,23-25]。尽管KGM具有诸多功能特性和健康益处,但水溶性低以及低浓度下的高黏性也造成制得的乳饮料口感不佳。羧甲基化是一种常用的多糖安全改性方法,改性不仅能改善多糖水溶性而且还能在很大程度上保留其生物活性[26]。研究表明,羧甲基魔芋葡甘露聚糖(carboxymethylated konjac glucomannan,CMKGM)可在保持KGM原有生物相容性和增稠性的基础上,大大提高其水溶性和水溶液稳定性[27-29]。本研究基于合成的一系列具有不同取代度和不同分子质量的CMKGM,通过对体系粒径、Zeta电位、表观黏度和不稳定性指数的测定,着重研究CMKGM在分子质量和取代度同时变化的情况下对PPD稳定行为的影响,评估其在中性和酸性条件下对PPD的稳定效果,并分析其不同稳定机理,以期发展新型乳饮料稳定剂,为植物蛋白基饮料配方的开发提供有价值的技术信息。
1 材料与方法
1.1 材料与试剂
KGM 湖北一致魔芋生物科技股份有限公司;NUTRALYS®S85F豌豆分离蛋白(纯度85%) 法国罗盖特公司;盐酸和柠檬酸等化学试剂均为国产分析纯;超纯水为实验室自制;CMKGM为基于文献[27]方法,制备7 种不同分子质量和不同取代度的样品,见表1。
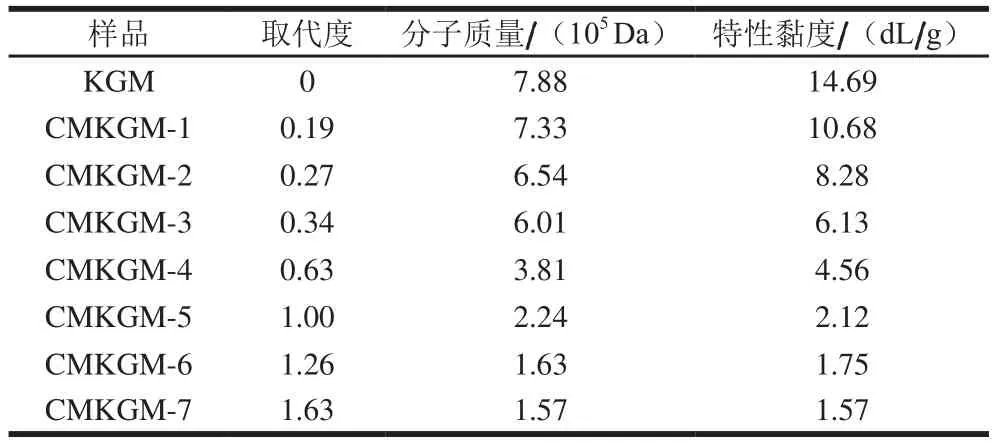
表1 不同取代度的CMKGM样品信息Table 1 Information about CMKGM with different degrees of substitution
1.2 仪器与设备
ME204/02电子天平 梅特勒-托利多仪器(上海)有限公司;MZ3004磁力搅拌器 上海志威电器有限公司;Milli-Q Plus超纯水系统 美国Millipore公司;HAAKE MARSIII旋转流变仪 美国Thermo Fisher公司;高压均质机 美国NanoDeBEE公司;LUMiSizer稳定性分析仪 德国LUM GmbH公司;Zetasizer Nano-ZS90粒径分析仪 英国马尔文仪器公司。
1.3 方法
1.3.1 PPD的制备
称取一定量的豌豆分离蛋白分散于超纯水中,在室温下搅拌1 h,并用高压均质机在50 MPa下循环均质7 次,获得质量分数1%的PPD。将CMKGM样品溶于超纯水中,配制不同质量分数的多糖溶液,然后将1% PPD与多糖溶液以1∶1的质量比混合后搅拌1 h,采用500 g/kg的柠檬酸调节pH值至3.5,继续搅拌1 h,获得多糖稳定的蛋白分散液。
1.3.2 不稳定指数测试
采用稳定性分析仪对新鲜制备的PPD-多糖复合物(中性和pH 3.5)进行稳定性测试。测试条件:转速3 000 r/min,光源865 nm,测试时长1.0 h,温度25 ℃。
1.3.3 Zeta电位和粒径测试
将PPD-多糖复合物分别用相应pH值的去离子水稀释100 倍,采用粒径分析仪分别测定体系在中性和pH 3.5条件下的Zeta电位和平均粒径,测试温度25 ℃,每个样品重复测定3 次。
1.3.4 表观黏度测试
在控制应力流变仪上进行PPD体系的稳态剪切流动行为测试。测试条件:采用60 mm平行板,平行板之间的间隙为0.5 mm,温度25 ℃,剪切速率范围0.01~1 000 s-1。实验时在夹具边缘滴加轻质硅油(10 mPa·s)进行密封,以减少实验过程中的水挥发,样品在测试温度下静置平衡5 min后开始测试。
2 结果与分析
2.1 质量分数一定条件下不同CMKGM对PPD体系的稳定效果比较
如图1所示,在透射曲线上,红线表示样品初始状态的透过率,绿线代表测试进行过程中样品的透过率。在离心过程中,密度大的分散相逐渐迁移到样品管底部,从而使上清液部分的透过率增加。通过透射曲线的变化可以反映出分散液的稳定性。一般而言,在离心过程中,透过率变化越大,样品越不稳定。基于透射曲线还能获得样品的不稳定指数,可定量表征不同样品稳定性的大小(图2)。不稳定指数的数值介于0~1之间,其中0表示体系非常稳定,而1代表体系非常不稳定。在稳定性评估中,以不稳定指数达到0.2或以下为稳定标准。
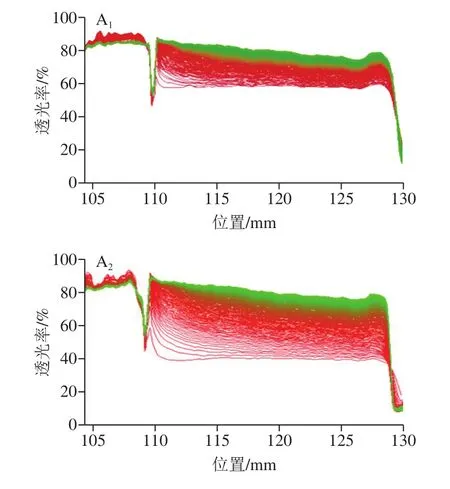

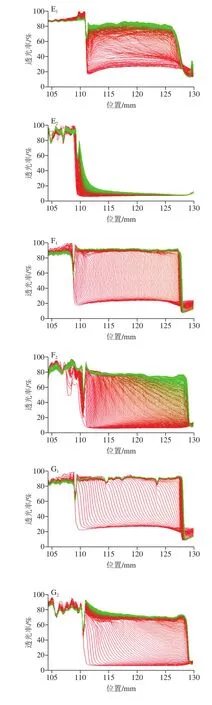
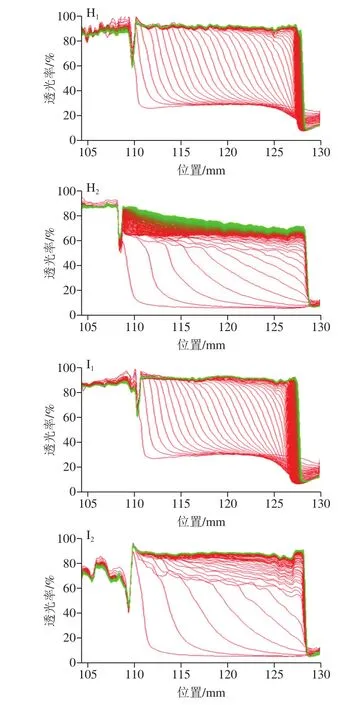
图1 中性和pH 3.5条件下质量分数1%的KGM和CMKGM的1% PPD的透过率变化Fig.1 Transmittance evolution of 1% PPD stabilized by 1% KGM or different CMKGM samples at neutral and acidic (pH 3.5) conditions

图2 中性和pH 3.5条件下质量分数1%的KGM和CMKGM的1% PPD的不稳定指数Fig.2 Instability index of 1% PPD stabilized by 1% KGM or different CMKGM samples at neutral and acidic conditions
由图1、2可知,在不添加稳定剂的情况下,PPD在中性和pH 3.5下均不稳定,且酸性条件下的不稳定程度远大于中性条件。这是由于豌豆蛋白在水中的溶解度低,在离心过程中容易发生聚集[9],特别是当pH值降低,接近豌豆蛋白等电点(~pH 4.5)时,蛋白颗粒之间的静电斥力减弱,更加剧了蛋白胶束的聚集和沉降。多糖的添加在很大程度上改善了体系的稳定性。仅质量分数1%的中性KGM,PPD在中性和酸性条件下都能表现出良好的稳定性。由于不产生有效吸附,这主要是由于KGM的增黏作用[21]。在中性条件下,当添加1%的具有不同取代度和不同分子质量的CMKGM样品时,仅有CMKGM-1能够有效稳定PPD,其他样品(CMKGM-2~CMKGM-7)均不能起到稳定作用。由于在中性条件下,豌豆蛋白颗粒和多糖分子均带负电荷,多糖的稳定作用主要来源于其增黏作用,然而对于CMKGM-2~CMKGM-7样品,由于分子质量逐渐降低,在相同质量分数下(1%)不能起到有效的增黏作用,故不能稳定PPD。在pH 3.5条件下,CMKGM-1、CMKGM-2和CMKGM-3均能在一定程度上保持PPD的稳定,这是因为在酸性条件下豌豆蛋白带正电,带负电的CMKGM能够与豌豆蛋白发生静电吸附使PPD-多糖复合物带负电,从而通过静电排斥作用和空间位阻作用阻碍蛋白颗粒的聚集。再加上未吸附多余多糖分子的增黏作用,两者共同维持了PPD体系的稳定。然而,尽管CMKGM-4~CMKGM-7这4 个样品的羧甲基的取代度增加有利于发挥其在酸性条件下稳定PPD体系中的静电排斥作用,但是由于分子质量过低导致增黏作用大幅减弱,使这些样品在质量分数1%的条件下不能稳定酸性PPD体系。
2.2 不同分子参数CMKGM对稳定PPD体系的临界添加量
如前所述,虽然添加质量分数1%的KGM能够有效稳定中性和酸性PPD体系,但对于不同的CMKGM样品,由于分子质量降低,在相同的添加量下(1%),大多数CMKGM不能有效稳定PPD体系。因此,确定不同取代度和不同分子质量CMKGM的临界稳定添加量,对于CMKGM在PPD体系稳定中的开发和利用具有重要指导意义。如图3A所示,CMKGM的分子质量越低,达到稳定所需的临界多糖添加量也越高。从CMKGM-1的1%,增大到CMKGM-7的20%才能稳定PPD。由此可见,尽管取代度高,但分子质量的高低是CMKGM稳定PPD的主导因素。过低的分子质量,不仅对PPD体系连续相的增黏效果减弱,而且吸附后不能在蛋白颗粒表面形成有效的空间位阻作用。需要指出,对于CMKGM-1、CMKGM-2和CMKGM-3这3 个样品,达到体系物理稳定(不稳定指数小于0.2)所需的多糖质量分数均在2%以下,从实际应用的角度更具有经济性。而且相比于未改性的KGM,改性后CMKGM的水溶性增加、分子质量有所降低,有望改善KGM黏度高带来的不良口感。
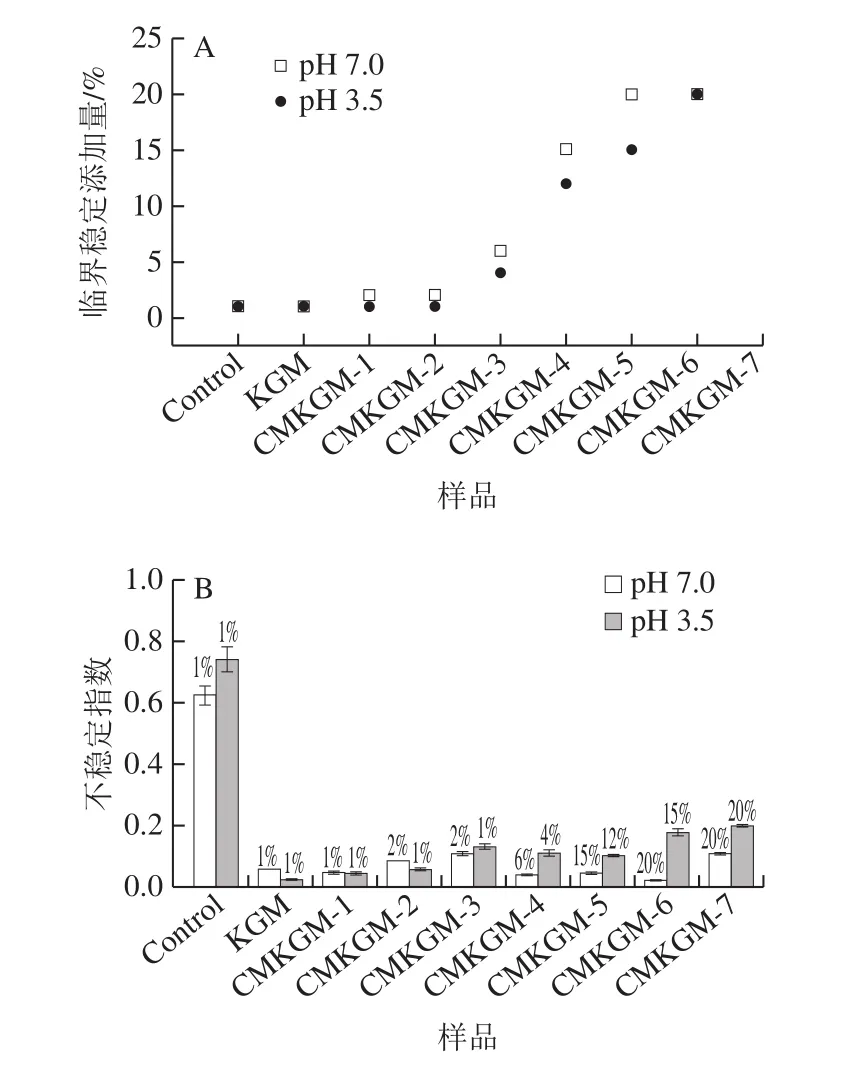
图3 中性和pH 3.5条件下不同CMKGM的临界稳定添加量(A)和相应PPD-多糖体系的不稳定指数(B)Fig.3 Critical stabilization concentrations (A) of KGM and different CMKGM samples for 1% PPDs and instability index (B) of systems at neutral and acidic conditions
2.3 PPD-CMKGM静电复合物的Zeta电位分析
PPD-多糖静电复合物的稳定性在很大程度上取决于分子之间的引力和斥力。Zeta电位可以反映颗粒之间静电相互作用的强弱。如图4所示,在中性条件下复合物的Zeta电位为负值,在酸性条件下为正值,且绝对值较小。加入KGM后,由于KGM为中性多糖,对Zeta电位影响较小。在中性条件下,加入相同质量分数的CMKGM后,复合物Zeta电位绝对值随取代度增加而增加。这是因为取代度越高,CMKGM所带负电荷量越高。在酸性条件下,加入相同质量分数的CMKGM后,Zeta电位由正变负,且绝对值随取代度的增加而增加。这是因为CMKGM吸附到豌豆蛋白表面形成静电复合物。此外,从图4A和图4B对比分析可以看到,无论在中性还是酸性条件下,对于同一种CMKGM,复合物Zeta电位的绝对值随CMKGM质量分数的增加而增大。总之,CMKGM的取代度越高,质量分数越大,复合物的Zeta电位绝对值越大。在中性条件下,豌豆蛋白和CMKGM都带负电,2 种生物高分子会发生热力学不相容,不利于体系稳定;同时豌豆蛋白上的局部正电荷可能与CMKGM发生静电吸附形成少量静电复合物,促进体系稳定。在酸性条件下,带正电的豌豆蛋白与带负电的CMKGM发生静电吸附形成大量静电复合物,复合物颗粒之间的静电斥力和空间位阻有利于体系稳定。
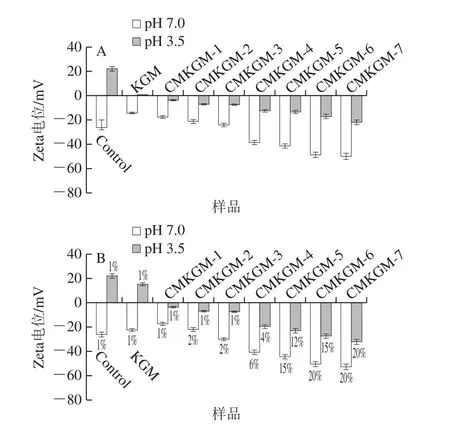
图4 中性和pH 3.5条件下当多糖质量分数为1%(A)和临界稳定添加量(B)时添加KGM和不同CMKGM的1% PPD的Zeta电位Fig.4 Zeta potential of 1% PPD stabilized by KGM or different CMKGM samples at a concentration of 1% (A) and at crititical stabilization concentration (B) under neutral and acidic conditions
2.4 PPD-CMKGM静电复合物的粒径分析
根据斯托克斯定律,较小的粒径和较高的连续相黏度有利于减缓颗粒的沉降速度,从而有助于提高分散液的物理稳定性[30]。在中性条件下,在PPD中加入质量分数1%的CMKGM后,粒径表现出不同程度的增加(图5A)。其原因主要从以下两方面考虑:第一,豌豆蛋白和CMKGM的热力学不相容促使蛋白发生聚集;第二,CMKGM通过与豌豆蛋白上的局部正电荷发生静电吸附包覆于表面。在酸性条件下,在PPD中加入质量分数1%的CMKGM后,粒径也有不同程度的增加,而且相比于取代度较低的样品,取代度较高的样品导致粒径增加较少。一方面,这是因为取代度越高的样品带电量大,与蛋白之间的吸附更为紧密;另一方面,高取代度样品的分子质量本身也小于低取代度样品(表1)。此外,在中性和酸性条件下,对于同种CMKGM,加入的多糖质量分数越大,复合物的粒径越大(图5B),这是因为CMKGM质量分数的增加使蛋白表面吸附的多糖数量增多,甚至可能发生多层吸附。
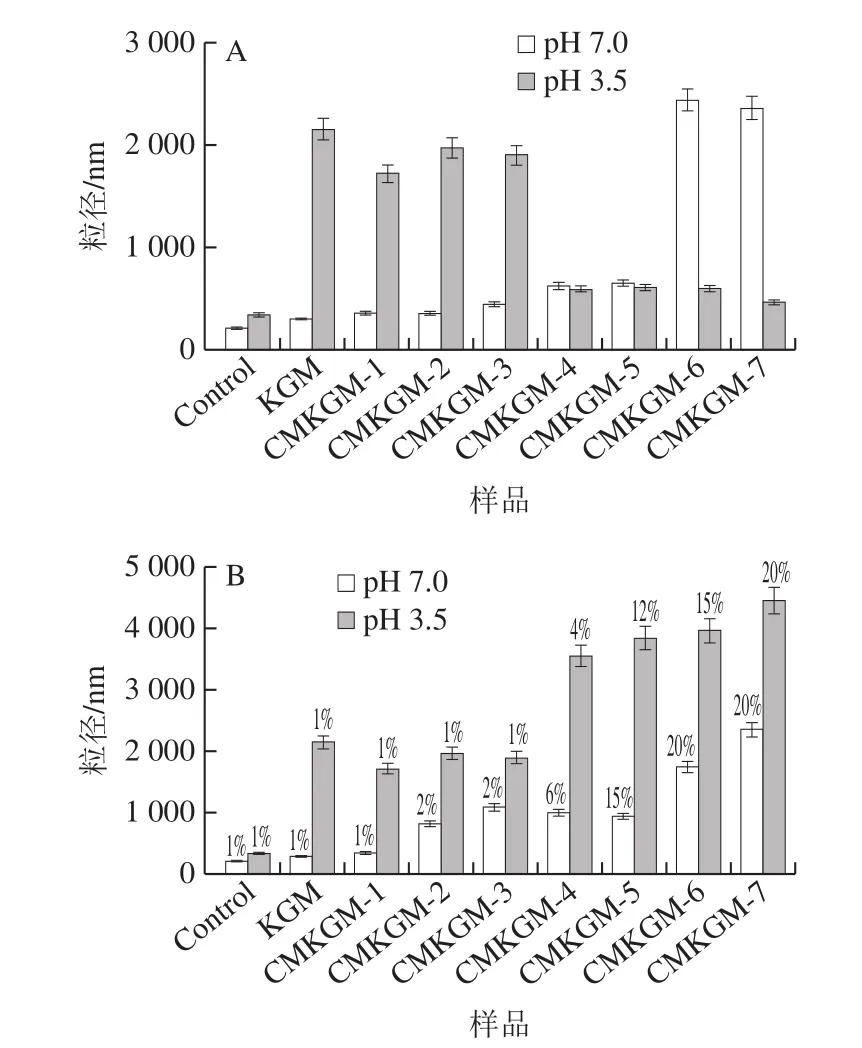
图5 中性和pH 3.5条件下当多糖质量分数为1%(A)和临界稳定添加量(B)时添加KGM和不同CMKGM的1% PPD的粒径Fig.5 Particle size of 1% PPD stabilized by KGM or different CMKGM samples at a concentration of 1% (A) and at crititical stabilization concentration (B) under neutral and acidic conditions
2.5 PPD-CMKGM体系的表观黏度分析
当多糖添加量为1%和临界稳定添加量时,PPD-多糖体系的表观黏度如图6所示。对比分析图6A1和A2可以看出,无论是中性还是酸性条件下,由于CMKGM分子质量随取代度升高而降低,加入相同质量分数1%的CMKGM,PPD体系的黏度随CMKGM取代度的增大而减小,其中CMKGM-2和CMKGM-3在50 s-1的剪切速率下的黏度处在0.1~2 Pa·s之间,这对于饮料来说黏稠性较为合适。对于同种多糖样品,在相同条件下,体系在酸性条件下(pH 3.5)的黏度均低于中性条件。这是因为CMKGM作为聚阴离子多糖,分子链上的部分—COO-基团在酸性条件下被质子化,使分子链内的静电斥力减小,分子构象更为紧凑,使体系的黏度降低;同时,由于带负电的多糖分子可与带正电的豌豆蛋白发生静电吸附,故相比于中性条件,在酸性条件下起增黏效果的CMKGM分子数量减少,也导致体系黏度的降低。
当增大CMKGM的质量分数使体系在中性(图6B1)和酸性(图6B2)条件下达到物理稳定时,也发现类似的现象,即添加相同质量分数的同种多糖时,在酸性条件下体系的黏度仍小于相应的中性条件。这进一步表明,在酸性条件下使体系达到物理稳定所需的增黏作用小于中性条件。CMKGM在酸性体系中的稳定作用在于吸附的CMKGM与蛋白质形成静电复合物增加了颗粒之间的静电斥力和空间位阻,同时未吸附的CMKGM可增加连续相的黏度,这与CMC在蛋白分散液酸性体系中的稳定作用相类似[17-18]。在不同取代度和不同分子质量的CMKGM样品中,CMKGM-2和CMKGM-3在较小的添加量下即可使PPD体系在酸性和中性条件下都能达到较好的稳定效果,而且黏度较KGM有所下降,可以改善KGM作为稳定剂的浓稠口感,对于饮料生产具有更好的适用性。
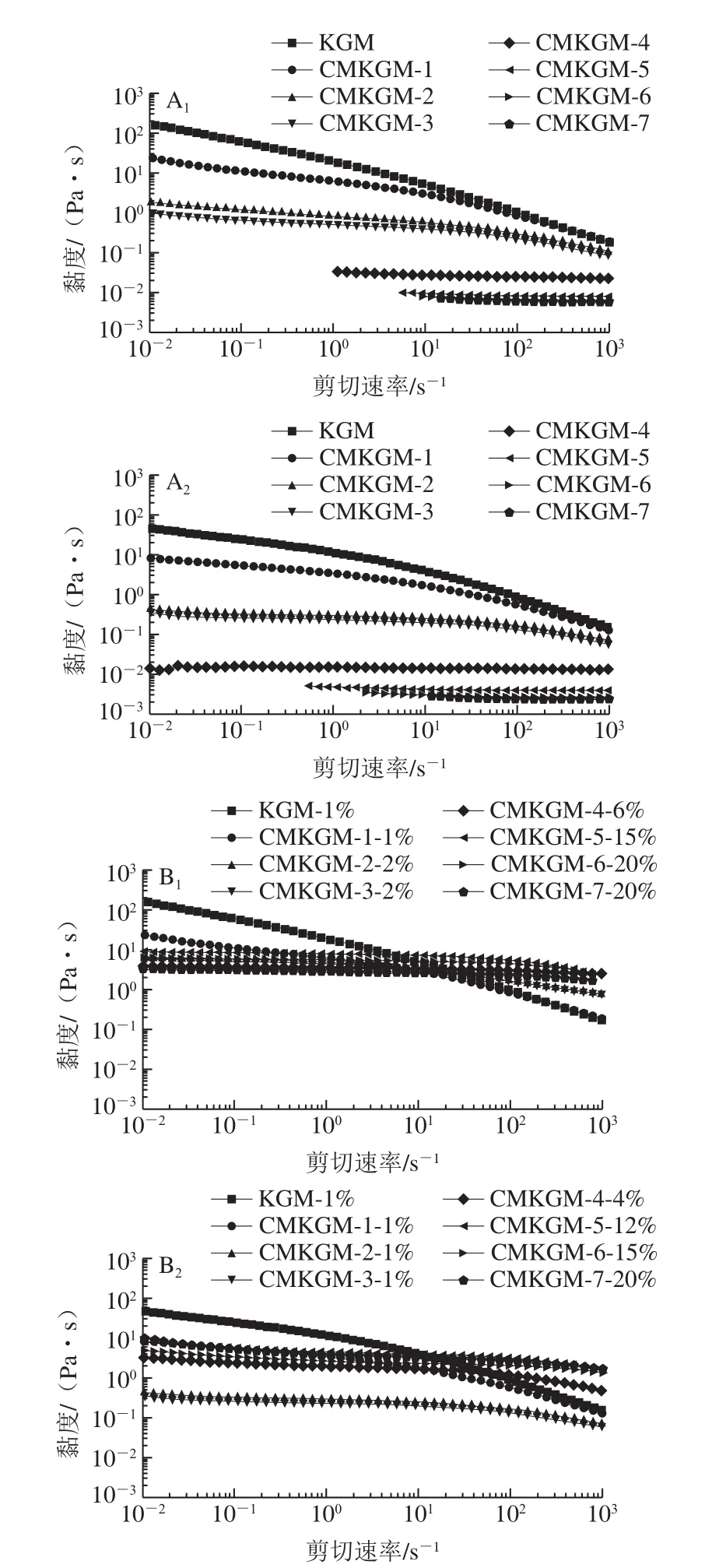
图6 当多糖质量分数分别为1%(A)和临界稳定添加量(B)时添加KGM和不同CMKGM的1%PPD在中性和pH 3.5的表观黏度Fig.6 Apparent viscosity of 1% PPD stabilized by KGM or different CMKGM samples at a concentration of 1% (A) and critical stabilization concentration (B) under neutral and acidic conditions
3 结 论
比较具有不同取代度和分子质量的CMKGM对中性和酸性PPD体系物理稳定性的影响。尽管高分子质量和高取代度稳定剂通常均有利于PPD体系稳定而低分子质量和低取代度均不利于体系稳定,但在CMKGM的分子质量和取代度同时变化的情况下,CMKGM分子质量的降低和取代度的增加对PPD的稳定有复杂的影响。随着取代度的增加,在分子质量逐渐降低的情况下,达到PPD体系稳定所需的CMKGM的质量分数逐渐增大,CMKGM分子质量对体系稳定性的影响大于取代度。在所制备的7 个改性样品中(CMKGM-1~CMKGM-7,分子质量依次降低而取代度依次升高),高分子质量低取代度的CMKGM-1、CMKGM-2和CMKGM-3在小于质量分数2%条件下即可使中性和酸性PPD体系均能达到良好的物理稳定性,而低分子质量高取代度的CMKGM需在较高的质量分数条件下才能稳定PPD体系。静电排斥、空间位阻效应和连续相高黏度为CMKGM提高PPD稳定性的主要因素。中性条件下,由于CMKGM不发生吸附,其对连续相的增黏作用是体系稳定的主导因素,而在酸性条件下,CMKGM对连续相的增黏作用和CMKGM与豌豆蛋白形成静电复合物后产生的静电斥力和空间位阻作用共同促使了体系的稳定。

