超高效液相色谱(UHPLC)对大黄饮片炮制前后化学成分定性定量分析
赵金秀,贾 勇,安志英,刘 震,杨雲琢
(廊坊市中医医院 中药房,河北 廊坊 065000)
中药需经过炮制后方可入药,核心原理是通过改变药物内在物质基础从而改变药性。中药炮制需要遵循辩证了解药物本身特性,以便调剂和制剂采用不同的制药技术[1]。化学成分群调控的药物生物活性及变化规律,利用化学工艺对中药炮制保留有效成分,对疾病治疗具有重要作用。大黄为我国传统中药植物,味微苦,寒性,初始记载《本经》中具有通利水谷及平胃、下气的功效。因药理活性广泛而适用于内外科、儿科、妇科及骨伤科等各科室中,常以不同炮制品入药[2]。超高效液相色谱(UPLC)是一种全新的检测技术,通过利用小颗粒填料等全新的检测方法而被应用于多个领域的技术研究中,例如医学、药物、生化等,具有通量高、灵敏度高的特点[3,4]。文献表明,UPLC 技术应用于中药领域中对于知晓中药组成,降低中药分离困难具有重要帮助[5]。
1 实验部分
1.1 仪器
ODS(C18)液相色谱仪(中国上海天普分析仪器);超声清洗器(中国杭州萧山余祝超声波设备厂);FA1004C 电子分析天平(中国青岛聚创环保集团);傅立叶变换红外显微镜(FT-IRmicroscope);UV-1102型紫外-可见分光光度计(上海天美科学)。
1.2 药物与试剂
生品药材大黄购自北京同仁堂。按照《中国人民共和国药典》相关的炮制方法,分别制备熟大黄及大黄炭。生大黄购自西安盛兴,批号:111001,由中国药品生物制品鉴定。
1.3 方法
1.3.1 大黄饮片制备
1.3.1.1 熟大黄制备 生大黄与黄酒按照2∶1 比例进行均匀搅拌,经2h 的闷润干预后,置入预先制作的蒸制处理器中,24h 后,待大黄表面呈现黑褐色,眉部呈现黄色褐色时进行自然风干处理。
1.3.1.2 大黄炭制备 将生大黄置入220℃的热锅中进行炒干,待表层呈现黑褐色,内部呈现焦褐色时,添加少量清水,火灭后取出。
1.3.2 对照品溶液的制备 分别量取适量的生大黄、熟大黄和大黄炭,电子天平称量后,放入20mL的量瓶中,加入甲醇超声溶解液到20mL,所得的溶液为混合对照品溶液。
1.3.3 供试品溶液 按本实验提取方法[6],取生大黄、熟大黄和大黄炭粉末过60 目筛,称量1g,超声提取30min 后,冷却,采用甲醛弥补缺少的剂量,均匀摇晃后,质量称量,继续过滤,取得过滤液3mL后,放入20mL 的容器中,甲醇稀释后再次摇匀,临近使用时采用0.45μm 滤膜过滤使用。
1.3.4 色谱条件 选择AgilentZorbaxC18柱(4.6mm 150mm,5m)进行实验,C18柱的流动相、柱温度、洗脱流速等进行观察,色谱柱条件为温度28℃,流向甲醇-0.1% H3PO4水溶液,梯度洗脱,见表1。流速0.8mL·min-1,柱温 25℃,检测波长 280nm,20μL,时间92min。
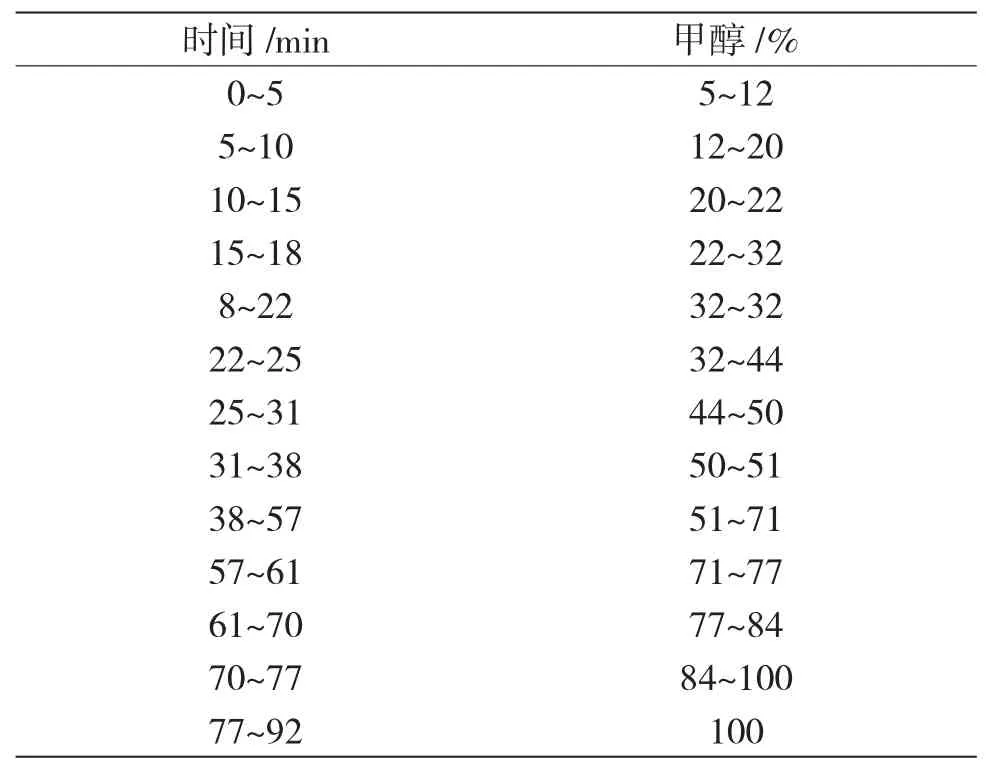
表1 样品甲醇的流动相洗脱梯度Tab.1 Mobile phase elution gradient of sample methanol
1.3.5 方法学考察 取供试品后,按照色谱条件连续实验5 次,计算RSD 值为0.08%表示精密度较好,按照上述色谱条件分别在 0、4、8、16、20、24h 记录峰值面积,RSD 为0.83%表示稳定性较好。取生大黄粉末,按照1.3.3 配制供试品溶液,按照色谱条件观察峰值面积,RSD 值为1.02%,此方法重复性较好。
2 结果及讨论
2.1 生大黄、熟大黄及大黄炭炮制前后UHPLC 指纹图比较
生大黄、熟大黄及大黄炭的UHPLC 指纹图存在差异,生大黄未经炮制蒽醌类含量较多,此外缩合鞣质含量增加,经炮制后的熟大黄及大黄炭中上述成分较少,但含有较多的没食子酸和蒽醌苷元物质。高效液相色谱发现在生大黄中蒽醌苷物质占比增加,其余炮制成品中蒽醌类占比较少,在检测的4 种蒽醌类成分中,大黄素8-O-β-D-葡萄糖苷占比较高,在熟大黄及大黄炭中几乎无表达。见图1。
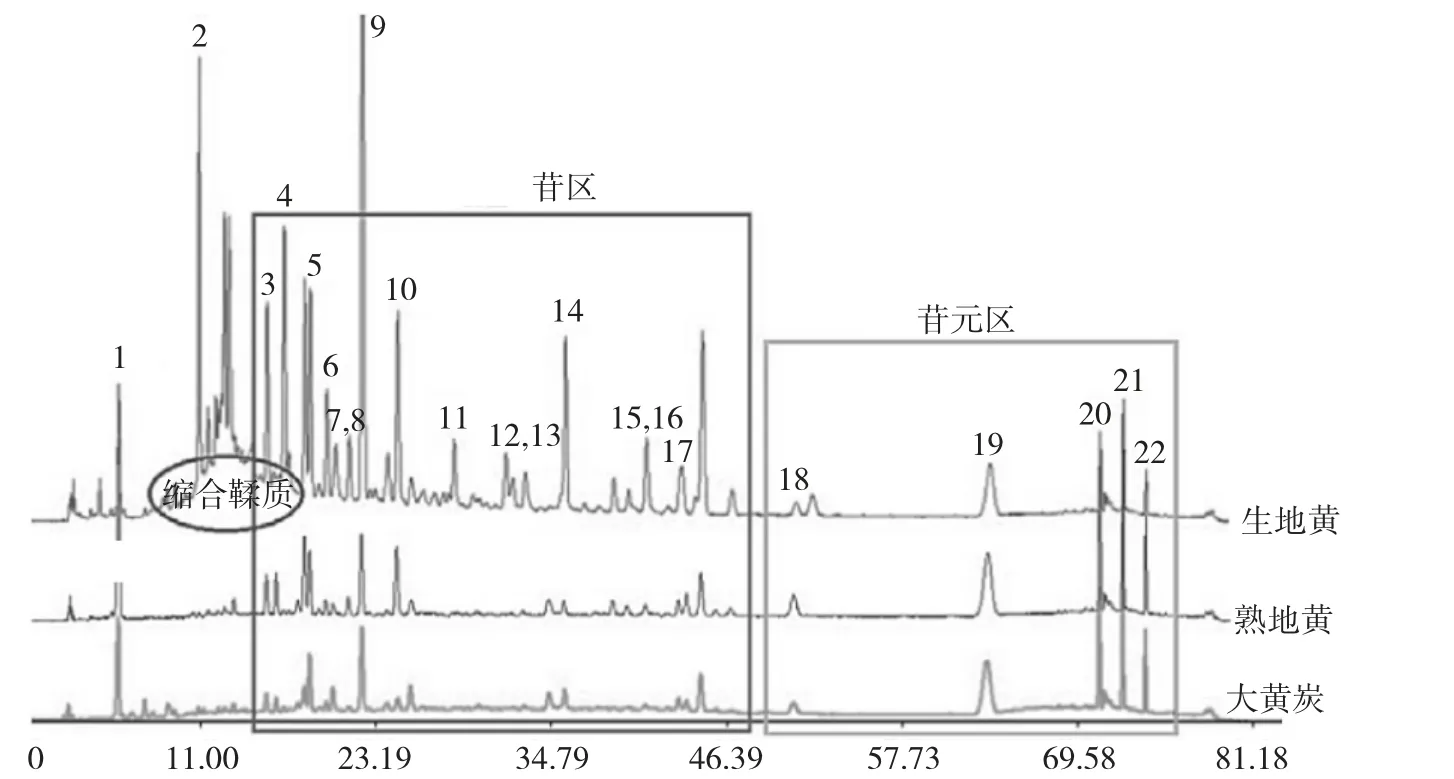
图1 生大黄、熟大黄及大黄炭UHPLC 指纹图谱分析(280nm)Fig.1 UHPLC fingerprint analysis of raw rhubarb, cooked rhubarb and rhubarb charcoal(280nm)
2.2 生大黄、熟大黄及大黄炭炮制前后游离蒽醌类成分变化
生大黄、熟大黄及大黄炭中,游离蒽醌类成分大黄酚占比最高的为生大黄,其余炮制成品中蒽醌类占比较少,而在熟大黄炮制中大黄酚表达较少,大黄素甲醚及芦荟大黄素增加,见图2。
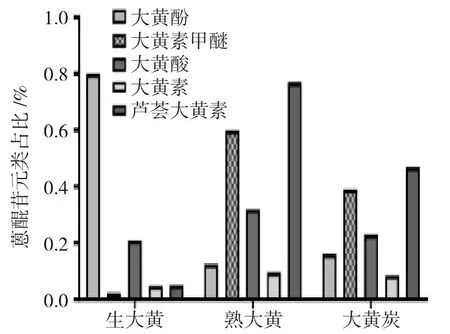
图2 生大黄、熟大黄及大黄炭蒽醌类成分比较Fig.2 Comparison of anthraquinone components in raw rhubarb, ripe rhubarb and rhubarb
在检测的4 种蒽醌类成分中,大黄素8-O-β-D-葡萄糖苷在生大黄中表达最高,在熟大黄及大黄炭中几乎无表达,大黄素8-O-β-D-葡萄糖苷在生大黄中经过炮制后蒽醌苷含量占比降低,说明熟大黄和大黄炭在物理加热升温等条件干预下,蒽醌苷类表达降低,或一部分蒽醌苷转化为苷元类物质,降低泻下作用,见图3。
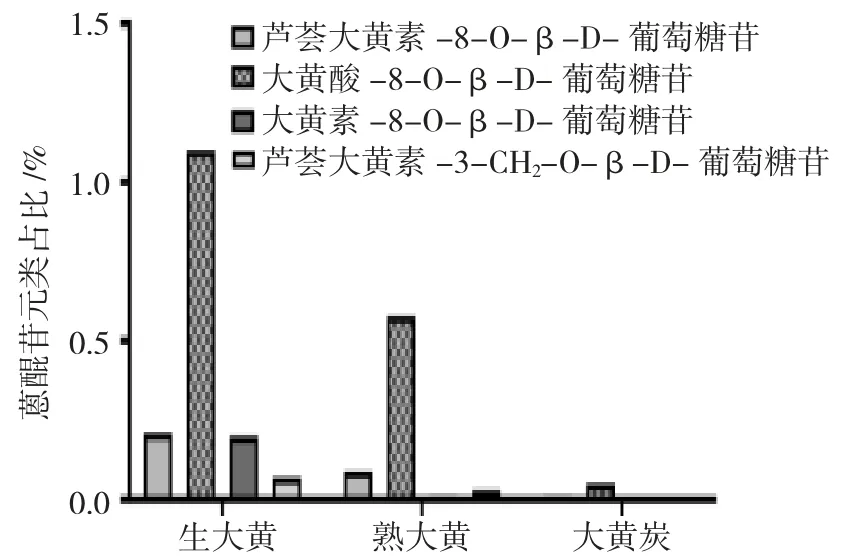
图3 生大黄、熟大黄及大黄炭蒽醌类成分比较Fig.3 Comparison of anthraquinone components in raw rhubarb, ripe rhubarb and rhubarb
2.3 生大黄、熟大黄及大黄炭炮制前后苯丁酮类成分的变化
生大黄、熟大黄及大黄炭炮制前后苯丁酮类成分存在改变,生大黄中4'-羟基苯基-2-丁酮-4'-O-β-D-(2"-O-没食子酰基-6"-O-(4'-羟基) 桂皮酰基)增多,熟大黄、大黄炭中降低,大黄炭中4'-羟基苯基-2-丁酮含量增加,剩余苯丁酮类成分含量降低。生大黄、熟大黄及大黄炭炮制前后苯丁酮类成分存在改变,生大黄中4'-羟基苯基-2-丁酮-4'-O-β-D-(2"-O-没食子酰基-6"-O-(4'-羟基)桂皮酰基增多,熟大黄、大黄炭中降低,大黄炭中4'-羟基苯基-2-丁酮含量增加,剩余苯丁酮类成分含量降低,炮制后苯丁酮苷、二苯乙烯苷在较强的炮制下,生物活性存在破坏,但是有与蒽醌类向苷元转化存在不同,蒽醌类化学产生苷元,而该类物质可分解成没食子酸,导致炮制后大黄中含量增加,见图4。
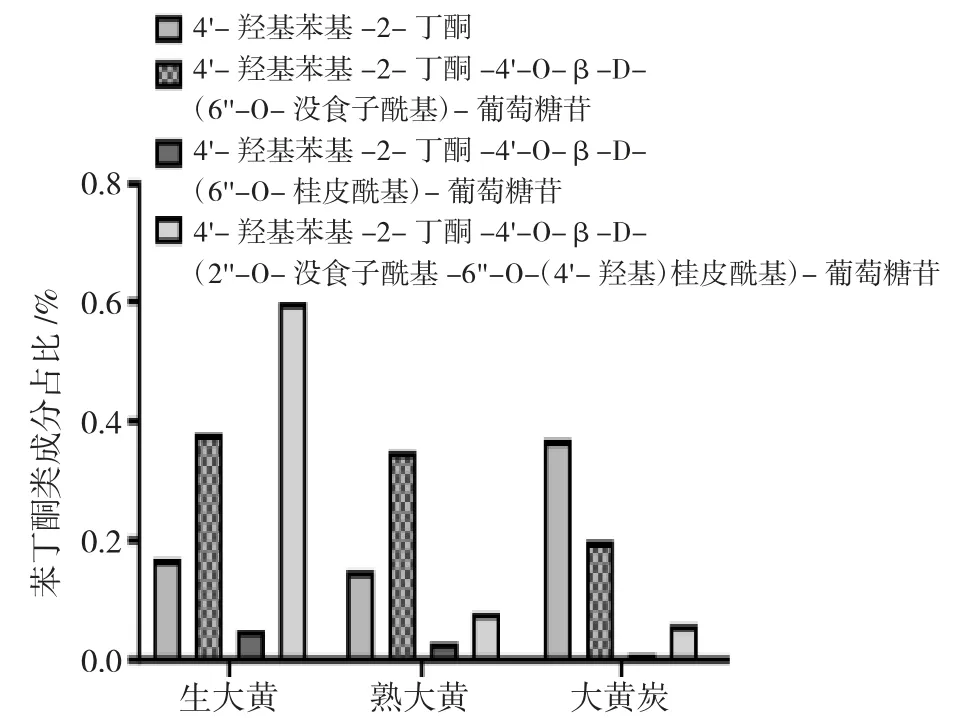
图4 生大黄、熟大黄及大黄炭炮制前后苯丁酮类成分的变化Fig.4 Change of phenytophenones in raw rhubarb, cooked rhubarb and rhubarb charcoal before and after processing
2.4 生大黄、熟大黄及大黄炭炮制前后二苯乙烯苷类成分的变化
生大黄、熟大黄及大黄炭炮制前后二苯乙烯苷类存在变化,二苯乙烯苷类成分均在熟大黄和大黄炭中含量降低。二苯乙烯苷是大黄中具有活性化合物,经炮制后变化规律与蒽醌苷变化存在差异,大黄中二苯乙烯苷含量占比较高,在熟大黄及大黄炭中能够具有增加没食子酸的作用,见图5。
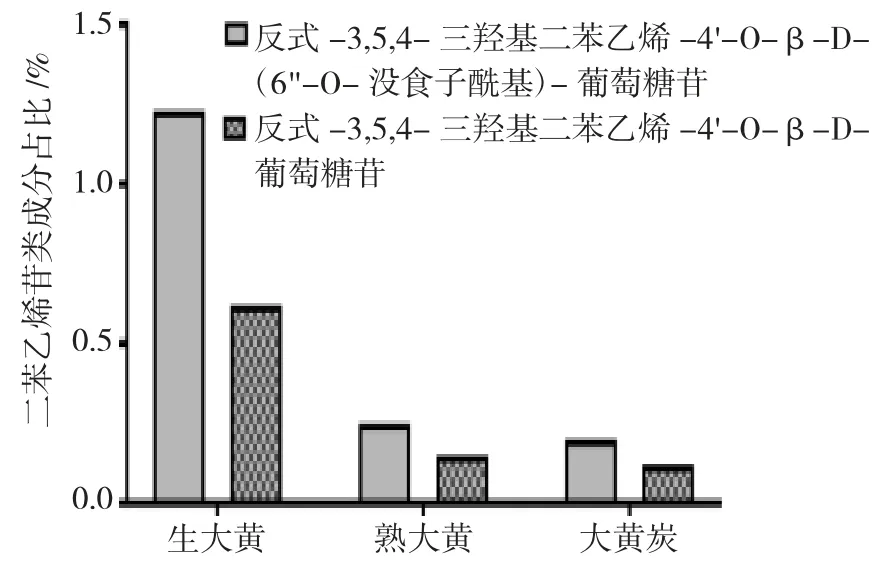
图5 生大黄、熟大黄及大黄炭炮制前后二苯乙烯苷类占比分析Fig.5 Analysis of the proportion of stilbene glycosides before and after processing of raw rhubarb, ripe rhubarb and rhubarb charcoal
2.5 生大黄、熟大黄及大黄炭炮制前后鞣质类成分占比分析
生大黄中鞣质类成分较多,熟大黄及大黄炭中鞣质类成分减少,没食子酸类物质增加,蒽醌苷类占比降低,说明,炮制后大黄泻下药效降低,而活血化瘀功效增加。鞣质类含量降低,与炮制过程遭到破坏而转化成没食子酸,进一步增加大黄炭中没食子酸含量占比有关。鞣质类生大黄未经炮制后并非具有收敛作用,而有显著的促进胃动力功效,而发挥促进胃动力主要物质为鞣质类炮制后而产生的没食子酸。而炮制后的熟大黄及大黄炭中没食子酸降低,这解释了长时间服用泻下药物大黄后导致便秘产生的原因,见图6。
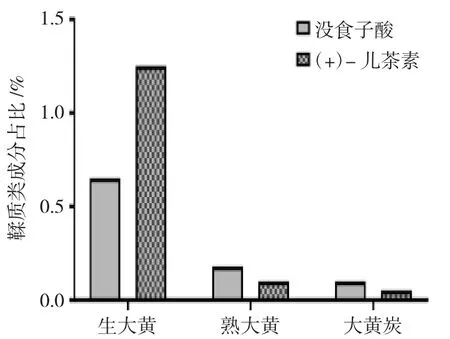
图6 生大黄、熟大黄及大黄炭炮制前后鞣质类成分Fig.6 Tannin composition of raw rhubarb, cooked rhubarb and rhubarb charcoal before and after processing
3 讨论
大黄饮片炮制加工需要遵循中医药理基础并在了解大黄饮片自身的理化特性的基础上开展加工处理,按照临床用药需求进行针对性的调剂和制剂[6,7]。蒽醌类成分是大黄主要效应成分,占比5%左右,以大黄酸、大黄素、芦荟大黄素、大黄酚和大黄素甲醚等为主。采用UHPLC 检测,样品以甲醇直接超声提取后检测蒽醌苷类成分,生大黄、熟大黄及大黄炭中蒽醌苷类成分含量均不断降低,表示在蒸制等过程中蒽醌类成分遭到破坏,向苷元转化,没食子酸占比升高[8,9]。UHPLC 指纹图显示:与生大黄相比,熟大黄及大黄炭中蒽醌苷类含量变化与大黄苦寒药效存在一定行,生大黄中蒽醌苷类占比升高,而在熟大黄及大黄炭中降低,而苯丁酮苷、二苯乙烯苷与蒽醌类占比变化存在相似性。揭示了大黄炮制前后质量的变化,具有较好的实践意义[10,11]。本研究具有一定的局限性,实验方法简单,后期本课题组会加强和其他相关研究单位合作,增加样本量,细化实验内容,为中药饮片炮制前后化学成分分析提供实验依据。
4 结论
结合传统及现代大黄药理苦寒性分为生大黄、熟大黄、大黄炭,通过UHPLC 观察化学成分变化,发现在生大黄、熟大黄、大黄炭顺序中缩合鞣质、蒽醌苷、苯丁酮苷类含量逐渐降低,没食子酸、蒽醌苷元类变化与之紧密相关,说明药理活性与化学成分变化存在一定的关联性。

