氢化可的松在石墨烯修饰电极上的电化学行为及测定*
郭红卫,马苑红,谭雪玲,钟 楠,余煜燊,李 岚
(嘉应学院化学与环境学院, 广东 梅州 514015)
石墨烯(GR)是一种由碳原子以sp2杂化组成,具有正六边形蜂巢状结构的二维纳米材料。此外,石墨烯具有比碳纳米管和金刚石更为优良的导电性能,且具有更高的比表面积和更发达的孔构造,可降低电解质离子在电极孔中的传递阻力[1]。在常温下石墨烯的电阻率极低,电子转移速率极快,电化学稳定性好,因此可用来制造导电速率更快、比表面积更大和活性位点更多的新型电极。
氢化可的松(Hydrocortisone,HC)是一短效的糖皮质激素[2],在临床上主要用于治疗肾上腺功能不全所引起的各种疾病[3]。这类激素对轻度脸部皮炎等病症也有明显的效果,但大量使用此激素会产生一定的抗药性,甚至会导致骨质疏松以及对中枢神经系统造成神经毒害等多种不良反应[4-6],因此,此类激素在化妆品中属于禁用成分,而寻找高效、便捷的检测手段具有学术与现实价值。现有的氢化可的松类激素的分析技术主要有荧光光谱法[7]、化学发光法[8]、高效液相色谱法以及色谱联用法[9-11]、生物和免疫传感器法等[12]。荧光光谱法检测限低,但选择性比较差;HPLC法与色谱联用法都具有高选择性等特点,但所需的仪器都较为昂贵;化学发光法和众多的生物和免疫传感器对氢化可的松具有灵敏的信号响应,然而这些方法会产生一定程度的化学污染,且与其他甾类化合物的交叉反应往往会在分析测量中引入一定误差。电化学方法在一定程度上可以弥补以上测量方法的不足[13]。现今,电化学法分类众多,应用广泛,同时具有较低的检出限,样品制备过程简单。并且在电极表面修饰不同类型的覆盖层如石墨烯[14]、碳纳米管等超高导电材料后可以有效提升方法的灵敏度[15],因此衍生出各类简便快捷的电化学分析检测手段。
我们通过电沉积石墨烯构建一种新型石墨烯修饰玻碳电极,结合差分脉冲伏安技术检测氢化可的松含量并探究其电化学行为,为检测药物、化妆品和食品中微量氢化可的松提供了一种新的方法。
1 实 验
1.1 主要仪器与试剂
所有伏安测量均在CHI660E电化学工作站(上海辰华仪器有限公司)上进行,使用经典的三电极体系。石墨烯修饰玻碳电极作为工作电极,铂片作为对电极,Hg/Hg2Cl2电极(饱和KCl)作为参比电极。
石墨烯,南京先丰纳米材料科技有限公司;氢化可的松(化学对照品),阿拉丁试剂(上海)有限公司。其余试剂均为分析纯试剂,所有实验用水为超纯水。
1.2 实验方法
1.2.1 GR/GCE电极的制备
每次使用前,将玻碳电极(直径为3 mm)在抛光布上依次用Al2O3颗粒(1.0、0.3 μm)抛光,超纯水冲洗后,按序在乙醇和超纯水中超声荡洗1 min,氮气吹干备用。
将石墨烯超声分散在水中,制得浓度为1 mg/mL的分散液,然后把10 mL 0.1 mol/L KCl溶液和1 mL 1 mg/mL石墨烯加入电解池,将GCE电极置于电解液中,并在+1.7 V恒电位电解30 min,即制得GR/GCE。
1.2.2 伏安测试
所有伏安测试均在0.1 mol/L磷酸盐缓冲溶液中进行,实验前向溶液通入氮气15 min除氧。
2 结果与讨论
2.1 GR/GCE电极对氢化可的松的电化学响应性能分析
用伏安法研究了GCE和GR/GCE电极对100 μg/mL氢化可的松的电化学响应性能(pH=6.0磷酸盐缓冲体系)。如图1所示,在GCE上氢化可的松仅有一很小的还原峰,其峰电位约为-1.49 V。然而在GR/GCE上,氢化可的松峰电流明显增加且峰电位正移(峰电位为-1.46 V),GR/GCE较GCE对氢化可的松电催化活性更好,这是由于石墨烯修饰电极具有更大的比表面积、更多的活性位点及更好的导电性能,有利于提高GR/GCE电极的检测灵敏度。

图1 氢化可的松在GCE(1)与GR/GCE(2)电极上的 循环伏安曲线Fig.1 Cyclic voltammetry curves of hydrocortisone at GCE (1) and GR/GCE (2)
2.2 氢化可的松在GR/GCE电极上的电化学反应机理
为了探讨氢化可的松在GR/GCE电极上的反应作用机理,在pH=6.0磷酸盐缓冲体系下,在扫速15~100 mV/s范围内,利用LSV考察了100 μg/mL氢化可的松的还原峰电流Ipc和扫速ν之间的关系。结果见图2,随着扫速ν的增加,氢化可的松的Ipc渐渐增大,Ipc~v0.5呈现线性关系,其线性回归方程为:Ipc=420.74v0.5-23.72(R=0.9978),说明了电极过程主要受扩散过程控制。

图2 不同扫速下氢化可的松的线性扫描伏安图Fig.2 Linear sweep voltammetry of hydrocortisone at different sweep rates
我们同时分析了氢化可的松的还原峰电位Epc和扫速ν之间的关系。由图2可知:随着扫速ν的增加,峰电位负移,这说明氢化可的松的电化学还原反应是不可逆的。根据Laviron理论[16],其电极电位和扫速符合以下方程:
其中,Epc为该反应的阴极峰电位,E0为该反应的标准电位,α为电化学传递系数,n为电子转移数,R为气体常数,T为绝对温度,F为法拉第常数。

图3 氢化可的松的峰电位Epc与logν线性关系拟合图Fig.3 The linear relationship between the peak potential Epc of hydrocortisone and logν
图3为还原峰电位Epc与扫速的对数logν的线性关系拟合图,可以观察到Epc~logν呈现线性关系,其线性回归方程为:Epc=-0.069 logv-1.58(R=0.996)。由图3的斜率,可得αn=0.86,不可逆过程的α通常为0.5,则n=1.72≈2,即电子转移数为2。因此,氢化可的松在GR/GCE电极表面的还原过程是两电子反应,机理如下:
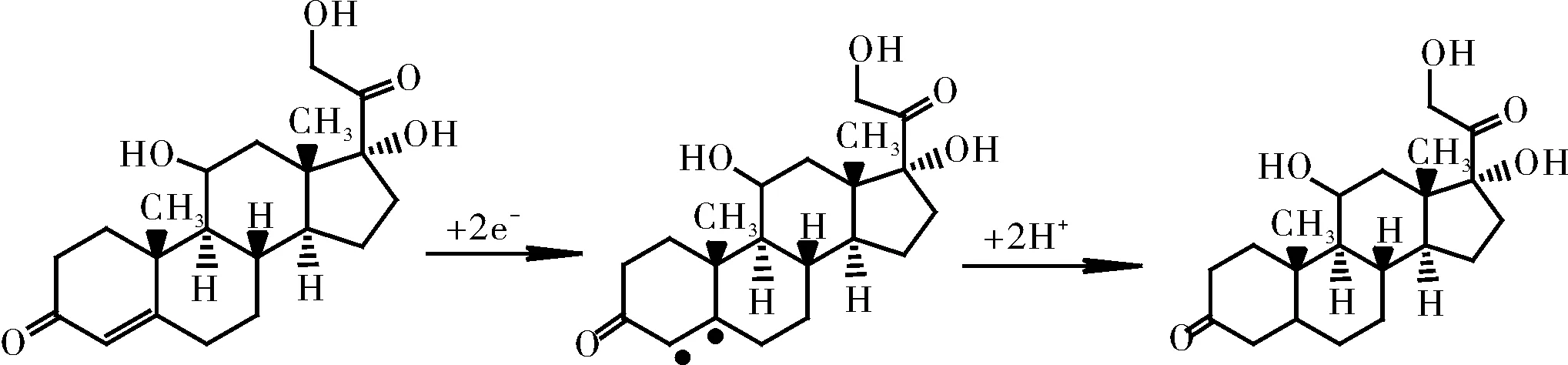
2.3 定量分析条件的优化
2.3.1 溶液酸度对测定的影响
根据反应机理,H+参与氢化可的松在GR/GCE电极上的还原过程,pH会影响检测结果的灵敏度,实验探究了不同pH对氢化可的松在GR/GCE电极上还原峰电流Ipc的影响。结果如图4,随着pH的增大,氢化可的松的Ipc先逐渐增大后明显减小,在pH=6.0时,Ipc达到最大值,因此,选取pH=6.0的磷酸盐缓冲溶液作为支持电解质。
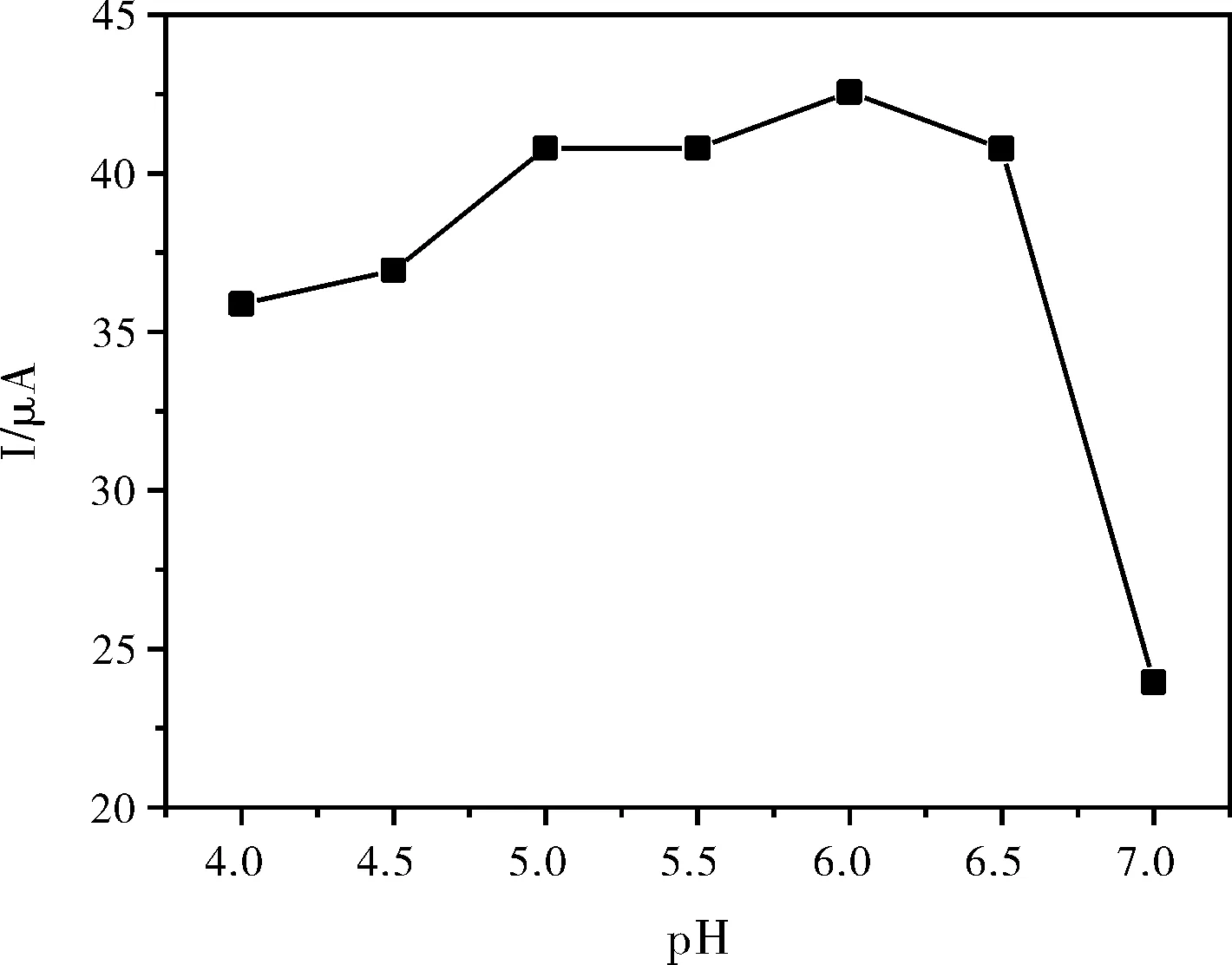
图4 pH对氢化可的松峰电流的影响Fig.4 Effect of pH on peak current of hydrocortisone
2.3.2 富集电位和富集时间对测定的影响
富集电位和富集时间是差分脉冲伏安法中的重要参数,对测定的准确性和灵敏度有显著影响。因此本实验考察了这些参数对氢化可的松在GR/GCE电极上伏安响应的影响,以提高电极的电分析性能。
图5显示了不同富集电位对100 μg/mL氢化可的松还原峰电流Ipc的影响。随着富集电位变得更正,氢化可的松的Ipc逐渐增大,当富集电位在0.3~0.6 V范围时,Ipc较大且稳定,故选择富集电位为0.4 V。
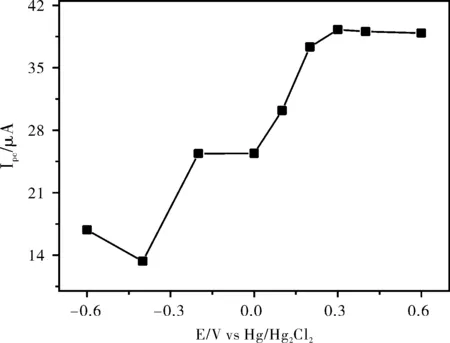
图5 富集电位对氢化可的松峰电流的影响Fig.5 Effect of enrichment voltage on peak current of hydrocortisone
图6显示了不同富集时间对100 μg/mL氢化可的松还原峰电流Ipc的影响,随着富集时间的增大,氢化可的松的Ipc逐渐增大,当富集时间在90~150 s范围时,Ipc较大且稳定。故选择富集时间为120 s。
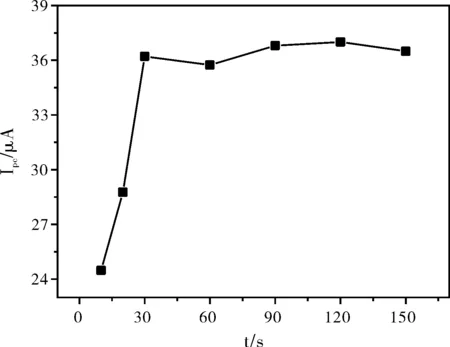
图6 富集时间对氢化可的松峰电流的影响Fig.6 Effect of enrichment time on peak current of hydrocortisone
2.4 标准工作曲线及方法检出限
在优化条件下,采用GR/GCE电极运用DPV技术(脉冲振幅0.05 V、脉冲宽度0.05 s和电压增幅0.003 V)检测氢化可的松,图7(a)为不同浓度氢化可的松在GR/GCE电极上的DPV 响应曲线。从图中可看出,随着氢化可的松浓度的增加,氢化可的松的还原峰电流Ipc逐渐增大。对其还原峰电流Ipc与logC之间的关系进行拟合,结果如图7(b),氢化可的松浓度在 0.2~100 μg/mL范围内, logC与Ipc具有线性关系。其线性回归方程为Ipc=13.8 logC+9.6 (R=0.996)。方法检出限为 0.02 μg/mL(S/N=3)。
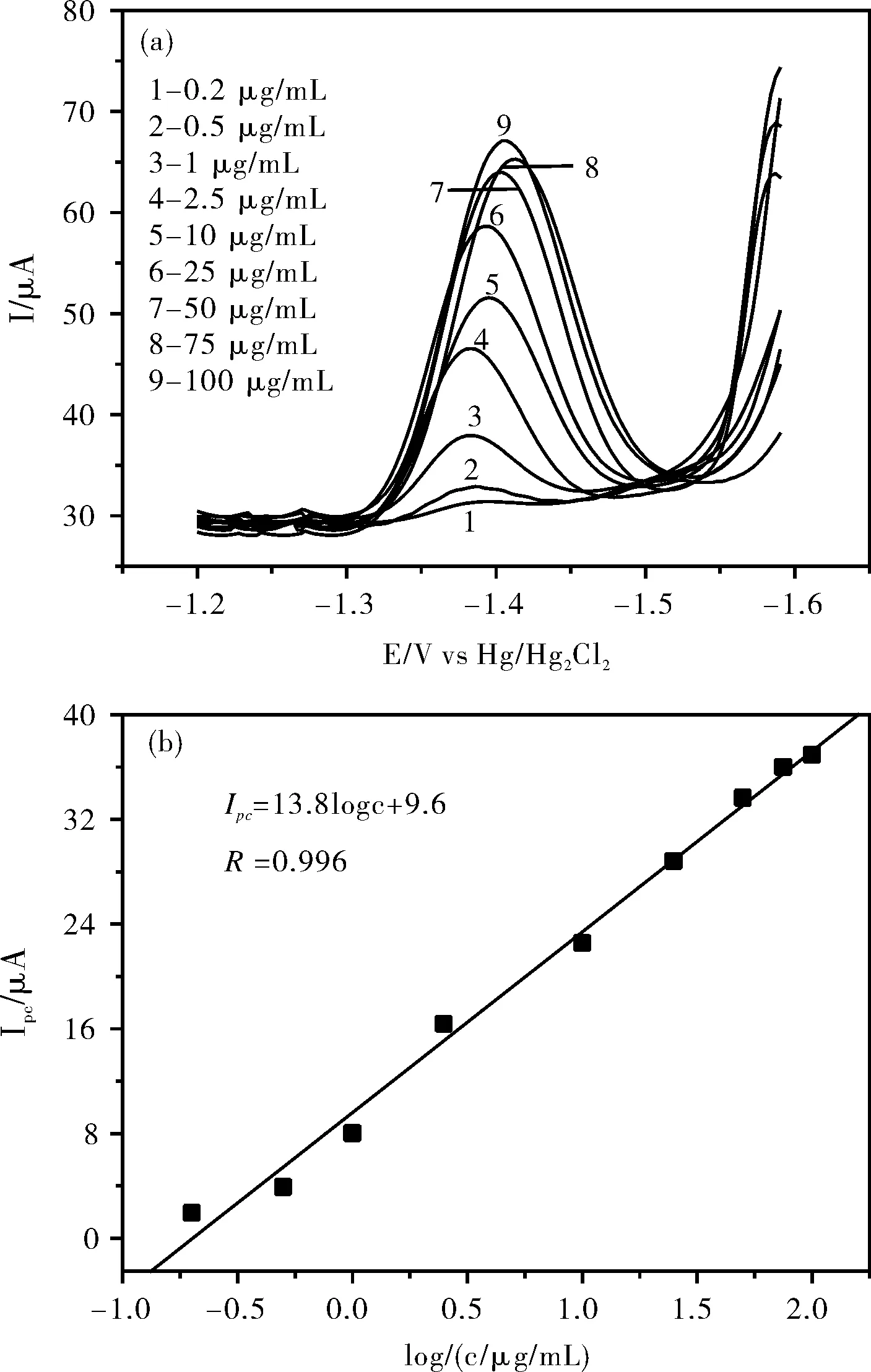
图7 (a) 不同浓度氢化可的松的DPV图; (b) 峰电流与logC的关系Fig.7 (a) DPV curves of hydrocortisone at different concentrations; (b) Relationship between peak current and log C
2.5 测定的精密度及抗干扰实验
用同一只GR/GCE电极对1 μg/mL氢化可的松溶液进行 12次测定,相对标准偏差为5%。结果表明该GR/GCE电极有较好的重现性。

2.6 回收率实验
在回收率实验中,在25 mL容量瓶中移入2 mL氢化可的松注射液,并用无水乙醇定容。利用DPV技术测其含量,并在样品中加入3个浓度水平的氢化可的松标准溶液,进行加标回收率测试,结果见表1。样品平均回收率为93~105%,说明GR/GCE电极用于实际样品中氢化可的松的检测有较好的准确度。

表1 氢化可的松回收率的测定(n=3)Table 1 Determination of recovery rate of hydrocortisone
3 结 论
通过电沉积石墨烯成功制备了石墨烯修饰电极,并研究了氢化可的松在修饰电极上的电化学行为。结果表明,GR/GCE对氢化可的松显示出较好的电催化活性,电极过程是一个两电子还原反应,并且电极反应速度受扩散控制。该电极用于氢化可的松的定量分析,显示出较低的检出限,较好的精密度和准确度及抗干扰能力。

