超声引导下竖脊肌平面阻滞对比腰方肌阻滞对腹腔镜胃癌根治术患者阿片类药物的节俭作用
杜翠英 王倩楠 张加强 崔明珠 索晓燕 许俊 朱永锋
河南大学人民医院河南省人民医院麻醉与围术期医学科,郑州 450000
胃癌是我国常见的恶性肿瘤之一,目前治疗胃癌的有效手段首选外科治疗[1],术后疼痛不仅给患者带来痛苦,急性术后疼痛还会增加应激反应,改变内分泌和免疫反应,导致慢性疼痛的发生[2]。有效镇痛对于促进患者的快速康复具有一定意义。竖脊肌平面阻滞(ESPB)和腰方肌阻滞(QLB)是两种新型的腹部手术术后镇痛方法[3-4]。ESPB是一种具有代表性的间接超声引导胸椎旁神经阻滞(TPVB)方法。大多数间接TPVBs包括ESPB均为筋膜间隙阻滞。在ESPB中,胸腰段肌筋膜平面之间注射大量液体可能会影响多肋间神经。多项临床研究表明,ESPB可为胸腹部提供良好的镇痛效果[5]。ESPB作为一种简单有效的阻滞技术,可应用于心胸外科手术。因此,它或许可以作为包括硬膜外阻滞或TPVB在内的标准治疗方案的替代。QLB是从腹横肌平面阻滞(TAPB)的基础上提出的围绕腰方肌进行的一种新的躯干阻滞方法。研究表明,QLB中局部麻醉药扩散的位置距离神经轴突和交感干更近,使其不仅有TAPB的效果,且在镇痛持续时间和对内脏痛的削弱方面有更明显的优势[6]。因此,QLB在腹部手术、下肢手术及腹部术后慢性疼痛的缓解等方面效果较好。然而,目前关于ESPB与QLB在腹部手术中应用的镇痛效果还缺乏前瞻性对照研究,两种方法用于胃癌根治术患者及术后镇痛效果有无区别和优劣,还没有研究进行比较。本研究拟对比超声引导下ESPB与QLB对行腹腔镜胃癌根治术患者阿片类药物的节俭作用,为腹腔镜胃癌手术麻醉及围术期镇痛提供依据。
1 资料与方法
1.1 一般资料 本研究已获得河南省人民医院伦理委员会批准,批件号(2019)伦审第(83)号,并与患者签署知情同意书。本研究的入选标准为2020年5月1日至2021年2月28日于河南省人民医院手术室择期全麻下行腹腔镜胃癌根治术的患者共60例;年龄40~65岁,性别不限;美国麻醉医师协会(ASA)分级Ⅰ~Ⅱ级;体质量指数(BMI)18~30 kg/m²。入选标准:经过常规术前准备的非急诊住院患者;自愿参加本研究并签署知情同意书。排除标准:(1)穿刺部位皮肤感染;(2)急性酒精中毒或乙醇依赖者;(3)对阿片类药物成瘾及耐药性者;(4)筛选前14 d内长期使用(连续使用≥3 d)阿片类镇痛药物或其他中枢神经系统抑制剂者;(5)筛选前3个月内患有心肌梗死或其他严重心脏疾病;(6)患者凝血功能不全或术中出现大出血等意外情况。使用随机数字表法对患者进行分组,将患者随机分为两组:E组(30例)和Q组(30例)。
1.2 方法
1.2.1 神经阻滞操作 术前1 h将患者接入手术室,常规连接心电图(ECG)、血压(BP)、脉搏血氧饱和度(SpO2)和脑电双频指数(BIS),开放外周静脉通路,局麻下行桡动脉穿刺并置管监测有创动脉血压,超声引导下右颈内静脉穿刺置管。E组和Q组患者分别行超声引导下ESPB和QLB,均注入0.33%的罗哌卡因(批号:NBBY,英国AstraZeneca公司)25 ml。超声引导下ESPB操作[7]:取俯卧位,常规消毒铺巾,采用Edge型超声(美国Sonosite公司),应用高频线阵探头横向扫描下识别斜方肌、竖脊肌、T7横突的结构,采用横向入路,平面内的方法,穿刺达到竖脊肌深面接触T7横突,回抽无血液、脑脊液后将药物注入竖脊肌和横突之间,注入后可见横突和竖脊肌被局麻药分离;对侧以同样的方法完成操作。超声引导下QLB操作[8]:取仰卧位,常规消毒铺巾,使用低频凸阵探头,将超声探头矢状位放在髂嵴和肋缘之间,辨认出腹外斜肌、腹内斜肌、腹横肌,然后超声探头向后移动直至确认腰方肌,前向后平面内进针,突破胸腰筋膜到达QLB1(外侧路QLB,即腰方肌前外侧与腹横筋膜的交界处)位置,回抽无血后将药物注入腰方肌和胸腰筋膜之间,注药后可见药物沿腰方肌和胸腰筋膜之间扩散,对侧以同样的方法完成操作。所有操作由同一位10年以上工作经验的麻醉副主任医师完成,由另一位麻醉主治医师完成术后镇痛效果的评价、处理和随访。
1.2.2 麻醉与术后镇痛 手术采用标准的全身麻醉,麻醉诱导:静脉推注咪达唑仑0.04 mg/kg,舒芬太尼0.5μg/kg,罗库溴铵0.8 mg/kg,依托咪酯0.3 mg/kg,待肌松满意后行气管插管机械通气。采用容量控制通气模式,潮气量6~8ml/kg,呼吸频率(RR)12次/min,吸呼比为1∶2。维持呼气末二氧化碳分压(PETCO2)35~45 mmHg(1 mmHg=0.133 kPa),维持气道峰压<25 cmH2O(1 cmH2O=0.098 kPa)。术中维持采用全凭静脉麻醉维持脑电双频指数(BIS)值40~60。微量泵入丙泊酚4~8 mg·kg-1·h-1,持续静脉输注瑞芬太尼0.25~2.00μg·kg-1·min-1,间断追加罗库溴铵0.3 mg/kg。维持BIS值40~60,将平均动脉血压和心率维持在基础值的20%以内。术毕接静脉自控镇痛泵,实施患者静脉自控镇痛(PCIA),PCIA泵配方为2μg/kg的舒芬太尼注射液(批号:91A11111,人福医药公司,中国)用生理盐水稀释至100 ml,参数设置为背景输注量2 ml/h,追加剂量为2 ml,锁定时间为15 min。当患者视觉模拟评分法(VAS)评分到达4分以上,需要静脉给予舒芬太尼0.05μg/kg进行急救镇痛。
1.3 观察指标 记录手术时间、麻醉时间及术中瑞芬太尼总用量;神经阻滞操作时间;记录两组患者术后2h、4h、6 h、24 h、48 h的VAS评分及各时间点舒芬太尼累计用量及PCIA的按压次数;记录恢复室急救镇痛的患者人数;记录术后不良反应的患者人数,常见的不良反应如恶心、呕吐、头晕、呼吸抑制(RR<6次/min或吸纯氧5 L/min时SpO2<92%)、皮肤瘙痒等。
1.4 统计分析 采用SPSS 22.0统计分析软件。所有的统计检验均采用双侧检验,P值小于或等于0.05将被认为所检验的差异有统计意义。符合正态分布的计量资料将采用均数±标准差(±s)进行统计描述,组间比较采用两独立样本t检验。计数资料采用频数(构成比)进行统计描述,组间比较采用χ2检验。
2 结 果
2.1 两组患者一般临床资料的比较 所有患者均完成神经阻滞,两组患者一般资料及术中资料各指标比较差异均无统计学意义(均P>0.05),具体见表1。
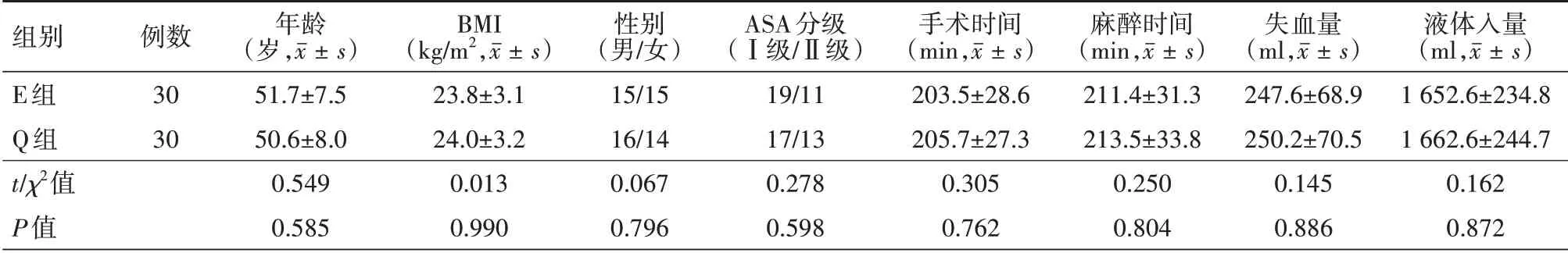
表1 两组行腹腔镜胃癌根治术患者一般临床资料的比较
2.2 两组神经阻滞操作时间和术中瑞芬太尼用量的比较 与E组比较,Q组患者神经阻滞操作时间较短(P<0.05),术中瑞芬太尼用量较少(P<0.05),具体见表2。
表2 两组行腹腔镜胃癌根治术患者神经阻滞操作时间和术中瑞芬太尼用量的比较(±s)
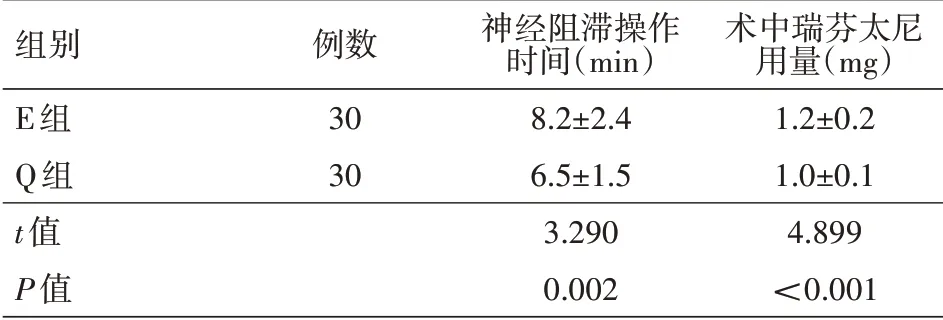
表2 两组行腹腔镜胃癌根治术患者神经阻滞操作时间和术中瑞芬太尼用量的比较(±s)
注:E组和Q组分别行超声引导下竖脊肌平面阻滞(ESPB)和腰方肌阻滞(QLB)
组别E组Q组t值P值例数30 30神经阻滞操作时间(min)8.2±2.4 6.5±1.5 3.290 0.002术中瑞芬太尼用量(mg)1.2±0.2 1.0±0.1 4.899<0.001
2.3 两组患者术后疼痛程度指标的比较 两组患者术后各时间点VAS评分、PCIA的按压次数、舒芬太尼用量差异均无统计学意义(均P>0.05),具体见表3。
表3 两组行腹腔镜胃癌根治术患者术后各时间点VAS评分、PCIA按压次数及舒芬太尼用量的比较(±s)
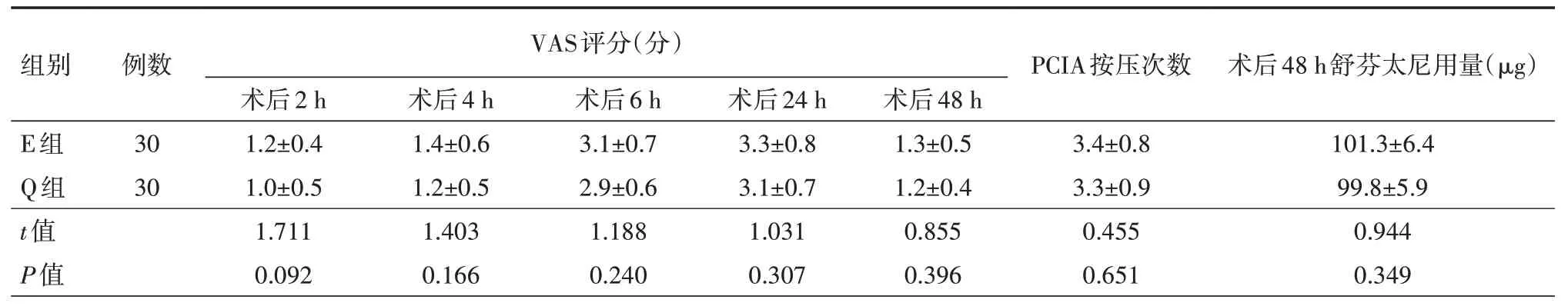
表3 两组行腹腔镜胃癌根治术患者术后各时间点VAS评分、PCIA按压次数及舒芬太尼用量的比较(±s)
注:E组和Q组分别行超声引导下竖脊肌平面阻滞(ESPB)和腰方肌阻滞(QLB);VAS为视觉模拟评分法,PCIA为患者静脉自控镇痛
?
2.4 两组患者术后不良反应发生率的比较 两组患者术后恶心、呕吐发生率差异均无统计学意义(均P>0.05)。两组患者均未发生不良事件,包括皮肤瘙痒、呼吸抑制、气胸、皮下血肿、双侧阻滞、胸腔内置管和局麻药中毒。具体见表4。
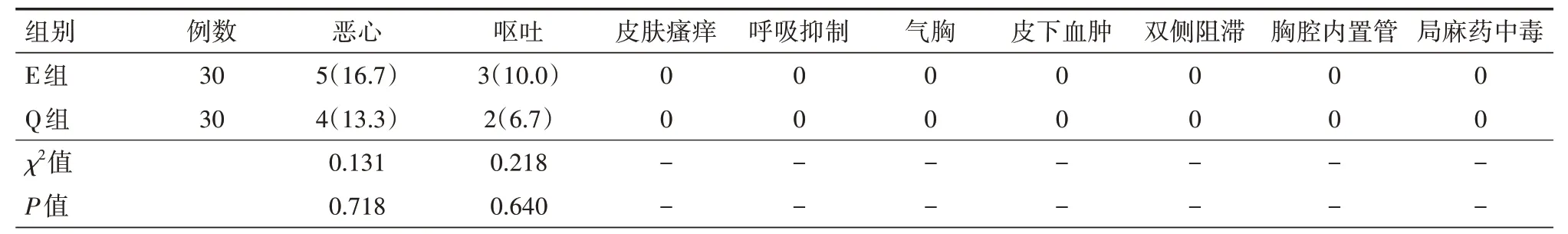
表4 两组行腹腔镜胃癌根治术患者术后不良反应发生率的比较[例(%)]
3 讨 论
对于腹部手术来说,目前最常用的术后镇痛方式是PCIA。PCIA具有起效快、无镇痛盲区、血药浓度相对稳定、可通过冲击剂量及时控制爆发痛,具有用药个体化、患者满意高等优点,但阿片类药物较易引起恶心呕吐、呼吸抑制、皮肤瘙痒等不良反应,不仅会加重切口疼痛,也可使缝合口裂开,甚至影响住院时间。因此优化镇痛模式是患者加速康复的先决条件之一。
目前临床上多建议采用围术期多模式镇痛方案,即采用不同机制的镇痛技术和镇痛药物,从各方面阻止疼痛刺激的传入,从而阻断疼痛信号的传递,改善患者术后康复[9-10]。既往术后多采用硬膜外镇痛,但硬膜外麻醉操作繁琐、并发症较多,目前在临床术后镇痛中的应用逐渐减少[11]。
近年来随着超声技术和区域神经阻滞技术的发展,麻醉医生一直在探索用于腹部手术镇痛更加安全有效的区域神经阻滞方法。竖脊肌平面阻滞是近几年出现的一种新型超声引导神经阻滞技术,为近几年研究的热点。2016年首次被Forero等[3]用于癌痛的治疗。临床研究证实ESPB可为腹部手术提供良好的镇痛效果。乔迎帅等[12]指出,ESPB可有效缓解腹腔镜胃癌根治术患者术后疼痛并降低炎性反应;Chin等[13]证实了胸7平面ESPB在腹腔镜胃减容手术后具有良好镇痛效果。前腹壁由T7~T12胸神经以及L1腰神经支配。Adhikary等[14]对3具新鲜尸体在T5椎体水平进行了单次注射ESPB,他们发现,20 ml放射造影剂混合物可以在2~5个层面产生硬膜外和神经孔间的扩散,其临床效果类似于胸椎旁阻滞,而在5~9个层面产生肋间扩散。我们总结出在T7水平的竖脊肌平面阻滞药液扩散范围可以涵盖T7~L1节段水平。因此,T7水平ESPB可以满足上腹部手术范围的镇痛。QLB由Blanco在2007年首次提出,随后QLB被广泛认识并进一步研究和改进[4]。QLB在腹部手术中的应用广泛,可为上腹部和下腹部手术提供良好的术后镇痛。Murouchi等[15]证实QLB阻滞范围可达T7~L4,并能阻断体表痛与内脏痛,为腹腔镜手术提供满意的镇痛效果。
超声引导下ESPB与QLB对行腹腔镜胃癌根治术患者术后的镇痛均有效果,但还没有研究对比两种方法的差别,本研究对两种方法进行对比研究,为腹腔镜胃癌手术麻醉及术后镇痛提供依据。本研究发现,Q组比E组神经阻滞操作时间更短。QLB和ESPB均为筋膜间隙阻滞,QLB患者平卧位就可以操作,超声下腰方肌和胸腰筋膜均易于辨认,操作简单;但是双侧ESPB需要患者侧卧位或俯卧位,并且超声先找到第12肋,顺肋骨找到第12胸椎横突,再向头端移动确认第7胸椎横突,操作步骤多,所以操作时间较QLB时间长。
本研究发现,与E组比较Q组患者术中瑞芬太尼用量较少,可能与两种阻滞的作用原理有关。目前多数学者倾向于认为,ESPB中局麻药通过竖脊肌平面间隙向头尾及中线方向扩散,通过肋横突孔及肋横突韧带间的裂隙进入椎旁间隙,并向脊神经背支及腹支起源处扩散[16-17]。基于这种机制,局麻药的扩散范围受个体解剖学特征影响很大,导致镇痛效果差异较大,另外这种间隙的渗漏需要较长的时间才能通过间隙达到阻滞效果;QLB通过把局麻药注射至腰方肌和胸腰筋膜之间,药物通过胸腰筋膜间扩散,阻滞椎旁同侧感觉运动、交感神经,起到镇痛作用,这种通过筋膜间隙的扩散就会更快起效。而两种阻滞均起效后阻滞效果相当,这与我们的实验结果一致,本研究两组患者术后各时间点VAS评分、PCIA按压次数及舒芬太尼用量差异均无统计学意义。
在我们的研究中,术前单次ESPB或QLB联合PCIA均可在术后静息48 h给患者提供良好的术后镇痛。需要考虑的一个问题是两组患者都存在个别术后VAS评分较其他患者升高,本研究的平均手术时间为4 h,神经阻滞主要负责术中镇痛,因此,这就解释了本研究中在术后6 h出现了有患者VAS评分增高的情况。本研究两组的恶心、呕吐等的发生率都不高,说明这两种方式在减少术后镇痛泵中舒芬太尼用量的同时使得阿片类药物引起的术后恶心、呕吐等的并发症也相应较少。
本研究的局限在于:第一,样本量小,未设立空白对照;第二,由于手术时间的原因,在手术前进行神经阻滞操作的时间有限,在神经阻滞操作后有些患者未能进行阻滞平面的测量,导致神经阻滞后是否达到有效的镇痛效果缺乏准确性;第三,本研究的主要研究指标存在一定程度的主观性;第四,多模式镇痛,不同阻滞之间的镇痛差异可能被其他互补的镇痛作用掩盖;最后,更多相关结果指标如住院时间、术后护理升级、医学经济学或更长时间的镇痛效果未被研究。以上不足之处我们会在以后的研究不断改进。
综上所述,超声引导下QLB较超声引导下ESPB的术中镇痛效果更佳,有明显的阿片类药物节俭作用。
利益冲突:作者已申明文章无相关利益冲突。

