18F-FDG PET/CT代谢参数预测老年食管鳞癌预后的价值
邱云亮,郭喆,孙晋,丁重阳*
1.南京森林警察学院刑事科学技术系,江苏 南京 210022;2.南京医科大学第一附属医院核医学科,江苏 南京 210029;*通信作者 丁重阳 chongyangding@163.com
食管癌是一种由食管鳞状上皮或腺上皮异常增生所致的恶性病变,是消化系统常见的恶性肿瘤,病理类型以食管鳞癌常见[1]。食管鳞癌好发于中老年人,随着我国人口老龄化,老年食管鳞癌患者逐渐增多,已成为老年人群常见的恶性肿瘤之一,也严重威胁着老年患者的生活质量和生存时间[2]。多项研究表明,治疗前18F-FDG PET/CT在判断肺癌、淋巴瘤等多种恶性肿瘤的预后方面具有重要临床价值[3-5],但该技术预测老年食管鳞癌患者的预后研究较少。本研究拟分析老年食管鳞癌患者治疗前18F-FDG PET/CT显像资料,探讨18F-FDG PET/CT代谢参数预测老年食管鳞癌患者预后的价值。
1 资料与方法
1.1 研究对象 回顾性选取2008年3月—2019年6月南京医科大学第一附属医院收治的老年食管鳞癌患者73例,男56例,女17例,年龄65~88岁,中位年龄70岁。临床分期:I期6例,Ⅱ期20例,Ⅲ期35例,Ⅳ期12例。纳入标准:①年龄≥65岁;②病理明确诊断为食管鳞癌;③18F-FDG PET/CT检查前均未行放化疗等肿瘤相关治疗;④随访资料完整。排除标准:①食管癌复发;②重复癌。所有患者检查前均签署知情同意书,本研究符合《赫尔辛基宣言》的原则。
采用门诊随访和电话随访,研究终点为总生存期(overall survival,OS)。OS为疾病诊断之日起至患者死亡或随访截止至2020年5月1日。
1.2 仪器与方法 采用西门子Biograph 16 HR PET/CT扫描仪,患者检查前空腹6 h,控制血糖≤11.1 mmol/L;注射18F-FDG(放化纯>95%)3.70~5.55 MBq/kg后,患者静卧1 h,排空膀胱后行PET/CT扫描。先行CT扫描,扫描参数:管电压120 kV,管电流140 mA,层厚3.75 mm,准直1.5 mm;再行PET数据采集:采用三维模式采集6~7个床位,2~3 min/床位。应用CT数据进行衰减校正,迭代法重建获得图像。
1.3 图像分析 由2位核医学科副主任医师采用盲法独立阅片,结果不一致时由科室集体讨论决定。通过图像处理工作站,采用肿瘤代谢评估软件对PET和CT数据进行处理。沿肿瘤病灶便于勾画感兴趣区,采用相对阈值法,以最大标准化摄取值(maximum standardized uptake value,SUVmax)的40%作为阈值,由软件自动在横断位、矢状位及冠状位上对病灶进行容积分割,得出食管癌原发灶的SUVmax、全身肿瘤代谢体积(total metabolic tumor volume,MTVtot)和全身病灶糖酵解总量(whole-body total lesion glycolysis,TLGwb)。
1.4 统计学方法 采用SPSS 17.0软件,不符合正态分布的计量资料以M(Q1,Q3)表示;采用受试者工作特征(ROC)曲线获得食管癌原发灶SUVmax、MTVtot及TLGwb的最佳界值点,若曲线下面积(AUC)较小,则以中位数为界值点。生存分析采用Kaplan-Meier法进行单因素分析,各研究因素间的组间比较采用Log-rank检验,采用COX比例风险模型进行多因素分析。以P<0.05为差异有统计学意义。
2 结果
2.118F-FDG PET/CT 73例食管鳞癌18F-FDG PET/CT显像均表现为18F-FDG高摄取,原发灶SUVmax、MTVtot、TLGwb分别为16.65(10.96,20.83)、11.97(6.02,23.66)cm3、103.33(44.67,240.32),见图1、2。共29例患者接受食管癌根治术,其中3例术后接受单纯放疗,5例术后接受单纯化疗,4例术后接受放化疗,17例术后未行放化疗。44例不能行手术治疗患者接受放化疗。
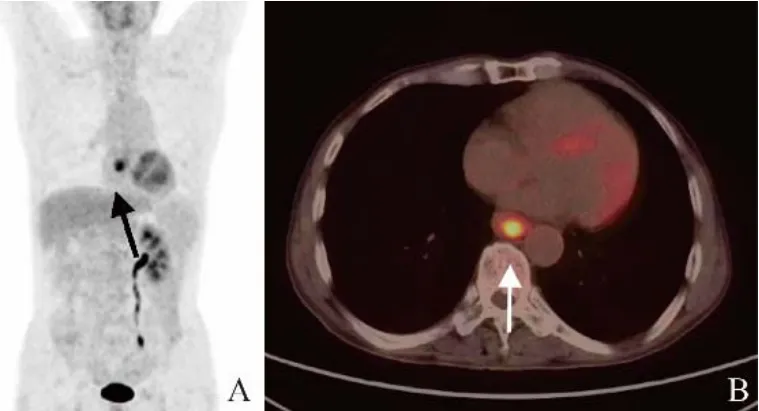
图1 男,67岁,食管鳞癌。A.18F-FDG PET/CT显像全身最大密度投影图示:食管中段18F-FDG代谢增高(箭),其余全身未见异常18F-FDG代谢增高灶;B.PET/CT横断层融合图像示:食管中段管壁增厚,管腔狭窄,18F-FDG摄取增高(箭),原发灶SUVmax、MTVtot、TLGwb分别为8.26、4.70 cm3、21.81;患者接受根治性手术切除,随访至2020年5月1日存活,OS 68个月

图2 男,76岁,食管鳞癌。A.18F-FDG PET/CT显像全身最大密度投影图示:全身多处18F-FDG代谢增高灶(箭);B.PET/CT横断层融合图像示:食管中段管壁增厚,管腔狭窄,18F-FDG摄取增高(箭);双肺多发转移,肝脏转移,多发骨转移;原发灶SUVmax、MTVtot、TLGwb分别为21.85、81.16 cm3、772.64;患者接受放化疗,疗效差,死亡,OS 4个月
2.2 ROC曲线判断SUVmax、MTVtot、TLGwb预测OS生存的最佳界值点 患者随访12~141个月,中位随访时间54个月,41例死亡。原发灶SUVmax、MTVtot、TLGwb预测患者OS的最佳界值点分别为12.56、9.28 cm3、150.98(表1、图3)。

表1 食管鳞癌原发灶SUVmax、MTVtot、TLGwb判断患者OS的ROC曲线分析
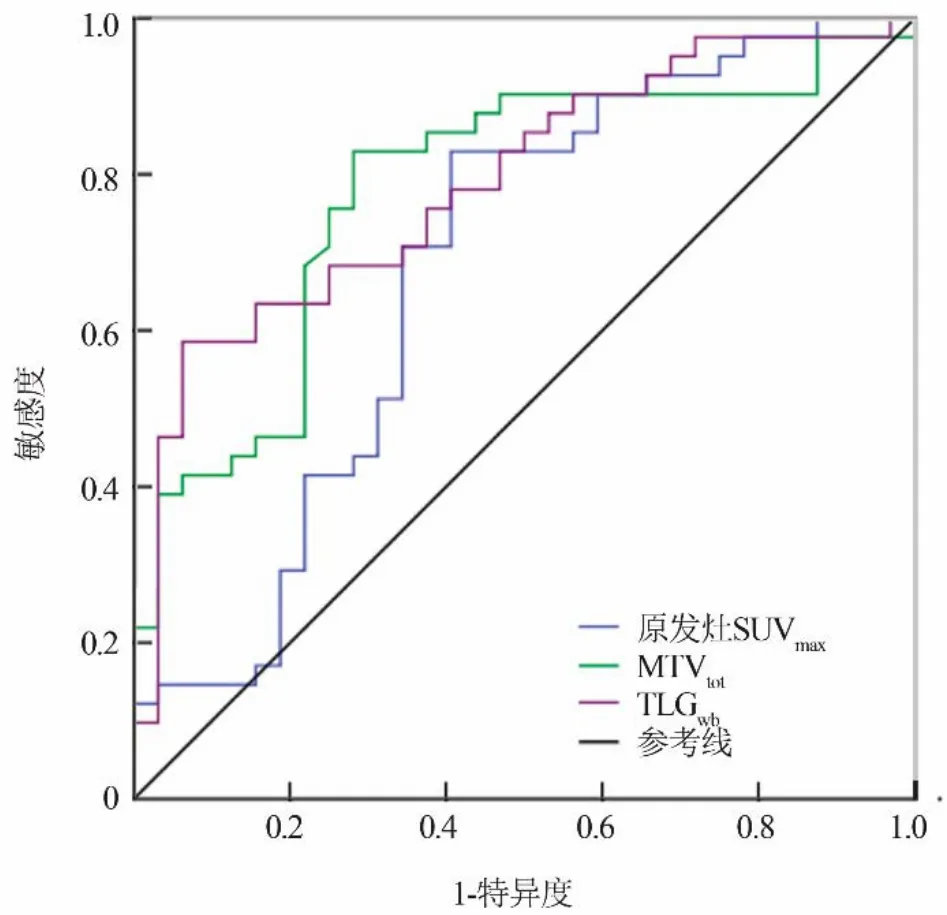
图3 食管鳞癌原发灶SUVmax、MTVtot、TLGwb的 ROC曲线
2.3 单因素及多因素分析 单因素生存分析结果显示:病理分化程度、N分期、M分期、TNM分期、原发灶SUVmax、MTVtot、TLGwb、手术是患者OS的影响因素(χ2=9.880、10.325、25.160、13.988、15.944、20.270、17.721、10.148,P<0.01),见图4~6;将单因素分析中具有统计学意义的相关因素进行COX多因素回归分析,结果显示:病理分化程度、M分期、MTVtot、TLGwb是影响老年食管鳞癌患者的独立预后因素(HR=4.459、4.679、2.806、2.391,P均<0.05),见表2、3。

图4 老年食管鳞癌患者原发灶SUVmax的总生存曲线
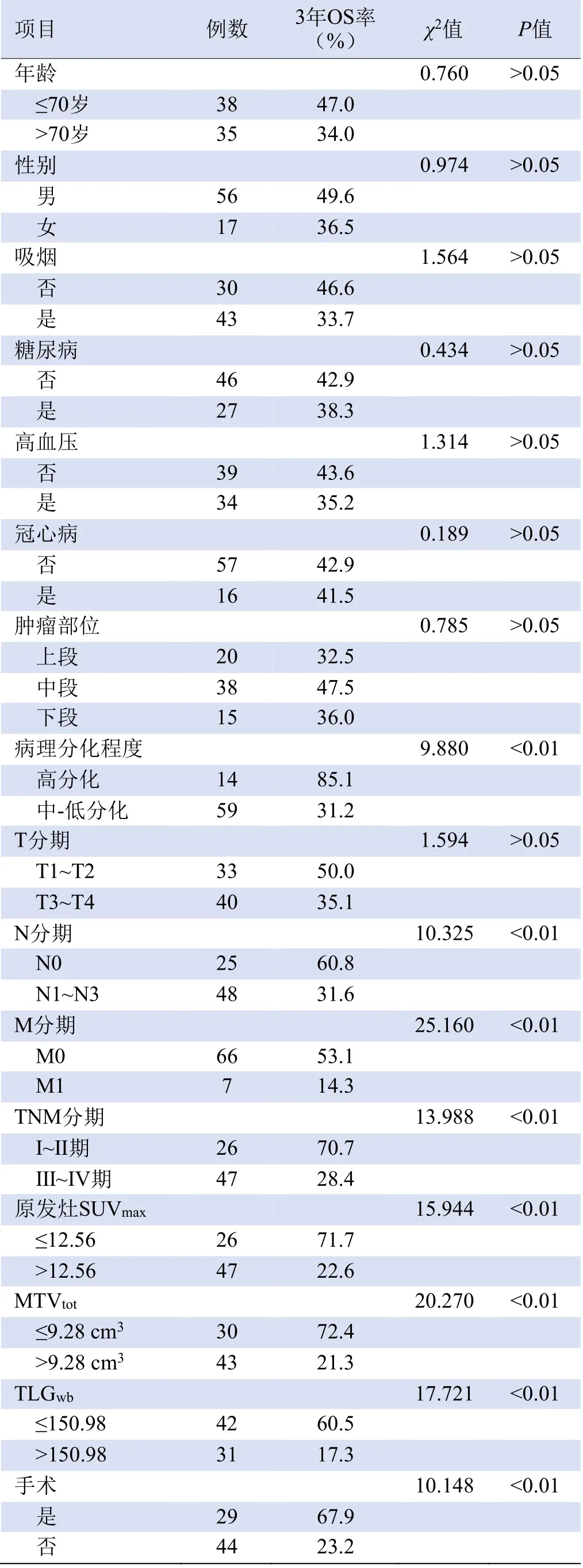
表2 73例老年食管鳞癌患者的单因素生存分析

表3 73例老年食管鳞癌患者的COX生存分析

图5 老年食管鳞癌患者原发灶MTVtot的总生存曲线

图6 老年食管鳞癌患者原发灶TLGwb的总生存曲线
3 讨论
老年患者生理功能减退,往往合并较多的并发症,且对手术及放化疗的耐受性较差,预后也较差。目前,对于老年食管鳞癌患者的预后评价指标尚缺乏统一标准,寻找具有较高价值的早期预后指标对临床制订治疗方案具有重要意义。SUVmax与恶性肿瘤预后的关系一直是研究热点,但其在食管癌预后中的价值目前尚存在争议。戴亮等[6]研究显示,食管癌原发灶SUVmax>6是预后不良的独立危险因素。而Takahashi等[7]研究表明,食管癌原发灶SUVmax不是影响患者预后的独立危险因素。
随着计算机技术及图形处理技术的发展,目前一些反映肿瘤负荷的代谢参数,如MTV、TLG,也逐步应用于临床。一项Meta分析[8]表明,食管癌原发灶SUVmax、MTV、TLG均是影响患者无病生存期及OS的独立危险因素,三者的预后评估能力无显著差异。Mantziari等[9]研究显示,MTV、TLG与患者的预后无关。丁重阳等[10]研究表明TLG是患者预后不良的危险因素,而原发灶SUVmax、SUVmean及MTV与预后无关。一项针对非小细胞肺癌的研究[11]表明,TLGwb>54.7是患者无进展生存时间的独立危险因素,MTVtot>9.5 cm3是患者OS不良的独立危险因素,而原发灶SUVmax、MTV、TLG均不是患者预后的独立影响因素。以上结论存在较多争议。目前,临床上大部分研究[8-12]主要是分析食管癌原发灶MTV和TLG的预后预测价值,较少分析MTVtot、TLGwb与预后的关系。
本研究重点分析了食管癌患者全身所有病灶MTVtot、TLGwb的预后价值,并未分析食管癌原发灶MTV和TLG的预后价值,主要是由于食管癌异质性较强,部分食管癌患者,尤其是恶性程度高的患者原发灶较小,但转移灶较多、较大。因此,食管癌原发灶的MTV并不能完全反映肿瘤的负荷,而MTVtot、TLGwb则是全身所有肿瘤病灶MTV、TLG的总和,更能反映患者全身肿瘤的负荷,也更能预测患者的预后。本研究结果显示,MTVtot>9.28 cm3、TLGwb>150.98是患者预后不良的独立危险因素,表明临床可根据治疗前18F-FDG PET/CT代谢参数(MTVtot、TLGwb)进行预后判断,MTVtot、TLGwb较高的患者预后较差,临床可对其进行较强强度的治疗;而MTVtot、TLGwb较低的患者预后相对较好,临床可适当调整治疗方案,减少放化疗所致的毒副作用,从而提高患者的生活质量,延长生存期。
本研究的局限性:首先,本研究不是前瞻性研究,患者资料的收集存在一定的偏倚,课题组将来有望设计前瞻性试验,进一步证实18F-FDG PET/CT预测老年食管鳞癌预后的价值;其次,本研究MTV的测量采取相对阈值法,可能会低估SUVmax较高患者的MTVtot及TLGwb值;最后,本研究样本量较少,且大部分患者为Ⅱ~Ⅲ期,I期和Ⅳ期患者相对较少,难以说明不同的临床分期是否会影响研究结果。将来有望收集更多的患者,减少临床因素的干扰,进一步证实18F-FDG PET/CT在老年食管鳞癌患者中的预测价值。
总之,老年食管鳞癌患者治疗前18F-FDG PET/CT显像所获得的MTVtot及TLGwb是影响患者预后的独立危险因素。MTVtot及TLGwb较高的患者预后相对较差,临床可参考治疗前18F-FDG PET/CT显像代谢,制订个体化治疗方案,从而达到精准治疗。

