碳源类型对地下水硝酸盐污染生物修复效果的影响研究李 飞,刘佩贵,单圣苏,李松达,唐石振
(合肥工业大学土木与水利工程学院,安徽 合肥 230009)
地下水作为一种宝贵的资源,在供水中发挥着不可替代的作用,但受农业施肥、地表水氨氮污染等问题的影响,部分地下水水源地面临硝酸盐氮超标的威胁,地下水硝酸盐污染日趋严重[1,2]。这也推动了地下水硝酸盐污染修复技术或方法方面的研究,众多学者从物理、化学和生物等角度分别提出了相应的原位或异位修复技术,其中,生物反硝化处理技术依靠自然界中的微生物反硝化作用使NO3—N最终转化为N2,具有运行成本低、无二次污染、占地空间小的优点。但在不额外提供电子供体情况下,自然脱氮速率较慢[3]。需要人为添加碳源。(即采用异养生物脱氮方法)。碳源类型分为固态碳源和液态碳源,目前的研究者对于固态碳源的研究较为深入,但是对于液态碳源如乙醇的研究比较少见,在同一种试验条件下,固态碳源和液态碳源对地下水硝酸盐氮的去除效果对比研究方面的文献或成果相对较少,为此,本文选取常用的三种碳源乙醇、棉花、餐盒作为碳源,并考虑碳源的空间分布形式,构建了柱试验装置,研究固态碳源和液态碳源对地下水硝酸盐氮的去除效果的影响程度,以筛选出较优的碳源,为地下水水源地的硝酸盐修复提供技术支撑。
1 试验方案与方法
1.1 试验方案
本次试验采用柱试验装置,柱子为塑料材质,上下无盖,底部用橡胶塞密封,外加液体胶确保密封效果。溶液从试验柱下方进入,值上端流出,确保充分反应。试验柱全长100 cm,直径20 cm,距底部5 cm为进水口,此后往上每隔20 cm设一出水口,用于取样检测样品溶液的三氮浓度(见表1和图1)。

表1 试验方案
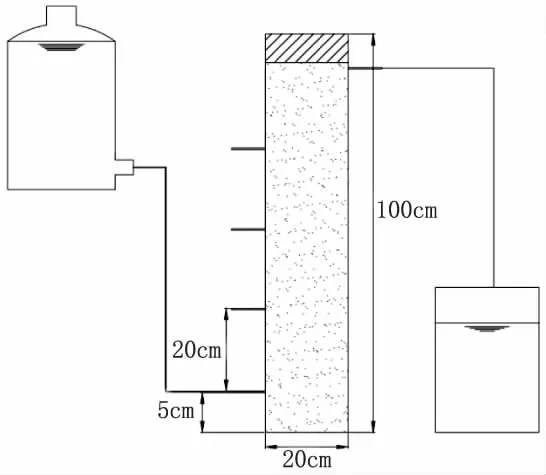
图1 试验装置图
用超纯水和KNO3配置浓度为25 mg/L的硝态氮初始溶液。选择液态碳源乙醇,固态碳源有棉花和餐盒两种,其中棉花的填充方式又分为均匀分布填充和集中填充两种填充方式,餐盒为均匀分布填充。
1.2 试验材料与方法
试验中细砂取自天然河砂,经筛分后粒径<0.1 mm,洗净后晾干使用,作为微生物附着的介质。
根据文献[6]的研究成果,选择C/N=2。在仅有碳源形式及填充方式不同的条件下开展试验,与硝酸盐浓度为25 mg/L相匹配的是餐盒5.77 g,棉花10.74 g,乙醇0.85 ml。试验在装置运行稳定后(流量基本稳定),从取样口定时取样观测,试验中测出溶液pH值及NO3--N、NO2--N、NH4+-N浓度。当观测到NO3--N浓度降低到某一浓度值稳定一段时间后浓度又开始增大并接近初始配置浓度25 mg/L时,停止试验。
本试验所选用的液态碳源乙醇事先加入到马氏瓶中与水均匀混合,然后通入到反应柱中,以此来达到均匀填充的目的。
棉花与餐盒事先做成微小的条状物或块状物,然后与沙子均匀混合之后填充到反应柱中,以此达到棉花与餐盒的均匀填充的目的。
同样将棉花做成微小的条状物或块状物,然后与将其与部分沙子混合之后先行填入反应柱中,继而继续填充沙子,达到棉花与餐盒的不均匀填充的目的。
通过盛有含硝酸盐水的马氏瓶通水,从反应柱的各个取水口取水测量其三氮浓度,来监测其去除效果。
2 试验结果与分析
2.1 三氮浓度变化分析
基于试验水样检测结果,分别得到了四个试验柱出水口硝酸根、亚硝酸盐浓度、铵根离子浓度变化情况,如图2、图3、图4所示。

图2 硝酸盐氮浓度变化过程线
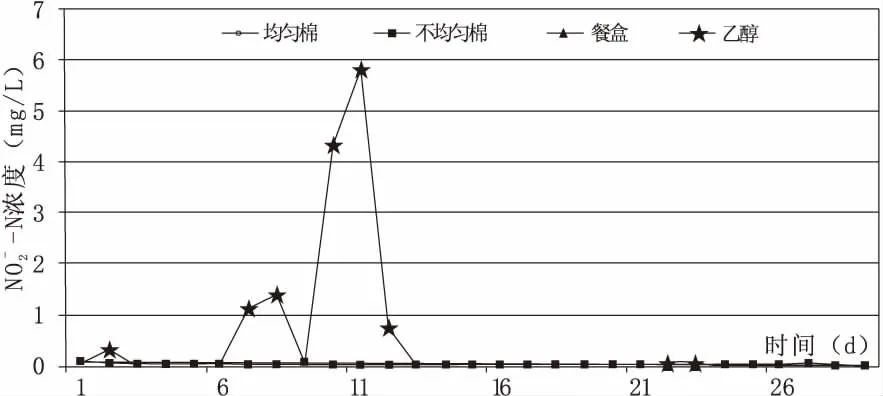
图3 亚硝酸盐氮浓度变化过程线

图4 铵盐氮浓度变化过程线
由图2可以看出,试验柱D中添加乙醇作为碳源时,硝酸盐氮浓度在第7 d明显下降,且浓度接近于0 mg/L,去除率达到了97%以上,且浓度相对稳定。而固体碳源在开始反应至第4天这段时间内,硝酸盐浓度较高,表明碳源还未释放发挥作用,随着反应时间增加,碳源逐渐释放,硝酸盐浓度开始下降,但不稳定,也间接表明碳源释放速率不稳定。
棉花作为碳源时,硝酸盐大致在16 d左右浓度不再下降,表明碳源释放结束,餐盒作为碳源时,则是在18d左右碳源释放结束,对地下水硝酸盐修复作用逐渐减弱直至消失,硝酸盐浓度逐渐恢复至初始浓度25 mg/L。
图3的亚硝酸盐浓度变化过程线表明,三种固态碳源的亚硝酸根浓度没有出现明显累积的现象,其浓度基于低于III水的标准0.1 mg/L。
但铵盐氮的浓度却存在不同程度的积累问题(图4)。可能是由于反应不充分造成的,但随着反应时间的增加,氨氮浓度逐渐降低,15 d左右后浓度均低于2 mg/L。
综上可以看出,固态碳源硝酸盐去除率普遍没有乙醇高。当棉花均匀填充时,其去除效果较不均匀填充较优,最高去除率达到了81.04%,且稳定天数较餐盒也长;不均匀棉和餐盒的最高去除率仅为70%和60%,但是餐盒总体的波动范围较不均匀棉的波动范围要小。
从单位质量去除率分析可以得出,1 g均匀棉、不均匀棉、餐盒、乙醇分别可以去除硝酸盐2.03 mg/L、1.62 mg/L、2.6 mg/L、42.76 mg/L。乙醇的单位质量去除率明显高于固态碳源,餐盒的单位质量去除率高于棉花。
2.2 pH值变化和渗透性能分析
在对pH值检测方面,在初始溶液pH=8.15的情况下,分别在运行时间3 d、7 d、12 d、17 d、23 d对各个试验柱进行pH值测定,结果显示,其值全部在8.0~9.0之间,pH并没有较大变化,说明试验过程中均未出现乙酸及氨氮积累问题。
试验开始前和结束后测得的其渗透系数如表2所示。总体上试验结束后介质的渗透系数均有所减小,分析原因可能是由于随着反应的进行,非活性微生物颗粒无法有效从反应体系中脱出,附在介质表现,致使介质的渗透性减小。

表2 渗透系数统计表
2.3 机制分析
固态碳源在反硝化过程中存在的反硝化机理可能是:固态碳源经由胞外酶(脂肪酶等)水解成大、小分子供微生物作为电子的供体,将硝酸盐还原为亚硝酸盐、一氧化氮、一氧化二氮等中间产物,最终还原为氮气。分析由图2中反映出来的各种碳源的处理效果可知,固态碳源的去除率普遍较低,固态碳源相较于液态碳源随配制的硝酸盐溶液一同通进试验柱促使乙醇与所配制的溶液深度混合的方式而言,固态碳源是事先直接填充到沙子中,待配制好的硝酸盐溶液进入试验中,才与硝酸盐溶液接触,因此固态碳源释放速率不及液态碳源那样稳定。
随着反应的进行,碳源释放量逐渐减少,释放速率逐渐趋于不稳定,溶液中碳源养分不足,导致大部分反硝化细菌进入休眠状态,进而引起反硝化作用不稳定,不彻底,所以表现为固态碳源整体的去除率不及液态碳源高,且去除率时高时低,去除率曲线有较大的波动情况。
3 结语
本文围绕地下水硝酸盐原位修复方法,结合室内柱试验,分析了不同种类碳源对硝酸盐修复效果的影响。结果表明:
(1)选取的三种碳源中(四种不同形态)液态碳源乙醇对硝酸盐的处理效果最好,去除率大于97%,且反应非常稳定。
(2)固态碳源的碳源释放速率不均匀,不能以稳定的速率释放碳源,导致溶液中养分利用不充分,使得大部分反硝化细菌休眠,造成固态碳源对硝酸盐修复的效果不佳。
(3)采用微生物方法进行浅层地下水硝酸盐污染的修复是有效的、可行的,特别是选择合适的碳源类型,配以合适的碳氮比,在环境适宜的情况下,能达到较好的去除硝酸盐浓度的效果。
(4)另外试验中发现温度对试验结果有一定的影响。温度通过影响反硝化细菌的活性进而影响到反硝化过程的速率,由于自然界温度不可控制,故在实际应用过程中需要考虑温度变化对硝酸盐去除效果的影响。

