2021年全国甲卷化学试题分析和备考策略
云南 夏永梅
2021年高考已落下帷幕,随着高考化学试卷的出炉,笔者认为甲卷化学试题呈现稳中求进的总体原则,持续稳定推进高考考试内容改革。试题充分发挥化学特点,精选试题情境,弘扬学科核心价值,考查关键能力。
一、2021年全国甲卷化学试题分析
1.落实基础,源于教材又高于教材
从表1可以看出,甲卷试题中直接来源于课本或对课本内容进行延伸拓展的分值占比很高,除此之外,试题中出现了大量的考生已知的物质,多数直接来自教材,试题对它们的性质进行了考查,例如第9题C选项制备的气体H2S出现在必修一91页资料卡片,并结合浓硫酸的性质考查了氧化还原规律。历年的试题中都可以找到大量来自于课本的内容,近几年来高三备考教师也都立足于教材,回归课本,但复习时知识的融合性不够,不能做到万变不离其宗。以课本习题为辅深挖教材,才能做到精准备考。

表1 来自教材的试题统计
2.重视信息获取与加工,凸显化学学科能力

表2 素材呈现方式
试题与往年一样呈现形式多样,提供了丰富的数据信息,考查学生信息整理能力。例如第12题提供了硫酸钡、碳酸钡阴阳离子浓度的负对数,要求学生提取数据信息,对数据信息进行加工,既保障了基础,又增加了试题的灵活性。
3.追本溯源,万变不离其宗
表3截取了甲卷中部分试题的具体考点,与历年试题考点进行对比,可以看出有较多的考点延续了近年的高频考点,知识点重复的较多,且同一物质在同一份试卷里面会在不同的题中考查,考点都是课本的知识点。在高三备考时学生会做大量的模拟题,但效果并不好,主要原因就是不会思考,不会变式。我们可以看一下几个相关试题:

表3 与历年全国卷考查点一样的题(部分)
(2021·全国甲卷·8节选)NA为阿伏加德罗常数的值。下列叙述正确的是
( )

(2020·全国卷Ⅲ·9节选)NA是阿伏加德罗常数的值。下列说法正确的是
( )

(2018·全国卷Ⅲ·8节选)下列叙述正确的是
( )

(2021·全国甲卷·8节选)NA为阿伏加德罗常数的值。下列叙述正确的是
( )

(2019·全国卷Ⅱ·8节选)已知NA是阿伏加德罗常数的值,下列说法错误的是
( )
C.1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
(2021·全国甲卷·8节选)NA为阿伏加德罗常数的值。下列叙述正确的是
( )
B.3 mol的NO2与H2O完全反应时转移的电子数为4NA
(2021·全国甲卷·9节选)实验室制备下列气体的方法可行的是
( )

气体方法B二氧化氮将铝片加到冷浓硝酸中
(2020·全国卷Ⅰ·9节选)下列气体去除杂质的方法中,不能实现目的的是
( )

气体(杂质)方法DNO(NO2)通过氢氧化钠溶液
从表1和表3中可以看出,教师在备考过程中不需要给学生提供大量的题,重在对教材的深挖及高考题的研究,这两种资料指导性、方向性强。
现在的学生喜欢做题但不喜欢钻研,同一内容稍微变式便无法解答,这样既没有效率,也没有成就感。根据分析可以看出,高考题都具有传承性,都重视在核心基础上提升学生的综合素质。因此我们在备考中要把课本上内容扩展延伸,真正实现万变不离其宗。
4.以实验体现化学魅力
从表4可以看出,实验考查内容分值占比很大,但现在的教学环境下,教学资源紧缺的中学实验教学薄弱,大部分教学都是以实验视频为主,学生没有真正体验过实验操作,甚至不了解实验仪器名称,所以应该把学生带入化学实验室,让学生真正体验化学实验魅力。
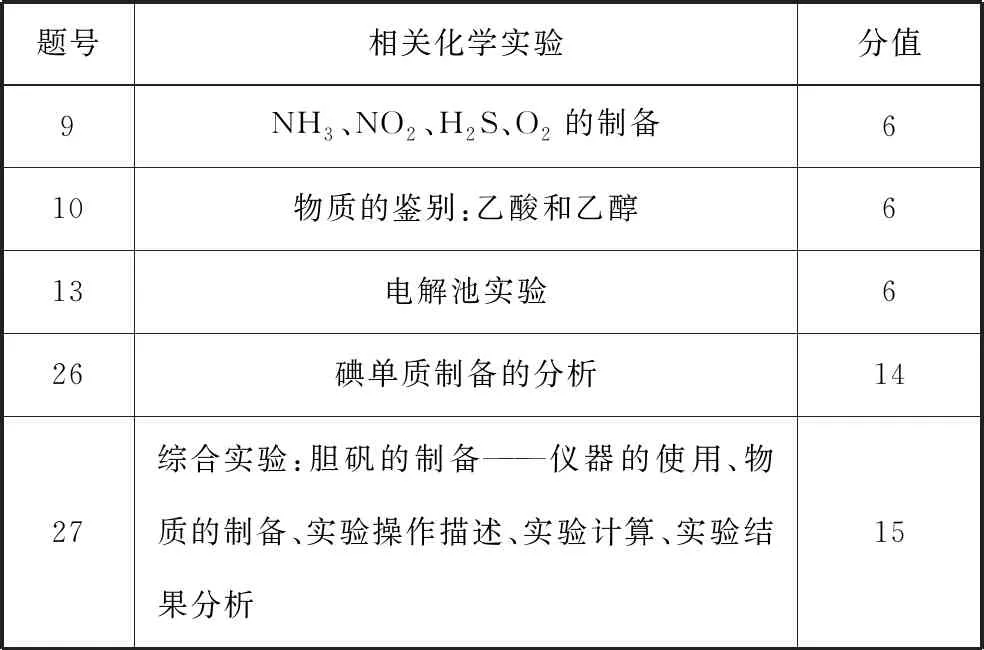
表4 与实验有关的试题
【例1】(2021·全国甲卷·9)实验室制备下列气体的方法可行的是
( )
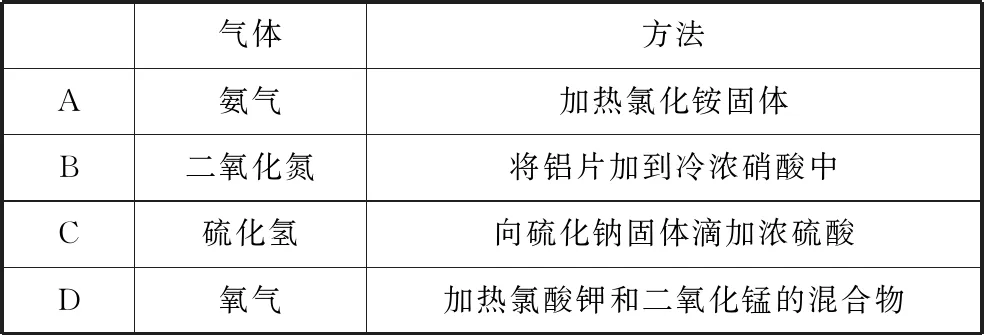
表5
【答案】D
【例2】(2021·全国甲卷·10)下列叙述正确的是
( )
A.甲醇既可发生取代反应也可发生加成反应
B.用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇
C.烷烃的沸点高低仅取决于碳原子数的多少
D.戊二烯与环戊烷互为同分异构体
【答案】B
5.体现核心素养的考查
核心素养是党的教育方针的具体化,是连接宏观教育理念、培养目标与具体教育实践的中间环节。全国甲卷的考查充分体现了化学学科素养。
【例3】(2021·全国甲卷·13)乙醛酸是一种重要的化工中间体,可采用如图1所示的电化学装置合成。图中的双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是

图1
( )
A.KBr在上述电化学合成过程中只起电解质的作用
C.制得2 mol乙醛酸,理论上外电路中迁移了1 mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移
【答案】D
试题以电解法合成乙醛酸(阴极和阳极都得到目标产物)为背景,提供装置图和反应信息。试题体现了证据推理和模型认知的考查,利用电化学基本原理和电池结构模型分析了电化学实际生产中的问题。
【例4】(2021·全国甲卷·28)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:

该反应一般认为通过如下步骤来实现:


总反应的ΔH=________kJ·mol-1;若反应①为慢反应,图2示意图中能体现上述反应能量变化的是________(填标号),判断的理由是_______________。




图2
(2)合成总反应在起始物n(H2)/n(CO2)=3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图3所示。

图3
①用各物质的平衡分压表示总反应的平衡常数,表达式Kp=________;
②图中对应等压过程的曲线是________,判断的理由是_______________;
③当x(CH3OH)=0.10时,CO2的平衡转化率α=________,反应条件可能为________或________。
【答案】(1)-49 A ΔH1为正值,ΔH2和ΔH为负值,反应①的活化能大于反应②的

②b 总反应ΔH<0,升高温度时平衡向逆反应方向移动,甲醇的物质的量分数最小
③33.3% 5×105Pa,210℃ 9×105Pa,250℃
试题以第五代制甲醇的方法为素材,肯定化学对社会发展的重大贡献,具有可持续发展意识和绿色化学观念,对与化学有关的社会热点问题做出正确的价值判断,凸显社会责任的化学学科核心素养。在设计试题时注重原理的考查,对平衡常数只要求写出表达式,重视模型的构建。转化率的计算是基于平衡思想的考查,使学生能够用动态平衡的观点分析化学反应。
二、2021年全国甲卷化学试题命题导向的备考启示
1.落实化学必备知识
化学学科考试为选拔具有学习潜能和创新精神的学生,考查学生接受、吸收、整合化学信息的能力,学生分析和解决问题的能力和化学实验与探究的能力。参照《普通高中化学课程标准(2017年版2020年修订)》(以下简称《课程标准》),将高考化学学科考试分为了必考内容和选考内容,必考内容包括:化学学科特点和基本研究方法、化学基本概念和基本理论、常见无机物及其应用、常见有机物及其应用和化学实验基础五个方面。选考内容为物质结构与性质和有机化学基础两个模块。
化学学科特点和基本研究方法包含从原子、分子水平认识物质,物质的组成、结构和性质的关系,实验和推理为基础的科学探究方法;化学基本概念和基本理论包含分子、原子、离子和原子团的概念,物理变化和化学变化,化合物和纯净物、单质和化合物、金属和非金属的概念,酸、碱、盐和氧化物的概念及相互关系,元素名称、符号、离子符号、原子结构示意图、电子式、分子式、结构式和结构简式,化学方程式和离子方程式;常见无机物及其应用包含Na、Mg、Al、Fe、Cu等金属元素和H、C、N、O、Si、S、Cl等非金属元素的单质及其化合物的性质及应用;常见有机物和应用包含了烷烃、烯烃、炔烃、芳香烃、卤代烃、醇、酚、醛、羧酸、酯的结构和性质以及他们之间的相互转化;物质结构与性质包含了原子结构与元素的性质、化学键与分子结构、分子间作用力与物质的性质、晶体结构与性质;化学实验包含仪器的用途和使用方法、化学实验基本操作、常见气体的实验室制法、物质检验、分离和提纯。
一轮复习备考核心重在基础,只有掌握必备知识,才能够提升综合能力。
2.重视情境教学
教育部颁布的《课程标准》中明确指出了“创设真实问题情境,促进学习方式转变”这一要求,实际上致力于解决一线教师面临的教学困难。
在教学中,教师有目的地引入或创设具有一定情绪色彩的、以形象为主题的生动具体的场景,以引发学生一定的态度体验,有利于激发学生的情感。真正的教学不是一味的灌输,而是能引起学生积极的、健康的情感体验,直接提高学生的学习积极性。中学阶段学生普遍存在学习动力不足的问题,而欢快活泼的课堂氛围是取得优良教学效果的重要条件,学生情感高涨有利于知识内化和深化。
3.加强信息获取能力的培养
化学试题中包含了大量的表格和图像,这些表格图像提供大量的数据信息,深入考查学生的信息加工能力。


