高通量测序技术的发展及其在临床检测中的应用
王玉静,陆梓涔,陈俊煜,陈毅歆,*,尤瑞娈
(1.厦门大学公共卫生学院,分子疫苗学和分子诊断学国家重点实验室,福建 厦门 361102;2.厦门大学生命科学学院,国家传染病诊断试剂与疫苗工程技术研究中心,福建 厦门 361102;3.厦门国际旅行卫生保健中心,福建 厦门 361100)
测序技术的出现,直观而深刻地揭露了核酸分子的深层信息,为人类进一步探索基因结构与功能提供了决定性的技术手段.高通量测序在过去约20年中得到了迅猛的发展,也成功实现了商业化,与之相关的基础应用、科研探究以及临床应用随之大幅增加[1].随着“精准医疗”概念的提出,临床应用上对高通量测序的需求越来越大,病原学诊断、检测与遗传病、肿瘤等疾病的精准诊断等应用领域对高通量测序技术的要求也越来越高.而在高通量测序技术出现之后,发生的几次世界性范围的传染性疫情中,高通量测序技术也逐渐扮演起重要的角色[2].高通量测序技术作为精准医疗的重要基石,对精准医疗做出了极大的贡献,在临床相关的病原微生物检测、临床肿瘤学、16SrRNA基因以及内转录组间隔区(internal transcribed spacer,ITS)测序、遗传疾病检测、传染病监测以及新型病毒的发掘等方面发挥出优势[3].高通量测序技术的发展历程、不同平台的特点、测序原理的差异以及不同领域的应用都是受到较多关注的焦点.本文将对以上关注焦点进行介绍与讨论,同时对高通量测序技术在临床检测中的应用进行详细阐述.
1 测序技术的发展历程
Frederick Sanger于1975年发明了“双脱氧链终止法”基因测序技术,这是科学史上出现的第一种基因测序技术[4];另一种基因测序技术是1977年Walter Gilbert发明的“化学测序法”[5].这两种测序技术均作为一代测序的标志性技术而广泛应用,其中双脱氧链终止法因操作更简便稳定而被更广泛应用.在过去的20年内,基因测序技术有了较大的进步与发展,一代测序仍然稳定占据部分市场,二代测序、三代测序也快速占据了较大的市场份额,基因测序技术在规模、通量以及应用上都有了极大的发展.一代测序虽然在过去50年内占据着极大的市场,然而其存在通量低、数据产出较低以及成本较高等问题,虽然目前有着不可取代的地位,但是仍然无法满足当前分子生物学、医学研究以及临床诊断对于高通量、高效率、高产出的测序需求.二代测序相对于一代测序而言准确率略微降低,但通量和产出增加,可以实现同时对多个样本进行测序,单位时间内的数据产出量相比于一代测序实现了数量级的增长.自2005年第一台二代测序仪器罗氏(Roche)454焦磷酸测序平台诞生以来,随后陆续推出的二代测序技术平台包括:2006年Illumina公司推出的Solexa测序平台、2007年美国ABI公司推出的SOLiD测序平台和2010年美国Life Technologies公司推出的半导体测序平台[6],各占据一定的市场份额.其中454 Life Science后来被Roche公司收购,但由于二代测序市场的竞争日趋激烈以及较新的测序方法出现,该测序方法被逐渐淘汰.2013年Roche公司宣布关闭454测序业务,并于2016年全面终止相关服务,454测序仪被市场淘汰.2008年Invitrogen公司和美国ABI公司合并成立Life Technologies公司,开始发展半导体测序,占据了部分测序市场,随之SOLiD测序也逐渐淡出市场.2006年开始Illumina公司进入了二代测序市场,且在此后的10年时间内,Illumina公司占据了大部分测序市场,于2010年开始陆续推出的Hiseq系列测序仪,更是迅速成为二代测序平台中的主流测序平台.
作为中国高通量测序的先驱,华大基因于2014年推出首款二代测序仪——BGISEQ-1000,继而在2016年陆续推出了BGISEQ-500等型号的测序仪.该测序平台在大规模DNA测序和小RNA分析中的能力已得到证明,但BGISEQ-500平台在转录组分析中的性能仍有待提升[7].每种测序平台都有自身特点,在数据产出量、测序读长、测序准确率以及测序成本等方面各有不同的表现[8].
二代测序技术平台尽管在测序通量、数据产出量以及应用领域上相较于一代测序有显著优势,但仍然存在一定的短板,如:测序读长较短导致在测序过程中会产生大量高度碎片化的重复片段,尤其在进行大基因组测序时,测序拼接成为一个较大的挑战;且相较于一代测序而言,二代测序所需的测序时间显著增加,尚不能完全满足临床样本的快速诊断需要[9].在此背景下,可满足长读长和快速测序需要的三代测序平台应运而生:2008年英国ONT公司首次推出了一款以纳米孔单分子测序为原理的测序仪器,但当时该平台还不够稳定,无法投入正常使用;2008年美国Helicos Bioscience公司以单分子测序(single molecule sequencing, SMS)技术为原理的Heliscope测序平台发布上市;2009年美国Pacific Bioscience公司推出了单分子实时(single molecule real-time,SMRT)测序技术;2014年英国ONT公司推出了MinION测序仪,可供用户使用.三代测序平台可以直接对给定的DNA或RNA模板进行测序,实现了真正意义上的实时测序,当核酸模板通过测序仪即可产生信号.相较于前两代测序平台,三代测序平台主要的改善有:1) 读长变长,可在一个反应内读取成千上万碱基的读长,理论上可达无限长;2) 测序流程简化,测序时间减少,在文库构建以及上机测序等流程上有所精简,减少了样本的测序时间;3) 避免了PCR扩增技术造成的扩增偏好;4) 可直接测定碱基上的修饰情况,如碱基甲基化[10].图1展示了基因测序发展历程中的里程碑事件.
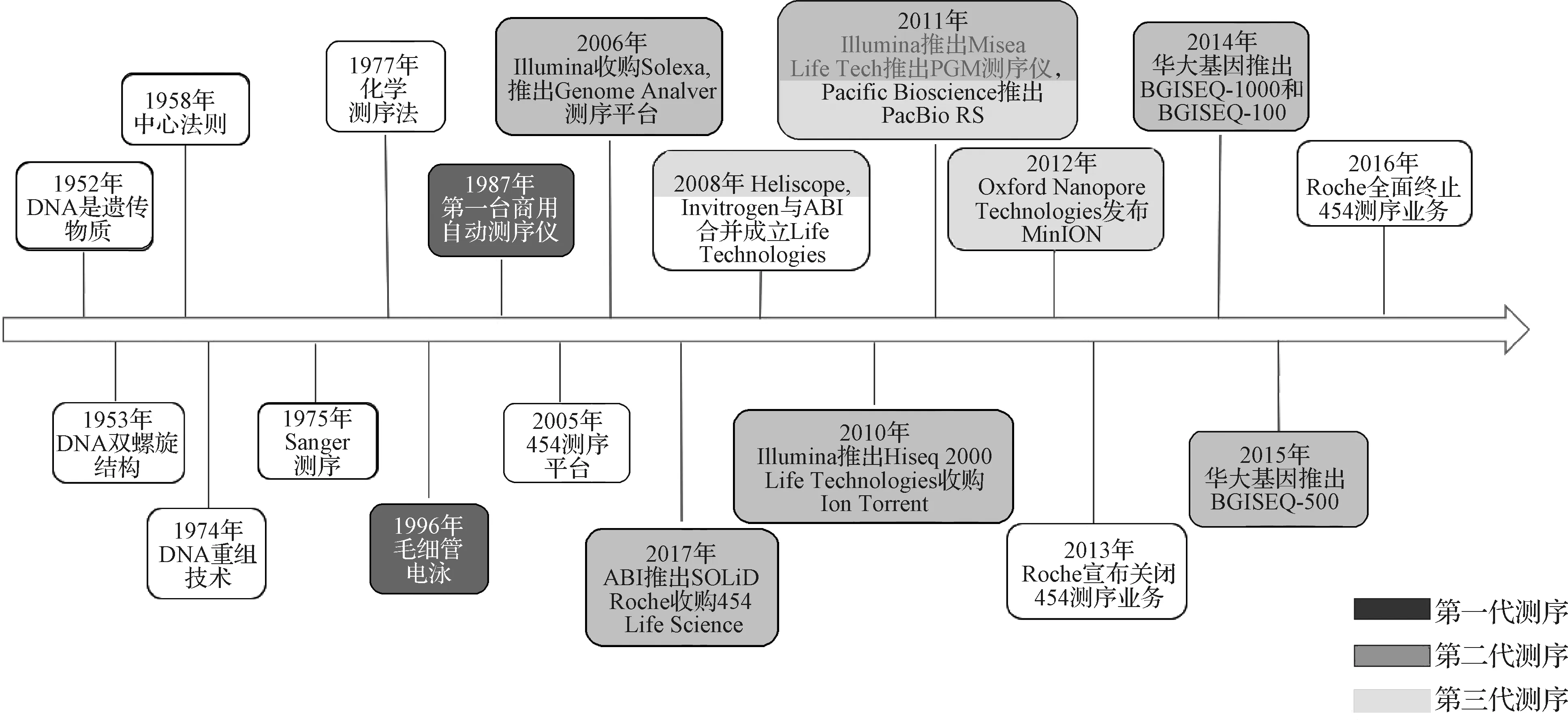
图1 测序技术发展时间轴
2 主流二代测序平台的发展概况
一代测序技术运用多年仍然生机蓬勃,二代测序技术更是在短时间内迅速崛起成为市场主流,并在近年来被广泛应用于临床病原体鉴定诊断中[11].不同于Sanger测序,二代测序将酶促DNA反应、碱基测序与数据收集同步进行,因此可以同时对数千到数十亿条DNA模板进行测序[12].以下三家公司的测序平台因不同的测序原理在各方面存在一定差异,但由于平台侧重点不同,都在不同时间段成为当时较主流的测序平台,并且侧重应用于不同领域.
2.1 罗氏454焦磷酸测序平台
Roche公司的454焦磷酸测序平台是国际上第一台相对较成熟的二代测序平台,属于循环微阵列法平台,其测序技术基础是边合成边测序(sequencing by synthesis,SBS)技术[13].该项测序技术的测序原理主要依靠荧光信号的生物发光,将模板进行PCR扩增后,与相应的引物杂交,并与三磷酸腺苷双磷酸酶、DNA聚合酶、ATP硫酸化酶、荧光素酶、底物荧光素酶和5’-磷酸硫腺苷共同孵育,然后进行相应的酶促反应;在每次实时测序实验中,模板只与一种脱氧核糖核苷三磷酸(dNTP)进行配对反应,在此酶促反应中,DNA聚合酶以该dNTP作为原料合成互补链,会释放出等物质的量的焦磷酸基团[13].
454测序技术的主要优势在于测序时间较短,且准确率较高(可达99%),在单位时间内产生的片段数量多.该测序平台在一次测序工作中可以产生100万条序列,序列的平均长度400 bp,数据总量约500 M.454测序平台已经被应用到多个方面,均取得了较理想的结果.454 Life Sciences被Roche公司收购后,Roche公司在454测序测序平台的基础上又相继推出GS FLX平台[14],由于后期二代测序市场上新的测序方法不断更迭以及该平台的测序成本较高等原因,该测序平台已于2016年宣布全面停止相关的测序服务.
2.2 Illumina测序平台
Illumina测序仪也称为Solexa分析仪,其测序原理与Sanger测序法类似,将合成核酸的原料dNTP用4种不同的荧光进行标记,并偶联可逆的终止剂,固相基质上可以容纳数百万的模板克隆,每个固相基质上可以同时读取10亿个碱基.2005年Solexa公司收购合并了仪器公司Lynx Therapeutics,新公司成功地将Solexa原型转化为商业测序仪器,2006年推出第一个Solexa测序仪——Genome Analyzer.该测序平台具有高精准度、高灵敏度、高特异性以及相对较低成本的特点,并在2010年成功推出Hiseq系列测序仪,目前在遗传疾病分析、肿瘤癌症检测以及功能基因组测序等领域占据主要的测序市场.Illumina Hiseq系列测序仪具有PE150的读长,相较于该系列其他测序仪读长较长,其优势主要在于其测序精准度最高可达99.9%,而且相较于其他二代测序平台测序成本较低,但该系列也有相应的缺点——序列读长较短[15].
2.3 SOLiD高通量测序仪
2006年7月,美国ABI公司推出SOLiD测序平台,该平台基本原理的特点在于每一步测序反应都是通过连接反应完成的,通过PCR反应进行平行扩增测序.SOLiD测序平台支持两种测序文库:一种是与Illumina测序平台的文库构建类似,均先将DNA模板片段化,在片段的DNA模板两端加上接头,即成功构建文库;另一种是配对末端文库,依靠酶切反应加上接头,成功构建文库[16].2010年末ABI公司发布了第五代测序系统——SOLiD 5500xl测序系统,该系统在读长、精准度以及数据产出量上都实现了较大进步,分别达到85 bp,99.99%和30 G,在未退出市场前,曾是二代测序平台中精准度最高的平台[16].
2008年在Life Technologies公司收购Ion Torrent公司之后,开始陆续推出Ion PGM和Ion Proton系列测序仪,且是该公司目前主推的测序仪,因此SOLiD测序平台逐渐淡出市场.2010年Life Technologies公司发布Ion PGM测序仪,目前有3款芯片并在不断改进,测序通量也在不断增加;2012年发布Ion Proton测序仪,拓展了该系列测序仪在更多领域的应用.2013年Life Technologies公司又被Thermo Fisher公司收购;2015年9月1日发布新产品S5系列Ion S5/the S5 XL,是Proton和PGM相结合产生的产品,相较于Proton,PGM新系列更加容易操作,且节省了较多的测序时间[3].
2.4 不同二代测序平台的比较分析
多种不同的二代测序平台在不同方面也有不同的表现.其中罗氏454测序仪作为最早问世的二代测序仪,读长较长,运行较快,然而检测成本较高,设备较大,可及性不高,且错误率也相对较高,目前在测序市场中已经停产;Illumina测序仪作为目前市场上应用最广泛的二代测序仪,读长较短,运行较慢,成本也相对较高,设备较大,对于实验人员要求较高,但测序错误率较低,适用于全基因组测序和宏基因组测序,应用领域广泛[7];SOLiD测序仪也是曾经较常见的二代测序仪,测序准确率较高,然而读长较短,运行较慢,常用于外显子测序和基因突变测序,目前也已淡出市场[12].
3 三代测序平台的发展现状
随着二代测序平台的成功应用,三代测序平台开始陆续推出.不同于二代测序平台的部分特点,三代测序在读长上进行了更大改善,测序时间也相应减少,测序流程更简便,测序设备更便携,测序成本更低.三代测序不依赖于PCR扩增技术,其最大特点就是SMS技术[17].目前市面上出现的SMS平台分别为美国Heliscope BioScience公司的SMS技术[17]、美国Pacific Bioscience公司的SMRT技术[18]、VisiGen Biotechnologies公司的荧光共振能量转移(fluorescence resonance energy transfer,FRET)技术[19]以及英国ONT公司推出的纳米孔SMS技术[10].
3.1 SMS测序平台
2008年,美国Helicos Bioscience公司推出HeliScope单分子测序平台,是继二代测序平台之后出现的第一个可以商品化应用的三代测序仪,其测序的主要原理是一种基于光学信号的SBS技术,但不同于二代测序的是该方法不依赖于PCR扩增技术,先随机将待测模板进行打断与筛选,在对片段化模板进行末端修复之后在片段3’-末端连接上50 bp结合有荧光标记的poly(A)尾巴,含接头的文库可以通过末端poly(A)尾巴结合固定在固相基质的Oligo d(T)探针上,类似于Solexa测序,该方法也需要将荧光染料标记的4种dNTP依次加入微反应中,在DNA聚合酶的催化反应下,通过碱基互补配对释放出相应的荧光信号,最后依靠增强型电荷耦合元件(intencified charge coupled device,ICCD)相机进行光学信号的收集[16],在测序上避免了扩增时引入的碱基错配以及扩增偏好性.该测序方法也存在相应的不足,就是对于光学信号收集的设备要求较高,并且在测序过程中由于信号较弱容易产生测序误差,导致准确率降低;因此该平台为提高精准度采取了两次测序(two-pass sequencing),增加了测序成本[20].然而由于该平台初始读长较短,约32 bp,且测序成本较高,测序准确率较低,错误率高达1%,所以该测序平台并未得到广泛的应用,2012年底Helicos正式申请破产保护.
3.2 SMRT测序平台
美国Pacific Bioscience公司推出的SMRT测序技术是目前三代测序平台中应用最广泛的一项测序技术.SMRT测序技术相较于其他测序技术而言有较大的优势,该方法同样基于对单个DNA分子进行测序,采用4种荧光标记的dNTP以及零级波导(zero-mode waveguide,ZMW)的纳米结构作为测序技术的主要基础.ZMW这种纳米结构是一种孔状纳米光电结构,光线在通过ZMW后会呈现指数级衰减,被衰减的光线最终只能使孔内靠近基质的部分被照亮;ZMW作为测序的微反应器,会提前在微反应器中结合测序反应所需要的phi29 DNA聚合酶;在构建文库时,将待测模板与引物结合,混合4种荧光标记的dNTP一同加入微反应器ZMW中;测序反应过程中,待测模板DNA以4种荧光标记的dNTP作为原料进行合成时,所连接的dNTP会因反应而在ZMW底部短暂停留,荧光收集设备则可以收集到配对dNTP的荧光信号,从而实现测序[21].该平台在读长上实现了较大的突破,其中PacBio RSⅡ测序平台最长读长能够达到30 kb,平均读长约8.5 kb,且该平台也具有三代测序平台普遍共有的优势——测序流程更简便,构建文库时间缩短,且不依赖于PCR扩增技术.然而与SMS技术类似,该测序技术同样依赖于单分子产生的荧光信号进行测序,因此测序的准确率偏低,最高仅可达到87.5%;尽管通过增加测序次数以及后期数据分析矫正,准确率可以提高,但是相对于Sanger测序以及二代测序,准确率仍然较低[21].
3.3 纳米孔SMS平台
2014年,英国ONT公司推出了第一个商用的测序平台——MinION,该测序平台的主要测序原理是基于待测模板通过生物纳米孔时不同碱基产生的不同电位差而实现电信号向碱基信号的转变.Nanopore测序系统主要由纳米孔、薄膜以及马达蛋白组成,其中马达蛋白是一种DNA解旋酶,在构建文库时,马达蛋白与接头会一同连接在待测模板的一端;当将制备好的文库滴加到纳米孔上时,马达蛋白通过解旋作用将双链DNA变为单链通过纳米孔;A、T、C、G 4个碱基通过纳米孔产生不同的电位差,这种电信号会被传导电子元件(application-specific integrated circuit,ASIC)以及MinKNOW软件接受并进行初级处理[22].该测序平台的序列读长与PacBio测序平台相似,达10 kb,理论上可达无限长.然而相较于PacBio测序平台,MinION测序平台的错误率更高,准确率仅65%~88%.
前期使用9.4版本芯片或者其他版本芯片Flow cell进行测序时,测序准确率非常低,仅约90%;后续平台推出9.5版本Flow cell芯片并且采用1D2(DNA正反链测序,相互矫正)建库方式,在一定程度上提升了测序准确率[23].
3.4 FRET测序平台
FRET测序平台在对样本核酸进行测序时,测序过程中4种脱氧核苷酸分子被4种不同的荧光受体所标记,随着测序引物延伸,4种不同的荧光受体会发出特异的荧光,不同的荧光分别代表不同的4种脱氧核苷酸分子.该测序平台由VisiGen Biotechnologies公司研发并推出,读长较长,平均读长在1 500 bp以上,测序准确率相对于其他三代测序平台较高,并且测序时长较短;但该平台因为缺乏具体应用的技术参数,所以并未得到广泛应用[19].
3.5 不同三代测序平台的比较分析
由于不同测序平台之间的测序原理与建库方式等有较大的不同,各测序平台侧重应用的领域也不尽相同,且不同测序平台的测序成本、测序时间以及测序准确率也有一定差异(表1).三代测序平台的读长都较长,且不依赖于PCR方式构建文库,测序成本较低,测序时间较短;然而相对于二代测序平台,三代测序平台的测序错误率都较高,后续数据处理分析非常依赖于处理软件与数据库的选择与使用.三代测序平台中,英国ONT公司的Nanopore测序仪对实验人员要求较小,可及性极高.对于目前的三代测序平台而言,如何提高测序的准确率是较受关注的方面.目前主流三代测序公司均在测序设备稳定性以及后续数据处理分析上进行了很大的改进与完善.

表1 三代测序平台对比
4 高通量测序平台的临床应用
Sanger测序作为传统检测方法中较典型的方法,由于该平台测序规模的短板,其应用的领域较有限.而高通量测序作为近几年较受关注的测序技术,在各大领域有着广泛的应用以及突出的效果[25],如临床预测、诊断、治疗相关领域.下文主要从与临床有关的不同领域对高通量测序的应用(表2)进行详细阐述.
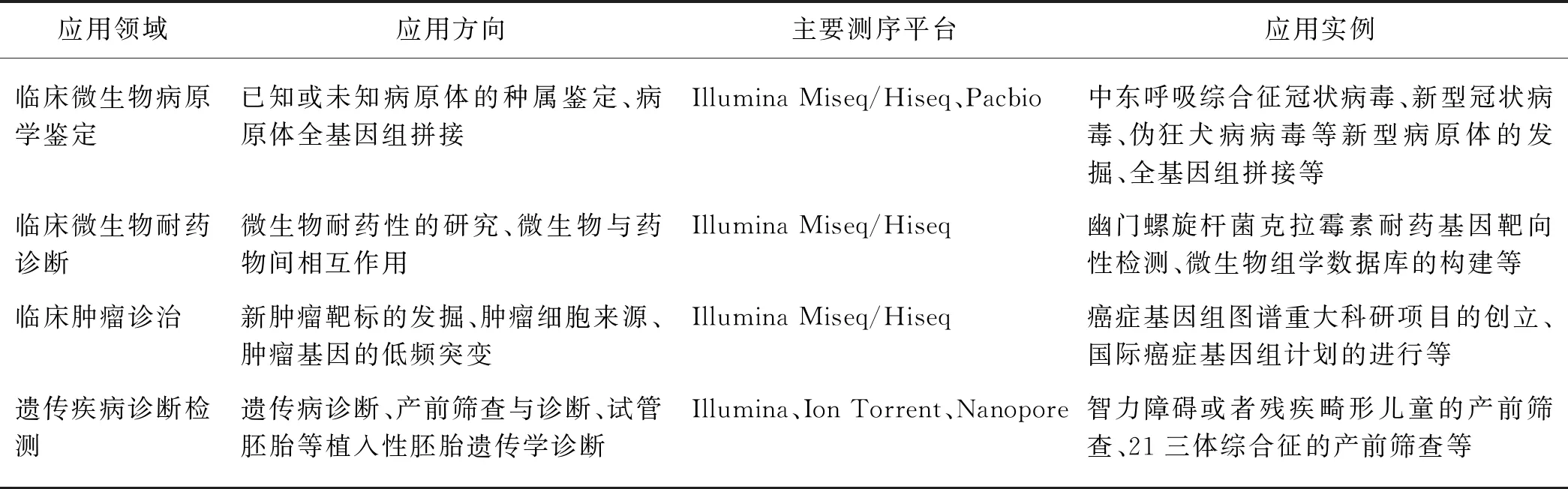
表2 高通量测序平台的临床应用
4.1 临床微生物病原学鉴定
细菌、真菌、支原体、衣原体、寄生虫、病毒等微生物与人体的健康系统稳定息息相关.人体中有着由细菌、真菌、病毒等微生物组成的庞大与复杂的胃肠道系统,且人体许多疾病的发生都与微生物系统的失调或微生物的入侵有着极其紧密的关系,而高通量测序技术的出现为这些微生物菌群的鉴定检测与研究提供了有力的技术支持[26].针对微生物病原学检测,基于测序策略的不同,主要可以分为以下3种:全基因组测序、靶向目标测序和宏基因组测序.
1) 全基因组测序是对未知基因组序列的物种进行个体的基因组测序.目前二代测序和三代测序均支持对个体物种进行全基因组测序,对于微生物的全基因组测序,可以准确从科、属、种水平上对样本中的微生物进行鉴定分析;并且可以根据对耐药基因和毒力基因的比对分析预测该种微生物的耐药情况以及预后情况;最重要的是,在发掘出罕见或者未知的微生物方面,全基因组测序必不可少[24].
Zhou等[27]基于二代测序平台以及扩增子测序等技术对一种未知的新型病毒进行全基因组测序,发现该病毒与人类冠状病毒HKU2相似,与蝙蝠体内寄宿的某种冠状病毒序列一致性达98.48%.研究人员基于二代测序平台对该新型冠状病毒进行全基因组测序,迅速掌握了该病毒的传染性与毒力的分子学基础,研究了该病毒的衍化过程,为其治疗与防控提供了有利的测序分析手段[27].Wu等[28]研究人员从武汉新冠肺炎患者的样本中提取到新型冠状病毒的RNA,并且通过Illumina Miseq对提取到的RNA进行了测序及全基因组序列拼接.研究人员共得到56 565 928个读取序列,对以上读取序列进行初步组装拼接之后,形成了384 096个重叠群,其中长度最长的一个重叠群(30 474 bp)具有较高的丰度,与一株从蝙蝠分离得到的bat SL-CoVZC45的基因序列一致性达89.1%[28].可见二代测序平台在新病毒发现上有很大的潜力,对于流行性疾病的诊断与治疗有重大意义.
在新发传染病未知病原体的发掘、微生物耐药性分析方面,Illumina测序平台相对而言使用较为广泛并且表现良好,其中未知病原体的全基因组测序目前主要依靠Illumina Miseq等测序仪完成,该测序仪在迅速、精准、高效获取病原体基因以及基因比对分析方面有着较好的表现.
2) 靶向目标测序是指对某物种的某特定区域或某特定功能的基因进行靶向测序.对于临床微生物病原学检测来说,主要集中于对细菌的16SrRNA基因进行靶向目标测序.16SrRNA基因是原核生物所特有的基因片段,由于该基因片段在细菌中普遍存在,既具有相对保守的区域又有高度可变的区域,所以经常被用作细菌鉴定分类的标准[29].根据16SrRNA基因序列的保守区设计相应的引物,对可变区进行靶向扩增,并基于高通量测序平台对可变区进行靶向目标测序,后期借助生物信息学分析手段对样本中细菌进行精准的种属鉴定.类似地,针对真菌的ITS靶向目标测序也可以对真菌进行精准的鉴定与分类.针对16SrRNA基因和ITS的靶向目标测序,不仅对微生物可以进行准确的科、属、种鉴定分析,还可以从序列信息中得到毒力基因信息,为抗生素药物的耐药性、代谢等临床学和流行病学研究提供一定的帮助.
Schloss等[30]通过PacBio SMS技术对16SrRNA基因进行测序,将从社区和自然环境中获取的人粪便样本、老鼠粪便样本以及土壤样本进行混合,并对样本进行相应的靶向测序,主要获取并分析了V4、V3~V5、V1~V3、V1~V5、V1~V6以及V1~V9等可变区的测序数据;基于数据分析处理方式将该测序平台对16SrRNA基因中的可变区V1~V9的测序错误率从0.69%降低至0.027%.在对物种多样性、微生物组成和微生物进化开展的研究中,种属鉴定的精准度再次提升.
3) 宏基因组测序是指从临床样本或者环境样本中直接提取全部微生物的核酸,构建宏基因组测序文库并进行测序.该方法不需要进行菌株分离培养,因此很大程度地避免了分离效率低和灵敏度低的问题.针对环境样本(如土壤、海水等中复杂的微生物群落)以及人体口腔、粪便、肠道等部位的样本,通过宏基因组测序可发现样本中一些无法培养或难以培养的微生物种类,发掘复杂样本中未知的罕见微生物种类[31].
Salipante等[32]发现一名男子临床症状为左下叶肺炎,口腔分泌物增加,有多个组织坏死,前期抗生素治疗方案效果不明显;研究人员基于Illumina Miseq测序仪对患者肺泡灌洗液样本进行宏基因组测序,并对测序数据进行较完善的处理分析,包括使用PANDAseq对配对的短序列进行组装拼接,通过USEARCH v6软件对拼接全长进行读取比对,将所得组装好的数据片段与核糖体数据库项目(the Ribosomal Database Project)中具有较为典型、代表性的数据库序列进行比对分类,使用DeeNuRP和Taxtastic对数据进行过滤与注释;通过对患者样本的宏基因组测序,发现样本中存在核粒梭形杆菌(Fusobacteriumnucleatum)和假单胞菌(Pseudomonasadaceae)等,并在之后细菌培养实验结果得到验证.
4.2 临床微生物耐药诊断
临床微生物病原学的诊断检测具有十分重大的意义,临床上对于微生物相关的研究与检测需求也很大.除上文提到的复杂样本的微生物种属鉴定外,高通量测序还广泛应用于微生物耐药性(antimicrobial resistance,AMR)研究中.临床上医院获得性感染的细菌用药治疗一直是医疗难点,主要是由于在长期的抗生物用药筛选中,许多病原体通过基因突变而获得对不同抗生素的耐药性,给临床治疗造成了极大影响.
目前,通过高通量测序深度挖掘并组建了药学相关的微生物组学数据库.根据该大数据库已经发现超过60种药物与微生物之间存在相互作用,后期高通量测序也可持续挖掘微生物的耐药性、微生物与药物间的相互作用,及其与人类遗传变异的相关性[33].
初亚男等[34]等基于焦磷酸测序技术建立了一种对幽门螺旋杆菌(Helicobacterpylori)克拉霉素耐药基因靶向性检测的方法,在获知耐药情况的同时还可以基于454测序平台进行半定量测定,并且可以根据半定量测定结果进行治疗效果的评估.该研究中对44例临床样本进行了不同方法的检测,比较了焦磷酸测序方法、快速尿素酶实验和13C呼气试验的灵敏度;幽门螺旋杆菌对克拉霉素的耐药突变主要是由于其23SrRNA基因中A2142G和A2143G两个单核苷酸多态性(SNP)位点的突变,通过焦磷酸测序技术可以直接检测到这两个SNP位点的突变[34].实验表明焦磷酸测序技术具备灵敏度高、检测速度快、半定量的特点,为临床诊断提供了一种供选择的高效方法,且可以针对临床患者对不同病原体的耐药性情况进行分子学诊断以及耐药情况与治疗效果的半定量检测.
现阶段,通过高通量测序可以靶向检测耐药基因的突变,为临床用药提供及时的指导意见,也为患者的预后情况提供预估标准[33].同时,高通量测序还广泛应用于与人类胃肠道菌群情况监测与重要疾病相关微生物感染的监控,例如肺纤维化和肺衰竭等[35].在高通量测序用于监测临床长期用药后胃肠道菌群的实时动态变化情况方面,测序平台的高通量、高输出、高效率对于实时监测呈现很大的临床价值.
4.3 临床肿瘤诊治中的应用
目前,高通量测序平台同样被广泛应用于临床肿瘤学相关的研究中,针对DNA或RNA测序相关的肿瘤细胞来源或者肿瘤基因的低频突变,以及寻找新的肿瘤靶标,呈现出很大的临床应用价值[36].临床肿瘤学的检测诊断主要涉及基于高通量测序平台的全基因组测序以及外显子测序,其中全基因组测序在前文已有介绍,外显子测序则是与肿瘤学紧密相关的测序技术,利用序列捕捉技术对全基因组外显子区域DNA序列进行特异性捕捉,富集扩增后再进行高通量测序.基因外显子序列在全基因组中是非常重要的一部分编码序列,用于表达体内功能性或结构性蛋白,与肿瘤的发生与扩散及其预测与治疗有着密不可分的联系[37].而外显子测序相对于全基因组测序更具有靶向性,且耗费的时间成本以及经济成本也更低,对于检测肿瘤细胞的低频突变以及基因组的单核苷酸多态性、碱基插入或缺失有着很大的优势.在癌症预防上,高通量测序平台可以用于肿瘤基因的突变筛查,指导癌症的防控工作;在癌症治疗上,通过高通量测序平台挖掘与癌症相关的基因,不仅可以发掘与癌症相关的诊断靶标,还可以发掘与之相关的治疗靶点,为临床提供具体的个性化用药指导[38].
癌症基因组图谱(the Cancer Genome Atlas,TCGA)重大科研项目的创立旨在绘制出一万个肿瘤基因组景观图谱.科研人员主要通过高通量测序对肿瘤细胞的低频、中频突变进行监测与分析,目前该项目已经发现近1 000万个与癌症相关的基因突变,为癌症的预测与治疗提供了十分有意义的临床参考[36].国际癌症基因组计划(the International Cancer Genome Consortium)利用测序及高通量突变检测方法识别与癌症发生发展相关的关键基因[39].该大规模项目有多个国家参与,已经发掘50多种不同癌症;通过高通量测序,在基因组学、表观遗传学以及转录组学方面对超过2.5万个癌症基因组进行了系统性研究与分析,对癌症的治疗和预后情况预测具有重要意义.
4.4 遗传疾病诊断检测
高通量测序平台的另一项较为重要的应用是遗传性疾病的检测诊断,主要包括遗传病诊断、产前筛查与诊断,以及试管胚胎等植入性胚胎遗传学诊断.研究人员对产妇进行无创产前基因检测,然后对基因检测异常的产妇的羊水或者脐带血细胞进行染色体G显带检测和荧光原位杂交(fluorescenceinsituhybridization,FISH)检测,作为确诊标准[40].高通量测序平台为遗传性疾病的诊断、新生儿疾病的早期诊断、产妇的无创检测都提供了极大的便利,降低了智力障碍或者残疾畸形儿童的出生率,大大减轻了家庭和社会的负担,在遗传性疾病的治疗与预防方面呈现出很大的临床应用价值.
史淑琼等[41]对4 708例孕妇进行血液的采集以及核酸提取,采用新一代高通量测序技术,结合生物信息分析,得出胎儿非整倍体及性染色体的风险率,对21、18、13三体高风险及可疑性染色异常的孕妇进一步行羊膜腔穿刺术获得染色体核型;经统计学分析,无创基因21、18、13三体检出率均为100%,漏诊率为0,假阳性率分别为0.04%(2/4 708),0.08%(4/4 708)和0.06%(3/4 708),阳性预测值分别为97.1%(67/69),78.9%(15/19)和50.0%(3/6),阴性预测值均为100%.
无创基因检测在临床检测诊断中表现出巨大的优势[42],既减少了不必要的产前有创性检测操作,增加了检测诊断的灵敏性与特异性,也大大降低了有先天遗传病儿童的出生率,呈现很大的临床应用价值.
5 展 望
随着分子生物学和科学技术的不断提高,高通量测序技术在短短20年内获得突飞猛进的发展.特别是“精准医疗”概念的提出,使高通量测序技术成为精准医疗的重要技术保障.尽管如此,高通量测序平台依然存在许多亟待改进和完善之处:1) 二代测序平台序列读长较短,且依赖于PCR扩增技术,容易造成读取序列的误差与偏好性,给后期生物信息学数据分析处理造成了较大的困难,为了增加测序的准确性,无疑会增加测序的时间成本以及经济成本,因此二代测序平台在后期需要提高序列的读长和精准性[43].2) 对于高通量测序平台,数据的分析处理是至关重要的步骤[44],目前测序市场上较为主流的Illumina和Nanopore测序平台等都有着各自个性化处理分析数据的标准流程,因此高通量测序平台对于实验人员的生物信息学基础有着十分高的要求;且由于数据处理分析方式的不同有时会产生不同的比对结果,往往没有一个“金标准”来进行校正与比较,所以后期需要进一步完善与改进数据分析处理的能力,提高平台的相对灵敏性与特异性,进一步构建相对准确与严格的标准化流程,提升平台的稳定性.3) 二代测序平台测序时间一般较长,主要时间消耗在准备样品、构建文库以及测序分析上,相对较长的测序时间对于急性传染病暴发的监控、临床样本的诊断鉴定,尤其是高危患者的病原学鉴定是极大的障碍.针对这一问题,三代测序平台的出现尽管大大缩短了测序时间,然而由于三代测序平台在准确性上比二代测序平台低,在广泛实际应用中依然存在障碍.总之,未来高通量测序平台还需要进一步缩短二代测序平台构建文库的时间并提高三代测序平台的准确性.
尽管高通量测序平台面临着十分巨大的挑战,在实际应用过程中依然存在许多问题,然而高通量测序在临床微生物病原学检测、感染相关病原体的诊断、肿瘤学研究、白血病等重大疾病诊断以及遗传性疾病的检测等方面都已发挥了很大的作用,也为相关学科研究提供了新的思路与技术,有望在更多领域呈现更大的临床与研究价值.

