没食子酸与大米淀粉的相互作用
韩雪琴,黄立新,郝娟,贾栩超,刘磊*
(1.广东省农业科学院蚕业与农产品加工研究所,农业农村部功能食品重点实验室,广东省农产品加工重点实验室,广东广州 510610)(2.华南理工大学食品科学与工程学院,广东广州 510640)
多酚是一类天然抗氧化剂,广泛存在于谷物、水果和蔬菜等植物中,按结构大致可分为酚酸、黄酮、芪类、木脂素类化合物和多酚聚合物等[1]。没食子酸,化学名称为3,4,5-三羟基苯甲酸,是化学结构最简单的天然多酚类化合物。研究表明没食子酸对人体健康具有多种有益效果,例如可以降低患某些癌症、II型糖尿病、肥胖、心血管疾病等慢性疾病的风险[2,3]。没食子酸对人体健康产生的有益影响与它的抗炎、抗氧化、抗衰老等生物活性密切相关[4,5]。因此,没食子酸在开发功能性食品和营养品等方面具有广阔的前景。
淀粉是人类食物的主要成分,也是人类获取生命活动所需能量的主要来源,其在分子水平上由两种主要类型的α-葡聚糖组成:线性直链淀粉和支链淀粉。从不同植物来源分离得到的淀粉在组成、颗粒形态结构及理化性质方面存在很大的差异。淀粉的理化性质及其与其他食物成分的相互作用在很大程度上决定了食品的整体品质和营养特性。近年来,利用多酚与淀粉之间的相互作用来调控淀粉类食品的感官与营养品质成为研究热点[6]。Li等[7]研究发现咖啡酸可以显著降低马铃薯淀粉糊的粘度值;然而,He等[8]研究发现槲皮素显著增加了苦荞麦淀粉糊粘度值。Zhu等[9]研究发现从石榴皮中提取的多酚能显著增加小麦淀粉的糊化初始温度和峰值温度,而对糊化最终温度和糊化焓值无显著影响。Wu等[10]的研究发现,茶多酚可显著降低大米淀粉的糊化温度和糊化焓值,促进了淀粉的糊化。任顺成等人[11]发现小麦淀粉在加入芦丁或槲皮素前后,糊化温度变化不显著,但显著降低了淀粉的糊化焓值。这些研究表明不同的多酚类物质对淀粉理化特性的影响是不同的。此外,以上报道都缺乏对多酚与淀粉复合物的结构进行研究,未能明确多酚与淀粉之间的相互作用方式。没食子酸是谷物中常见的一种酚酸[12],具有良好的抗氧化活性。Zhu等[13]发现没食子酸可显著降低小麦淀粉糊化的峰值粘度,降低其最低粘度和终值粘度。任顺成等[14]研究发现没食子酸可降低玉米淀粉的糊化温度,并增大其糊化焓值。目前关于没食子酸与淀粉相互作用的研究主要集中在对淀粉理化特性的影响方面,淀粉的理化特性与其结构密切相关,因此关于没食子酸与淀粉的相互作用还有待深入研究。
大米淀粉作为大米的主要成分,因其具有独特的物理化学性质被广泛应用于食品工业中。本研究以大米淀粉为对象,分析没食子酸对大米淀粉理化性质、分子结构及晶体结构的影响,并揭示没食子酸与大米淀粉相互作用的关系,为没食子酸在淀粉基食品中的应用提供指导。
1 材料与方法
1.1 材料与试剂
大米淀粉(直链淀粉含量11.78%±0.02%,水分含量11.04%±0.02%),无锡泰花淀粉有限公司;没食子酸,上海源叶生物有限公司。
1.2 仪器与设备
GL224I型电子天平,塞多利斯科学仪器(北京)有限公司;电热鼓风干燥箱,上海-恒科学仪器有限公司;D-37520离心机,德国Thermo Fisher Scientific公司;DF-101型集热式恒温水浴锅,巩义市予华仪器有限责任公司;ST85B3-1冷冻干燥机,美国Milirock公司;PHS-3C精密pH计,上海仪电科学仪器股份有限公司;Starch Master2快速粘度测试仪,瑞典Perten公司;S-3400N扫描电子显微镜,日本HITACHI公司;AR1500EX流变仪,美国TA公司;DSC200F3差示扫描量热仪,德国NETZSCH公司;YQ105-6700傅里叶红外光谱仪,美国NICOLET公司;X-射线衍射仪,日本Rigaku公司。
1.3 方法
1.3.1 大米淀粉与没食子酸复合物及相应混合物的制备
称取样品3.0 g(干基)大米淀粉(RS)置于离心管中,向离心管中分别添加5%、10%、15%、20%(W/W淀粉干基)没食子酸(GA)并加入蒸馏水,使得样品总量为28 g。将淀粉样品经涡旋振荡混匀后,95 ℃恒温水浴中糊化20 min,糊化前5 min涡旋振荡混匀几次,冷却至室温后放入-80 ℃冰箱冷冻后冻干,粉碎,过100目筛,得到没食子酸与大米淀粉的复合物样品。淀粉和没食子酸的混合物可通过在实验前简单地将所需比例(10%W/W)的相应糊化冻干的大米淀粉和没食子酸混合而制得。
1.3.2 膨胀度与溶解度
参考Karunaratne等[15]方法并稍作改动测定大米淀粉的膨胀度与溶解度:准确称取淀粉150 mg(W0)置于离心管中,加入10 mL水并涡旋10 s。按比例加入没食子酸(5~20%,W/W)到各离心管中,并设置不加没食子酸的空白对照组。将离心管在85 ℃的条件下水浴30 min,每隔2 min涡旋混合。然后立即将离心管转移到冰水浴中冷却,以2000 ×g离心30 min,然后将上清液转移到小铝盒中。粘附在离心管壁物质被认为是沉积物,测量沉积物的重量(Ws)。将含有上清液的小铝盒置于105 ℃的烘箱中干燥直至恒重(W1)。由式(1)和(2)分别计算水溶性指数(WSI)和膨胀度:
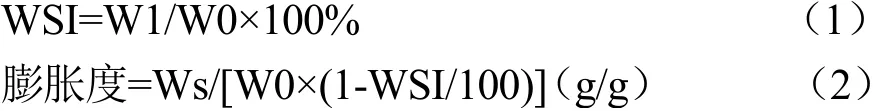
式中:
W1——上清液干燥至恒重后的质量,mg;
W0——称取的淀粉质量,mg;
Ws——离心后沉淀的质量,mg。
1.3.3 差式扫描量热分析
参考改进Xiao等[16]的方法进行测定:空钳锅作参比,样品量约3.0 mg,水样比为2:1,压盖密封,静置24 h,测试前在30 ℃下平衡2 min,温度范围30~90 ℃,速率10 ℃/min。记录初始温度To、峰值温度Tp、终止温度Tc,计算糊化焓值ΔH。
1.3.4 淀粉糊化性质的测定
参考Li等[7]方法并稍作改动测定大米淀粉糊化特性:取样品3.0 g(干基)淀粉置于测试用的铝筒内,分别添加5%、10%、15%、20%(W/W淀粉干基)没食子酸至铝筒内,并加入蒸馏水,使得样品总量为28 g。混合均匀,用pH计测定样品的pH值后置于RVA中测定粘度性质。搅拌器起始以960 r/min的转动速度进行转动,接着以160 r/min的转动速度旋转直至测定完成,测定一个样品耗时13 min。记录测定样品的糊化温度,峰值粘度(PV),热糊粘度(HPV,最低粘度)和50 ℃下的冷糊粘度(CPV,最终粘度),通过计算得到两个附加参数:崩解值(PV-HPV)和回生值(CPV-HPV)。
1.3.5 流变学特性的测定
实验采用平板-平板测量系统,平板直径为40 mm,平板间距1 mm。将淀粉样品经涡旋振荡混匀后加载到流变仪的板上,擦去平板外多余的淀粉乳,加上盖板,再在平板周围涂抹花生油,防止样品水分散失。静态与动态流变学实验条件参考Zhu等[14]的方法并稍作改动。
静态流变特性的测定:将5%淀粉乳液(70 mg淀粉+1.4 mL蒸馏水或70 mg淀粉+3.5、7、10.5、14 mg没食子酸+1.4 mL蒸馏水)在25 ℃的条件下平衡1 min。然后在剪切应力为5 Pa的条件下,温度以10 ℃/min的升温速率从25 ℃升至95 ℃,并从95 ℃降至25 ℃,此后将样品在25 ℃的条件下进行静态剪切流变实验。测量剪切速率从0.1~800 s-1递增(上行线),再从800~0.1 s-1递减(下行线)范围变化情况。采用Herschel-Bulkley方程(如下所示)对流变曲线进行模型拟合分析:

式中:
τ——剪切应力,Pa;
τ0——屈服应力,Pa;
K——稠度系数,Pa·sn;
γ——剪切速率,s-1;
n——流动特征指数,无量纲。
动态流变特性的测定:将制备的淀粉乳液(250 mg淀粉+1.25 mL蒸馏水或250 mg淀粉+12.5、25、37.5、50 mg没食子酸+1.25 mL蒸馏水)在25 ℃的条件下平衡1 min。在应变为2%,频率为1 Hz,温度为25 ℃的条件下平衡1 min,并在此条件下进行温度扫描实验。温度以2 ℃/min的升温速率从25 ℃升至95 ℃,后从95 ℃降至25 ℃,每个数量级取10个点,得到储能模量(G’)、损耗模量(G”)和损耗因子Tanδ(G”/G’)的变化趋势。进行温度扫描得到的淀粉凝胶在25 ℃的条件下平衡1 min后进行频率扫描实验。设置温度为25 ℃,应变为2%,扫描频率范围为0.1~20 Hz,每个数量级取10个点,得到储能模量(G’)、损耗模量(G”)和损耗因子Tanδ(G”/G’)随角频率的变化趋势。
1.3.6 傅里叶红外光谱分析
将1.3.1中的得到的样品,分别用玛瑙石研钵研磨,得到粉末样品,将样品和溴化钾放入玛瑙研钵中,再研磨混合均匀,压片,置于红外光谱仪在4000~400 cm-1波数范围进行扫描。用Omnic8.2软件对800~1200 cm-1范围内的谱图进行基线校准和去卷积处理。去卷积的峰宽为40 cm-1,增强因子为1.9。
1.3.7 X-射线衍射分析
将1.3.1中的得到的样品放到盘上,用玻片将样品压平,然后上机测试。测定条件:电压40 kV,电流30 mA,衍射角2θ扫描范围为4~40 °,扫描速度为0.164 °/s,步长0.013 °。
1.4 数据分析
在每次试验中均进行了3次平行试验,每个数据均为3次平行试验的平均值,使用Origin 9.0软件对数据进行处理,并使用SPSS 17.0软件对数据进行统计分析,没食子酸对大米淀粉理化特性的影响试验分析中采用最小显著差异(p<0.05)的方法。
2 结果与分析
2.1 溶解度与膨胀度分析
溶解度与膨胀度反应了淀粉与水相互作用力的大小。淀粉颗粒结构在加热过程中变得松动甚至崩解,从而使极性基团暴露与水分子通过氢键结合,直链淀粉和小的支链淀粉从膨胀的淀粉颗粒中溶出。从表1可以看出,淀粉溶解度随着没食子酸的增加而显著增大,当没食子酸添加量为20%时,大米淀粉的溶解度由5.98%增加至18.73%,这与Zhu等[15]的研究一致。淀粉溶解度的增加归因于淀粉与水分子相互作用的增强,没食子酸具有很多酚羟基,溶于水后能够与大米淀粉通过氢键结合,从而促进了淀粉的溶出,增加了其溶解度。没食子酸显著地降低了大米淀粉的pH值,当没食子酸的添加量为20%时,淀粉的pH值从7.09降低为2.71。没食子酸溶于水后pH值的降低也会对淀粉的溶解度产生影响[17]。
淀粉的膨胀特性实际为其糊化进程动力学,它包括淀粉的松弛、膨胀和收缩三个阶段[17]。从表1可以看出,没食子酸可抑制大米淀粉在加热过程中的膨胀,其添加量为5%时,大米淀粉的膨胀度从15.02%降至9.27%。没食子酸含有较多羟基,能够与水分子通过氢键发生相互作用,阻碍水分子的运动,从而抑制淀粉在加热过程中的吸水膨胀。没食子酸的加入显著地改变了体系的pH,pH值的改变可能限制了淀粉颗粒在水中的膨胀,降低了淀粉的膨胀度。郑学玲等[18]的研究表明:特定的小分子物质可和直链淀粉和支链淀粉的侧链形成稳定的络合物,从而限制颗粒的糊化膨胀。

表1 没食子酸对大米淀粉溶解度、膨胀度及pH值的影响Table 1 Effect of gallic acid on water solubility index, swelling power and pH of rice starch
2.2 热力学特性分析
没食子酸对大米淀粉糊化热力学特性的影响如表2所示。从表中可以看出,没食子酸对淀粉的糊化温度的影响显著,且与其添加量有关。当没食子酸的添加量为20%时,相比于原淀粉,其To、Tp和Tc值分别降低了20.39%、19.04%和15.43%。淀粉颗粒中,最不稳定的和最稳定的微晶熔融温度分别由To和Tc表示,实验结果表明没食子酸对大米淀粉不稳定和稳定微晶均产生了显著的影响。随着没食子酸含量的增加,大米淀粉的糊化焓值呈现先降低后增大的趋势,在没食子酸添加量为10%时,其糊化焓值为9.62 J/g,较原淀粉降低了23.59%。以上结果表明,添加没食子酸后,淀粉颗粒能够在较低的温度下发生膨胀糊化,说明没食子酸的添加降低了大米淀粉的热稳定性。

表2 没食子酸对大米淀粉糊化温度和焓值的影响Table 2 Effect of gallic acid on gelatinization temperatures and enthalpy of rice starch
在本实验中,添加没食子酸后,淀粉的糊化热力学特性发生了显著改变,主要有以下三方面原因。首先,没食子酸是多羟基化合物,可以与水分子相互作用并改变水溶液的pH和离子强度,从而改变淀粉颗粒的周围环境。有研究表明,pH值可显著影响淀粉的糊化过程中的热力学特性[19]。其次没食子酸溶解在水中的部分,会对淀粉-水体系产生干扰,酚羟基及羧基为其能够与淀粉-水基质的相互作用(氢键)提供了潜在的结合位点。溶解的没食子酸能与糊化过程中溶出的淀粉链发生相互作用(氢键,范德华力),与此同时也会与体系中的淀粉竞争水分子,限制了水分子的流动性,在一定程度上降低了淀粉颗粒的糊化程度,从而降低了淀粉的糊化焓值。而添加的未溶解的没食子酸,在有水的条件下会在60~70 ℃有熔融峰。当没食子酸的添加量为15%和20%时,未溶解的没食子酸产生的熔融峰与淀粉的糊化峰发生重叠,从而导致其糊化焓值的变大。此外,与多酚具有大量的羟基结构有关,这些亲水性的羟基可能与支链淀粉的侧链相互作用,并在不同程度上与淀粉颗粒的无定形区域结合,改变微晶区与无定形区之间的耦合力,使得淀粉颗粒发生变化,从而引起大米淀粉的糊化温度与焓值发生变化[9,16]。
2.3 糊化特性分析
没食子酸对大米淀粉粘度特性的影响如表3所示。从表中可以看出,随着没食子酸添加量的增加,大米淀粉混合体系的峰值粘度、成糊温度、最低粘度和终值粘度均显著降低。没食子酸添加量为20%时,大米淀粉的峰值粘度、成糊温度、最低粘度和终值粘度分别降低了7.13%、6.55%、43.76%和44.77%。与原淀粉相比,低添加量的没食子酸降低了淀粉的崩解值,随着添加量的增加,该值显著增加。随着没食子酸浓度的增大,大米淀粉的回生值显著降低(40.99%~46.05%)。

表3 没食子酸对大米淀粉糊化特性的影响Table 3 Effect of gallic acid on pasting properties of rice starch
淀粉峰值粘度反映大米淀粉的分子间力,崩解值(即抗剪切和耐热性能)反映淀粉糊的热稳定性[11]。没食子酸的添加减弱了大米淀粉的分子间力,使淀粉糊热稳定性降低,但随着添加量的增加,其热稳定性呈现上升趋势。这可能是由于溶解的没食子酸可与淀粉聚合物链相互作用,未溶解的没食子酸晶体进一步稀释淀粉基质,使淀粉相互作用的频率降低,从而减弱的淀粉的分子间作用力。同时减少了直链淀粉双螺旋状结构的交联缠绕,降低了糊状物在冷却过程中的粘度。回生值(最终粘度和最低粘度的差值)反映的是淀粉冷糊的稳定性,也是淀粉老化趋势的一个重要参数。在初期老化过程中,回生值的大小主要与直链淀粉分子的重结晶相关。随着没食子酸添加量的增加,大米淀粉的回生值显著减小。可能是由于多酚分子上有羟基,可通过氢键和范德华力等与淀粉分子的侧链形成复合物[13],复合物的形成抑制了淀粉的重结晶,延缓了淀粉的老化。此外,多酚的羟基会减少体系内淀粉颗粒可利用的自由水含量,阻碍淀粉分子的重新排布和缔合,从而起到抑制回生的作用。
2.4 流变特性分析
静态流变学是对样品施加线性增大或减少的稳态剪切速率,反映样品结构随剪切速率变化的规律。从图1可以看出,淀粉糊在流动中所需的剪切应力随剪切速率增大而增大,而在相同的剪切速率下,不同淀粉样品之间的剪切力存在显著性差异。没食子酸的添加显著降低了淀粉糊所需剪切应力,说明此时复合物体系在流动过程中需要的剪切应力也相应减小。

图1 没食子酸与大米淀粉混合体系静态流变学曲线Fig.1 Static rheological curves of gallic acid and rice starch mixtures
采用幂律方程(Herschel-Bulkley)对图1中各数据点进行回归拟合,结果见表4,由表可知,各样品的拟合系数R2均在0.99之上,表明该模型对曲线的拟合有较高的精度。流体指数n均小于1,说明添加没食子酸后淀粉糊在该剪切区域内均呈现典型的假塑性流体,具有剪切变稀性[20]。大米淀粉与没食子酸混合物的上行曲线中n值随着没食子酸浓度的增加有下降趋势,当没食子酸的浓度为20%时产生显著差异。而在下行线中,加入没食子酸后,n值显著增大。说明加入没食子酸的加入,对淀粉糊液上行和下行曲线流动流动指数的影响不同。K与增稠能力有关,K越大,增稠效果越好。加入低浓度没食子酸后,对淀粉糊的K值影响较小,不能达到增稠的目的。屈服应力(τ0)表示样品开始流动所需的最小应力,其值越大,说明要使淀粉糊发生流动所需的应力也越大。与原淀粉的屈服值相比,没食子酸的添加显著降低了大米淀粉的屈服值,随着添加浓度的增大,该值有增大趋势。可能是由于没食子酸降低了淀粉分子之间的交联,抑制了淀粉凝胶三维网状结构的形成,使其流动需要的剪切应力减小。由不同浓度的没食子酸对淀粉的静态流变学行为产生不同程度的影响,在实际生产中应该根据加工条件所需,选择没食子酸的添加量。

表4 没食子酸与大米淀粉混合溶液静态流变拟合参数Table 4 Herschel-Bulkley parameters for gallic acid and rice starch mixtures
动态流变学提供了有关淀粉体系在加热和冷却过程中的弹性和粘性行为的信息。动态流变学可通过储存模量G’、损耗模量G”与损耗角正切tanδ(G”/G’)来表征。通过对动态流变的分析,得到部分特征值,结果如表5所示。相比于原淀粉G’max值(2694.50),没食子酸的添加显著降低了淀粉凝胶的G'max值,并具有浓度依赖性。说明随着没食子酸的添加,淀粉分子之间相互作用减弱,阻碍了淀粉凝胶网络结构的形成,其凝胶体系弹性降低。当温度进一步升高至95 ℃时,淀粉凝胶的储存模量降低,可能是由于继续升温会导致淀粉颗粒进一步破裂和崩解,并使溶胀的淀粉颗粒中残留的结晶区域完全融化,同时流变测量过程中的剪切应力也可能导致淀粉糊状网络的断裂,使凝胶网络结构减弱;而温度的逐渐升高也加剧了分子的布朗运动,导致分子间间距增大,从而使链段更容易活动,从而使淀粉凝胶的弹性模量降低[21]。当没食子酸的添加量为5%~20%时,G’95℃值在248.20~53.72范围内,添加没食子酸显著降低了淀粉的储能模量(G’95℃)。可能是由于没食子酸的添加减少了淀粉糊体系结构内部的直链淀粉分子链间的缠结点,从而削弱了淀粉凝胶体系的网络结构,使得体系对加热更敏感。当温度逐渐降低后,淀粉的G’值开始上升,这可归因于溶胀颗粒释放出的直链淀粉链分子间的重新排列[22]。而没食子酸的添加降低了淀粉糊的G’25℃值,说明没食子酸抑制了淀粉分子间的重新排列。tanδ是G”与G’的比值,tanδ越大,体系的粘性比例越大,可流动性强,反之则弹性比例较大。在整个升温与降温的过程中,tanδ的值都小于1,淀粉与多酚形成的凝胶表现出一种典型的弱凝胶动态流变学特性。综上可知,没食子酸的添加,能对凝胶结构产生破坏作用。

表5 没食子酸与大米淀粉混合体系的动态流变特性Fig.5 Dynamic rheological properties of gallic acid and rice starch mixtures
在0.1~20 Hz范围对淀粉凝胶进行动态频率扫描,以进一步探究没食子酸对淀粉凝胶的粘弹性的影响。当振荡频率为20 Hz时,原淀粉的G’值为1103.50 Pa,当没食子酸的添加量为20%时,G’值降低了89.46%。说明添加没食子酸后的凝胶体系的稳定性变差,易受频率的影响。可能是由于没食子酸的加入,延缓了淀粉链之间的相互交联,从而削弱了淀粉凝胶体系的网络结构。在测量过程中所有样品的G”远小于G’,说明淀粉体系弹性占主导位置。没食子酸的添加,显著升高了淀粉凝胶的tanδ20Hz值,体系的粘性比例增大,可流动性增强,使体系更具有流体性质。
2.5 傅里叶红外光谱分析
在FT-IR图谱上,不同的化学键在不同的波长位置有相对应的吸收峰。可以通过光谱上特征吸收峰的变化来判断相应化学键的变化,从而研究淀粉及淀粉-没食子酸复合物光谱之间的差异性,用于指示复合时化学结构的变化。没食子酸表现出典型的酚类特征,在3200~3550 cm-1处的特征峰为苯环上-OH的伸缩振动。在1365 cm-1处是-OH的平面弯曲振动,在1450~1600 cm-1处是苯环C=C的伸缩振动,在1200~1300 cm-1范围内是C-O和C-C的伸缩振动[23]。
图2 为淀粉、没食子酸与大米淀粉混合物及复合物的红外光谱图,淀粉样品在3382 cm-1附近有一个极强且宽的吸收峰,主要是O-H键伸缩振动吸收;其它的吸收峰也都与淀粉有相同的归属[24]。与原淀粉相比,没食子酸与淀粉的复合物在1536、1450 cm-1出现吸收峰,可能是由于没食子酸的苯环C=C伸缩振动。而相比于原淀粉和物理混合的样品,没食子酸(添加量10%以上)与大米淀粉的复合物在1676 cm-1处产生弱吸收峰,说明可能发生了相互作用。从图中可以看出随着没食子酸浓度的增大,在3384 cm-1附近的吸收峰强度减小,说明羟基的数量减少,由此推测没食子酸与淀粉主要通过氢键发生相互作用。1045 cm-1附近的吸收峰是淀粉结晶区的结构特征,对应于淀粉聚集态结构中的有序结构;1022 cm-1附近的吸收峰则是淀粉非晶区的结构特征,对应于淀粉大分子的无规线团结构。(1045/1022) cm-1的峰强度比值,被看作是淀粉有序结构的指标,其比值越大,有序度越高[25]。其比值计算结果如表6所示,从表中可以看出,复合物的比值比原淀粉小,并且随着浓度的增大,其比值变小。由此可以看出,随着没食子酸浓度的增大,淀粉结晶区的结构特征逐渐减弱,而非晶区的结构特征逐渐增强,淀粉的有序结构降低。研究结果与王晨等[26]一致。

图2 没食子酸-大米淀粉复和物的红外光谱图Fig.2 Infrared spectra of rice starch and gallic acid complexes

表6 复合物FT-IR去卷积波谱的1047与1022 cm-1的峰强度比值比较Table 6 The ratios of the absorbance of the bands at 1047 cm-1/1022 cm-1 for deconvoluted FT-IR spectra of complexes
2.6 X-射线衍射分析
没食子酸在衍射角为8.0、16.1、19.0、25.2、27.5、32.6 °处有较强的衍射峰[27]。天然大米淀粉在衍射角为15.0、17.0、17.9、22.8 °处有较强吸收峰,属于典型的A型结晶结构[28]。在淀粉糊化后观察到淀粉衍射峰发生了显著变化,其在2θ为17、20 °时出现衍射峰,说明大米淀粉糊化后结晶型由A型变为B+V型。且淀粉原有的尖锐的特征峰变成了相对平坦的“馒头峰”,淀粉结晶度显著降低,说明淀粉的结晶结构消失,呈无定形态。
从图3可以看出,没食子酸与大米淀粉经过混合后在8.0、16、19.1、25.3、27.7 °处出现了没食子酸的衍射峰,但在复合物中并没有观察到相应的衍射峰。且复合物在12.7 °处出现衍射峰,可能是由于没食子酸的溶解性较好,能与淀粉发生相互作用,从而形成了特殊的晶体结构。在大米淀粉与没食子酸复合物的衍射峰中并未观察到V型复合物相关特征衍射峰(7.0、13.1、20.0 °),可能是由于对于直链淀粉螺旋腔来说,没食子酸可能不具有足够的疏水性,且溶解的没食子酸和淀粉链之间主要通过氢键发生相互作用,与红外研究结果一致。

图3 没食子酸-大米淀粉复合物的衍射图Fig.3 Diffraction of rice starch and gallic acid complexes
3 结论
没食子酸增加了淀粉的溶解度,而限制了大米淀粉在加热过程中的吸水膨胀,说明没食子酸改变了淀粉与水之间的相互作用。没食子酸显著降低大米淀粉糊化温度及糊化焓值,说明没食子酸的添加能够促进大米淀粉的糊化。RVA表明添加没食子酸降低了大米淀粉的峰值粘度、最低粘度和最终粘度值及回生值,说明没食子酸抑制了大米淀粉的老化进程。流变学实验表明添加没食子酸后淀粉糊呈现典型的假塑性流体,具有剪切变稀性,并降低了淀粉在升温过程中的储存模量和损耗模量值。说明淀粉分子之间相互作用减弱,没食子酸阻碍了淀粉凝胶网络结构的形成,其凝胶体系粘弹性降低。红外光谱表明没食子酸与淀粉的复合物在1676 cm-1出现新的吸收峰,X-衍射图谱也表明,没食子酸与淀粉复合物在2θ=12.7 °产生小的结晶峰,说明大米淀粉与没食子酸发生了相互作用。没食子酸与淀粉复合物在3382 cm-1附近的吸收峰强度减小,表明没食子酸与淀粉主要通过氢键发生相互作用。添加没食子酸后大米淀粉(1045/1022) cm-1峰强度比值减小,说明大米淀粉有序性降低。因此,本研究可为淀粉类产品的改性及没食子酸在淀粉基功能性食品中的应用提供科学依据。

