高活性晶面锐钛矿型TiO2纳米材料的溶剂热法制备及其光催化性能
杜意恩 牛宪军 李万喜 高淑雅 李玉梅
(1晋中学院化学化工系,晋中 030619)
(2新疆工程学院化学与环境工程学院,乌鲁木齐 830023)
0 引 言
近年来,设计和合成具有特定形貌和高活性晶面暴露的无机半导体纳米材料受到了研究者的广泛关注[1]。在各种半导体材料中,二氧化钛(TiO2)作为一种宽禁带半导体,因具有生物和化学惰性、成本低、光生空穴的氧化能力强以及对光化学腐蚀的长期稳定性等优点,被认为是最有前途的光催化剂之一[2-3]。因此,TiO2被广泛用在光催化剂[4]、太阳能电池[5]、锂离子电池[6]、传感器[7]等领域。然而,就实际应用而言,TiO2的光催化效率还需要进一步提高。在自然界中,TiO2主要有锐钛矿型(空间群:I41/amd)、金红石型(空间群:P42/mnm)和板钛矿型(空间群:Pbca)3种晶体结构,其中锐钛矿型TiO2被认为是催化活性最高的催化剂[8]。锐钛矿型TiO2的光催化性能主要由其粒径、比表面积、结晶性、形貌和暴露晶面等因素决定[9]。一般来说,粒径越小、比表面积越大、结晶性越好和暴露晶面能量越高,锐钛矿型TiO2的光催化性能就越优越。对于锐钛矿型TiO2,平均表面能由低到高的顺序为{101}晶面(0.44 J·m-2)<{010}和{100}晶面(0.54 J·m-2)<{001}晶面(0.90 J·m-2)<{111}晶面(1.60 J·m-2)[10-11]。然而,在晶体生长过程中,具有高表面能的晶面通常会迅速减少,以使表面能最小。因此,在平衡条件下,锐钛矿型TiO2晶体是由等腰梯形组成的8个{101}晶面和平面正方形组成的2个{001}晶面构成的截头八面体[12]。鉴于此,在过去的十多年里,研究者在设计、合成具有特定形貌和高暴露活性晶面的锐钛矿型TiO2方面做出了大量的努力。自从Wen等[13]首次报道(010)晶面暴露的锐钛矿型TiO2纳米晶以来,晶面对锐钛矿型TiO2光催化活性的影响已被广泛研究。例如,Yang等[14]以TiF4为钛源,HF为形貌控制剂,通过溶剂热法制备了暴露64% {001}晶面的锐钛矿型TiO2纳米片,该纳米片的光反应活性是商业化P25的5倍。Sun等[15]以钛酸四丁酯为钛源,以乙酸和N,N-二甲基甲酰胺为形貌控制剂,通过溶剂热法制备了暴露{001}晶面的菱形状锐钛矿型TiO2纳米片,与商业化锐钛矿TiO2相比,该纳米片在降解甲基橙过程中表现出了优越的光催化活性。Liu等[16]以钛粉末为钛源,以HF和H2O2为形貌控制剂,通过水热法制备了暴露75% {001}晶面的方块体状锐钛矿型TiO2纳米片,该纳米片在降解亚甲基蓝过程中的光催化活性是商业化P25的4倍。Zhao等[17]以四异丙醇钛为钛源,以丙三醇和异丙醇为溶剂,通过溶剂热法制备了由暴露{010}晶面纳米带组成的多孔锐钛矿型TiO2微米球,该微米球是一种有效的光催化剂,其催化活性是商业化P25的2倍多。Chen等[18]以纤铁矿型层状钛酸盐K0.80Li0.27Ti1.73O4获得的H1.07Ti1.73O4纳米片胶态溶液为前驱体,通过常规水热法或微波法制备了主要暴露{010}晶面的不同形貌锐钛矿型TiO2纳米晶,与商业化P25和ST20相比,这些纳米晶在染料敏化太阳能电池中显示了优越的光伏性能。近年来,我们课题组以层状钛酸盐K2Ti4O9、Li2TiO3、Na2Ti3O7等为钛源,在存在或缺少形貌控制剂的条件下,通过水热法制备了主要暴露{010}、{001}、[111]-晶面或几个晶面共暴露的不同形貌锐钛矿型TiO2纳米晶,这些纳米晶在光催化降解有机染料过程中显示出了优越的光催化性能[19-22]。
我们采用溶剂热法制备高活性晶面锐钛矿型TiO2纳米材料,通过多种表征手段对其结构、形貌、孔径分布、光学性质、载流子的迁移和重组速率等进行表征,以罗丹明B和对硝基苯酚为目标降解物来评价其光催化性能,并对其循环性能进行了探讨。
1 实验部分
1.1 试剂与仪器
试剂包括:钛酸四丁酯(AR,天津市大茂化学试剂厂)、无水乙醇(AR,天津市科密欧化学试剂有限公司)、甲酸(AR,北京化工厂)、罗丹明B(AR,北京化工厂)、乙酸(AR,天津市天新精细化工开发中心)、氢氟酸(40%,天津市永大化学试剂有限公司)、三乙胺(AR,天津市申泰化学试剂有限公司)、氟化铵(AR,天津市永大化学试剂有限公司)、聚乙二醇600(AR,上海化学试剂采购供应经销站)、氢氧化钠(AR,天津市恒兴化学试剂制造有限公司)、二氧化钛(AR,天津市博迪化工有限公司,标记为BD-TiO2)、蛋清(直接从鸡蛋中获取)。
仪器包括:电热恒温鼓风干燥箱(HGZE-Ⅱ/H-101-1型,上海跃进医疗器械有限公司)、磁力加热搅拌器(HJ-4型,金坛市城西峥嵘实验仪器厂)、箱式高温烧结炉(KSL-1400X-A1型,合肥科晶材料技术有限公司)、电子天平(ESJ200-4型,沈阳龙腾电子有限公司)、超声波清洗器(JP-020型,深圳市洁盟清洗设备有限公司)、紫外可见分光光度计(TU-1901型,北京普析通用仪器有限责任公司)、高速台式离心机(SC-3616型,湘仪离心机仪器有限公司)、紫外线UV固化灯(A-250型,上海铭耀玻璃五金工具厂)、循环水真空泵(SHZ-D(Ⅲ)型,河南巩义市予华仪器有限责任公司)、X射线粉末衍射仪(XRD,XRD-6100型,日本岛津株式会社,Cu靶Kα辐射,λ=0.154 18 nm,工作电压40 kV,工作电流30mA,扫描范围5°~80°,扫描 速 度 8(°)·min-1)、场 发 射 扫 描 电 子 显 微 镜(FESEM,REGULUS-8100型,日本日立高新技术株式会社,加速电压5.0 kV,工作电流10μA)、透射电子显微镜(TEM,JEM-2100F型,日本JEOL株式会社,加速电压200 kV)、全自动比表面积和孔隙度分析仪(ASAP-2020型,美国麦克仪器公司)、荧光光谱仪(HORIBA FlUOROMAX-4型,美国HORIBA科学仪器事业部(Jobin Yvon光谱技术)堀场)、电化学阻抗谱分析仪(EIS,CHI660E,上海成华仪器有限公司)、紫外可见近红外分光光度计(UV-Vis-NIR,Cary-5000型,安捷伦科技有限公司)。
1.2 制备过程
室温条件下,将20mL无水乙醇、20mL钛酸四丁酯、2mL蛋清、1mL聚乙二醇600依次加入到标号为1、2、3、4、5、6的6个聚四氟乙烯反应釜中,放置在磁力搅拌器上搅拌使其混合均匀(加入2mL蛋清是为了增加所合成样品的比表面积,加入1mL聚乙二醇600是为了增加蛋清在钛酸四丁酯乙醇溶液中的分散性)。然后分别量取甲酸(formic acid,FA)、乙酸(ethanoic acid,HAc)、氢氟酸(hydrofluoric acid,HF)、三乙胺(triethylamine,TEA)各2mL作为形貌控制剂,滴加至标号为1、2、3、4的4个反应釜中;称取0.508 0 g氟化铵(ammonium fluoride,NH4F)固体加入标号为5的反应釜中;标号为6的反应釜中不再加入任何形貌控制剂。6个反应釜中溶液搅拌均匀之后,密封,放入恒温鼓风干燥箱中,将温度设置为180℃,反应24 h,自然冷却至室温后抽滤。然后将抽滤得到的样品干燥后,放入高温箱式烧结炉中560℃加热4 h,降到室温后,取出研磨,得到的产品分别标记为 FA-TiO2、HAc-TiO2、HF-TiO2、TEA-TiO2、NH4F-TiO2和 NO-TiO2,然后装袋。
1.3 光催化性能测试
称量0.021 1 g罗丹明B(或对硝基苯酚)放入50 m L小烧杯中,向其中加入适量去离子水,并用玻璃棒搅拌使其溶解。将小烧杯中的溶液转移到2 L容量瓶中,用去离子水洗涤小烧杯3次,洗涤液也转移到容量瓶中,然后加蒸馏水稀释到刻度线,定容,摇匀。分别称取FA-TiO2、HAc-TiO2、HF-TiO2和NO-TiO2各0.075 g,加入到4个250mL烧杯中,并取相同质量的BD-TiO2及NO-TiO2进行对照。分别向其中加入上述所配制的罗丹明B溶液150mL,将其放置在磁力搅拌器上,搅拌均匀,在密闭黑暗的环境中静置储存48 h,以达到吸附-脱附平衡。然后取上层清液5mL于离心管(6mL)中保存备用,将剩下的试液以一定速率进行磁力搅拌,待均匀后置于UV固化灯下(波长为365 nm)进行UV照射,UV灯距离烧杯中溶液液面的距离约为30 cm。每反应15min取5 mL悬浮液,离心分离,去除TiO2晶体。降解率由光催化实验前后罗丹明B溶液(或对硝基苯酚溶液)的浓度变化确定:,式中,c0是暗吸附结束后光照开始时罗丹明B溶液(或对硝基苯酚溶液)的浓度,ct是光照一段时间后罗丹明B溶液(或对硝基苯酚溶液)的浓度。通过对上述相同浓度的罗丹明B溶液进行第2次和第3次降解实验,考察了所制备的TiO2催化剂的稳定性和循环利用性。
2 结果与讨论
2.1 XRD分析
图1为存在和缺少控制剂时通过溶剂热法制备的TiO2和商业化BD-TiO2样品的XRD图。从XRD图中可以看出,当甲酸、乙酸、氢氟酸和无控制剂存在时所制备的 FA-TiO2、HAc-TiO2、HF-TiO2和 NOTiO2样品都是锐钛矿型TiO2(PDF No.21-1272,四方晶系,空间群:I41/amd),其在 2θ=25.50°、37.10°、38.08°、48.26°、54.26°、55.34°、63.08°、68.80°、70.58°和 75.46°处的衍射峰分别对应于(101)、(004)、(112)、(200)、(105)、(211)、(204)、(116)、(220)和(215)晶面。其中,(101)晶面衍射峰强度增强的顺序为HF-TiO2>FA-TiO2>HAc-TiO2>NO-TiO2,表明以氢氟酸为形貌控制剂时所合成的HF-TiO2样品的颗粒尺寸最大,结晶性最好。根据锐钛矿型TiO2的(101)和(116)晶面计算出的晶面间距略有不同,FA-TiO2和HAc-TiO2的衍射峰向高角度(低晶面间距)稍微偏移,这是由于甲酸和乙酸的引入导致晶格间距减小。
从图1中还可以看出,当以三乙胺和氟化铵为形貌控制剂时,得到的TEA-TiO2和NH4F-TiO2不是纯相,除锐钛矿型TiO2外,还有其他不确定相。图1g是商业化BD-TiO2的XRD图,从图中可以看出,BD-TiO2为锐钛矿和金红石的混合相,其中锐钛矿型TiO2的比例为 96.83% (主晶相),金红石型 TiO2的比例为3.17% (次晶相)[22]。上述分析表明,形貌控制剂对产品的合成具有重要的影响,在合成TiO2时,只有选择合适的试剂,才能合成出所需要的产品。因此,我们仅对制备的纯相锐钛矿型TiO2进行研究,而不对非纯相TEA-TiO2和NH4F-TiO2样品进行研究。

图1 (a~e)存在和(f)不存在控制剂时制备的TiO2及(g)商业化BD-TiO2的XRD图Fig.1 XRD patterns of TiO2prepared in the(a~e)presence and(f)absence of capping agent and(g)commercial BD-TiO2
2.2 FESEM和HRTEM分析
图2是在形貌控制剂甲酸、乙酸和氢氟酸存在下以及无控制剂存在时所合成的锐钛矿型TiO2样品的形貌。从图2a~2c中可以看出,当存在形貌控制剂时,所制备的TiO2样品是由方块状、菱形六面体状、近似球状和不规则形状等多种形貌的纳米颗粒组成的,其中以立方体状和长方体状为主。对于FA-TiO2、HAc-TiO2和 HF-TiO2样品,利用粒径分布计算软件测得150个纳米粒子的颗粒尺寸范围分别为12.4~23.7 nm、12.5~33.7 nm、13.9~39.9 nm,平均粒径分别为20.9、20.6、23.9 nm。由此可见,在不同形貌控制剂存在下,所制备的锐钛矿型TiO2的粒径大小不均匀且颗粒发生了显著的团聚,这是由于纳米颗粒的表面活性高以及纳米颗粒间存在非常强的吸引力[23]。对于制备的NO-TiO2样品,尽管也存在很多纳米颗粒(12.0~24.0 nm,平均粒径22.1 nm),然而这些纳米粒子的结晶性非常差,且团聚现象更加严重,除此之外,还存在一些长度范围为190~465 nm的大颗粒,如图2d所示。商业化BD-TiO2主要是由方块状、截头四角双锥状、球状和其他形状的纳米颗粒组成的,纳米颗粒的粒径范围为32.7~100.9 nm,平均粒径为60.7 nm,且这些颗粒团聚成蘑菇云状,如图2e所示。
利用能谱仪测定的不同锐钛矿型TiO2样品中各元素的原子分数如表1所示。从表1可以看出,商业化BD-TiO2中仅含有Ti和O两种元素;而对于所合成的 FA-TiO2、HAc-TiO2和 NO-TiO2样品,除了Ti和O两种元素外,还含有来自蛋清的C和Na元素。对于HF-TiO2,除了Ti、O、C、Na四种元素外,还含有F元素,这是F-离子钝化在晶面上难以除去造成的[24]。
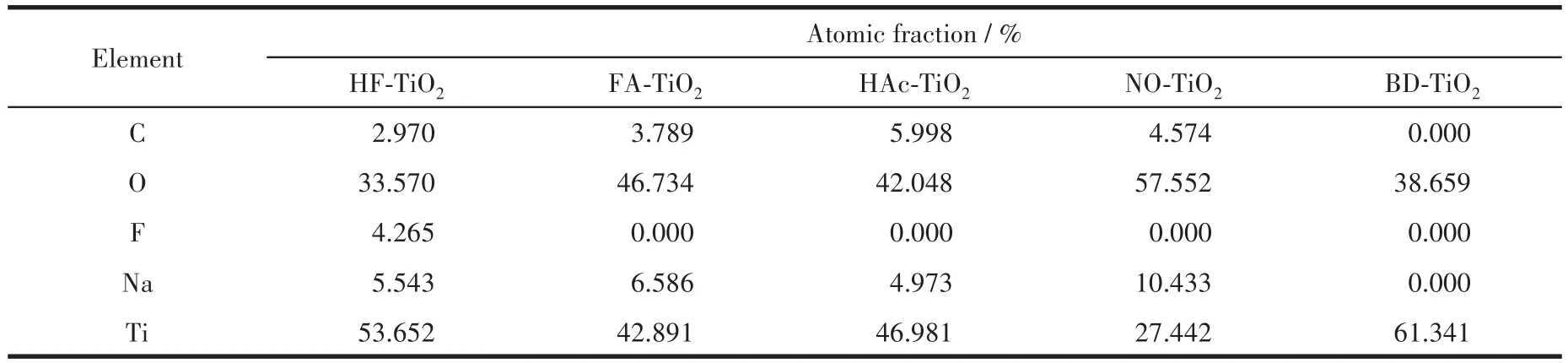
表1 利用能谱仪测定的TiO2样品中各元素的原子分数Table 1 Atomic fraction of each element in different TiO 2 samples determined by energy dispersive analysis spectrometer
HRTEM图进一步证实了所制备的TiO2具有典型的单晶性质,如图3和4所示。对于FA-TiO2样品,在方块状晶体的上表面观察到晶面间距皆为0.350 nm的2组晶格条纹,二者之间的夹角为82°(图3a),与热力学稳定的锐钛矿型 TiO2的(101)和(011)晶面以及二者之间的夹角吻合得较好[23]。由于2组晶格条纹分别平行于方块状晶体的侧面,因此,方块状晶体的4个侧面和上下表面暴露的晶面分别是{101}晶面和垂直于[111]-晶带轴的晶面(标记为[111]-晶面)。在菱形六面体状晶体的上表面观察到晶面间距为0.350和0.240 nm的2组晶格条纹,分别对应于锐钛矿型TiO2的(101)和(004)晶面,且二者之间的夹角为68.3°,表明菱形六面体状晶体的上下表面暴露{010}晶面(图3a)。从图3b中可以看出,在类似方块状晶体的上表面观察到晶面间距为0.350和0.171 nm的2组晶格条纹,分别对应于锐钛矿型TiO2(101)晶面和(105)晶面,且二者之间的夹角为85°,表明类似方块状晶体的上下表面暴露{010}晶面。图3b中,晶面间距为0.343 nm的晶格条纹对应于锐钛矿型TiO2的(101)晶面。

图3 (a、b)FA-TiO2和(c、d)HAc-TiO2的HRTEM图Fig.3 HRTEM images of(a,b)FA-TiO2and(c,d)HAc-TiO2

图4 (a、b)HF-TiO2和(c、d)NO-TiO2的HRTEM图Fig.4 HRTEM images of(a,b)HF-TiO2and(c,d)NO-TiO2
对于HAc-TiO2样品,在方块状晶体的上表面观察到晶面间距皆为0.350 nm(或0.347或0.349 nm)的2组晶格条纹,二者之间的夹角为82°,且2组晶格条纹分别平行于方块状晶体的侧面,如图3c、3d所示,表明方块状晶体的4个侧面和上下表面暴露的分别是{101}晶面和[111]-晶面。方块状晶体暴露[111]-晶面可通过快速傅里叶变换进一步确定,如图3d中插图所示。
对于HF-TiO2样品,在不规则状晶体的上表面观察到晶面间距为0.349和0.236 nm的2组晶格条纹,分别对应于锐钛矿型TiO2的(101)和(004)晶面,且二者之间的夹角为68.3°(图4a),表明不规则状晶体的上下表面暴露{010}晶面。利用快速傅里叶变换进一步确定不规则状晶体暴露的是{010}晶面,如图4a中插图所示。在方块状晶体的上表面观察到晶面间距为0.349 nm的一组晶格条纹,对应于锐钛矿型TiO2(101)晶面,且该组条纹平行于方块状晶体的一组侧面,表明方块状晶体的一组侧面暴露的是{101}晶面(图4a)。从图4b可以看出,在方块状晶体的上表面观察到晶面间距为0.354和0.354 nm的2组晶格条纹,分别对应锐钛矿型TiO2的(101)和(011)晶面,且二者之间的夹角为82°,表明方块状晶体的上下表面和4个侧面分别暴露[111]-晶面和{101}晶面。此外,在图4b中,还观察到晶面间距为0.347 nm(或0.354 nm)的晶格条纹,对应于锐钛矿型TiO2的(101)晶面。
对于NO-TiO2样品,从图4c可以看出,在方块状晶体的上表面观察到晶面间距为0.353 nm的2组晶格条纹,对应于锐钛矿型TiO2(101)和(011)晶面,且该组条纹平行于方块状晶体的4个侧面,表明方块状晶体的4个侧面和上下表面分别暴露的是{101}晶面和[111]-晶面。同时,在图4c中还观察到晶面间距为0.351和0.354 nm的晶格条纹,均对应{101}晶面。从图4d可以看出,晶面间距为0.351 nm的晶格条纹对应{101}晶面(或{011}晶面),表明方块状晶体的4个侧面和上下表面暴露的是{101}晶面和[111]-晶面。
2.3 N2吸附-脱附分析
所制备的 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化BD-TiO2纳米颗粒的N2吸附-脱附等温线和计算得到的孔径分布(Barrett-Joyner-Halenda法)和比表面积(Brunauer-Emmett-Teller法)数据如图5和表2所示。从图5a中可以看出,所制备的TiO2纳米材料和商业化BD-TiO2纳米材料的吸附-脱附等温线都属于Ⅳ型(BDDT分类)[25],其中FA-TiO2、HAc-TiO2和NO-TiO2具有典型的H2回滞环(介孔材料),HF-TiO2具有典型的H1回滞环(多孔材料),而BD-TiO2具有典型的H3回滞环(由于纳米颗粒的聚集而形成的狭窄的裂隙状空隙)。从图5b和表2中可以看出,孔径分布由窄到宽的顺序为HAc-TiO2<FA-TiO2<NO-TiO2<BD-TiO2<HF-TiO2。从表2可知,FA-TiO2纳米颗粒具有最大的比表面积,分别是HAc-TiO2、HF-TiO2、NO-TiO2和 BD-TiO2纳米颗粒的 1.07倍、1.16倍、2.83倍和10.82倍。可以看出,形貌控制剂的加入有利于增加所合成TiO2的比表面积,而比表面积的增加有利于在TiO2纳米颗粒表面吸附更多的罗丹明B或对硝基苯酚分子,从而促进光催化活性的提高。
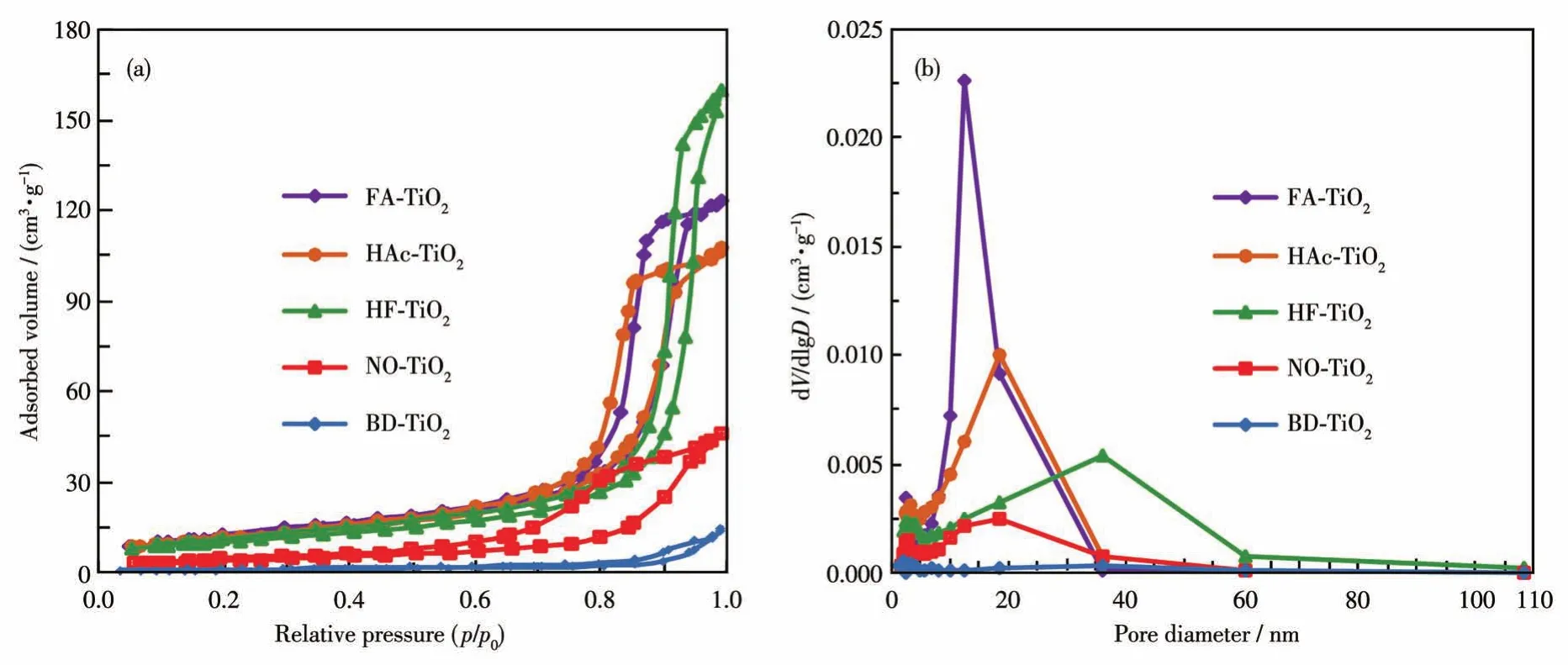
图5 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化BD-TiO2的(a)N2吸附-脱附等温线和(b)孔径分布Fig.5 (a)N2adsorption-desorption isotherms and(b)pore size distributions of FA-TiO2,HAc-TiO2,HF-TiO2,NO-TiO2,and commercial BD-TiO2

表2 样品的孔径、孔体积和比表面积参数Table 2 Pore size,pore volume and specific surface area(SBET)parameters of the samples
2.4 UV-Vis-NIR光谱分析
通过UV-Vis-NIR光谱分析了FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化 BD-TiO2的光吸附性能。与商业化BD-TiO2不同(阈值约为425 nm),所制备的 FA-TiO2、HAc-TiO2、HF-TiO2和 NO-TiO2样品都显示出几乎相同的固有吸收边缘,其吸收边缘明显向短波长移动(即发生蓝移)[26],阈值约为400 nm(图6),表明是否存在形貌控制剂或控制剂的种类并不影响所合成的锐钛矿型TiO2的内部结构。对于所制备的TiO2样品,在紫外光区光吸收强度增加的顺序为 HF-TiO2>FA-TiO2>HAc-TiO2>NO-TiO2>BD-TiO2,而在可见光区光吸收强度几乎完全相同。BD-TiO2样品在紫外光区的光吸收强度最小,而在可见光区的光吸收强度最大,可能与BD-TiO2是锐钛矿型TiO2和金红石型TiO2混合相有关。
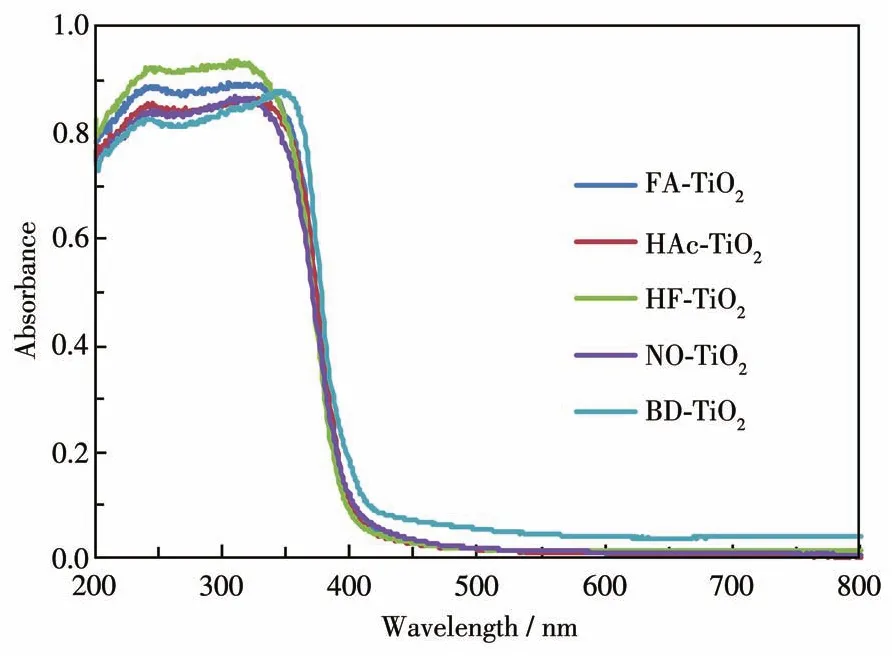
图6 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化BD-TiO2的UV-Vis-NIR谱图Fig.6 UV-Vis-NIR spectra of FA-TiO2,HAc-TiO2,HF-TiO2,NO-TiO2,and commercial BD-TiO2
2.5 光致发光光谱分析
光致发光光谱能够揭示光催化剂中载流子(电子和空穴)的迁移和缺陷的形成,有助于了解载流子在光催化剂表面的重组速率[27]。图7为制备的FATiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化 BD-TiO2在320 nm激发下的光致发光光谱,可以看出,所有样品的光致发光光谱曲线基本一致。TiO2样品的稳态荧光光谱在 398、408、437、449、468、481、492和553 nm处有强烈的发射峰。在398 nm处的第一个发射峰归因于锐钛矿型TiO2带-带光致发光过程中的发射,而其他的所有发射峰归因于迁移到TiO2表面的载流子的强烈重组[28-29]。从图7中可以看出,光致发光光谱强度增加的顺序为NO-TiO2>BD-TiO2>HAc-TiO2>FA-TiO2>HF-TiO2。HF-TiO2的光致发光强度最低,表明{101}/{010}/[111]-晶面共存以及较高结晶度和较大比表面积的协同作用有利于抑制光生电子-光生空穴的复合,从而有利于光生载流子的寿命延长和光催化性能的提高[28,30]。与此相反,NO-TiO2的光致发光强度最高,表明光生载流子的复合率最高,光催化性能最低。
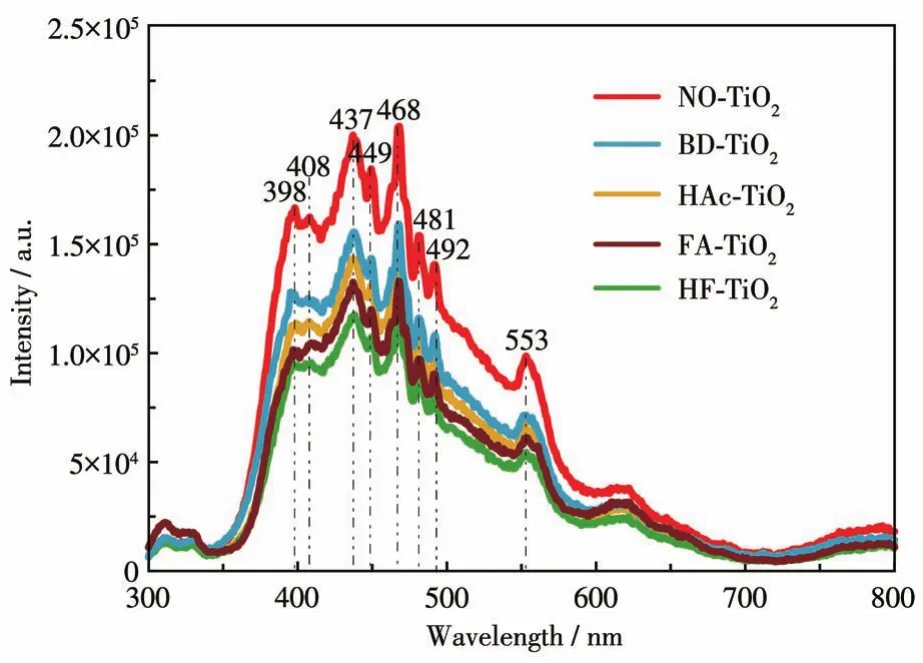
图7 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化BD-TiO2的光致发光光谱图Fig.7 Photoluminescence spectra of FA-TiO2,HAc-TiO2,HF-TiO2,NO-TiO2,and commercial BD-TiO2
2.6 电化学阻抗分析
电化学阻抗谱测试被认为是研究光催化反应中电子传递和重组的一种强有力的技术。图8是在0.1 Hz~0.1MHz频率范围内,交流振幅为0.01 V时得到的不同TiO2样品的Nyquist谱图。一般而言,Nyquist谱图弧半径越小,电荷转移电阻越小,电荷在电解液与半导体界面处的转移越快[31-33]。HF-TiO2的Nyquist谱图在高频率下呈现半圆形,说明在界面处的电荷转移电阻较低、复合电阻较小、电极表面电荷转移效率较高。与HF-TiO2相比,FA-TiO2和HAc-TiO2(或 NO-TiO2和 BD-TiO2)的 Nyquist谱图呈现相似的变化趋势,并且在高频率下没有呈现半圆形,表明其电子-空穴分离效率较低。
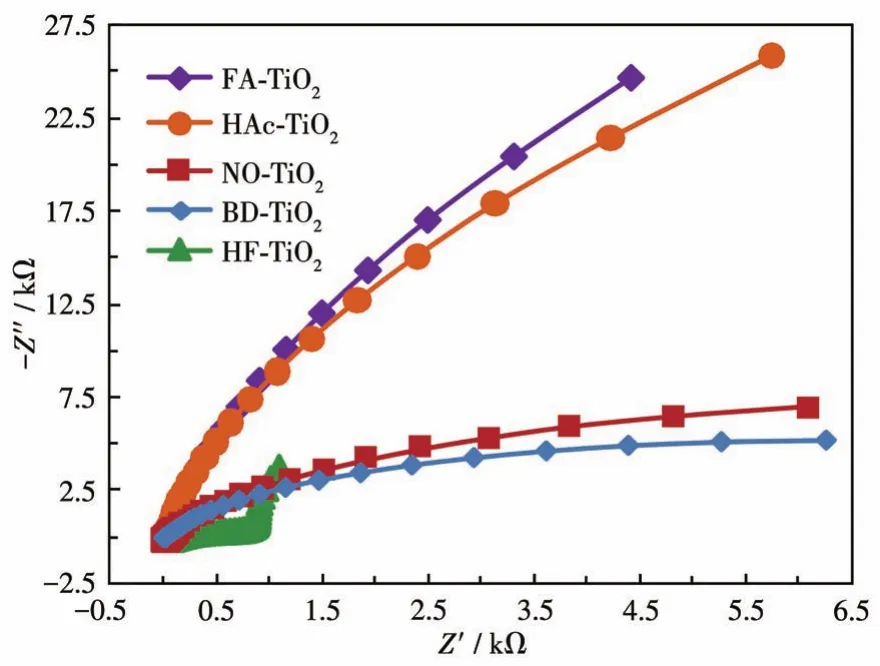
图8 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和商业化BD-TiO2的Nyquist谱图Fig.8 Nyquist spectra of FA-TiO2,HAc-TiO2,HF-TiO2,NO-TiO2,and commercial BD-TiO2
2.7 光催化性能
通过测定紫外线照射下罗丹明B溶液(λmax=554 nm)和对硝基苯酚溶液(λmax=400 nm)的降解情况,比较了 FA-TiO2、HAc-TiO2、HF-TiO2、NO-TiO2和 BDTiO2的光催化性能。图9a和9b分别为罗丹明B和对硝基苯酚溶液在不同催化剂存在的条件下随光照射时间变化的降解率曲线。从图9a中可以看出,在光照射120min时,罗丹明B溶液降解率增加的顺序 为 Blank(3.83% )<NO-TiO2(19.93% )<BD-TiO2(72.01% )<HAc-TiO2(82.48% )<FA-TiO2(91.79% )<HFTiO2(97.35% )。即HF-TiO2在光催化降解罗丹明B溶液时显示了最高的光催化活性,其降解率分别是FA-TiO2、HAc-TiO2、BD-TiO2、NO-TiO2和 Blank 样品的1.06倍、1.18倍、1.35倍、4.88倍和25.42倍。从图9b中可以看出,HF-TiO2在光催化降解对硝基苯酚溶液时显示了最高的光催化活性,在光照射120min时,其降解率(68.57% )分别是 FA-TiO2(63.07% )、HAc-TiO2(60.20% )、BD-TiO2(29.38% )、NO-TiO2(11.83% )和Blank(4.31% )的1.09倍、1.14倍、2.33倍、5.80倍和15.90倍,降解的对硝基苯酚最终矿化为CO2和H2O[34]。从上述分析可以看出,所制备的TiO2纳米材料对不同有机染料的降解能力不同。
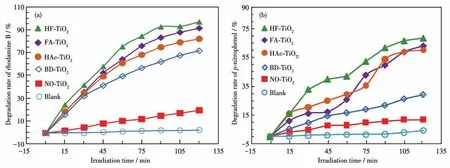
图9 缺少或存在TiO2催化剂时罗丹明B溶液(a)和对硝基苯酚溶液(b)随紫外光照射时间变化的降解率曲线Fig.9 Degradation rate curves of(a)rhodamine B solution and(b)p-nitrophenol solution changed with ultraviolet irradiation time in the absence or presence of TiO2catalysts
众所周知,光催化剂的光催化活性与晶型、颗粒尺寸、孔径分布、结晶度、光生载流子的分离效率、比表面积和暴露晶面等诸多因素有关[35-36]。一般来说,与金红石型和板钛矿型TiO2相比,锐钛矿型TiO2在光催化降解有机污染物过程中具有最高的光催化活性。然而,金红石型和锐钛矿型TiO2的异质结连接,能够加速光生载流子的迁移和抑制光生电子-空穴的重组,从而促使光催化性能的提高[37]。BD-TiO2是金红石型和锐钛矿型TiO2的复合物,存在异质结结构,因此与合成的锐钛矿型TiO2相比,BD-TiO2应该具有最高的光催化活性。然而,BD-TiO2的光催化活性仅高于NO-TiO2,说明其他因素对光催化活性也具有重要的影响。对于所合成的锐钛矿型TiO2,颗粒尺寸增加的顺序为HAc-TiO2(20.6 nm)≈FA-TiO2(20.9 nm)<NO-TiO2(22.1 nm)<HFTiO2(23.9 nm),比表面积增加的顺序为NO-TiO2(15 m2·g-1)<HF-TiO2(37 m2·g-1)<HAc-TiO2(41 m2·g-1)<FA-TiO2(43m2·g-1),结晶性增加的顺序为 NO-TiO2<HAc-TiO2<FA-TiO2<HF-TiO2。与其他样品相比,NOTiO2的比表面积明显较小,是其结晶性差和团聚严重造成的。一般来说,颗粒尺寸越小,结晶性越小,比表面积越大,催化剂的催化活性越高[38]。因此,FA-TiO2或HAc-TiO2在光催化降解罗丹明B溶液或对硝基苯酚溶液过程中应该显示最高的光催化活性,然而这与实验结果不相符,说明除了颗粒尺寸、比表面积、结晶性外,其他因素对光催化活性也具有重要影响。基于上述讨论可知,所合成的锐钛矿型TiO2主要是由方块状、菱形六面体状、近似球形状和不规则形状等纳米颗粒组成的,其主要暴露晶面是{101}/{010}/[111]-晶面(FA-TiO2、HF-TiO2)和{101}/[111]-晶面(HAc-TiO2、NO-TiO2)。对于锐钛矿型TiO2,平均表面能增加的顺序为{101}晶面(0.44 J·m-2)<{010}晶面(0.53 J·m-2)<{001}晶面(0.90 J·m-2)<{111}晶面(1.61 J·m-2)[11]。一般来说,平均表面能越高,光催化活性越高。然而,与其他晶面相比,{010}晶面具有优越的表面原子结构和表面电子结构,二者协同作用,使其在光催化过程中显示了最高的光催化活性[39]。因此,FA-TiO2和HF-TiO2样品的催化活性高于HAc-TiO2和NO-TiO2样品。又由于HF-TiO2为多孔材料,孔体积大,在紫外光区的吸光度最大,使其具有最高的光催化活性。此外,较低的光致发光强度和较小的Nyquist谱图弧半径可以加速电解液与半导体界面处的电荷转移,抑制电子和空穴的复合,从而提高光催化活性[28,30-33]。综上所述,所制备的TiO2样品光催化活性增加的顺序为NO-TiO2<HAc-TiO2<FA-TiO2<HF-TiO2。
所制备的TiO2和BD-TiO2样品连续3次催化循环降解罗丹明B的性能如图10所示。催化循环研究是在反应120min后回收使用过的TiO2样品,在后续的反应循环中与新的TiO2样品一起重复3次。回收的TiO2样品用水和乙醇清洗,在空气中干燥,然后在下一次催化试验中重复使用。结果表明,对于制备的无控制剂-TiO2样品,经过3次循环试验后催化活性降低了82.40%,说明该样品作为催化剂是不合适的。而经过3次循环试验,FA-TiO2、HAc-TiO2、HF-TiO2和商业BD-TiO2样品的催化活性分别下降了12.78%、9.44%、5.53% 和7.06%。每个循环后的轻微下降归因于对污染物的吸收和活性点的减少。尽管光催化活性略有下降,但在连续的重复使用实验中,这些TiO2颗粒仍然保持了较高的活性,说明制备的 FA-TiO2、HAc-TiO2和 HF-TiO2样品对有机污染物的去除是稳定、有效的。

图10 不同的TiO2光催化材料在紫外光照射下降解罗丹明B溶液的循环性能Fig.10 Recycled performances of different TiO2 photocatalytic materials for photodegradation of rhodamine B solution under ultraviolet light irradiation
3 结 论
以钛酸丁酯为钛源,以甲酸、乙酸和氢氟酸为形貌控制剂,利用溶剂热法制备了共暴露{101}/{010}/[111]-晶面(FA-TiO2和 HF-TiO2)和{101}/[111]-晶面(HAc-TiO2和NO-TiO2)的方块状、菱形六面体状和近似球形状的锐钛矿型TiO2纳米材料。研究结果表明,在紫外光照射120min时,HF-TiO2对罗丹明B溶液(或对硝基苯酚溶液)的降解率最高,高达97.35% (或 68.57% ),分别是 FA-TiO2、HAc-TiO2、BDTiO2和NO-TiO2的 1.06倍(或 1.09倍)、1.18倍(或1.14倍)、1.35倍(或2.33倍)和4.88倍(或5.80倍)。在光催化过程中,HF-TiO2显示出最高的光催化活性,归因于其较高的比表面积、最高的结晶性、最大的孔体积、最大的光吸收强度、共暴露的{101}/{010}/[111]-晶面、最低的光致发光强度、最快的电荷转移速率和最小的载流子复合率的协同作用。所制备的FATiO2、HAc-TiO2和HF-TiO2光催化剂对有机污染物罗丹明B具有稳定、有效的去除作用,在降解印染污水中的有机染料方面具有潜在的应用价值。
- 无机化学学报的其它文章
- Synthesis,Structures and Catalytic Activity in Knoevenagel Condensation Reaction of Cu(Ⅱ)/Co(Ⅱ)/Ni(Ⅱ) Coordination Polymers Based on Ether-Bridged Tetracarboxylic Acid
- 结晶氮化碳的制备与改性策略
- 双二芳基乙烯配体构建的Ag(Ⅰ)配合物及多色光致变色性质
- 多吡啶类双核镍配合物的合成、晶体结构及抗癌活性
- 掺镁铝酸三钙制备及其共去除水体中氮磷的性能
- 一维纳米材料Cs0.2WO3和W18O49长度与红外吸收关联性的Mie散射理论推导及实验验证

