利用P204铜锰液除杂制备工业级碳酸锰
谢小凯,谢明伟,游称斌
利用P204铜锰液除杂制备工业级碳酸锰
谢小凯,谢明伟,游称斌
(赣州腾远钴业新材料股份有限公司,江西 赣州 341000)
研究了利用P204萃取净化浸钴液后的负载有机相,使用硫酸进行反萃,反萃下来的铜锰液进行深度除铁、铝、锌、钴、铜、钙等杂质,回收硫酸锰,具体工艺包括:取204反萃液,锰质量浓度约为50 g·L-1,加入理论量1.2倍的活性氧化锰进行氧化溶液中的Fe2+,锰液加入配制好的硫化钠水溶液进行除锌、钴、铜,再使用氨水调节溶液pH至5.0进行除铝,加入溶液中Ca2+摩尔浓度2倍的氟化钠,在90 ℃下反应2 h进行除钙。通过前述工艺铁、锌、钴、铜、铝、钙的净化率高达95%以上。最后以净化除杂后的硫酸锰为锰源,加入配制好的碳酸氢氨溶液使用沉淀法制备碳酸锰,最后通过过滤洗涤得到工业级碳酸锰。结果表明:通过上述除杂工艺,杂质金属离子和钠离子含量均达到工业级碳酸锰的要求,锰的回收率高达90%。
浸钴液;硫酸锰;除杂;碳酸锰
近年来,随着三元锂电池的高速发展,锰系列产品在制备三元前驱体中占有着重要地位。本文主要论述合理回收利用锰资源,制备工业级碳酸锰。目前,有关合理利用钴冶炼过程中P204产生的铜锰液制备硫酸锰、碳酸锰等锰系列产品的研究较少,大部分研究都集中于锰矿浸出液除杂、硫酸锰溶液深度净化除杂、三元锂电池回收镍钴锰等。合理利用一切锰资源,也是迫在眉睫[1]。
试验采用分步沉淀法进行净化硫酸锰溶液,以钴浸液P204反萃液(也称铜锰液)为原料,进行分步除铁、除锌、除铜铝得到初步净化的硫酸锰溶液,再进行化学沉淀得到碳酸锰[2-5]。
1 实验部分
1.1 试验原料
试剂:MnO2,分析纯;NaF,分析纯;氨水,分析纯;碳酸氢氨,工业级。
原料:铜锰液,取自赣州腾远钴业新材料有限公司P204反萃段锰液,料液分析结果见表1。
注:其余金属杂质均小于0.001 g·L-1。
1.2 试验设备
FL-1实验室可调电炉,恒速搅拌器,SHB-Ⅲ型循环水式多用真空泵,奥克斯在线pH计,电感耦合等离子体发射光谱仪,A3AFG型原子吸收分光光度计,电子天平。
1.3 实验原理及方法
铜锰液净化除杂过程包括如下4个步骤。
1)活性氧化锰氧化Fe2+:
2Fe2++MnO2+4H+→2Fe3++ Mn2++2H2O。 (1)
生成的Fe3+在pH高于1.8时发生水解生成氢氧化铁沉淀,过滤除去。
2)硫化钠除锌、钴、铜:
Co2++Na2S→CoS↓+2Na+; (2)
Cu2++Na2S→CuS↓+2Na+; (3)
Zn2++ Na2S→ZnS↓+2Na+。 (4)
3)氨水调节溶液pH除铝。
4)氟化钠脱钙:
2NaF+Ca2+→CaF2↓+2Na+。 (5)
待上述料液除杂后,净化料液即可作为生产碳酸锰的锰源,净化料液加入配好浓度的碳酸钠溶液,加入硫酸锰溶液中,即可生成碳酸锰,生成的碳酸锰经过陈化、洗涤后即得所需工业级碳酸锰。
具体步骤:取一定体积铜锰液,加入适量活性MnO2,搅拌反应30 min,过滤后取滤液,加入配制好浓度的Na2S水溶液,进行除锌钴,过滤后加入适量氨水调节溶液pH至5.0左右,搅拌反应一段时间,再加入Ca2+摩尔质量两倍的NaF,调节溶液温度,搅拌反应一定时间,过滤。取滤液,加入配制好浓度的碳酸氢氨溶液,待锰沉定完全后,将溶液进行陈化,洗涤,烘干后得到工业级碳酸锰。
2 结果与讨论
2.1 活性氧化锰氧化除铁
取一定体积204反萃下来的铜锰液溶液,加入活性氧化锰进行氧化溶液中的Fe2+,因铜锰液溶液中Fe2+浓度较低,加入少许活性氧化锰即可将二价铁离子氧化为三价,因料液pH超过2,氧化反应完毕后直接过滤,即可除去溶液中的Fe2+。
为研究活性氧化锰加入量对Fe2+去除效果的影响,取一定量的铜锰液,升高温度至50 ℃,加入活性氧化锰,反应30 min,过滤后测定溶液中Fe2+质量浓度。活性氧化锰的加入量对Fe2+去除影响试验结果如图1所示。
2.2 硫化钠除锌、钴、铜
取一定体积的除铁后铜锰液,加入200 g·L-1的硫化钠溶液,使溶液中的锌与钴与硫离子结合形成硫化锌、硫化钴沉淀,由于硫化锌和硫化钴的sp较低,硫化钠加入后,迅速生成沉淀,反应完毕后,过滤,取滤液分析锌、钴、铜、锰离子。
为了研究硫化钠溶液加入量对锌、钴、铜、锰去除的影响,取一定量的除铁后铜锰液,升高温度至50 ℃,加入200 g·L-1的硫化钠溶液,反应1 h,过滤,取滤液分析溶液中的锌、钴、铜、锰去除率。硫化钠加入量对锌、钴、铜、锰去除率的影响如图2所示。
由图2可知,随着硫化钠加入量的增加,锌、钴、铜的去除率不断增加,当达到理论量两倍时,锌、钴、铜去除率均达到99%以上,继续增加硫化钠的量,溶液中锰的损失也不断上升,因此加入硫化钠的量为理论量的2倍即可。
2.3 氨水调节溶液pH除铝
取去除锌、钴、铜后的硫酸锰溶液,加入适量氨水调节溶液pH,使溶液中的杂质铝进行水解沉淀,过滤后分析溶液中的Al3+质量浓度。
为了研究溶液pH对铝离子去除率的影响,取除锌、钴、铜后的硫酸锰溶液,升高温度至50 ℃,加入稀氨水调节溶液pH,反应1 h,过滤,取滤液分析Al3+去除率。溶液pH对Al3+去除率的影响如图3所示。
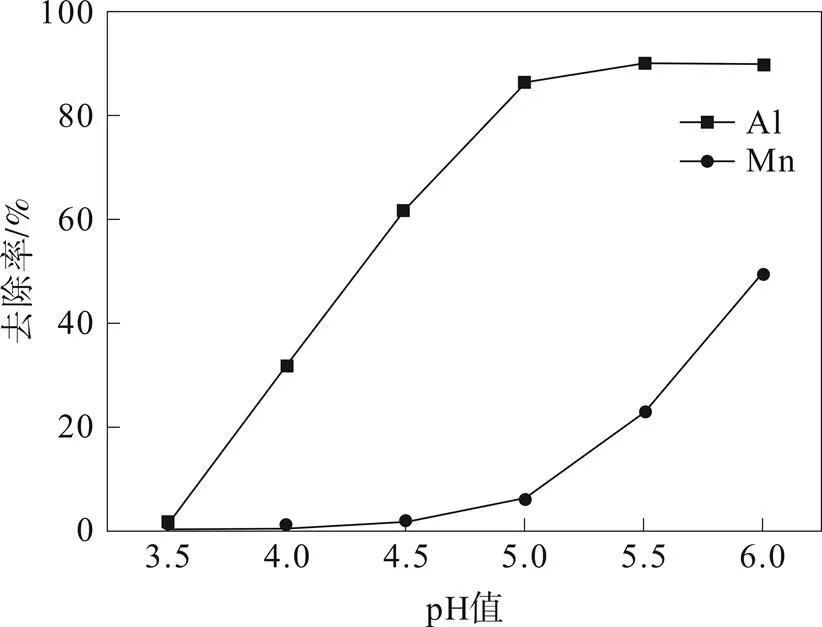
图3 溶液pH对Al3+去除率的影响
由图3可知,随着pH的增加,铝的去除率呈现上升趋势;随着pH的上升,锰有部分损失。综合考虑,试验中氨水调节溶液pH为5.0左右即可。
2.4 氟化钠脱钙
取除铝后的硫酸锰溶液,由于pH已经在5左右,此步骤不对溶液pH处理,加入适量氟化钠固体,保持一定温度,进行脱钙,过滤后取溶液分析钙离子去除率。
2.4.1 温度对氟化钠除钙的影响
取除铝后的硫酸锰溶液,加入理论量2倍的氟化钠,升高温度对溶液进行脱钙,反应时间2 h,过滤分析钙离子去除率。温度对Ca2+去除的影响如 图4所示。
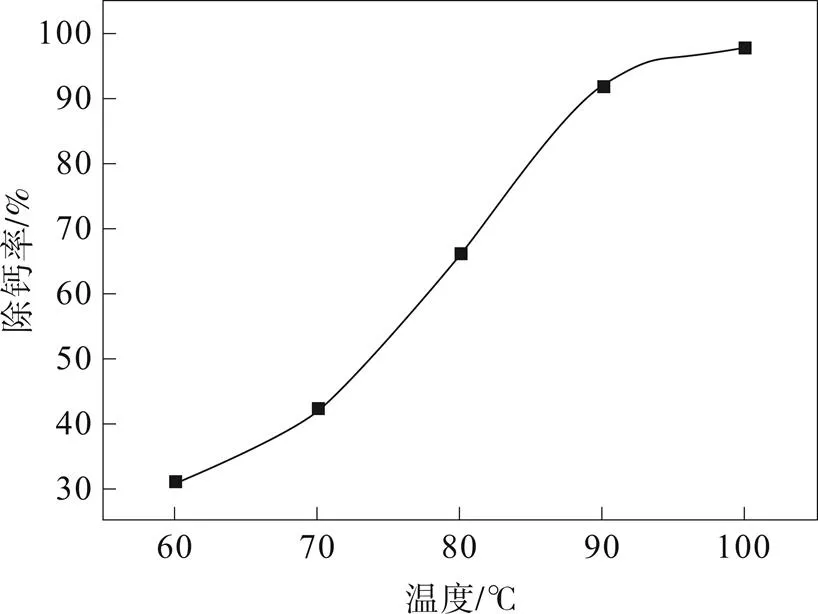
图4 温度对钙离子去除的影响
由图4可知,随着温度的升高,除钙率上升,当温度上升至90 ℃ 时,除钙率达到92%,考虑到能耗的影响,试验中控制除钙温度在90 ℃。
2.4.2 氟化钠加入量对脱钙的影响
取除铝后的硫酸锰溶液,升高温度至90 ℃,加入一定量的氟化钠,保持温度搅拌反应2 h,过滤,取滤液分析溶液中Ca2+去除率。氟化钠加入量对Ca2+去除的影响如图5。
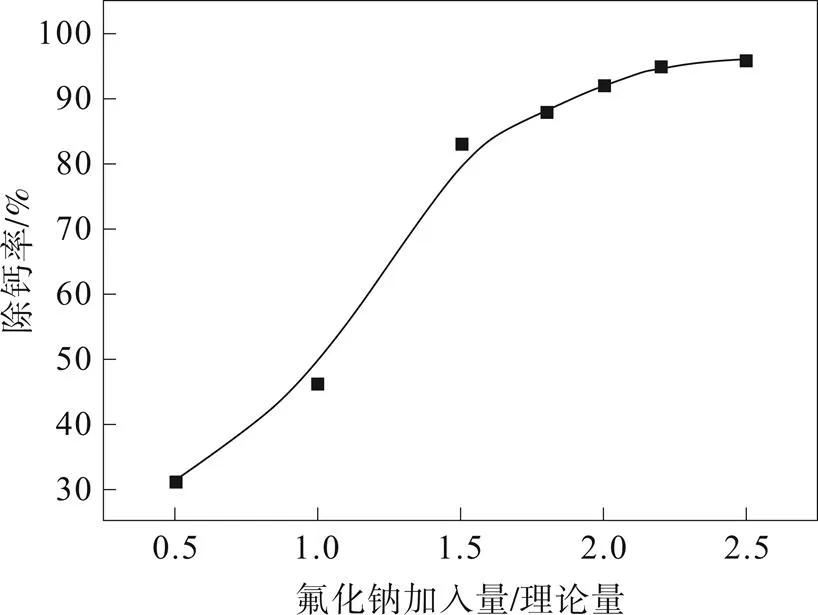
图5 氟化钠加入量对Ca2+去除的影响
由图5可知,随着氟化钠加入量的增加,Ca2+去除率上升,当达到理论量2倍时,除钙率上升变得更缓,因此试验中氟化钠加入量控制在2倍理论量即可。
2.5 除杂后液进行碳酸氢氨沉锰
取除杂后硫酸锰溶液,加入150 g·L-1的碳酸氢氨溶液,保持一定温度,对硫酸锰溶液进行沉碳酸锰。除杂后硫酸锰溶液分析结果如表2所示。

表2 除杂后锰液金属组成
2.5.1 碳酸氢铵加入量对锰的回收率影响
取上述表2锰液,加入150 g·L-1的碳酸氢氨溶液,保持溶液温度为室温即可,加完碳酸氢铵溶液后,继续搅拌反应30 min后过滤。碳酸氢铵加入量对锰回收率的影响如图6所示。

图6 碳酸氢铵加入量对锰回收率的影响
由图6可知,碳酸氢铵加入量为理论量的1.5倍时,金属锰的回收率高达98%。因此试验中,碳酸氢铵加入量为理论量的1.5倍即可。
2.5.2 碳酸锰洗涤
碳酸氢铵沉淀得到的碳酸锰,经过陈化后,需用纯水洗涤两遍,确保可溶性杂质不会附着在碳酸锰晶体表面。铜锰液经过一系列的除杂后,进行碳酸氢铵沉锰,所得碳酸锰质量分析结果见表3。
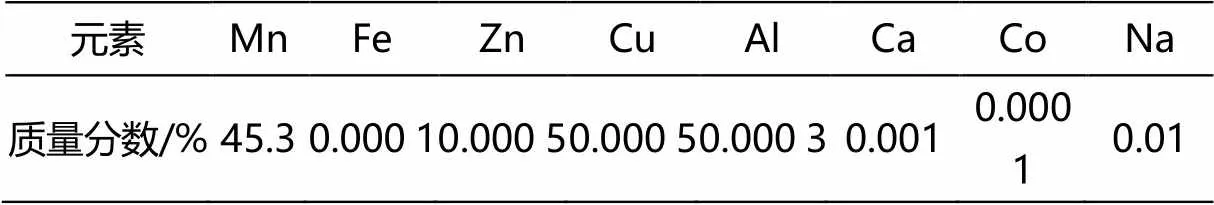
表3 碳酸锰产品质量分析表
3 结 论
1)针对钴冶炼厂204反萃液中硫酸锰杂质含量较高,采用多级分步化学法联合除杂,制得除杂后硫酸锰后,进行碳酸氢氨沉锰,试验结果表明铁、锌、钴、铜、铝、钙的除杂率均在95%以上,能够达到制备工业级碳酸锰的标准。
2)除杂过程中,使用的沉淀剂主要引入金属Na+,沉淀完后,进行2遍纯水洗涤即可解决碳酸锰产品中Na+超标的问题。
3)生产碳酸锰过程中,硫化钠除杂以及氨水调节pH阶段会有部分金属锰的损失,但锰的总回收率可达90%以上。
[1] 谭柱中,梅光贵,李维健.锰冶金学[M].长沙:中南大学出版社,2004.
[2] 陈海春,薛昊.锂离子电池石墨负极材料改性研究[J].辽宁化工,2020,49(8):927-930.
[3] 胡国荣,周玉琳,彭忠东.用工业硫酸锰制取高纯碳酸锰的工艺研[J].中国锰业,2008,25(2):14-17.
[4] 周登凤,李军旗,杨志彬.硫酸锰深度净化的研究[J]贵州工业大学学报(自然科学版),2006,35(1):4-6.
[5] 李军旗,张国才,毛小浩.氯化锰溶液净化工艺[J].有色金属,2011,63(2):172-174.
[6] 张宏,赵凯,陈飞宇,等.电池级高纯一水硫酸锰的发展与 应用前景[J].中国锰业,2014,32(2):6-8.
[7] 罗昌璃,龙海平,农德连.高纯硫酸锰的工业生产实践[J].中国锰业, 2007,25(4):51-53.
[8] 刘洪刚,朱国才.氟化锰沉淀脱除还原氧化锰矿浸出液中钙镁[J].矿冶,2007,16(4):25-28.
[9] 袁万钟,迟玉兰,辛剑,等.无机化学[M].北京:高等教育出版社,2001.
Preparation of Industrial Grade Manganese Carbonate by Removing Impurity From P204 Copper Manganese Solution
,,
(Ganzhou Tengyuan Gobalt New Material Co., Ltd., Ganzhou Jiangxi 341000, China)
The process of recovering manganese sulfate from the copper and manganese solution extracted by sulfuric acid after purifying the loaded organic content of cobalt leaching solution with P204 extraction was studied. The impurities such as iron, aluminum, zinc,cobalt,copper and calcium were deeply removed from the copper and manganese solution extracted by sulfuric acid. The specific process included: taking 204 extraction solution with manganese mass concentration approximately 50 g·L-1, adding 1.2 times the theoretical amount of active manganese oxide to oxidize Fe2+in the solution,prepared sodium sulfide aqueous solution was added to remove zinc, cobalt, and copper, and then ammonia was used to adjust the pH of the solution to 5.0 to remove aluminum, and sodium fluoride with 2 times the molar concentration of Ca2+in the solution was added, and the reaction was carried out at 90 ℃ for 2 h for Ca2+removal. The purification rate of iron, zinc, cobalt, copper, aluminum and calcium by the above process was as high as 95%. Finally, manganese carbonate was prepared by precipitation method with purified manganese sulfate as manganese source, and adding prepared ammonia bicarbonate solution. Industrial grade manganese carbonate was obtained by filtration and washing.The results showed that, through the above-mentioned impurity removal process, the content of impurity metal ions and sodium ions reached the requirements of industrial grade manganese carbonate, and the recovery rate of manganese was as high as 90%.
Cobalt leaching liquid; Manganese sulfate; Impurity removal; Manganese carbonate
2021-03-22
谢小凯(1994-),男,江西省赣州人,工程师,2017年毕业于江西理工大学冶金工程专业,研究方向:新能源材料研发。
TQ137.1+2
A
1004-0935(2021)10-1467-04

