原位合成Bi3O4Br/Bi12O17Br2光催化剂及其对磺胺甲噁唑降解性能
李 瑞,张 潇,张璐璐,谢芳霞,张小超,王雅文,樊彩梅,
(1.太原理工大学环境科学与工程学院,太原 030024; 2.太原理工大学化学化工学院,太原 030024)
0 引 言
自21世纪以来,随着全球经济的飞速发展,环境污染问题日益加重,特别是近年来,水生生态系统中的药物化合物被认为是一种新型的水体污染。临床学者发现,水体中含有药物污染物近2 000多种,其中致癌物大约有109种,促癌物大约19种,致突变物大约44种等[1]。在众多污染物中,磺胺类药物作为我国使用量最大的一类抗生素,具有广谱抗菌性、成本低、稳定性高等特征,被广泛应用于临床医学、水产、畜牧等抗感染治疗[2]。但此类药物不能被人类或动物完全代谢,受药后约30%~90%的磺胺类药物会以化合物、代谢物或其组合物排出体外,同时由于其广泛的消耗、低生物降解性和亲水性使其在水环境中持续积累,目前已成为地表水中常见的污染物之一,经常在地表水体、地下水、饮用水甚至是经过处理后的水体中检测到[3-5]。此污染物的存在不仅对微生物、藻类和某些植物具有高毒性,而且还能诱导耐药性生物和耐药基因的出现,对水生生物甚至人类健康造成极其严重的危害[6]。因此寻找一种有效且环保的方法来降解和消除水环境中的磺胺类药物成为了目前的研究重点。
目前磺胺类抗生素的处理方法主要有生物、物理、臭氧氧化、芬顿和半导体光催化法等几种。其中半导体光催化技术作为一种兴起的新型高级氧化技术,具有能耗低、成本低、无毒、无二次污染等优点,在难降解有机污染物方面表现出了良好的处理能力,被认为是最具发展前景的绿色环保技术[7]。但其受限于光生电子和空穴的复合,使得此种技术效率较低[8]。因此,阻止光生电子和空穴在催化剂体相和表面的复合是提高光催化效率的有效途径。
非化学计量比溴氧铋光催化剂(BixOyBrz)由于独特的层状结构和光生电子间接跃迁模式,使得其在本质属性上拥有比其他催化剂较高的光生电子-空穴分离效率[9],同时又兼具合适的能带结构、优良的水稳定性及环境友好性等优点,故受到了学者们的关注[10-11]。但其光生电子-空穴对的复合时间(10-9s)仍然远远小于光生电子空穴反应所需的时间(10-3s)。因此,如何对BixOyBrz光催化剂进行改性进而提高其光生电子-空穴寿命,成为目前的研究热点。
原位构筑异质结光催化剂可以在复合催化剂之间形成作用力强且接触紧密的界面,从而为电子和空穴的有效转移和分离提供较强的化学界面,是一种提升光催化性能常用的改性方法[12-13]。相关研究表明BixOyBrz光催化剂之间可以通过Br-的溢出和补充实现彼此间的原位转化,同时保持相近的晶型结构[14],进而彼此间形成电荷转移电阻较小的界面,从而促进光生载流子分离率的提升。由此可见,对于提升BixOyBrz光催化剂的活性,原位构筑BixOyBrz/BixOyBrz复合光催化剂是一种值得深入研究的改性手段。
基于以上启发,本文采用简易的水解-焙烧法原位合成了Bi3O4Br/Bi12O17Br2复合光催化剂,并以磺胺类抗生素中具有代表性的磺胺甲噁唑(SMX)为模拟药物污染物,在模拟太阳光下进行了光催化性能测试。通过X射线衍射(XRD)、X射线光电子能谱(XPS)、扫描电子显微镜(SEM)、紫外可见漫反射光谱(UV-Vis DRS)、电化学阻抗(EIS)、光致发光光谱(PL)对催化剂进行了表征。结果表明,Bi3O4Br/Bi12O17Br2复合光催化剂被成功制备。且与纯Bi3O4Br、Bi12O17Br2相比,复合光催化剂展示了良好的SMX降解性能,这归因于其较强的光生载流子分离率和较低的界面电荷转移电阻。最后基于自由基捕获实验和催化剂能带结构分析了Bi3O4Br/Bi12O17Br2复合光催化剂的降解机理。
1 实 验
1.1 主要试剂与材料
五水硝酸铋(Bi(NO3)3·5H2O,分析纯,≥99.0%,国药集团化学试剂责任有限公司);溴酸钠(NaBrO3,分析纯,≥99.0%,天津市光复科技发展有限公司);氨水(NH3·H2O,分析纯,≥99.7%,天津市科密欧化学试剂有限公司);磺胺甲噁唑(SMX,分析纯,≥98%,上海阿拉丁生化科技股份有限公司),其他试剂均为分析纯(中国国药集团)。
1.2 主要仪器
紫外可见分光光度仪(Varian Cary 50,瓦里安(中国)有限公司);氙灯光源系统(PLS-SXE 300,北京泊菲莱科技有限公司);电化学工作站(CHI-660E,上海辰华仪器有限公司);X射线衍射仪(XRD,Rigaku D/Max 2500,日本);扫描电子显微镜(SEM, JSM-7001F,日本);X射线光电子能谱仪(XPS,VG MultiLab 2000,美国);紫外可见分光光度计(UV-Vis DRS,UV-2450,日本);光致发光光谱仪(PL,Cary-300,美国)。
1.3 催化剂的制备
首先,将0.01 mol Bi(NO3)3·5H2O粉末完全溶解于50 mL蒸馏水中,记为A溶液;将0.01 mol NaBrO3粉末完全溶解于另外40 mL蒸馏水中,记为B溶液。其次,将B溶液缓慢倒入A溶液中,混合均匀后,加入3 mL NH3·H2O调节pH值,继续反应3 h,整个过程控制反应温度为20 ℃。接着将所得产物经抽滤、洗涤、干燥后收集。最后将收集的样品分别在马弗炉中于250 ℃、300 ℃、350 ℃、400 ℃、450 ℃、500 ℃、550 ℃、650 ℃、750 ℃下焙烧,将所得样品分别标记为B250、B300、B350、B400、B450、B500、B550、B650、B750。
1.4 催化剂表征与光电性能测试
采用XRD对样品的结构进行表征,辐射源为Cu Kα,管电压和管电流分别为40 kV和30 mA。样品的形貌通过SEM进行表征,加速电压设为10 kV。样品的表面元素用XPS进行定性分析,发射源为Mg Kα,工作电压为20 kV。催化剂的吸光特性采用UV-Vis DRS进行表征。采用PL对催化剂的电子空穴分离率进行表征。
电化学阻抗谱图,通过电化学工作站CHI-660E和三电极体系来进行测试。其中三电极体系为:样品分散在氧化铟锡(ITO)玻璃上制成1 cm×1 cm的薄膜作为工作电极,Pt片作为对电极,Ag/AgCl电极作为参比电极。电解质溶液为1 mol/L Na2SO4溶液,光源为300 W氙灯。
1.5 光催化活性评价
所制备样品的光催化活性通过模拟太阳光照射下对磺胺甲噁唑(SMX)溶液的降解率来评定。其中模拟太阳光为不加滤波片的300 W氙灯系统,波长范围为320~780 nm(PLS-SXE 300,北京泊菲莱科技有限公司)。具体的操作步骤为:首先将0.05 g催化剂分散于100 mL SMX(10 mg/L)溶液中。然后,将悬浮液在黑暗中搅拌以达到吸附-解吸平衡,待平衡后,将悬浮液暴露于光下照射,每间隔一定时间,取出3 mL悬浮液离心取上清液,用紫外可见分光光度计测试样品吸光度。最后以降解液特征峰(254 nm)处的吸光度值为纵坐标,反应时间为横坐标作图,利用公式:D=(1-Ct/C0)×100%,计算得出磺胺甲噁唑的降解率(其中D为降解率,C0为降解液的初始浓度值,Ct为反应进行一定时间后降解液的浓度值)。其中灯和反应器之间的距离设置为20 cm,所有实验均在25 ℃恒温水浴锅中进行。
2 结果与讨论
2.1 光催化剂的表征
用XRD探究所制备催化剂的组成和晶型结构,结果如图1所示。图1(a)为不同温度下所制备样品的XRD图谱,为便于分析,对其中B300、B400、B550样品的XRD进行了单独分析。如图1(b)所示,当焙烧温度为300 ℃时,所制备样品B300的衍射峰与Bi3O4Br的标准卡JCPDS 84-0793相对应,其中2θ为28°、29°、31°的衍射峰分别与Bi3O4Br的(006)、(114)、(020)晶面相对应,证明在300 ℃下焙烧时,形成了Bi3O4Br光催化剂,且其XRD各衍射峰较尖锐,表明催化剂结晶度良好。此外,由XRD标准卡信息可知,所合成的Bi3O4Br是斜方晶系,晶格参数为:a=0.570 51 nm,b=0.569 35 nm,c=1.894 9 nm,α=β=γ=90°。当焙烧温度为550 ℃时,如图1(d)所示,所得样品B550的衍射峰与Bi12O17Br2的标准卡JCPDS 37-0701相对应,其中2θ为28.9°、32.7°、45°、46.9°的衍射峰分别与Bi12O17Br2的(117)、(200)、(2 0 12)、(220)晶面相对应,证明在550 ℃下焙烧时,形成了Bi12O17Br2光催化剂,且其XRD各衍射峰比较尖锐,表明催化剂结晶度良好。此外,由XRD标准卡信息可知,所合成的Bi12O17Br2属于四方晶系,晶格参数为:a=0.547 2 nm,b=0.547 2 nm,c=3.567 nm,α=β=γ=90°。值得注意的是,当焙烧温度为400 ℃时,如图1(c)所示,B400催化剂的衍射峰能够同时匹配Bi3O4Br的衍射峰和Bi12O17Br2的衍射峰,表明Bi3O4Br/Bi12O17Br2复合光催化剂被成功制备,且其XRD各衍射峰比较尖锐,表明催化剂结晶度良好。
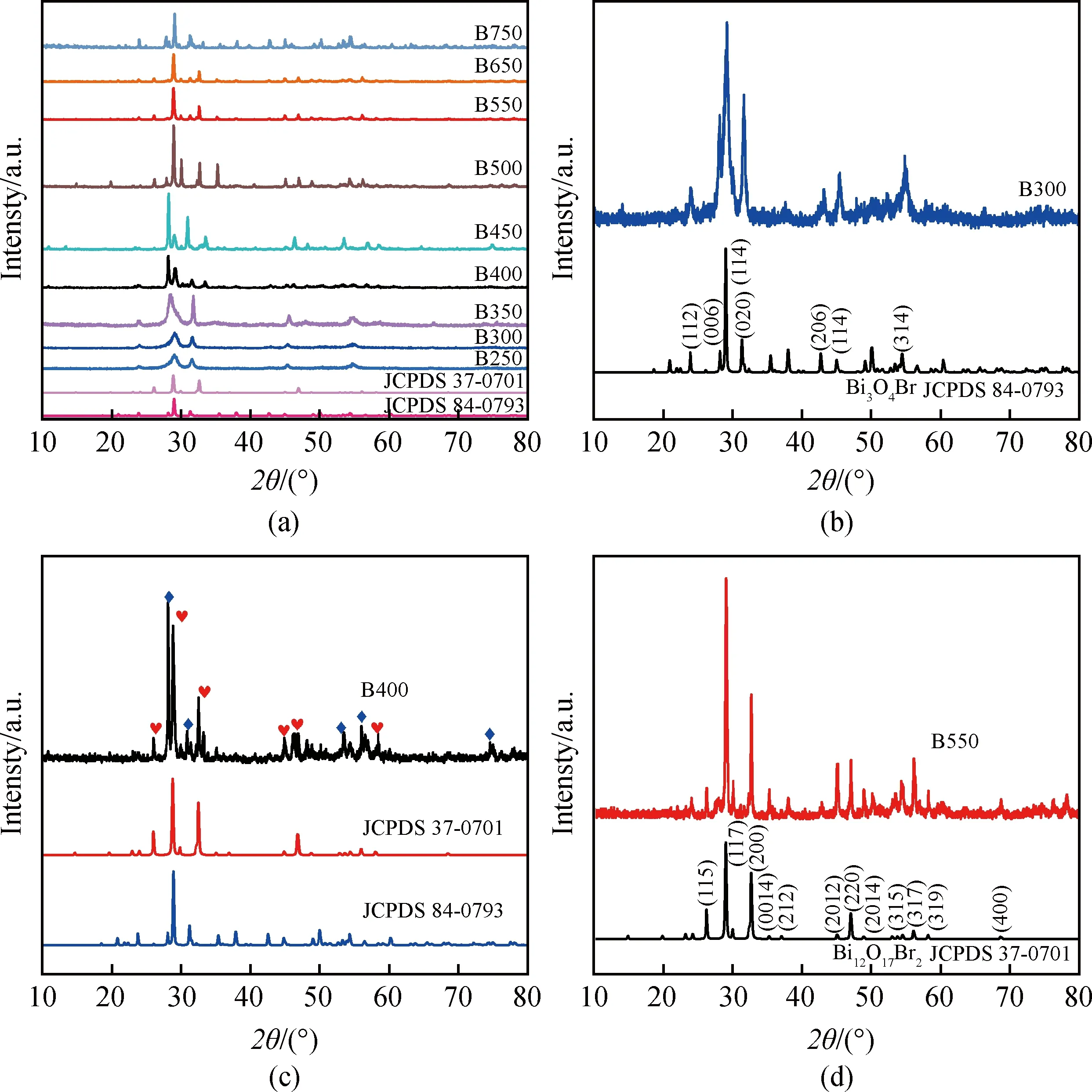
图1 不同温度下所制备样品的XRD图谱Fig.1 XRD patterns of as-prepared samples at different temperatures
为了明确所制备样品的形貌结构,采用SEM对不同条件下所制催化剂的微观形貌进行了表征。由图2可以看出,当焙烧温度为300 ℃时,纯Bi3O4Br催化剂为片状结构,当焙烧温度为550 ℃时,纯Bi12O17Br2催化剂为棍状结构,而当焙烧温度为400 ℃时,发现其具有两种结构,一种为Bi3O4Br催化剂的片状结构,另一种为Bi12O17Br2催化剂的棍状结构,表明当焙烧温度为400 ℃时,形成的样品为Bi3O4Br和Bi12O17Br2的复合物,该现象与XRD表征结果相一致,进一步证明Bi3O4Br/Bi12O17Br2复合催化剂的成功合成。且Bi3O4Br的片状结构与Bi12O17Br2的棍状结构呈现出穿插、紧贴现象,这种结构增大了两种催化剂的接触面积,促进了电子空穴对的分离,提高了光催化性能[15]。

图2 所制备催化剂的SEM照片Fig.2 SEM images of as-prepared catalysts
实验中采用氮气吸附脱附表征对所制催化剂的比表面积进行了分析,结果如图3和表1所示。从中可以看出,所制备样品的氮气吸附脱附曲线在P/P0为0.8~1.0的范围内出现了明显的滞回环,属于典型的Ⅳ型等温线,证明它们都是介孔结构。此外随焙烧温度的升高,所制备样品的比表面积先增大后减小,在400 ℃(B400)时最大,这是由于Bi3O4Br的片状结构与Bi12O17Br2的棍状结构呈现出穿插、紧贴现象,因此其具有最大的表面积,进而展示出较强的吸附污染物能力。其中Bi3O4Br(B300)、Bi3O4Br/Bi12O17Br2(B400)、Bi12O17Br2(B550)比表面积分别是6.003 3 m2·g-1、10.405 2 m2·g-1、6.005 1 m2·g-1。结合光催化降解实验发现Bi3O4Br/Bi12O17Br2活性高是因为它具有较大的比表面积和孔体积,这种高比表面积、高孔体积的多孔结构为光催化反应提供了大量活性位点,有利于污染物的吸附与降解。
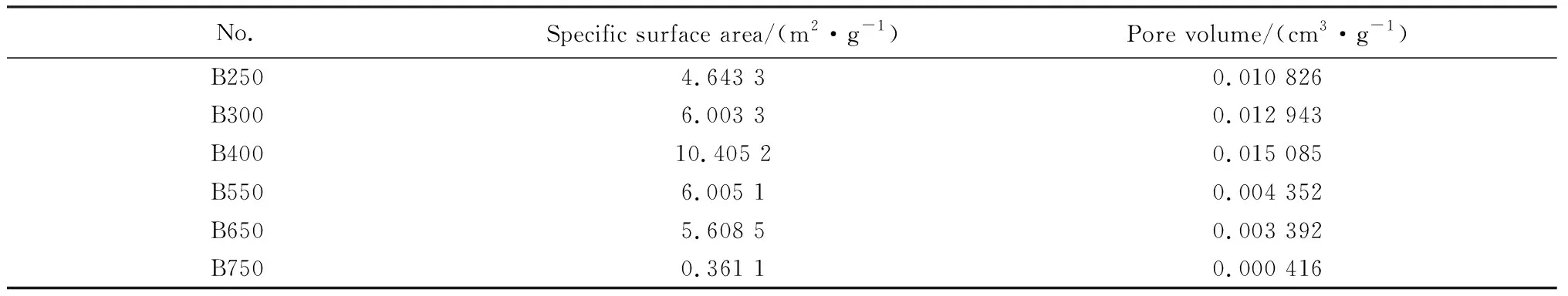
表1 所制备催化剂的比表面积和孔体积Table 1 Specific surface area and pore volume of as-prepared catalysts
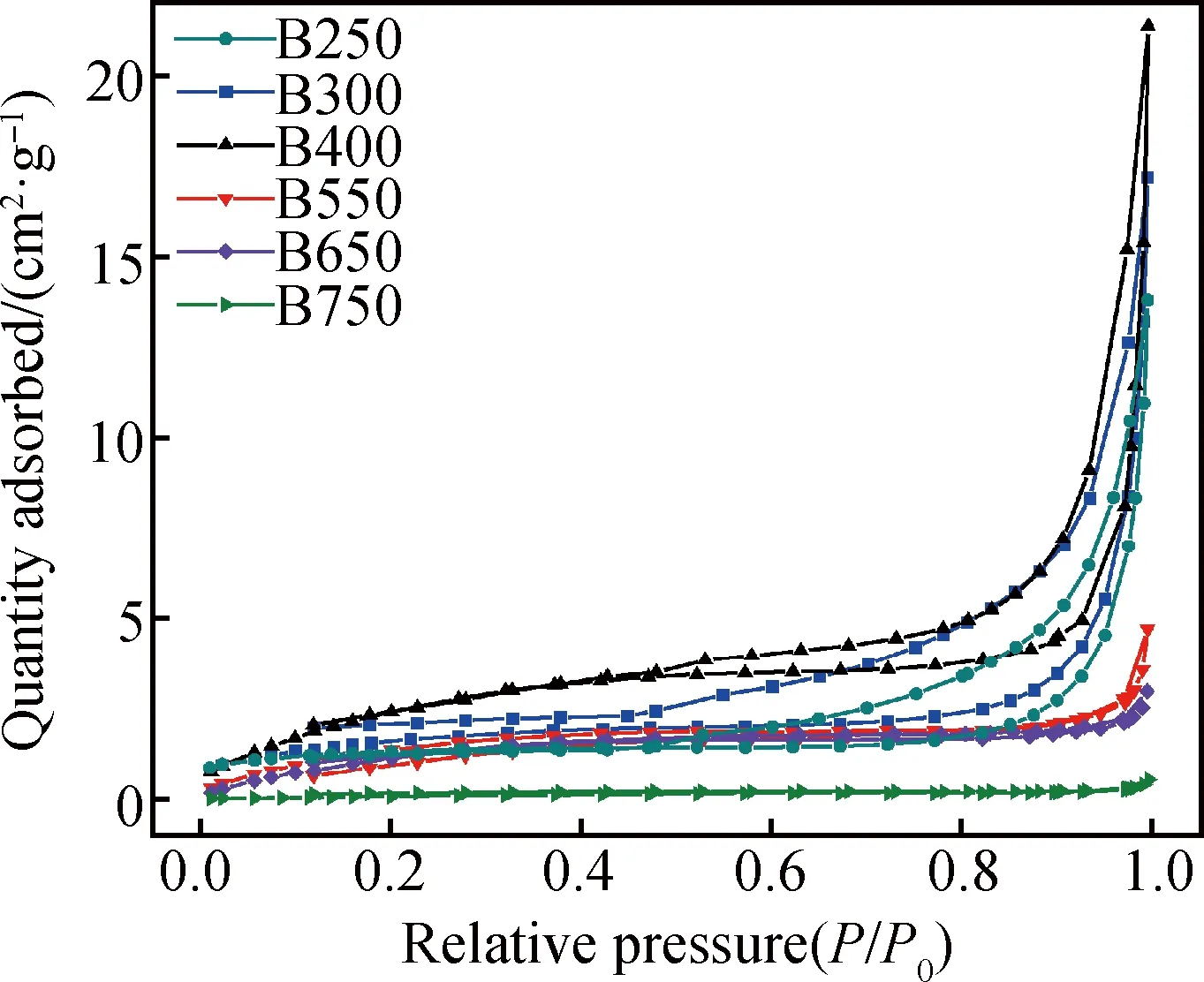
图3 所制备催化剂的氮气吸附脱附曲线Fig.3 Nitrogen adsorption and desorption curves of as-prepared catalysts
此外,本文还通过XPS对B300、B400、B550三个样品的元素组成及化学价态进行了表征,如图4(a)所示。从中可以看出,三个样品主要由Bi、O、Br和C元素组成,其中C元素的峰主要来自实验中样品表面所吸附的碳原子[16]。图4(b)、4(c)、4(d)分别展示了Bi3O4Br、Bi3O4Br/Bi12O17Br2以及Bi12O17Br2样品的Bi 4f,Br 3d、O 1s高分辨谱图。如图4(b)所示,Bi在164.11 eV、164.23 eV、164.25 eV与158.82 eV、158.88 eV、158.94 eV处所拟合的峰分别对应于Bi 4f5/2、Bi 4f7/2轨道,由此可知在这些样品中Bi是以+3价的形式存在[17]。如图4(c)所示,Br在69.33 eV、69.46 eV、69.56 eV与68.30 eV、68.44 eV、68.56 eV处的结合能分别与Br 3d3/2与Br 3d5/2相对应,说明三个样品中的Br均以-1价形式存在[18-19]。最后,三种样品的O 1s图谱如图4(d)所示,其中O在531.56 eV、531.33 eV、531.29 eV处的结合能表明O元素主要来自催化剂表面吸附的水或羟基中的氧,而O在529.59 eV、529.61 eV、529.65 eV的峰则表明催化剂中有Bi-O键的存在[20-21]。从上述分析结果可以看出:相较于纯的Bi3O4Br和Bi12O17Br2样品,Bi3O4Br/Bi12O17Br2复合催化剂的配位环境发生了变化,进一步证明了复合催化剂中Bi3O4Br和Bi12O17Br2之间存在着相互作用,表明Bi3O4Br/Bi12O17Br2复合光催化剂的成功制备。

图4 所制备催化剂的XPS谱图。(a)全谱;(b)Bi 4f;(c)Br 3d;(d)O 1sFig.4 XPS spectra of as-prepared catalysts. (a) Survey; (b) Bi 4f; (c) Br 3d; (d) O 1s
接着,采用紫外可见漫反射光谱(UV-Vis DRS)对所制催化剂的吸光特性进行表征,结果如图5所示。从图5(a)中可以看出,B300、B400、B550催化剂的吸收带边分别是485 nm、495 nm、512 nm。根据αhν=A(hν-Eg)n/2,其中α、h、ν、Eg与A分别为吸附系数、普朗克常数、光频率、带隙能,以及常数(直接带隙半导体n=1;间接带隙半导体n=4),计算得出Bi3O4Br(B300)和Bi12O17Br2(B550)的带隙分别为2.30 eV、2.20 eV,如图5(b)所示[22-23]。为阐明样品的能带结构,本文结合价带XPS光谱(VB-XPS)和Mott-Schottky谱图(MS)进行分析:首先,Mott-Schottky曲线用于获得所制备半导体催化剂的类型和平带电位(EFB)。如图5(c)所示,相对于Ag/AgCl电极,B300和B550的EFB分别为-0.63 eV和-0.70 eV,相对于标准氢电极(NHE)分别为-0.41 eV和-0.48 eV。且由B300和B550的1/C2和电势的比值表现为正斜率,因此其均为n型半导体,所以其费米能级Ef=EFB,因此B300和B550的Ef分别为-0.41 eV和-0.48 eV[10,24]。其次,VB-XPS用于测量催化剂的费米能级(Ef)和价带电势(EVB)之间的能隙(Evf)[25]。由图5(d)可得,B300和B550的Evf分别为1.86 eV和1.75 eV。最后,根据EVB=Evf+EFB,ECB=EVB-Eg,得出Bi3O4Br和Bi12O17Br2的EVB分别为1.45 V和1.27 V,ECB分别为-0.85 V和-0.93 V。

图5 B300、B400、B550样品的(a)UV-Vis DRS,(b)带隙计算图,(c)Mott-Schottky曲线图和(d)VB-XPS图Fig.5 (a) UV-Vis DRS, (b) plots of (ɑhν)1/2 versus photo energy (hν) of the samples, (c) Mott-Schottky curves and (d) VB-XPS spectra of B300, B400 and B550 samples
最后,对所制催化剂进行了一系列电化学性能测试。其中电化学阻抗(EIS)结果如图6(a)所示,Nyquist曲线半径反映了光催化剂的电子转移阻力,曲线半径越小,表明电荷分离效率越高。从中可以看出,Bi3O4Br/Bi12O17Br2(B400)比Bi12O17Br2(B550)和Bi3O4Br(B300)表现出更小的Nyquist曲线半径,表明其具有更好的电荷转移与电子空穴对分离能力,因此其展示出较优的光催化性能[26]。此外,光致发光谱(PL)通常用来阐述光生电子和空穴的复合能力,测试结果如图6(b)所示。由图可以看出Bi3O4Br/Bi12O17Br2复合催化剂的峰均低于Bi3O4Br与Bi12O17Br2,证明复合结构可以有效地抑制电子空穴对的复合[13]。EIS和PL光谱的综合结果证实了Bi3O4Br/Bi12O17Br2复合催化剂结构的有益作用,它促进了电荷的分离和转移,进而抑制了光生载流子的重组。

图6 所制备催化剂的(a)交流阻抗谱和(b)光致发光光谱Fig.6 (a) Electrochemical impedance spectra and (b) PL spectra of as-prepared catalysts
2.2 光催化剂活性测试
通过降解磺胺甲噁唑(SMX)来评价所制催化剂的光催化活性,结果如图7(a)所示。从中可以看出,在无光催化剂存在时,SMX在模拟太阳光下几乎未被降解,说明在本实验条件下,SMX的光解可以忽略不计。而随着制备过程中焙烧温度的升高,催化剂的活性先升高后降低,并在焙烧温度为400 ℃、催化剂为Bi3O4Br/Bi12O17Br2时达到最佳,经模拟太阳光照射30 min,SMX的降解率可以达到87%。相比纯Bi3O4Br和Bi12O17Br2催化剂,降解率分别提升了30%和24%。表明Bi3O4Br/Bi12O17Br2复合结构的形成有助于光催化性能的提高,同时结合BET、PL、EIS等表征,可以得出活性提高的主要原因在于随着焙烧温度的上升,所制催化剂的组成和晶型发生了变化,进而影响了催化剂的比表面积、能带结构,以及对太阳光的吸收能力和光生电荷的转移、分离能力。其中Bi3O4Br/Bi12O17Br2复合光催化剂由于具有大的比表面积有利于降解物的吸附及提供更多的反应活性位点,拥有高的电荷转移以及电子空穴对分离能力有利于光生电子空穴对参与反应,故此催化剂表现出了最优的光催化降解SMX性能。
催化剂的稳定性是其实际应用中的另一个关键因素[27]。因此,为了能够研究Bi3O4Br/Bi12O17Br2的稳定性,进行了SMX的光催化降解循环实验,如图7(b)所示。在循环过程中对使用过的Bi3O4Br/Bi12O17Br2不做任何处理,仅在空气下干燥后再次进行循环实验。从结果可以看出,Bi3O4Br/Bi12O17Br2催化剂的光催化活性在四次循环后仍表现出较好的降解活性,30 min内SMX的降解率仍可达到86.1%,表明其稳定性较好。由以上结论可以看出Bi3O4Br/Bi12O17Br2复合材料具有优异的光催化活性和较高的稳定性,因此,其有望成为一种高效的磺胺类药物水处理光催化剂。

图7 所制备催化剂:(a)在模拟太阳光下对磺胺甲恶唑的降解活性和(b)循环稳定性Fig.7 (a) Photocatalytic degradation activity of SMX and (b) recycling experiments of as-prepared catalysts under simulated solar irradiation
2.3 光催化机理分析
为了明确所制Bi3O4Br/Bi12O17Br2光催化剂的降解机理,对其进行了捕获剂实验和能带结构分析。其中捕获剂实验中分别用叔丁醇(IBP)、草酸铵(AO)、和氮气(N2)对活性物种·OH、h+、和·O2-进行了捕获,所得结果如图8(a)所示,从中可以看出,Bi3O4Br/Bi12O17Br2光催化剂的活性随着草酸铵和氮气的加入明显降低,而加入叔丁醇并没有使光催化剂的活性有明显的变化,说明Bi3O4Br/Bi12O17Br2光催化剂在降解过程中起主要作用的活性物种为h+和·O2-,而·OH几乎不起作用[13]。
其次,在能带结构分析中,计算了Bi3O4Br和Bi12O17Br2的能带位置。计算得出Bi3O4Br的价带(VB)值为1.45 V,导带(CB)值为-0.85 V,Bi12O17Br2的VB值为1.27 V,CB值为-0.93 V。
基于以上捕获剂实验和能带结构分析,推测出Bi3O4Br/Bi12O17Br2光催化剂的反应机理,如图8(b)所示。在Bi3O4Br/Bi12O17Br2复合催化剂体系中,首先两个催化剂均被光激发产生光生电子-空穴对,其后Bi12O17Br2导带上的电子移动到Bi3O4Br导带上,并与催化剂表面吸附的O2反应生成·O2-,之后与催化剂吸附的SMX发生降解反应。同时Bi3O4Br价带上的空穴迁移到Bi12O17Br2价带,直接参与光催化降解SMX反应。从而有效地促进了电荷的分离和转移,抑制了光生载流子的重组,最终Bi3O4Br/Bi12O17Br2复合催化剂体系表现出了较佳的光催化活性。

图8 Bi3O4Br/Bi12O17Br2复合催化剂的(a)捕获剂实验结果和(b)降解机理图Fig.8 (a) Scavenging experiment results and (b) photocatalytic degradation mechanism of Bi3O4Br/Bi12O17Br2
3 结 论
(1)本论文采用简单的水解-焙烧法,制备出了纯Bi3O4Br和Bi12O17Br2及Bi3O4Br/Bi12O17Br2复合催化剂。复合催化剂展示出优异的光催化活性,在模拟太阳光下照射30 min时,磺胺甲噁唑降解率达到87%,相比纯Bi3O4Br和Bi12O17Br2催化剂,它的降解率分别提升了30%和24%。
(2)XRD、SEM、XPS、EIS、PL和降解机理分析表明,复合催化剂优异的光催化活性归因于Bi3O4Br和Bi12O17Br2之间密切的界面接触以及强的相互作用,为电子和空穴的有效转移和分离提供了较强的化学界面,有利于光诱导载流子的分离。
(3)Bi3O4Br/Bi12O17Br2光催化剂在降解过程中起主要作用的活性物种为h+和·O2-。
——潘桂棠光生的地质情怀

