AIIR重建算法对70 kVp低管电压扫描主动脉CTA图像质量影响的研究
游永春,李万江,钟思华,帅桃,刘洪川,李真林
1.四川大学华西医院 放射科,四川 成都 610041;2.上海联影医疗科技股份有限公司 中央研究院,上海 201870
引言
主动脉夹层及动脉瘤是心血管系统疾病中的危急重症,因其发病后致死率可达40%[1-2]。主动脉CT血管成像(Computed Tomography Angiography,CTA)因具有广泛的可用性、扫描速度快和诊断准确性较高等优点,是诊断主动脉疾病最常用的影像学检查方法[3]。然而,主动脉CTA扫描存在X线电离辐射损伤、对比剂高速注射引发血管破裂与对比剂肾病等风险[4]。因此,研究者多通过降低管电压、增大螺距、降低对比剂流速及对比剂总量等方式以达到降低辐射剂量和对比剂用量的目的[5-6]。已有研究报道70 kV管电压结合迭代重建算法(Iterative Reconstruction,IR)能够有效地降低主动脉CTA的辐射剂量并提高图像质量[7],IR算法需要较长的处理时间以及充足的投影数据[8],并且应用范围有限,通常仅适用于体质指数(Body Mass Index,BMI)<25 kg/m2的患者。随着计算机重建技术的不断进步,人工智能图像域降噪算法相较于IR算法有更高的降噪能力[9]。目前,一种基于人工智能技术的迭代重建算法被提出,该算法结合了人工智能与迭代重建算法的优点,能够有效抑制噪声,使得重建出来的图像噪声更低、图像质量更高。然而,人工智能迭代重建(Artificial Intelligence Iterative Reconstruction,AIIR)算法有不同的重建等级,在低剂量CTA扫描时,最佳AIIR算法的等级选择是多少还未明确。因此,本研究探讨70 kVp低管电压下行主动脉CTA扫描时,AIIR算法对主动脉CTA图像质量的影响,并与混合迭代重建(Karl)图像进行对比。
1 对象与方法
1.1 研究对象
前瞻性纳入2021年3月至5月于四川大学华西医院行主动脉CTA检查的患者。排除标准:① 呼吸无法自主配合及意识不清、躁动的患者;② 对比剂过敏及严重心肾功能不全;③ 其他原因不能配合检查;④ 妊娠期妇女。根据排除标准,本研究总共纳入50例患者,其中男38例,女12例,平均年龄(58.34±14.16)岁,BMI为(23.61±2.83)kg/m2。其中A型主动脉夹层2例,主动脉夹层支架术后11例,动脉瘤25例,无主动脉病变12例。本研究通过我院生物医学伦理审查委员会批准,并在中国临床研究中心注册[批准文号2019年审(742)号,注册号为ChiCTR1900028475]。
1.2 研究方法
采用320排螺旋CT(上海联影 uCT960+)扫描,扫描范围锁骨至耻骨联合,扫描前对患者进行呼吸训练。扫描参数:管电压70 kV,管电流自动调节技术,参考管电流设置100 mAs,旋转时间0.5 s,螺距0.9937。所有患者经肘前静脉使用高压注射器注入高浓度非离子型对比剂碘美普尔(含碘400 mgI/mL),注射流速为3 mL/s,总量0.5 mL/kg,对比剂注射完毕后,以相同流速再注入30 mL生理盐水。血管监测扫描采用对比剂智能追踪技术,监测层面放置于降主动脉(气管分叉下2 cm),触发阈值为150 HU,达到阈值后延迟时间4 s触发扫描。
1.3 AIIR重建算法
AIIR是一种基于人工智能技术的模型迭代重建算法,对于传统模型迭代重建算法,其优化函数如式(1)。
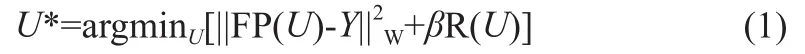
其中,U*为目标图像,U为输入图像,Y为原始数据,β为正则化系数,FP(U)为迭代过程,R(U)为正则化过程。对于该优化函数,AIIR则采用了一种卷积神经网络替代正则化项R(U),通过该神经网络学习图像中的噪声及纹理特征,能够根据所输入的图像自动地识别图像中的有用信号与噪声,从而实现图像质量提升与噪声抑制[10]。在网络训练过程中,将多组常规剂量的模型迭代重建图像及其相对应的模拟低剂量图像同时输入网络中,经过多轮训练,网络便能够充分学习信号与噪声之间的关系。因此,相比模型迭代重建算法,使用AIIR对图像进行重建,更能够有效地减少图像的噪声与伪影。此外,AIIR通过设置5个重建等级来控制图像噪声水平,在临床使用中可根据重建部位及使用习惯进行调整。
1.4 图像重建
50例患者的主动脉CTA原始数据传入探索者平台(ulnnovation-CT,R001,上海联影)进行多组重建,重建层厚、层间距均为0.5 mm。由于Karl 5级得到临床普遍认可,并且Karl 5级重建的图像最优[11-12],所以本研究选择Karl 5级重建图像作为参考。重建算法分别为AIIR 1-5级及Karl 5级,共获得6组重建数据。再将重建数据传入后处理工作站(uWS-CT),采用最大密度投影(Maximum Intensity Projection,MIP)的后处理方法重建图像。
1.5 图像评价
1.5.1 客观评价
在主动脉根部层面测量升主动脉;肺动脉干分叉层面测量降主动脉;腹腔干层面测量腹主动脉;髂动脉分叉下2 cm层面测量左髂动脉、右髂动脉以及同层面脊柱旁的肌肉的CT值和SD值。6组图像所有感兴趣区(Region of Interest,ROI)大小、形态、位置保持一致,ROI选择避开金属支架及运动引起的伪影层面、钙化斑块等,ROI测量均选择真腔。计算ROI的信噪比(Signal to Noise Ratio,SNR)和对比噪声比(Contrast to Noise Ratio,CNR),计算公式为式(2)~ (3)。

1.5.2 主观评价
分别由两名具有5年和10年工作经验的高年资放射科诊断医师采用盲法和随机的方式独立评估50例患者的所有重建图像。采用5分法评价总体图像质量:5分:主动脉边界光滑,三维重组图像管腔对比度极好,噪声低,无伪影;4分:主动脉边界光滑,三维重组图像管腔对比度好,噪声小,有少量伪影;3分:主动脉边界欠清,三维重组图像管腔对比度尚可,噪声明显,有伪影,尚可满足诊断;2分:主动脉边界毛躁,三维重组图像管腔对比度差,伪影较重;1分:主动脉边界毛躁,三维重组图像管腔对比度极差,伪影严重。另外采用李克特5分法对图像“蜡像感”程度进行评价:1分:完全可接受图像的“蜡像感”情况,图像细节显示清晰;2分:可接受图像的“蜡像感”情况,图像细节显示较清晰;3分:尚可接受图像的“蜡像感”情况,图像细节显示一般;4分:不能接受图像的“蜡像感”情况,图像细节显示模糊;5分:完全不能接受图像的“蜡像感”情况,图像细节丢失严重[13-15]。
1.6 统计学分析
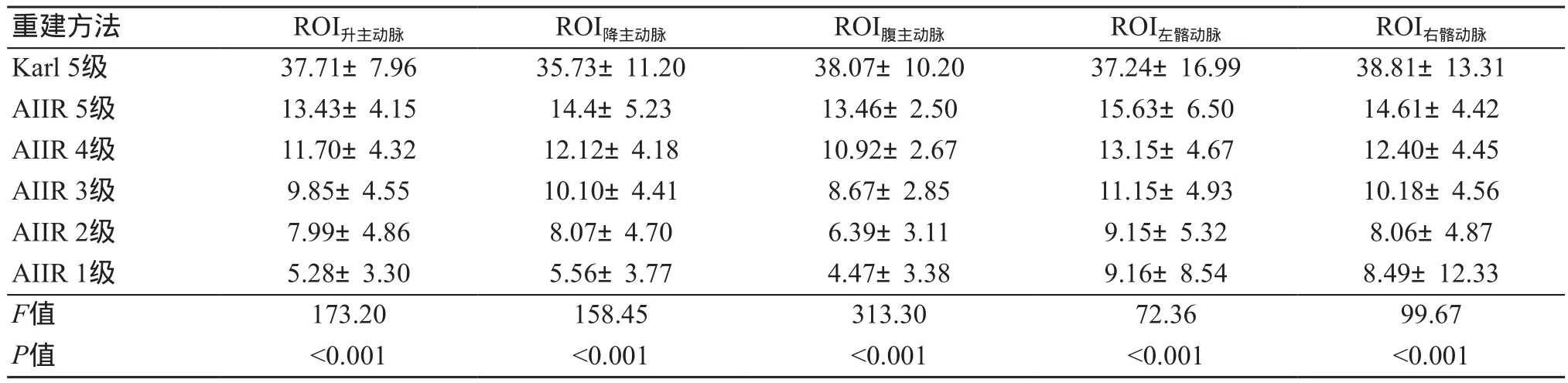
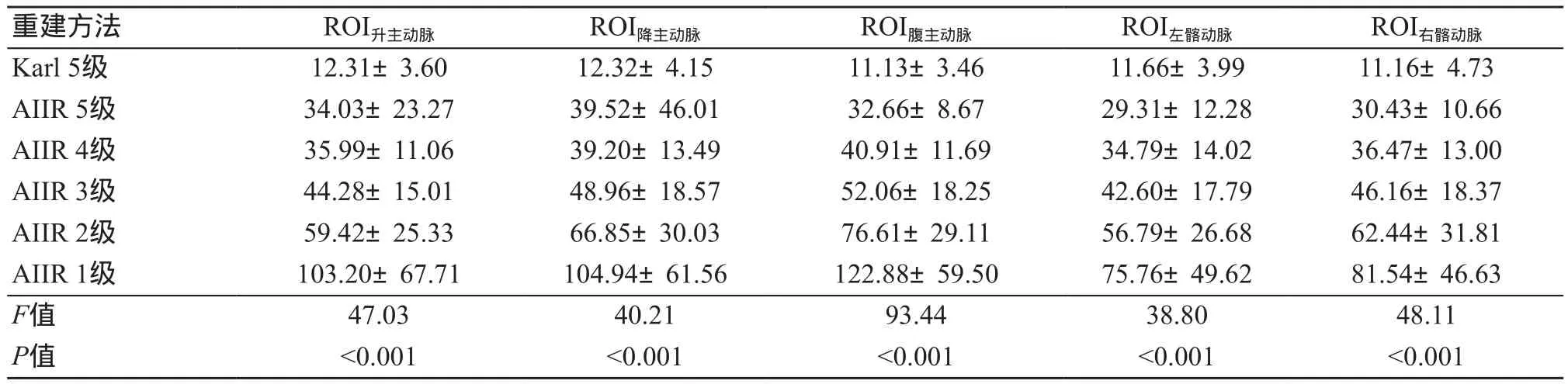
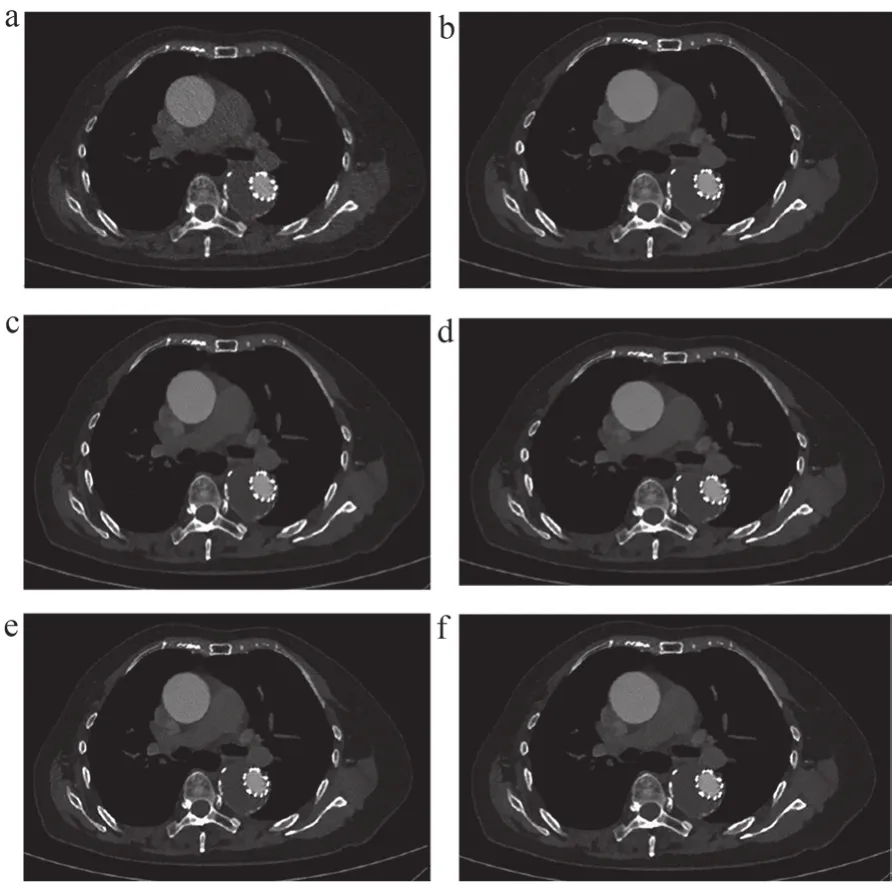
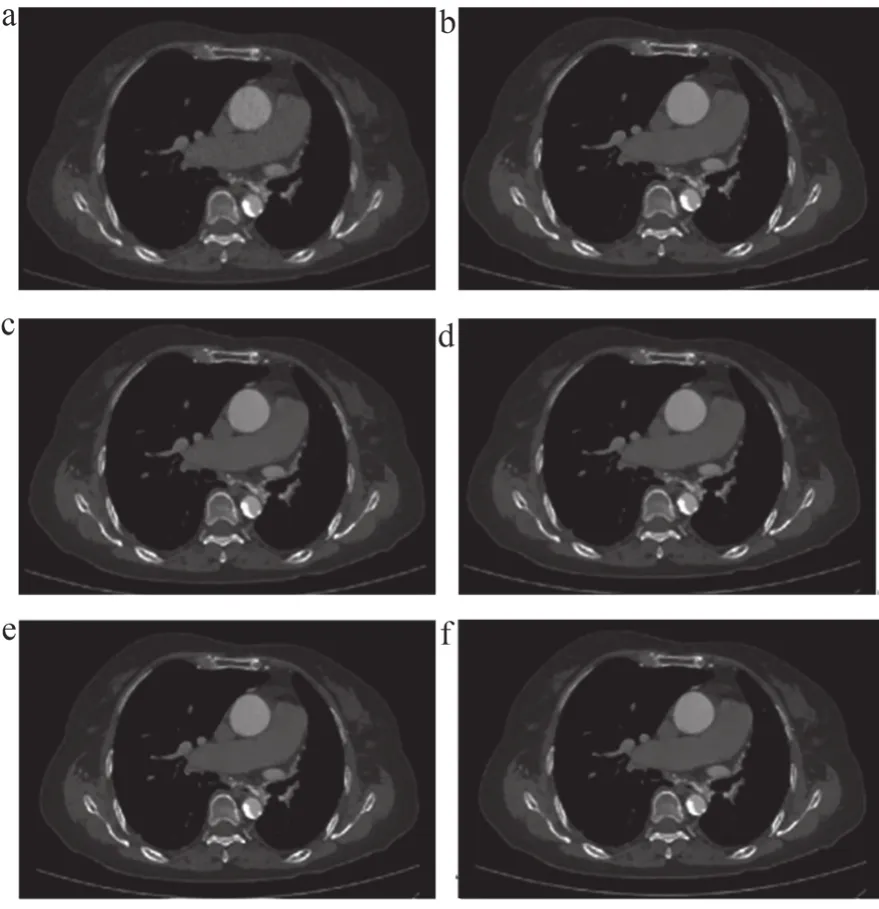
采用SPSS 23.0统计分析软件对数据进行分析。计量资料用均数±标准差表示。采用单因素方差分析(One-Way ANOVA)比较6组图像间客观评价指标(SD、SNR、CNR)的大小,并采用LSD进行事后两两检验。图像总体质量及图像“蜡像感”情况的主观评分对比采用Fridman检验,两名诊断医师对图像质量主观评分的一致性评价采用Cohen Kappa检验(Kappa值≥0.75一致性良好,0.4 通过数据统计分析后,6组重建方式所得图像各血管(升主动脉、降主动脉、腹主动脉、左髂动脉、右髂动脉)的SD值、SNR、CNR之间,差异均具有统计学意义(P<0.05)。随着重建等级的升高,AIIR组的SD值升高,SNR和CNR降低,差异均具有统计学意义(P<0.05),但其SD值、SNR和CNR均优于Karl组。见表1~3。 表1 6组重建图像的SD值分析(n=50) 表2 6组重建图像的SNR值分析(n=50) 表3 6组重建图像的CNR值分析(n=50) 不同算法重建图像质量及图像细节分析主观评分差异具有统计学意义(P<0.05),在图像总体质量方面,AIIR 5级评分高于其余各组图像。随着AIIR重建算法等级的升高,图像细节显示主观评分逐级降低,其中AIIR 5级图像“蜡像感”评分最低,图像“蜡像感”程度完全可接受,细节显示清晰。两名医师之间的主观评分具有较好的一致性(Kappa=0.57~0.87,P<0.001),见表4和图1~2。 图1 患者女,77岁,主动脉夹层腔内支架修复术后 图2 患者女,70岁,胸痛入院,降主动脉广泛钙化,管腔狭窄,最窄约0.8 cm 表4 两名放射科医师图像质量评分结果(n=50) CTA作为主动脉疾病诊断常用的检查方法被广泛应用于临床,但由于主动脉扫描范围广,导致辐射剂量大。近年来,随着CT新技术的不断更替,低剂量扫描与迭代重建算法结合进而改善主动脉图像质量的研究已经成为热点。作为一种全新的基于人工智能技术的迭代重建算法,AIIR在提升低剂量图像质量方面具有巨大的潜力。因此,本研究探讨在低剂量扫描情况下,AIIR不同重建等级对主动脉CTA图像质量的影响,同时与传统迭代重建算法Karl进行比较。 本研究分别采用Karl 5级和AIIR 1~5级,共6种不同重建算法对扫描数据进行重建,并通过主客观评价的方式评估主动脉图像质量。相比于Karl算法,AIIR算法在各个重建等级下均能够显著地提高主动脉的SNR及CNR,随着AIIR重建等级的降低,SNR及CNR逐渐升高,但是图像出现“蜡像感”的程度增加,存在图像失真的情况。从主观评分结果分析,在总体图像质量方面,AIIR 5级评分最高,所得主动脉图像边界光滑,噪声低,无伪影。在重建所得图像“蜡像”感方面,AIIR 5级的评分最低,图像“蜡像感”程度完全可接受,对于细节的显示也最好。对于AIIR 1~4级,重建所得图像的“蜡像感”较强,存在图像失真与细节丢失的情况。这是因为高频噪声被去除,改变了图像的纹理结构,需通过提高重建等级,逐渐恢复图像中的高频噪声,才能有利于细节的显示。综合主客观评分,在保证图像整体质量与真实感的情况下,AIIR 5级的效果最佳。本研究采用了低管电压(70 kV)作为实验的扫描方案,由于管电压降低,使X射线的能量接近碘对比剂的K边缘值,增加对比剂的光电效应,从而提高血管与背景组织的对比度。因此,可以进一步降低对比剂流速及总量(3 mL/s、0.5 mL/kg),进而降低对比剂渗漏的风险,实现“三低”扫描[16]。研究中平均对比剂用量为(32.91±5.28) mL,平均有效辐射剂量为(1.56±0.16)mSv,但由于管电压的降低,导致图像质量下降,需结合图像重建算法进一步降低图像噪声以达到临床诊断需求。因此,可以结合AIIR技术,实现“三低”扫描,进一步改善图像质量。 目前主要的迭代重建算法包括:混合迭代重建、统计计数迭代重建以及模型迭代重建[17-19]。迭代重建算法的主要原理是对投影的模拟图像进行迭代,并对投影数据进行迭代修正,以此达到降低图像噪声的目的[20-22]。但是这些算法在减少图像噪声与伪影的同时,也会改变原始数据中噪声的分布情况,使得图像纹理结构改变,进而在一定程度上影响临床诊断[23],因此,不能使用过高的迭代重建等级,最常用的迭代重建技术ASIR-V权重通常选择40%~60%[24],由于不能使用过高的迭代等级,低剂量通常应用于小体重患者。随着人工智能技术的快速发展,基于人工智能技术的图像重建算法逐渐应用于医学领域中。该算法在训练过程中,通过大数据能够充分学习图像中信号与噪声的关系,以及噪声的频率分布情况,在不改变图像纹理结构的情况下,实现图像降噪。因此,为了兼顾图像降噪与维持图像质量,AIIR重建算法将人工智能技术引入模型迭代重建中,由此不仅能够去除低剂量图像中的条纹伪影,还可以实现图像降噪,使得重建出来的图像具有较好的对比度及细节显示。 本研究存在一些不足之处:① 研究样本量少,仅研究50例患者,因此,增加样本量及获取更为详尽的研究数据有待后期进一步探索;② 本研究着重讨论图像质量,未对主动脉各种疾病进行分类研究,将在以后的研究中进一步探讨。 综上所述,在低管电压下行主动脉扫描时,AIIR重建算法能够显著降低图像噪声。并且在改善图像质量及维持图像真实感的情况下,AIIR 5级算法在70 kV低管电压扫描条件下降噪效能最佳,既能提高图像修正能力,也能提高血管与背景噪声的对比。2 结果
2.1 图像质量客观评价
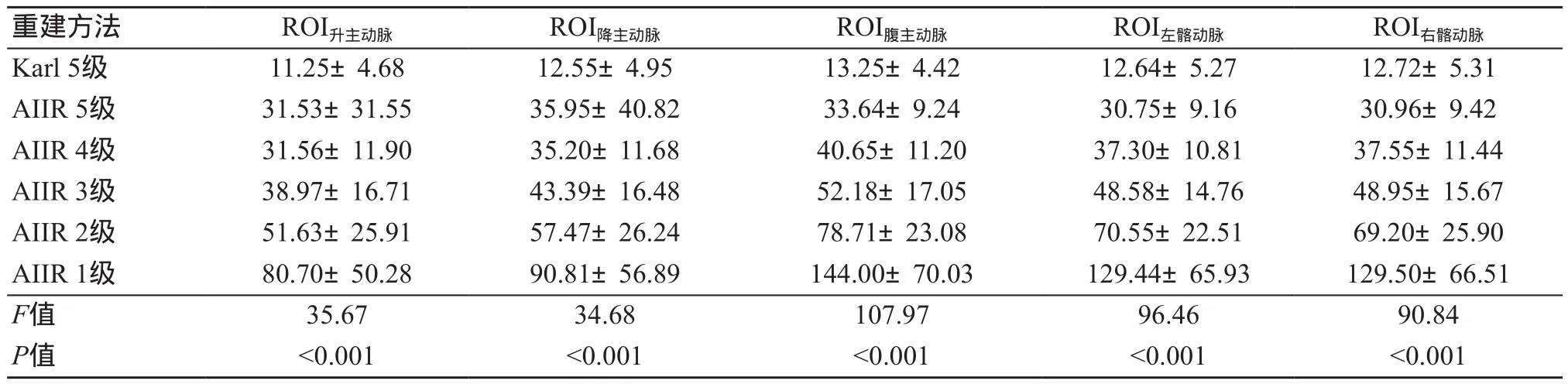
2.2 图像质量主观评价
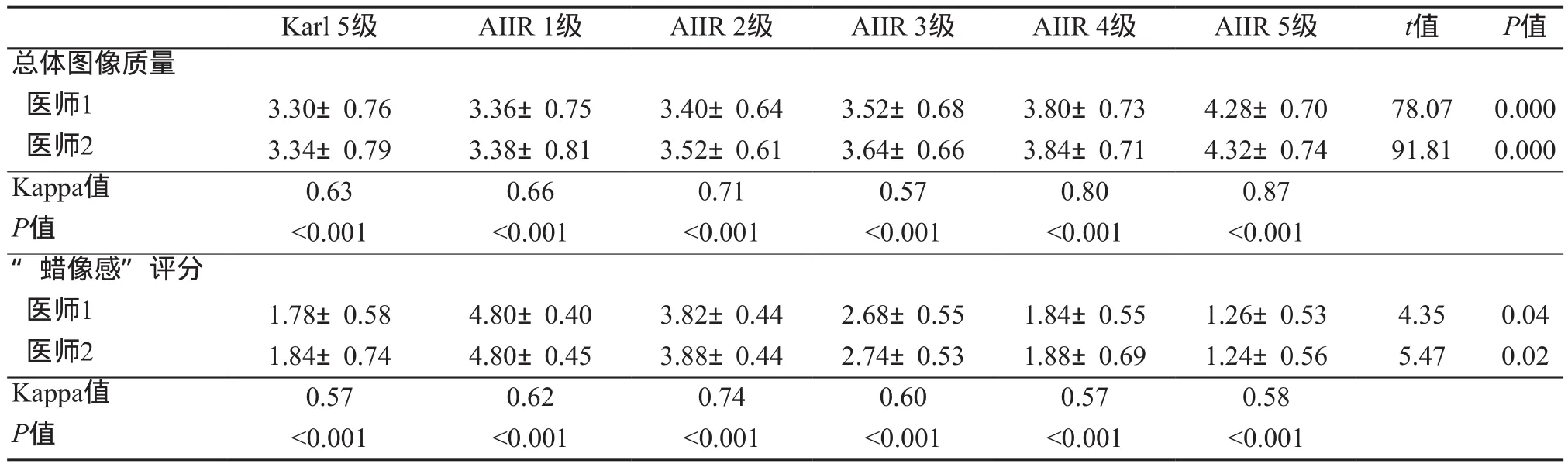
3 讨论