四酸敞口-低温蒸干-原子荧光光谱法测定地球化学样品中的硒❶
刘金龙 王艳超 张霞
中化地质矿山总局地质研究院,北京 100013
硒是稀散元素,其地球化学行为在很大程度上与硫的行为相似。我国的硒矿主要集中在西北和长江中下游。硒是多金属矿床的指示元素,可有效的运用到多金属矿的勘查中[1-4]。除此之外,硒还被广泛应用于玻璃工业、冶金工业、电子工业、国防工业、化工、医学和农业。因此建立一种检出限低、精密度高、操作简单快速、适合地质化学样品批量测定的方法具有非常重要的现实意义。
目前常用测定硒的方法有氢化物-原子荧光光谱法[5-9]、分光光度法[10]、原子吸收光谱法[11]、电感耦合等离子体发射光谱法[12]、电感耦合等离子体质谱法[13]。分光光度法测定繁琐;原子吸收法测定样品灵敏度不高、稳定性不足;电感耦合等离子体发射光谱法需要增加气动雾化装置,样品实际利用率低,且灵敏度不够;电感耦合等离子体质谱技术受到同位素的干扰严重。氢化物-原子荧光光谱法测定地质化学样品中的硒具有操作简便、分析速度快、灵敏度高、干扰小等优点,被广泛应用到地质、冶金、环境样品中硒的测定。
由于硒元素具有易挥发性,许多专家和学者如柴昌信[14]、郑民奇[15]、董亚妮[16]、梁丽娜[17]等提出,前处理要蒸至小体积,防止硒元素挥发;虽然前处理溶矿方法不同,但都需要保持溶液状态,从而防止硒的损失。在实际操作中,由于样品量过大,很难保证小体积状态,通常是蒸至湿盐状态,影响实验效率和结果的稳定性。另外一般硒元素溶矿方法采用两酸或者三酸的溶矿模式,笔者发现采用HCl-HNO3-HClO4-HF四酸处理样品,准确度和稳定性都有一定程度的提高,溶矿效果比两酸、三酸效果会更好。
1 测试方法
1.1 仪器及工作条件
本次测试采用的原子荧光光谱仪为AF-640A原子荧光光谱仪(北京瑞利分析仪器公司);硒高强度空心阴极灯。仪器的最佳工作参数见表1。
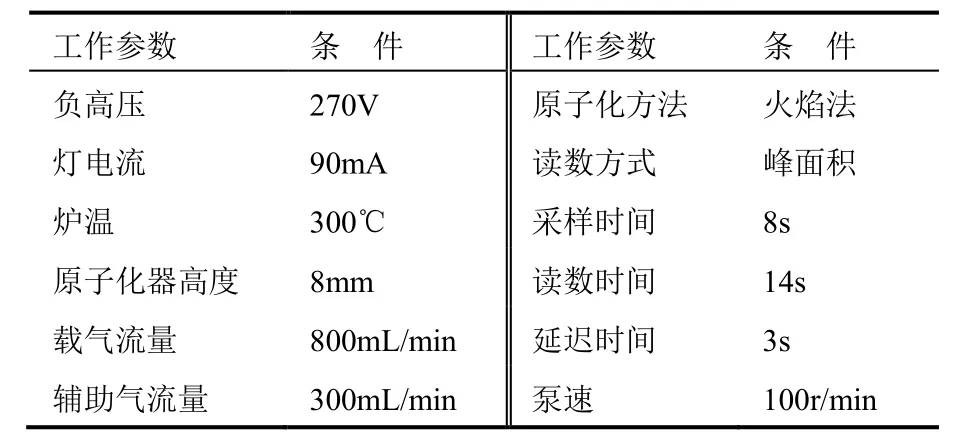
表1 仪器最佳参数 Table 1 Optimum Instrument Parameters
1.2 主要试剂
主要试剂为硒粉、三氯化铁、硼氢化钾、氢氧化钾、王水、硝酸、氢氟酸、高氯酸、盐酸。其中盐酸、硝酸为优级纯,其他试剂为分析纯,水为去离子水。
1.3 主要溶液配制
硒标准储备溶液:称取0.1000g光谱纯硒粉,置于200mL烧杯中,盖上表面皿,沿杯壁加入20mL(1∶1)HNO3溶液,于自动控温电热板上低温加热溶解。取下,加3mL HClO4,加热至高氯酸冒白烟,取下冷却,用水吹洗表面皿和烧杯壁,继续加热至冒白烟。冷却至室温,移入100mL容量瓶中,用水稀释至刻度,摇匀,得c(Se)=1000μg/mL。
移取上述溶液(1000μg/mL),逐级稀释10000倍,得c(Se)=100ng/mL。
将上述溶液稀释100倍,制得硒标准使用溶液c(Se)=1.0ng/mL。
Fe3+盐溶液(25mg/mL):121g三氯化铁(FeCl3·6H2O)溶于200mL(1∶1)HCI中,移入1000mL容量瓶中,补加300mL盐酸,定容,摇匀。
硼氢化钾溶液(20g/L):2g氢氧化钾溶于200mL水中,加20g硼氢化钾(分析纯)片使之溶解,用水稀释至1000mL。用时现配。
1.4 实验方法
本文采用HCl-HNO3-HClO4-HF四酸处理样品,具体溶矿方式为:称取0.2500g地球化学样品于聚四氟乙烯坩埚中,加少量水润湿,加入10mL逆王水,置于电热板上低温加热,控温溶解1h。再加入10mL混合酸(VHF:VHClO4=5∶2),继续升温蒸发至刚冒白烟时,控制电热板在低温140℃下蒸干。然后用10mL(1∶1)盐酸提取,在低温电热板上加热2~3min,取下,冷却,移入25mL比色管中,再加入1mL Fe3+盐溶液(25mg/mL),用去离子水稀释至刻度,摇匀。以10%盐酸为载流,20g/L硼氢化钾为反应溶液,原子荧光光谱仪测定。
2 测试结果与讨论
本文采用HCl-HNO3-HClO4-HF四酸处理样品,且样品前处理用逆王水溶矿,起预消解的作用。之后续用氢氟酸、高氯酸完全分解样品。由于硒为易挥发性元素,在溶矿过程中,高温下硒元素逸出,使结果偏低,所以本体系在高氯酸冒烟后控制温度140℃左右蒸干,最大限度的降低了样品分解时易挥发元素硒的损失,使测定结果更加准确。
2.1 溶液蒸干温度的影响
由于硒为易挥发元素,所以首选溶液制备时蒸至湿盐状,以防止硒元素的挥发,可是在实际生产中,如果样品量过大,湿盐状保证起来就有一定难度,影响最后结果的准确性。本试验多目标12个地球化学样品一级国家标准物质,每个标准物质测试12份,按照上述方法进行实验,以验证溶液蒸至湿盐状或者低温蒸干和高温蒸干的影响,结果见表2。

表2 提取液最终状态结果对比 Table 2 Comparison of the final state of the extract
多目标地球化学样品规范[18]中要求不大于0.05,RSD%小于10%。由上表可知,高温蒸干中12个标准物质有6个大于0.05,不符合要求。
溶液蒸至湿盐状和低温蒸干的准确度和稳定性都满足要求,且蒸至湿盐状明显比低温蒸干RSD%值偏低,说明蒸至湿盐状比低温蒸干稳定性更好。但是由于样品量大、电热板温度不均匀等原因,保证每一个样品都是湿盐状,操作起来很是繁琐,而低温蒸干只要控制好温度,操作起来相对简单,所以在都满足要求的情况下,选择低温蒸干。
2.2 前处理逆王水的用量
本方法前处理样品先加入逆王水溶矿,将样品预溶解,再加入硝酸和氢氟酸完全打开样品,最后用盐酸提取。这里就会涉及到前处理逆王水和最后用的盐酸的用量。本文选取地球化学样品一级国家标准物质GSD-9,按照上述实验过程,每份样品做12次,以确定前处理所需逆王水用量。结果见表3。

表3 逆王水用量 Table 3 Reverse aqua regia dosage
由表3可以看出随着逆王水用量的增加,结果的准确度和稳定性有明显的改善作用,当逆王水为10mL时趋于稳定,所以选择逆王水10mL。
2.3 提取液的选择
由于硒元素具有挥发性,且最后溶液中硒IV价被还原到VI价,柴昌信等[14]提出提取液中不能存在硝酸根离子,会使硒元素结果偏低,可是郑民奇等[15]提出溶液介质为硝酸,所以本文选取地球化学样品一级国家标准物质GSD-9,按照上述实验方法进行实验,每份样品做12次,改变提取液介质为20%硝酸、20%盐酸和20%王水,并且计算每组信号强度,结果见表4。
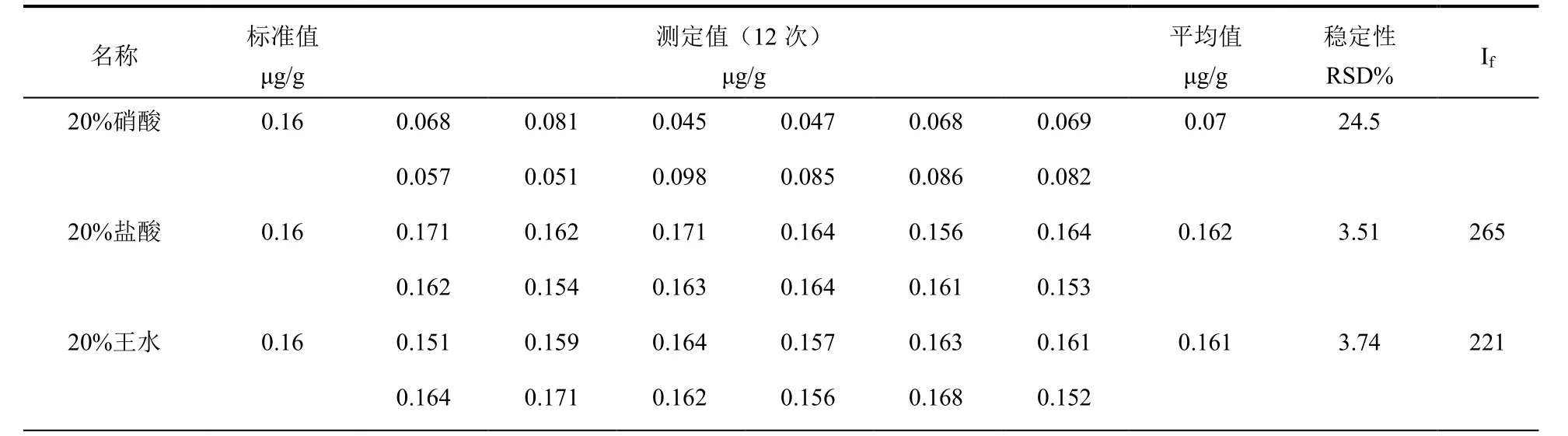
表4 提取液的选择 Table 4 Selection of extract
由表4可知硝酸溶液提取测定结果不准确。盐酸和王水测定结果的准确度和稳定性都符合要求,且相差不大,但是盐酸比王水荧光强度稍强,且盐酸相对王水更加简单,所以选择盐酸为介质。
2.4 提取液盐酸的用量
选取标准物质GSD-9,按照前面实验步骤选择不同提取液(1∶1)盐酸的用量。固定其他测定条件,测定硒元素荧光强度,结果见图1。
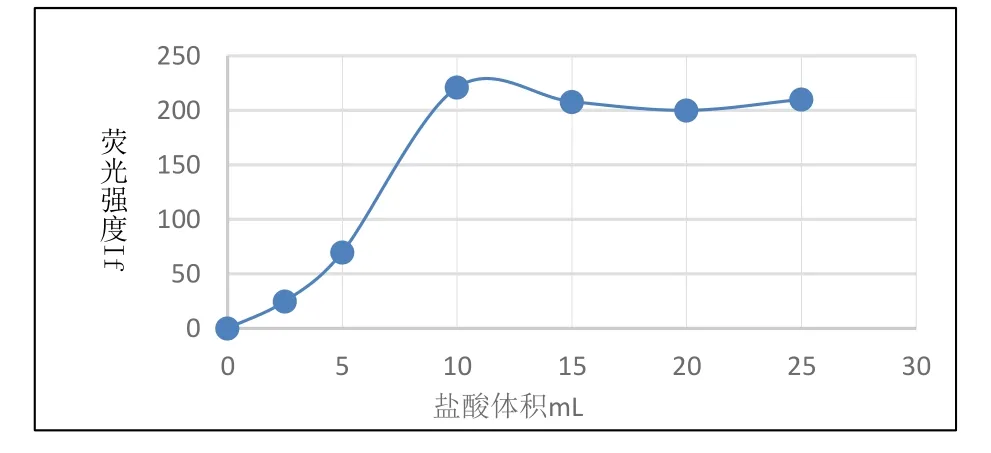
图1 盐酸体积与荧光强度之间关系 Fig. 1 Relationship between HCl volume and fluorescence intensity
由图1可以看出,随着盐酸用量的增大荧光强度有突变效果,当盐酸体积为10mL时,趋于稳定,信号最强,所以选择盐酸体积为10mL。
2.5 硼氢化钾与铁盐浓度
原子荧光中硼氢化钾与硒反应生成硒化氢(H2Se),当硼氢化钾浓度过低时不能与硒完全反应,使结果偏低;然而当溶液中硼氢化钾浓度过高时,会加剧与盐酸的反应生成大量氢气,从而抑制了硼氢化钾与硒的反应。选择不同浓度的硼氢化钾溶液,测定地球化学样品一级标准物质GSD-9的荧光强度,发现当硼氢化钾浓度超过20g/L时,硒荧光强度趋于稳定,所以选择硼氢化钾浓度为20g/L,这与董亚妮等[16]提出的硼氢化钾浓度基本一致。
原子荧光法测定样品中的硒时,会受到铜、铅等离子的干扰,加入铁盐能有效抑制这些干扰的发生。根据实验结果发现随着铁盐浓度的增大信号值也会相应增加,当铁盐浓度大于0.7mg/mL时趋于稳定。考虑到干扰的情况,并根据梁丽娜等[17]对铁盐的报导,本实验选择铁盐浓度为1.00mg/mL。当溶液中干扰离子含量较高时,可适当增加铁盐含量。
2.6 标准曲线和方法检出限
移取硒标准溶液c(Se)=100ng/mL于100mL容量瓶中,配置成0.00、0.20、0.50、1.00、2.00、4.00、8.00、10.00、20.00、50.00ng/L的标准溶液,其中加入40mL(1:1)盐酸溶液、4mL Fe3+盐溶液(25mg/mL),线性范围内与荧光强度呈良好的线性关系:y=7.658x-4.824,相关系数为0.9994,同时测定12个空白溶液,以三倍标准偏差计算硒的检出限为0.0043μg/g,结果见表5。
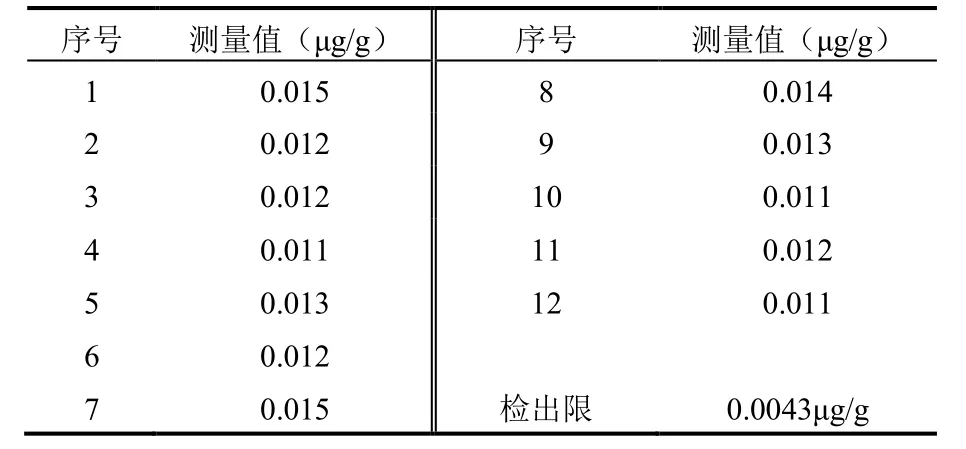
表5 硒元素检出限 Table 5 Detection Limits of Selenium
2.7 方法准确度和精密度
本试验选择12个地球化学样品一级国家标准物质,每个标准物质平行12份,按照实验方法进行准确度实验,计算相对误差和加标回收率;对样品进行平行分析,计算相对标准偏差。结果见表6。

表6 方法准确度与精密度 Table 6 Method Accuracy and Precision
由表6中可以看出标准物质相对误差范围为-7.27%~8.89%,加标回收率为94.5%~105%,多次测定相对标准偏差均小于10%,符合多目标地球化学样品规范[18]的要求。
3 结论
本文采用HCl-HNO3-HClO4-HF四酸处理样品,低温蒸干,防止硒元素挥发,盐酸提取将硒还原为Ⅳ价状态,铁盐抑制过渡金属离子的干扰,直接氢化物-原子荧光光谱仪测定。该方法检出限为0.0043μg/g,准确度相对误差范围为-7.27%~8.89%,加标回收率为94.5%~105%,精密度相对标准偏差小于10%,方法速度快,过程简单,易于控制,适合大批量样品的分析。

