栀子饮片、标准汤剂、中间体、配方颗粒的HPLC 指纹图谱相关性研究
展 月,赵 俞,鄢必新,刘 鑫,徐 云,秦思莲,李生勇,王 鑫*
(1.吉林修正药业新药开发有限公司,长春130103;2. 修正药药业集团股份有限公司,通化134001)
栀子为茜草科植物栀子Gardenia jasminoides Ellis 的干燥成熟果实,味苦,性寒;归心、肺及三焦经;具有泻火除烦,清热利湿,凉血解毒;外用消肿止痛的功效;临床主要用于热病心烦,湿热黄疸,淋证涩痛,血热吐衄,目赤肿痛,火毒疮疡;外治扭挫伤痛等症。现代药理表明栀子中含多种化学成分,包括环烯醚萜苷类、三萜类、黄酮类、有机酸酯类等,其中山栀苷、栀子苷等环烯醚萜苷类成分为栀子的主要有效成分。 本研究采用HPLC 法,建立栀子饮片、标准汤剂、中间体、配方颗粒指纹图谱,评价其相关性,为栀子配方颗粒制备全过程的质量控制提供科学参考依据[1]。
1 材料
1.1 试剂
乙腈、甲酸为色谱纯;甲醇为分析纯;水为纯化水。
1.2 仪器
AE205DU 型分析天平 (上海梅特勒-托利多仪器有限公司);KQ-300DE 型数控超声波清洗器 (昆山市超声仪器有限公司);Ultimate 3000 高效液相色谱仪DAD 检测器。
1.3 试药
栀子饮片15 批(4 批购自江西临川批号:YC040-161010、YC009 -160904、YC009 -161008、YC009 -161009;3 批购自湖南平江:YC009-161005、YC009-161006、YC009-161007;4 批购自湖北宜昌:YC009-170411、YC009 -170412、YC009 -170413、YC009 -170414;4 批购自江西樟树:YC009-160901、YC009-160902、YC009-170416、YC009-170417);栀子对照药材 (批号:120986-201309); 栀子苷对照品 (批号:110749-201316)、 鸡矢藤次苷甲酯 (批号:110749-201316)、羟异栀子苷(批号:110749-201316)、Jasminoside B(批号:110749-201316)、京尼平-1-龙胆二糖苷(批号:110749-201316)、山栀子苷(批号:110749-201316)、苦藏花素(批号:110749-201316),购自中国食品药品检定研究院。
2 方法与结果
2.1 栀子片、标准汤剂、中间体、配方颗粒中栀子苷含量测定
2.1.1 色谱条件与系统适用性[2-3]
以十八烷基硅烷键合硅胶为填充剂; 以乙腈-水(15∶85 ) 为流动相,流速为1.0mL/min,柱温为30℃,检测波长238nm,进样量10μL。 理论板数按栀子苷峰计算应不低于1500。
2.1.2 溶液制备
2.1.2.1 对照品溶液制备
取栀子苷对照品适量, 精密称定, 加甲醇制成每1ml 分别含30μg 的溶液,即得。
2.1.2.2 供品溶液制备
栀子饮片供试品溶液的制备同2020 《中国药典》栀子饮片项下方法,栀子标准汤剂、中间体、配方颗粒供试品制备方法: 取本品约0.1g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,密塞,称定重量,超声处理(功率250W,频率40kHz)30 分钟,取出,放冷,再称定重量,再用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液3ml,置25ml 量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.1.2.3 样品含量测定
结果见表1, 栀子饮片中栀子苷含量均大于1.5%,符合《中国药典》2020 年版一部 “栀子” 项下有关的各项规定。通过对15 批栀子饮片及其制备的标准汤剂冻干粉、中间体、成品栀子苷含量测定研究,栀子苷含量范围为12.0%~17.6%,平均含量为14.8%,中间体(干膏粉) 栀子苷含量范围为13.1%~17.6%, 平均含量为14.5%,配方颗粒栀子苷含量范围为9.1%~15.9%,平均含量为12.6%,
从表1 数据可发现栀子标准汤剂、中间体、配方颗粒,栀子苷含量相差小于±3,说明三者含量基本一致,栀子标准汤剂出膏率范围为19.1~29.0%,栀子苷转移率范围为57.0~85.2%,栀子中间体的浸膏收率范围为17.2~28.0%,栀子苷转移率范围为61.0~73.2%,均在栀子标准汤剂出膏率及栀子苷转移率范围之内, 说明栀子配方颗粒制备工艺合理, 因栀子配方颗粒在制备过程中加入辅料,故栀子苷含量较中间体低。
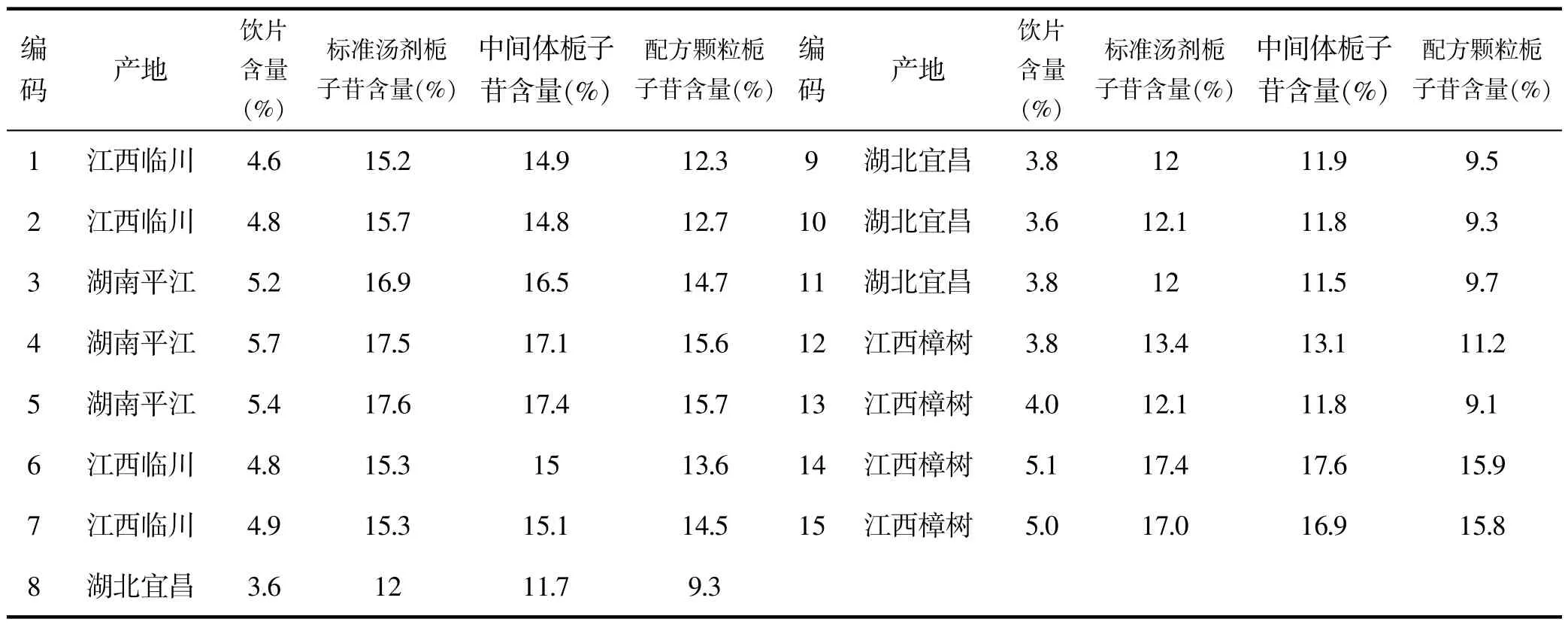
表1 栀子饮片、标准汤剂、中间体、配方颗粒中栀子苷含量
2.2 栀子饮片、标准汤剂、中间体、配方颗粒HPLC 指纹图谱的建立
2.2.1 色谱条件与系统适用性试验
色谱柱:Kromasil 100-5-C18( 250mm×4.6 mm,5μm);流动相:以乙腈为流动相A,以0.5%甲酸溶液为流动相B,梯度洗脱(0~10min,1%A→4%A;10~25min,4%A;25~50min,4%A→8%A;50~55min,8%A→10%A;55~65min,10%A→12%A;65~80min,12%A。 ) 流速为1ml/min; 检测波长为254nm; 柱温为35℃, 进样量:10μl。 理论板数按栀子苷峰计算应不低于1500。
2.2.2 参照物溶液制备
取山栀子苷、鸡矢藤次苷甲酯、羟异栀子苷、Jasminoside B、京尼平-1-龙胆二糖苷、栀子苷、苦藏花素适量,精密称定,分别加甲醇制成每1ml 分别含0.2mg的混合溶液,即得。取栀子对照药材约0.3g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,密塞,称定重量,超声处理(功率250W,频率40kHz)30 分钟,取出,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.3 供试品溶液制备方法[4,5]
栀子饮片:取本品粉末(过四号筛)约0.3g,精密称定, 精密加甲醇50ml, 称定重量, 超声处理 (功率250W,频率40kHz)30 分钟,取出,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,即得。
栀子标准汤剂、配方颗粒、中间体:取本品约0.1g,精密称定, 置具塞锥形瓶中, 精密加入甲醇50ml,密塞,称定重量,超声处理(功率250W,频率40kHz)30分钟,取出,放冷,再称定重量,再用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液3ml,置25ml 量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.3 方法学考察
2.3.1 精密度试验
取同一批栀子标准汤剂,按照2.2.3 项下条件制备供试品溶液连续进样6 次,记录色谱图,结果各共有峰相对保留时间和相对峰面积RSD<3%, 表明精密度良好。
2.3.2 重复性试验
取同一批次栀子标准汤剂供试品6 份,按照2.2.3项下条件制备供试品溶液, 结果各共有峰相对保留时间和相对峰面积RSD<3% ,表明重复性良好。
2.3.3 稳定性试验
取同一批次栀子标准汤剂样品,按2.2.3 项下制备供试品溶液,分别在0、2、4、8、12、24、48h 进样,结果各共有峰相对保留时间和相对峰面积RSD<3%, 表明供试品溶液在48h 内稳定性良好。
2.4 样品的测定
取15 批栀子饮片、标准汤剂、中间体、配方颗粒供试品溶液10μL, 参照物溶液, 按照2.2.1 项下条件检测。 详见图1-4。
图1 栀子饮片HPLC 指纹图谱共有模式图
图2 栀子标准汤剂HPLC 指纹图谱及其对照指纹图谱
图3 栀子配方颗粒中间体HPLC 指纹图谱及其对照指纹图谱

图4 栀子配方颗粒HPLC 指纹图谱及其对照指纹图谱
2.5 共有峰标定
将15 批栀子饮片、标准汤剂、中间体、配方颗粒HPLC 指纹图谱数据导入 “中药色谱指纹图谱相似度评价系统”( 2012 版) 选择时间宽度为0.1,中位数法生成对照指纹图谱,经比较分析后确定栀子饮片、标准汤剂、中间体、配方颗粒均有9 个共有峰。 15 批栀子饮片、中间体、标准汤剂、配方颗粒指纹图谱相似度范围在0.9~1。 各批次供试品指纹图谱与对照图谱进行比较,计算其相似度,结果见表2。 结果显示,15 批饮片、标准汤剂、中间体、配方颗粒指纹图谱与对照指纹图谱的相似度均在0.9 以上,说明15 批不同产地的栀子饮片化学成分具有良好的相似性; 栀子配方颗粒生产工艺稳定。 与山栀子苷、鸡矢藤次苷甲酯、羟异栀子苷、Jasminoside B、京尼平-1-龙胆二糖苷、栀子苷、苦藏花素对照品色谱图进行对比,确认配方颗粒HPLC 指纹图谱中1 号峰为山栀子苷、2 号峰为鸡矢藤次苷甲酯、3 号峰为羟异栀子苷、4 号峰为Jasminoside B、5 号峰为京尼平-1-龙胆二糖苷、6 号峰为栀子苷7 号峰为苦藏花素;结果见图5。
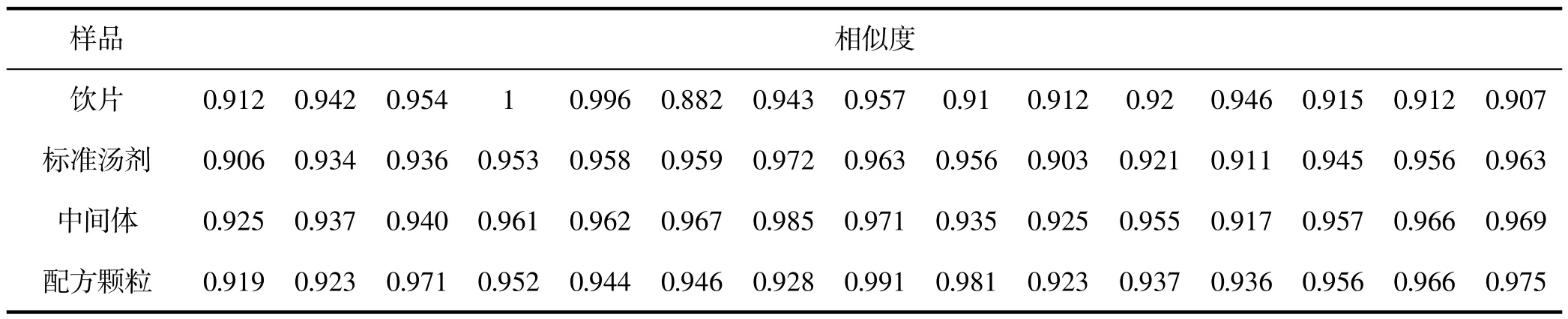
表2 15 批栀子饮片、中间体、标准汤剂及配方颗粒的指纹图谱相似度
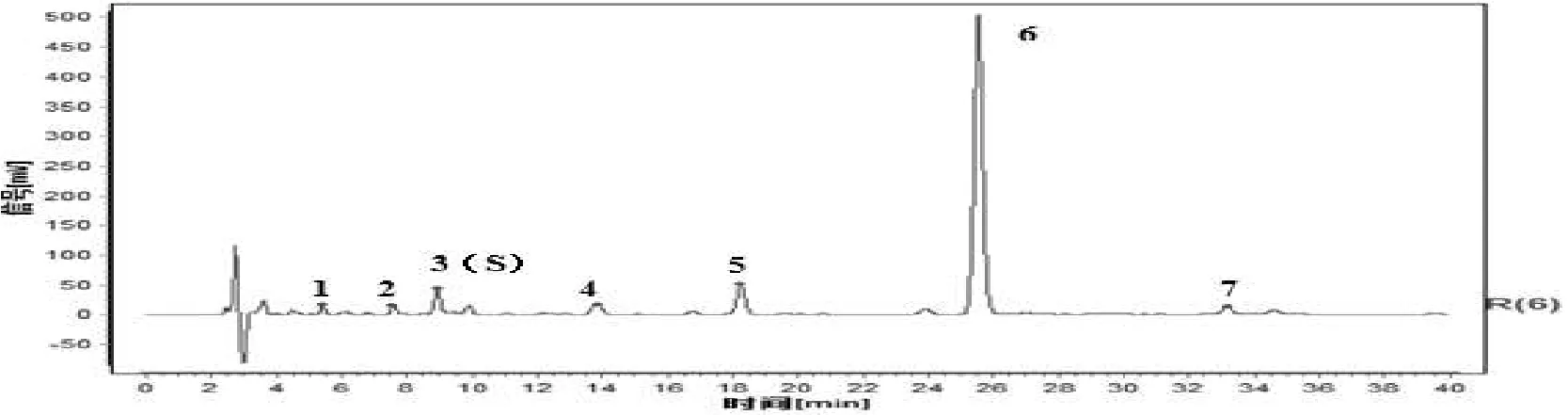
图5 共有峰指认
2.6 相关性分析
栀子饮片、标准汤剂、中间体、配方颗粒HPLC 对照指纹图谱比较结果见图6, 并采用相似度评价软件评价四者图谱的相似度,结果见表3,结果表明栀子配方颗粒的9 个共有特征峰在栀子标准汤剂、饮片、中间体中均有显示,由表3 可以看出栀子配方颗粒对照指纹图谱与饮片、标准汤剂、中间体的对照指纹图谱相似度在0.9 以上,结合15 批栀子饮片、中间体、标准汤剂、配方颗粒指纹图谱相似度范围在0.9~1,说明栀子配方颗粒和栀子饮片、中间体、标准汤剂成分一致,四者指纹图谱具有良好的相关性, 为采用HPLC 指纹图谱对栀子配方颗粒生产全过程进行控制提供试实验依据[6]。

表3 栀子饮片、标准汤剂、中间体、配方颗粒HPLC 对照指纹图谱相似度结果
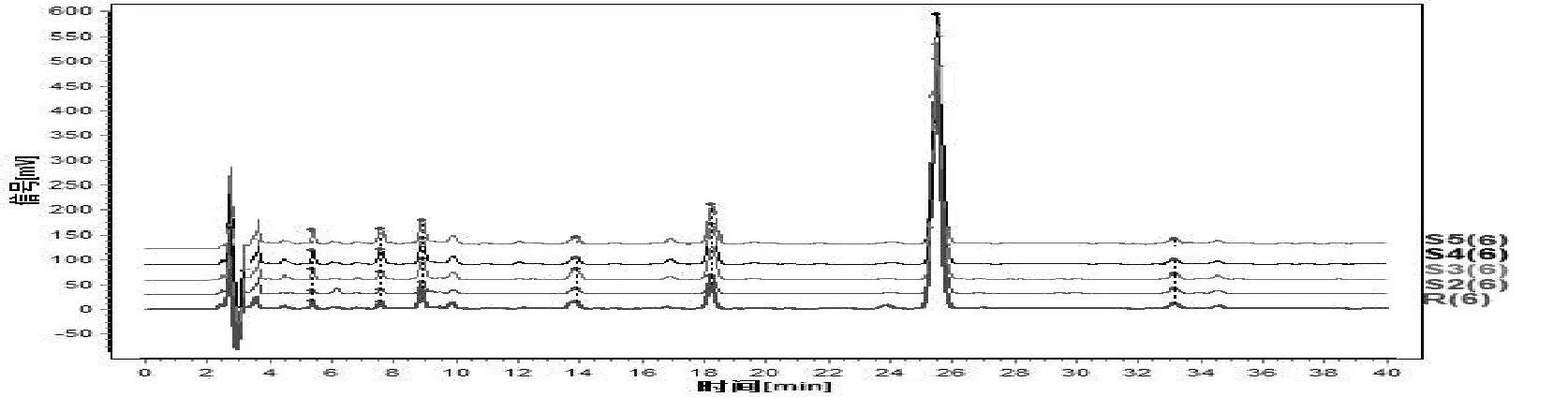
图6 栀子饮片(1) 、标准汤剂(2) 、中间体(3) 及配方颗粒(4) 的HPLC 对照指纹图谱比较

