基于PDMS微结构的气道平滑肌舒张药物评测装置*
高蔷, 王龙飞, 邓林红, 王翔
(常州大学生物医学工程与健康科学研究院,常州 213164)
1 引 言
哮喘是一种以气道高反应性和气道壁重构为特征的慢性阻塞性气道疾病。虽然其发病机理尚不清楚[1],但已有研究表明作为气道壁的重要组成部分,气道平滑肌细胞(ASMC)是哮喘发生时导致气道狭窄的主要效应细胞。ASMC的异常收缩增加了气道内部的机械应力,使气道狭窄[2]。因此,ASMC是治疗哮喘的主要靶细胞[2-4]。临床上舒张ASMC的药物主要包括β2受体激动剂、糖皮质激素、胆碱受体拮抗剂等[3,5-7]。例如,盐酸异丙肾上腺素(ISO,一种β2受体激动剂)通过与ASMC的β2受体结合,引发ASMC产生cAMP信号分子,进而导致ASMC松弛[8-10]。然而,此类药物具有导致心律失常、低氧血症等副作用,长期使用还会导致ASMC的舒张能力下降,使哮喘进一步恶化。因此,筛选新一代的靶向气道平滑肌的舒张药物非常重要,而如何准确、快速测量药物的细胞舒张效应是评价药物有效性的关键。
目前已建立了从动物到细胞水平的多种用于评价ASMC舒张药物的方法[11]。动物模型虽然对药物作用产生完整生理反应,却无法用于对ASMC的收缩状态的直接测量[12-13]。组织切片法保留了体内的部分真实结构,可用于直接观测ASMC的收缩状态。但是,源自动物的组织无法真实反映药物对人体组织的作用[14]。2D体外细胞培养技术可以培养人源平滑肌细胞,但由于缺少可能调节平滑肌力学响应的胞外基质,无法较好地模拟体内的生化和物理环境[15-16]。因此,通过3D细胞培养构建微组织部分模拟体内环境的技术更具优势[14]。这些培养在小培养皿中的微组织由细胞和基质(如胶原蛋白、纤连蛋白等)共同构成[17-23]。遗憾的是人们仅能从其收缩面积的变化来间接判断药物的作用,无法获得平滑肌的力学测量数据[16]。因此,如何准确地测量药物处理前后微组织的收缩力仍是一个挑战。
本研究设计并制备了一种基于PDMS微结构的细胞力学传感器,利用3D细胞培养在其表面构建ASMC微组织。实验表明,培养在PDMS微结构上的ASMC和胶原混合物能自发较快地收缩,48h后形成力学稳定的微组织。通过测量微弦的弹性系数和间距可以计算出ASMC微组织的收缩力。对微组织进行药物处理并测量了微组织的收缩和舒张力的变化,结果显示,该检测装置具有较高的灵敏度和可靠性。
2 材料与方法
2.1 材料、试剂与仪器
Sylgard 184(美国Dow Corning公司);三氯(1H,1H,2H,2H—全氟辛基)硅烷(美国Sigma公司);聚乙烯醇(PVA)、组胺(上海阿拉丁生化科技股份有限公司);鼠尾I型胶原(美国Advanced Biomatrix公司);杜氏改良培养基(dulbecco′s modified eagle medium,DMEM)、胎牛血清(fetal bovine serum,FBS)、青霉素、链霉素及胰蛋白酶(美国gibco公司);二甲基亚砜(dimethyl sulfoxide,DMSO)(上海凌风化学试剂有限公司);细胞松弛素D(美国Sigma 公司);硅脂(美国Baysilone公司);盐酸异丙肾上腺素(ISO)(上海源叶生物科技有限公司)。
CO2细胞培养箱(日本三洋公司);生物安全柜(BSC-1300ⅡA2,苏州安泰空气技术有限公司);超级纯水仪(Milli Q Plus,Integral 10,美国Millipore公司);倒置显微镜(Primo Vert)、倒置荧光显微镜(cell observer)、激光共聚焦显微镜(LSM 710)(德国Zeiss公司);体视显微镜(S8APO,德国Leica公司;等离子清洗机(Potentlube PT-5S,深圳三和波达机电科技有限公司)。
2.2 方法
2.2.1PDMS微弦的制备 首先将Sylgard 184和交联剂以10:1 比例混合并浇筑在硅模具上,高温固化后得到聚二甲基硅氧烷(PDMS)负模。再将PDMS负模表面涂布2%PVA的脱模剂。将PDMS预聚物加入负模的微槽内80℃固化4 h(1∶10 PDMS)后,微槽两端位置粘合两个2 mm高的PDMS矩形支持块。两个支持块通过等离子处理,键合于一个14 mm圆形盖玻片上。将装置浸泡在水中过夜后,剥离反模得到PDMS微弦结构。最后将微弦装置放置于24孔培养皿中备用。
2.2.2PDMS微丝弹性系数的测量 首先将待测微弦水平放置于精密天平上。利用微操悬臂上装载的不锈钢针头对微弦中央位置施加垂直载荷。以20 μm为步进距离,分别记录微操悬臂下降距离和相应的天平读数。通过重力加速度常数将质量(mg)转换为力(mN),得到微弦载荷-形变曲线,其斜率即为微弦的弹性系数(k)。
2.2.3细胞培养和药物处理 本研究采用参考文献[6]原代提取的大鼠气道平滑肌细胞(8-10代)培养于含10%胎牛血清的低糖DMEM中,置于37℃、5% CO2培养箱。I型胶原蛋白首先经pH中性调解后,再与一定数量的细胞混合,得到终浓度为106个细胞/mL和2 mg/mL胶原蛋白的混合物。4℃条件下,将细胞胶原混合物(6 μL)滴加于微弦中央位置,37℃培养箱30 min固化后,再向培养板孔中加入1 mL培养基,然后置于培养箱或显微镜下进行长期成像。
为进行药物处理实验,微组织培养48 h后,将培养基换成无血清培养基并孵育12 h。药物梯度实验时,每40 min由低到高依次向培养孔中加入100 μL含药物的预热培养。
2.2.4微组织的相差与荧光成像 倒置荧光显微镜的多点成像载物台可同时对24孔板内的多个微组织目标进行长时自动成像。显微镜的环境维持系统可维持37℃,5%CO2浓度的细胞培养环境。使用5×/0.16NA物镜和ORCA-Flash4.0相机(日本滨松)进行相差成像(30 min/帧)。
采用Calcein-AM/ PI双染色试剂盒检测微组织内细胞存活。药物处理后,微组织经2 M Calcein-AM和1 μM PI在黑暗中孵育15 min。更换为新鲜培养基后,用Zeiss 710 共聚焦显微镜于20×/0.5NA物镜下分别在绿色(488 nm)和红色(570 nm)通道对微组织成像。
2.2.5细胞收缩和舒张力的计算及图像分析 使用Image J测量两微弦中间位置之间的像素距离并根据相机的参像素数换算为距离单位。微组织的力(F)根据微弦位移距离(D)和弹性系数(k)计算:F=kD。微组织内细胞的矢量迁移分析通过ImageJ中的粒子图像测速(PIV)插件进行分析,并得到相对应的图像。使用GraphPad Prism 6进行t检验,P<0.05即认为差异具有统计学意义。
3 结果
3.1 PDMS微弦的表征
本研究采用PDMS微弦结构作为细胞的应力传感器。我们首先对由模具灌注成型的微弦进行了形态和力学表征。
由图1(a)可知,扫描电镜图像显示微弦表面光滑,平行且均匀。测量不同批次制备的结构的宽度、间距和高度,结果表明不同批次的微丝尺寸无显著性差异,见图1(b)。PDMS聚合物是良好的弹性材料,微米尺度的PDMS结构可在微牛级作用力下发生形变。微弦扰度变化与受力载荷呈线性关系,见图1(c)。因此,根据胡克定律,我们计算得出该PDMS微弦结构的弹性系数为0.05 μN/μm。
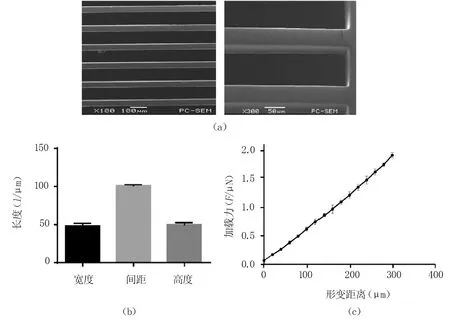
图1 PDMS微弦的表征
3.2 微组织的形成及其收缩力测量
当细胞-胶原混合物加载到微弦中央部位后,胶原在37℃环境中固化。随培养时间延长,该混合物在细胞的作用下持续收缩成一个椭球状微组织,见图2(a)。我们利用粒子图像测速分析方法来跟踪微组织内细胞的运动轨迹,发现微组织周边的细胞比中央部分的细胞的迁移速度更快,其速度在第10 h达到最高,超过0.5 μm/min,见图2(b)。
微组织的收缩导致2根微弦的间距逐渐减小。根据测量的微弦间距和其弹性系数,计算得出该过程中微组织的收缩力的变化。由图2(c)可知,密度为106个细胞/mL的微组织经30h培养后,其收缩力区域稳定,并达到约9 μN。但微组织含有较低密度的细胞时(105个细胞/mL),其收缩力显著下降,最高值约为2 μN。为测量较为明显的舒张作用,本研究将采用含高密度细胞的微组织进行药物实验。
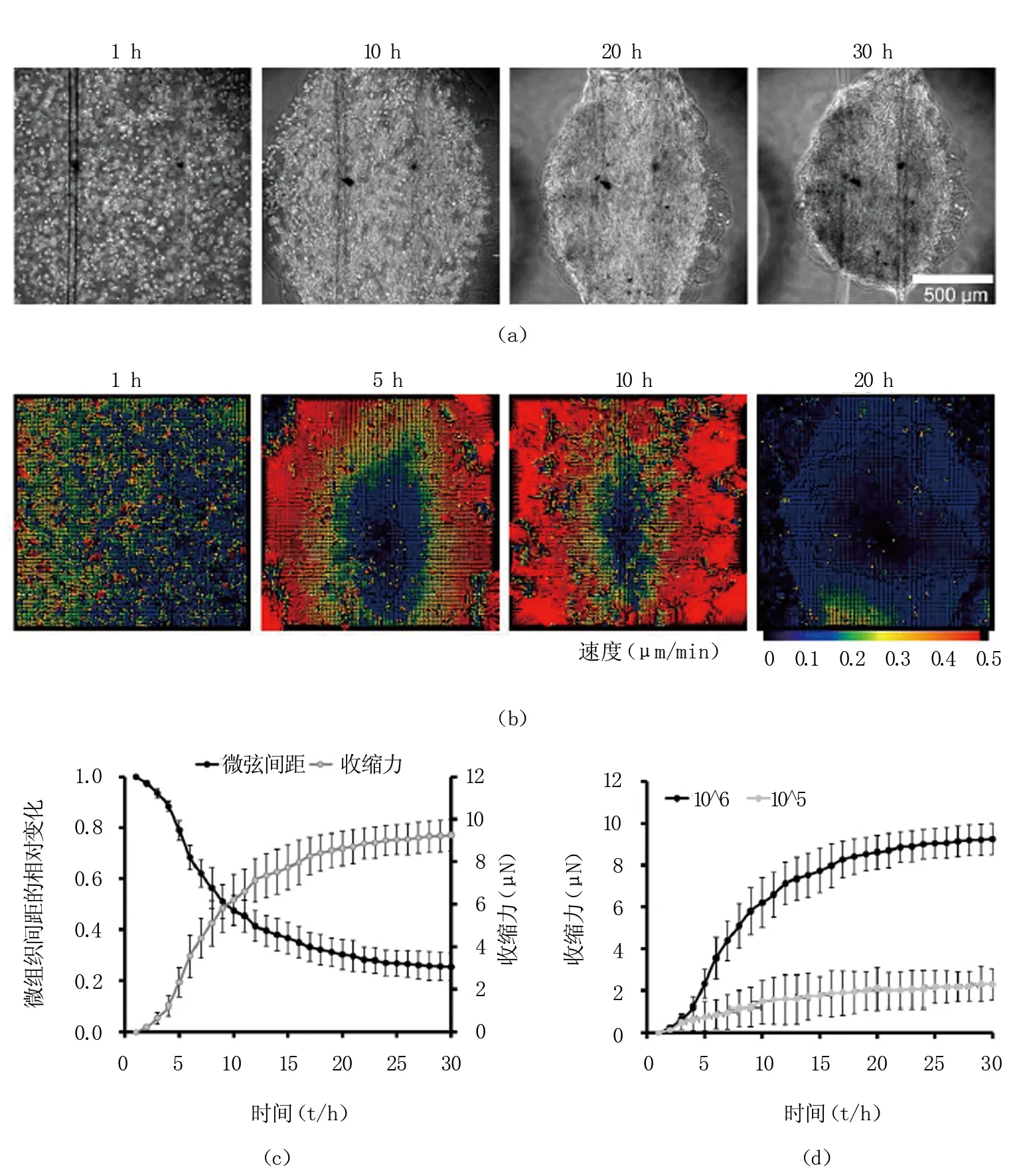
图2 ASMC微组织在PDMS微结构上
3.3 药物诱导微组织在PDMS微结构上发生变化
为模拟哮喘中ASMC的异常收缩态,本研究利用组胺来刺激微组织收缩。由图3(a)可知,与未经组胺处理的对照组相比,微组织经100μM组胺处理30min后的收缩力增大了8倍。随后,本研究通过细胞松弛素D解除肌动蛋白细胞骨架张力来确定ASMC微组织的可舒张的范围。10 μM细胞松弛素 D处理30 min可大幅削弱ASMC的收缩力,见图3(b)。该结果证明在微结构上构建的微组织可以测量0.04~0.20 μN间的力学变化。为评测该测量范围内舒张药物的效果,本研究使用临床药物ISO来处理微结构上的ASMC微组织。由图3(c)可知,处于收缩态的微组织(组胺处理组)对1μM ISO更为敏感。而对照组在100 μM ISO处理时才产生较大幅度的舒张。进一步的实验表明,两组样品均在500 μM ISO处理时产生最大舒张力。通过对药物处理后微组织进行细胞存活检测,我们发现高浓度ISO处理并未导致细胞死亡,见图3(d),证明其舒张作用不是由于细胞死亡引发。值得注意的是,当药物浓度进一步增大到2 mM后,其舒张作用削弱,见图3(c)。高浓度ISO舒张作用下降的机制还有待进一步研究。
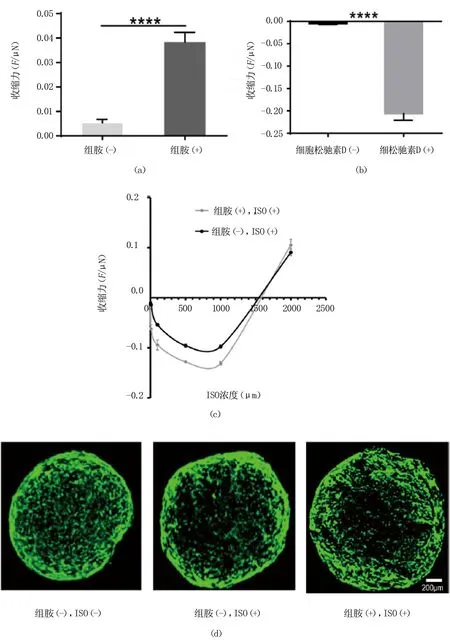
图3 ASMC微组织用于梯度加舒张药物实验
4 讨论
本研究设计并制备了一种简单的细胞力学测量装置,并在其上面成功地构建了细胞微组织。利用PDMS微结构检测出临床药物ISO的有效浓度范围,当ISO药物浓度达到2 mM以上,其促舒张作用下降,提示用药浓度不能过高。本研究还发现模拟哮喘中处于收缩态的平滑肌微组织对ISO更为敏感,说明ISO对哮喘中的平滑肌细胞具有一定的特异性舒张作用。综上,本研究建立的检测细胞力学和药物评测的方法,能实时定量检测到药物导致的细胞收缩力的变化,可灵敏、方便地筛选出抗哮喘药物。

