硫辛酸注射液热原反应因素实验研究
田恩圣,潘春芬,田雨阳,戴晓莉,张君茹
(1.山东省食品药品审评查验中心,山东 济南 250014;2.淄博市市级机关医院,山东 淄博 255000;3.湖北大学生命科学学院,湖北 武汉430000;4.山东省药学科学院,山东 济南 250100)
热原反应是注射剂经常出现的不良反应,危害极大,可引起人体发热、恶心、呕吐等反应,严重者也导致休克甚至死亡[1]。药品质量标准中用鲎试剂或者兔法进行检验。本文对有疑似热原反应较多的硫辛酸注射液,通过设计毒理试验,研究引发热原反应的因素,为生产该品种的企业提供参考。
1 仪器与材料
1.1 仪器 WRY-C热原测温仪(上海黄海药检仪器有限公司);SC-3012低速离心机(安徽中科中佳科学仪器有限公司); SSW-600-2S型电热恒温水浴锅(上海博迅);754N紫外分光光度计(上海精科分析仪器厂);紫外可见分光光度计UV7(梅特勒-托利多国际有限公司);TAL-40D型试管恒温仪(湛江安度斯生物有限公司)。
1.2 药品与试剂 鲎试剂(批号:1708230,湛江博康生物有限公司);内毒素标准品(批号:150601-201783,中国食品药品检定研究院);硫辛酸实验样品(国内某企业);硫辛酸注射液对照样品(国内某企业);游离血红蛋白检测试剂盒(批号:171205,北京百奥莱博科技有限公司)。
1.3 实验动物及环境 新西兰兔16只,普通级,2.2~2.5 kg,由济南西岭角养殖繁育中心提供,生产许可证号:SCXK(鲁)20150001。饲养温度20~25 ℃,日温差≤5 ℃,湿度40%~70%,昼夜明暗交替时间12 h/12 h。
2 方法
2.1 热原试验[2]参考《中国药典》2020年版(四部)中的热原检查法进行。取筛选合格的新西兰兔6只,分为硫辛酸注射液实验组和硫辛酸注射液对照品组。测定其正常体温后15 min以内,自耳静脉缓缓注入温热至约38 ℃的硫辛酸注射液30 mg·kg-1,给药体积为1 mL·kg-1。然后每隔30 min按测量其体温1次,共测6次,以6次体温中最高的一次减去正常体温,即为该兔体温的升高温度(℃)。如3只试验兔中有1只体温升高0.6 ℃或高于0.6 ℃,或3只试验兔体温升高的总和达1.3 ℃或高于1.3 ℃,应另取5只试验兔复试,检查方法同上。
2.2 内毒素检查[2-3]内毒素限值:≤0.25 EU·mg-1(实验用样品),≤0.4 EU·mg-1(国内某企业对照样品),采用《中国药典》2015年版细菌内毒素检查法检验,先计算最大稀释倍数MVD(MVD=CL/λ),将供试品按照最大稀释倍数稀释制成2支供试品管和2支供试品阳性对照(用该浓度的供试品稀释液将内毒素标准品制成2λ浓度),另取2支加入细菌内毒素检查用水作为阴性对照,2支加入2λ浓度的内毒素标准溶液作为阳性对照,将各管按照标准要求,保温(60±2)min后,观察并记录结果。
2.3 体外溶血试验[4-5]采用2%新西兰兔红细胞悬液为实验系统,硫辛酸注射液配制成30 mg·mL-1溶液,0.9%氯化钠注射液为阴性对照,注射用水为阳性对照。2%红细胞悬液的制备,供试液、红细胞悬液、生理盐水的加入方法均按2015年版药典方法进行,计算溶血率:用分光光度计法用0.9%氯化钠注射液调零后,于545 nm波长处测定供试品及对照品各管上清液吸收度,A为供试品各管上清液吸收度,B为0.9%氯化钠注射液对照管上清液吸收度,C为灭菌注射用水管上清液吸收度。
溶血率(%)=(A-B)/(C-B)×100%
2.4 体内溶血试验[6]采用新西兰兔6只进行试验,静脉注射给药,剂量为30 mg·kg-1,给药浓度30 mg·mL-1,给药容积为1 mL·kg-1,给药1次。药前、药后2 h分别兔耳中动脉采血约2 mL,置于含有EDTAK2的抗凝管中,离心后分离血浆,测定血浆中游离血红蛋白(FHB)含量。

3 结果
3.1 热原检查结果 结果显示,实验组硫辛酸注射液在30 mg·kg-1剂量下,第一次试验的3只兔体温升高均超过0.6 ℃,复检的5只兔体温升高亦均超过0.6 ℃,判断热原反应为阳性,而硫辛酸注射液对照组3只新西兰兔体温升高值均小于0.6 ℃,热原反应为阴性,结果见表1~2。
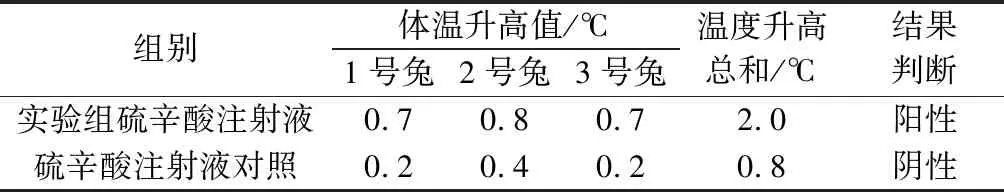
表1 硫辛酸注射液第一次热原检查结果

表2 硫辛酸注射液第二次热原检查结果
3.2 细菌内毒素结果 结果显示,实验组硫辛酸注射液和对照品细菌内毒素检查结果均为阴性,内毒素含量符合要求,结果见表3。

表3 硫辛酸注射液内毒素检查结果
3.3 体外溶血试验结果 结果显示,实验组硫辛酸注射液在30 mg·mL-1浓度下,加样0.3 mL后溶血率大于5%,有明显的溶血反应发生,结果为阳性,而对照硫辛酸注射液溶血率小于5%,结果为阴性。结果见表4。
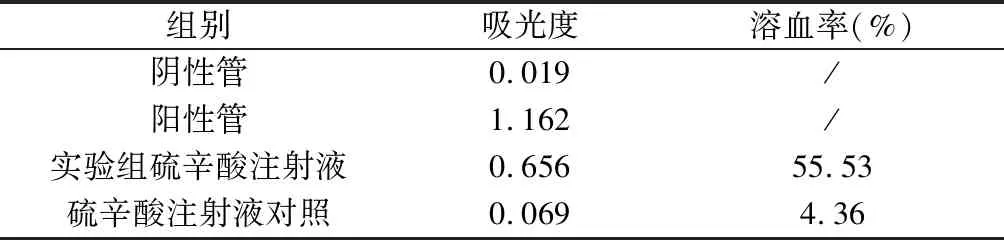
表4 硫辛酸注射液体外溶血试验结果
3.4 体内溶血试验结果 给药前比较,给药后实验组硫辛酸注射液组兔血浆中游离血红蛋白含量显著升高(P<0.01),而硫辛酸对照组兔血浆中游离血红蛋白含量变化不明显(P>0.05)。说明实验组硫辛酸注射液可引起新西兰兔体内溶血作用,结果见表5。
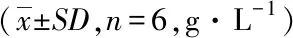
表5 硫辛酸注射液体内溶血试验结果
4 讨论
临床上热原反应较为常见,引发人体产生热原反应的物质为致热源,也就是导致机体发热的源头物质。致热源包括外源性致热源和内源性致热源两大类。外源性致热源(exogenous pyrogen)种类甚多,而注射中最主要的致热源为细菌内毒素[7-8]。药品质量标准中热原检查通过鲎试剂法或兔法很容易即可判断。本实验对实验组硫辛酸注射液进行了兔法检查热原反应,结果为阳性,而鲎试剂法检查热原反应,结果为阴性,故分析热原反应并非内毒素引起,而有其他致热源引起。为了进一步探讨引起热原反应的原因,进一步开展了溶血试验。
体外溶血试验结果显示,实验组硫辛酸注射液在30 mg·mL-1浓度下,会引起兔红细胞溶血反应,为了进一步验证体内是否溶血,本文采用了新西兰兔给予30 mg·kg-1剂量开展了体内溶血试验,通过检测血浆中游离血红蛋白含量反应是否存在溶血[9]。实验结果显示,给药后2 h,血浆中游离血红蛋白含量较给药前显著升高,说明存在明显的溶血反应。结合体内外溶血和热原反应试验结果,分析实验组硫辛酸注射液热原反应阳性的可能原因为药品本身引发红细胞破裂,导致严重溶血,同时对其他细胞也可能存在破坏作用,释放激素和(或)细胞因子等内热原,导致机体体温升高[9]。通过本研究可提示药品出现热原反应阳性时,未必是细菌内毒素超标,也可能是溶血等其他因素所致,应多方面查找原因,以便于发现问题,解决问题,保障临床用药安全。

