改性淀粉对水样中铜离子的吸附性能研究
苗秀荣 , 王雪萍
(太原工业学院 环境与安全工程系 , 山西 太原 030008)
随着工业化规模增大和人类活动的增多,大量的工业废水被排入收纳水体。据不完全统计,每年都会有大量的重金属通过各种途径进入到环境生态系统当中,其中铜有14.7万t,汞有1.2万t,砷有12.5万t,并且这一数据还在逐年增长[1]。铜会影响人体的造血功能、部分酶的活性及内分泌系统的稳定。若摄取铜过量,会引发呕吐、腹痛。铜阻碍农作物的生长。同时,铜也不利于水体的自净过程[2]。本文用交联剂对淀粉进行改性,得到的复合淀粉具有多种改性淀粉独有的性能优势,对水样中的铜离子进行吸附性能研究。
1 实验部分
1.1 淀粉微球的制备
称取1.697 4 g可溶性淀粉和0.576 8 gβ-环糊精于150 mL容量瓶,加入15 mL蒸馏水,搅拌后制得淀粉乳。加入1 mol/L的氢氧化钠碱性溶液,在pH值计的测量下调节至溶液的pH值为11,在85 ℃的恒温水浴锅中静置几分钟使其发生糊化作用,淀粉完全溶解后制得的溶液称为水相。
分别将不同质量的乳化剂司盘60及吐温60混合后加入大豆油中,放置在60 ℃的水浴锅中,辅以搅拌使其溶解,考察两种乳化剂的质量比与乳化剂添加量是否会影响制得溶液的稳定性。两种乳化剂质量比(司盘60∶吐温60)达到9∶1时,且乳化剂的添加量为1 g/(100 mL)(油相)时溶液稳定性好。当乳化剂的加入量较小时,由于界面所吸附的分子少,界面膜的韧度低,易形成较大粒径的液滴,溶液的稳定性差[2]。但加入过多,稳定性变差,会导致其乳化能力丧失。
称取8.009 1 g司盘60和0.889 9 g吐温60,放置于60 ℃的水浴锅中,慢慢溶解混合。冷却后变成的固体,就是复配乳化剂。称取0.591 8 g复配乳化剂,加入60 mL的大豆油,放置于70 ℃的水浴锅中,并缓慢搅拌5 min左右,待完全溶解后得到的溶液称为油相。
在搅拌油相的同时缓慢滴入水相,在搅拌的作用下,会得到均匀的反相乳液,加入6 mL环氧氯丙烷作交联剂,在50 ℃的气浴恒温振荡器中振荡3 h后,对溶液进行离心操作。撇除上层油相,对剩余的部分依次用乙酸乙酯、无水乙醇、丙酮进行多次洗涤,最后在50 ℃的烘箱中烘干,研磨过后得到目标产品淀粉微球。
1.2 测试淀粉微球的性能
1.2.1测试溶解度
称取0.2 g的淀粉微球于150 mL的容量瓶中,加入4 mL的蒸馏水,在90 ℃的气浴恒温振荡器中振荡20 min,观察其状态。
1.2.2测试溶胀性
称取0.2 g淀粉微球于150 mL的容量瓶,加入20 mL蒸馏水,放在82 ℃恒温水浴锅中静置2 min并辅以搅拌。发生溶胀后取出冷却至室温。称量选取的滤纸的质量为m0,用滤纸进行过滤,得到滤纸加淀粉微球的质量为m1。在110 ℃烘箱中干燥后得滤纸加淀粉微球的质量为m2。通过下式计算得淀粉的溶胀度:
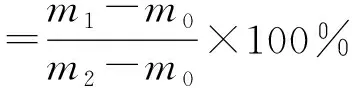
本实验测得,m0为0.544 0 g,m1为1.804 4 g,m2为1.169 5 g,则溶胀度为201.50%。
2 结果与讨论
2.1 温度对吸附能力的影响
称取50 mL配制的铜离子浓度为30 mg/L的废水于锥形瓶中。将其pH值调节为6,加入0.5 g的淀粉微球后,封上一层保鲜膜,然后分别在20、25、30、35、40、50 ℃的温度下进行振荡,振荡125 min后取样,测其吸光度。根据绘制的标准曲线得到铜离子的浓度,从而确定吸附的情况,实验结果见图1。
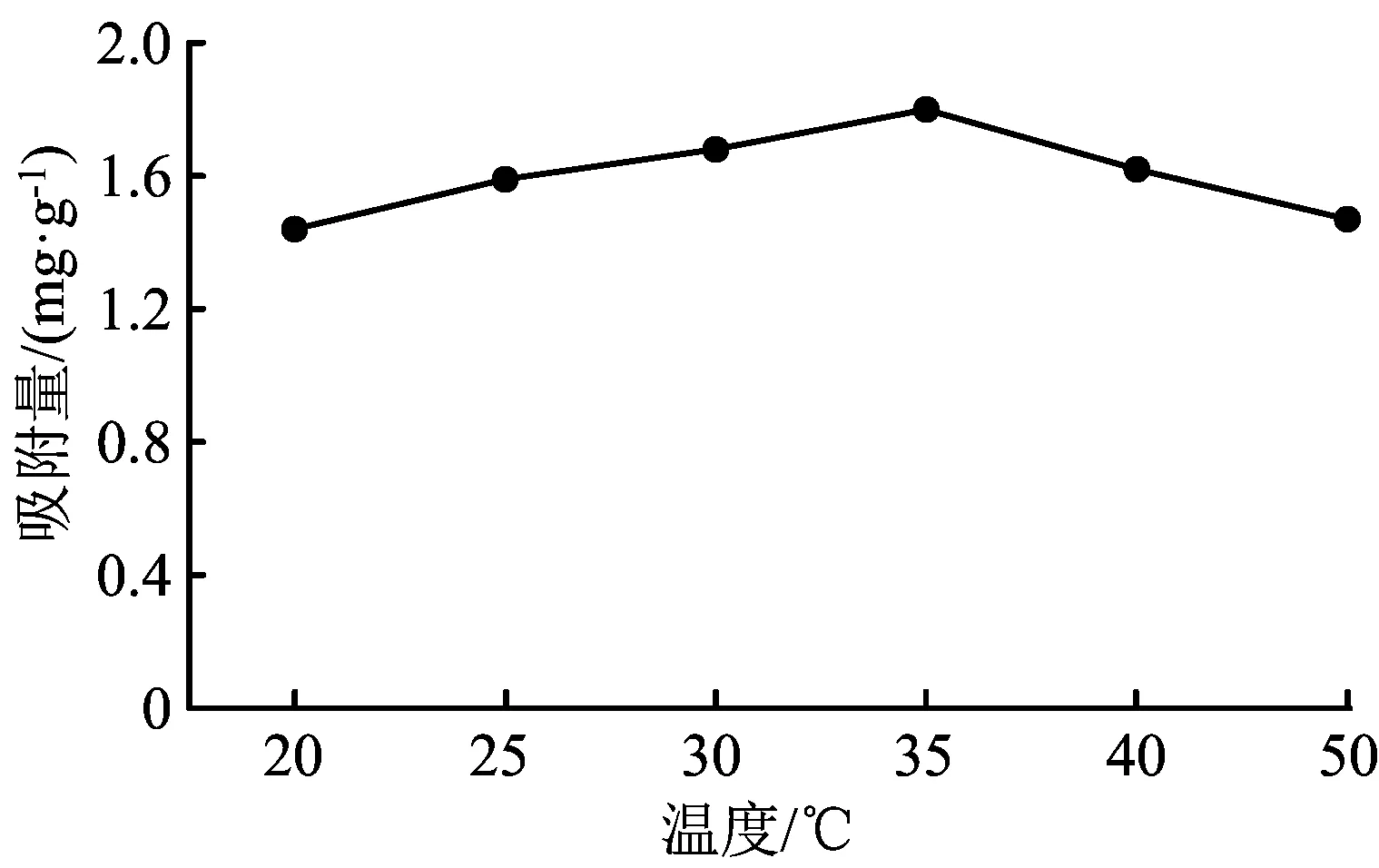
图1 温度与吸附量的关系曲线
由图1可以看出,淀粉微球吸附铜离子的量开始随温度升高而增大,到达最高点后又随温度的升高降低。而且,在30~35 ℃内吸附量较大。郑水林等[3]研究认为,温度升高会加快离子运动的速率,碰撞的几率增大从而吸附的能力大。但是温度过高会使已经被吸附的铜离子发生解析,吸附铜离子的最适宜的温度是35 ℃。
2.2 pH值对吸附能力的影响
称取50 mL配制的铜离子浓度为30 mg/L的废水于锥形瓶中,将其pH值分别调节为1、2、3、4、5、6、7,依次向锥形瓶内加入0.5 g的淀粉微球并且封上一层保鲜膜,放于振荡器中。调节温度为36 ℃,待125 min后取样,测其吸光度,根据绘制的标准曲线得到铜离子的浓度,从而确定吸附的情况,实验结果如图2所示。
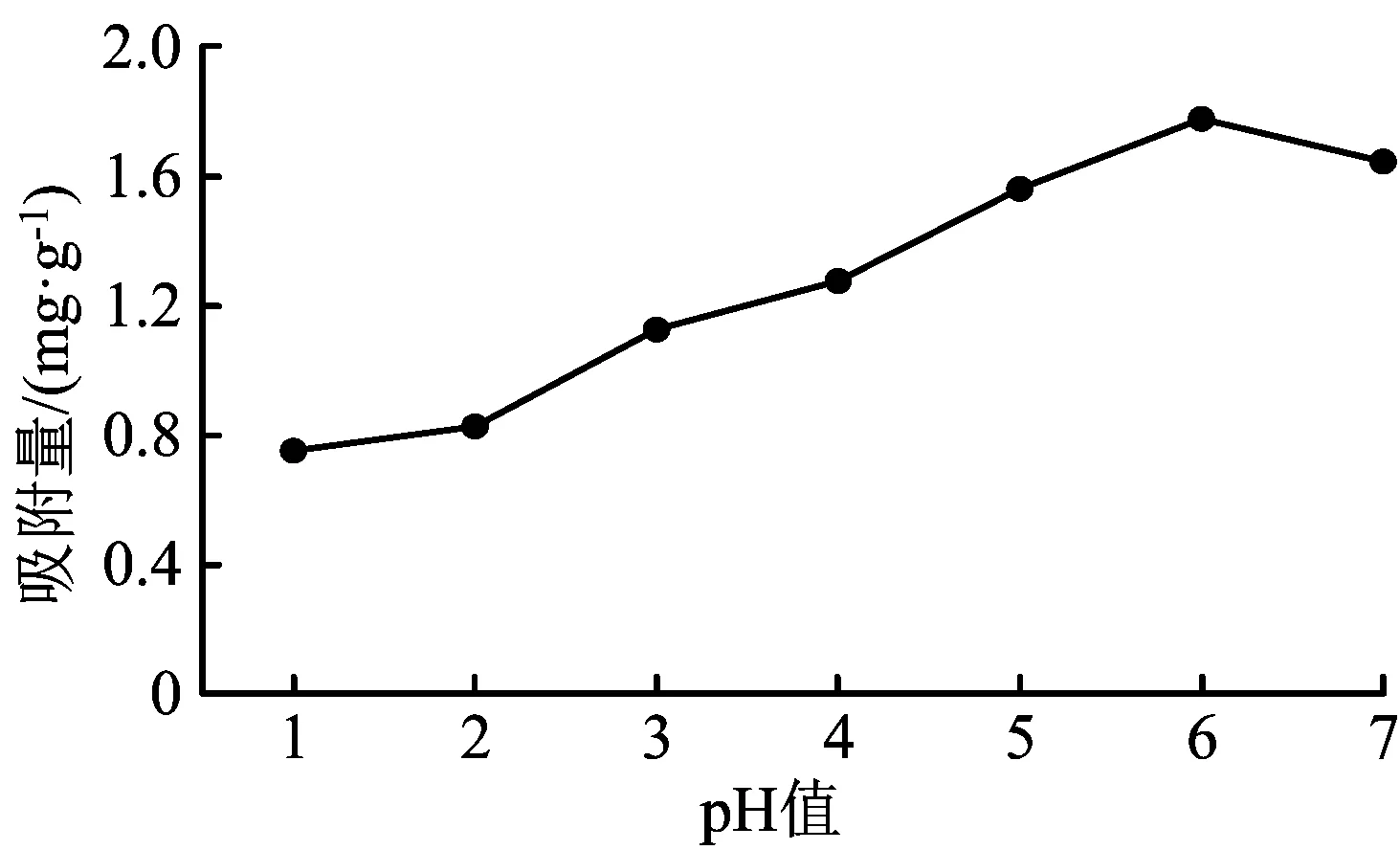
图2 pH值与吸附量的关系曲线
从图2可以看到,吸附量随着pH值的增大而增加;但在pH值>6后,吸附量又开始减少。原因是pH值对复合淀粉表面吸附位点的带电性有影响,也对金属离子的离子水化学有影响。当pH值为1~2时,溶液中H+的浓度很高,迁移碰撞的可能性远超过Cu2+,此时对铜离子的吸附量小。当pH值不断增加,表面吸附位点的带电性变成负值,就会有更多的Cu2+被吸附。当pH值>6,溶液中的OH-会与Cu2+结合并沉淀下来,这也是吸附量又降低的原因,吸附铜离子最适宜的pH值是6。
2.3 时间对吸附能力的影响
称取50 mL配制的铜离子浓度为30 mg/L的废水于锥形瓶中,将其pH值调节为6,向内加入0.5 g的淀粉微球并且封上一层保鲜膜,在35 ℃下的振荡器中以一定转速振荡,分别在25、50、75、100、125、150 min的时间取样,测其吸光度。根据绘制的标准曲线得到铜离子的浓度,从而确定吸附的情况,实验结果如图3所示。
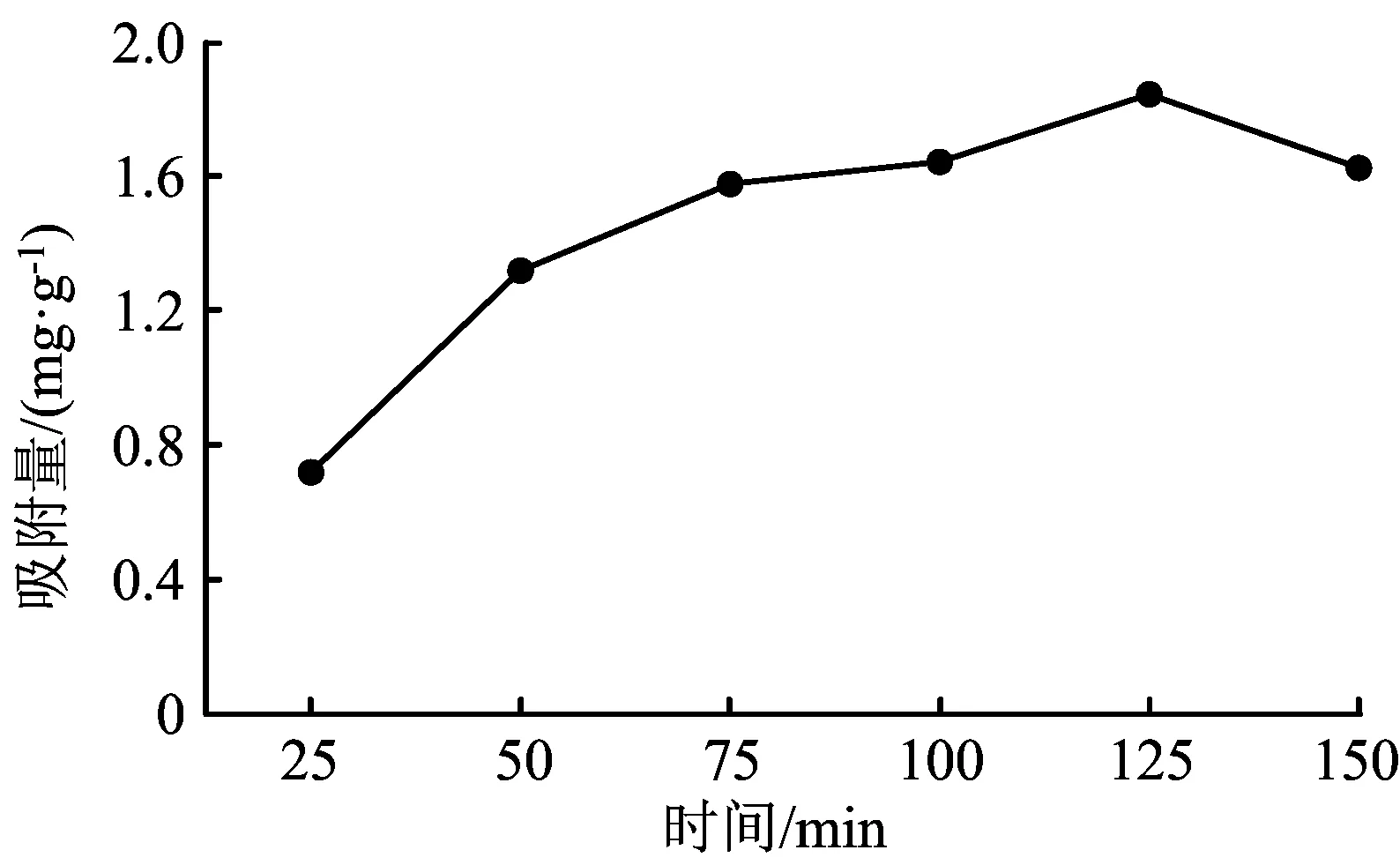
图3 时间与吸附量的关系曲线
由图3可知,吸附量随着时间的延长而增加。经分析,开始阶段随着时间的延长吸附效果比较明显,原因是有许多活性位点参与吸附反应。随着反应的进行,吸附位点减少并且根据同性相斥的原理,使游离的Cu2+进入粒子孔隙内部的可能性减少[4]。到125 min后,已经被吸附的部分Cu2+可能会由于相互碰撞发生解吸,使吸附量降低,吸附铜离子最适宜的时间是125 min。
2.4 Cu2+的初始浓度对吸附能力的影响
称取50 mL的铜离子浓度分别为1、2、3、4、5、6 mg/L的废水于锥形瓶中,将其pH值调节为6,向内加入0.5 g的淀粉微球并且封上一层保鲜膜,放于35 ℃的振荡器内,充分振荡,待125 min后取样。测其吸光度,根据绘制的标准曲线铜离子的浓度,从而确定吸附的情况,实验结果如图4所示。
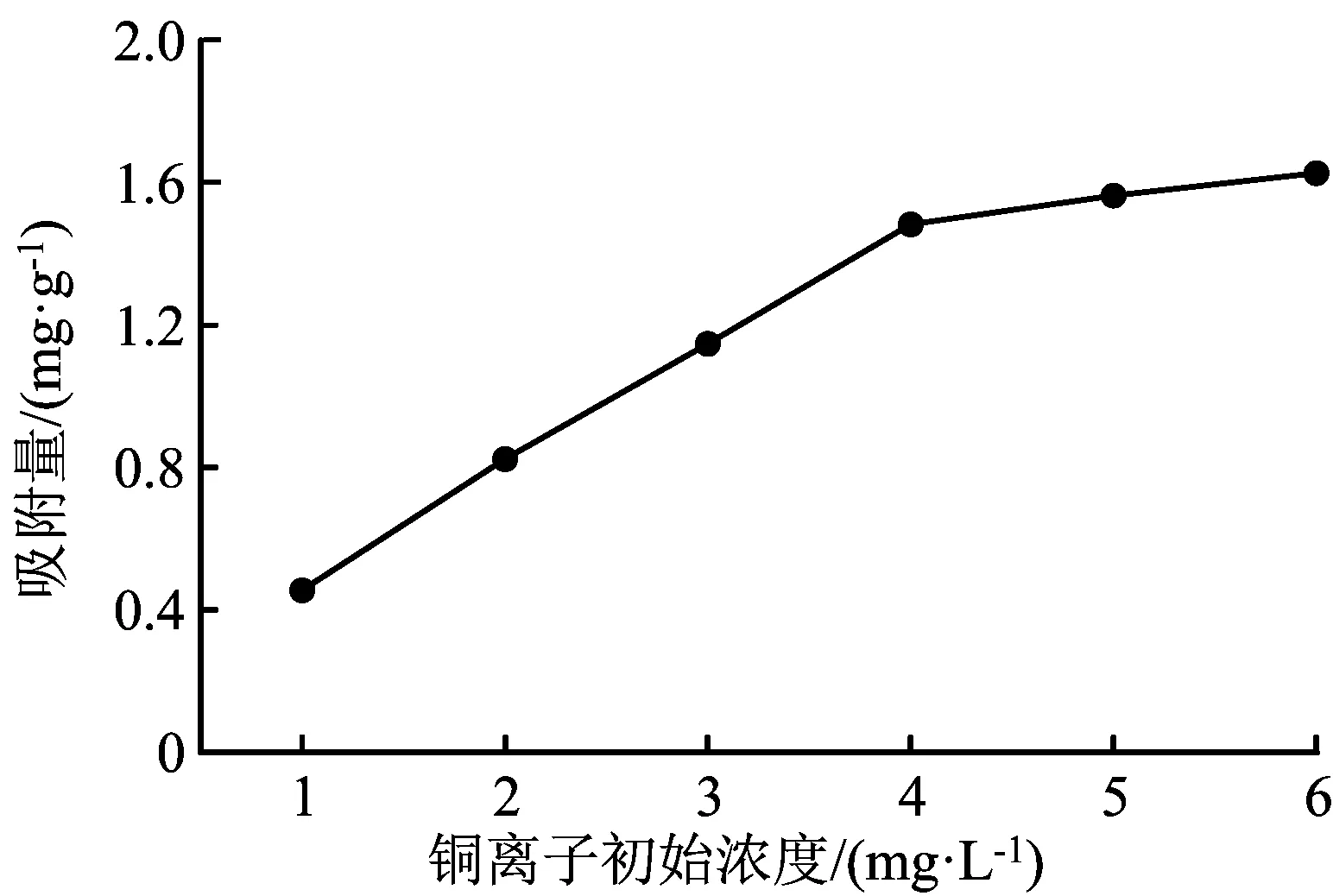
图4 铜离子初始浓度与吸附量的关系曲线
由图4可知,在标准曲线测定上限范围内,复合淀粉微球的吸附量与铜离子的初始浓度成正比关系。原因是随着浓度的增加,碰撞被捕捉的可能性就增大,但随着淀粉微球的吸附位达到饱和,吸附量就不再增加,而是保持相对稳定[5]。
3 结论
乳化剂复配过程中,司盘60和吐温60的质量比为9∶1时,得到的溶液稳定性好,并且当复配乳化剂的添加量为1 g/(100 mL)(油相)时,溶液稳定,分散性较均一。对复合淀粉微球溶解性测定的实验表明,改性后的淀粉即使在沸水中其溶解能力也较差,说明有部分淀粉发生了交联反应;对复合淀粉微球溶胀性测定的实验表明,交联剂可能会抑制淀粉的溶胀性能。对铜离子的吸附实验表明:复合淀粉微球在35 ℃,铜离子初始浓度为6 mg/L,吸为附时间125 min,pH值为6的条件下,吸附效果最佳。

