含氟三联苯类异硫氰酸酯类液晶合成与微波性能研究
兰 庚, 曹秋豪, 欧阳慧琦, 张智勇*, 汪相如, 高时汉
(1. 武汉轻工大学 化学与环境工程学院, 湖北 武汉 430023;2. 电子科技大学 光电科学与工程学院, 四川 成都 611730;3. 广州海格通信集团股份有限公司, 广东 广州 510663)
1 引 言
微波是一种高频率的电磁波,它具有传播稳定、受干扰小等特征,是通讯技术发展中的研究对象。微波移相器则是卫星通讯、相控阵雷达天线的核心部件[1]。近年来随着微波(5~40 GHz)通讯技术在卫星网络通讯、导航、航海、车载自动化驾驶及搜寻救援等方面的应用发展与日俱增,传统的铁氧体、二极管和铁电薄膜等移相器[2]因其体积大、信息容量小、调频范围窄、制造工艺复杂、成本高等问题而无法满足现代通信发展需求。
向列相液晶是一种既具有液体的流动性,又具有晶体有序性和各向异性的有机物,在电、磁和光等外场作用下诱导出介电常数(Δε)和双折射率(Δn)连续变化,并且其微波介电损耗随着频率的增加而呈现下降趋势,与传统移相器的损耗规律相反;同时,液晶器件还具有驱动电压和制造成本低、工业化容易等优点,因此成为微波移相器用可调谐介质材料的有力竞争者[3]。液晶通过外加偏置电压实现介电常数连续变化,当微波在液晶介质中进行传播时,变化的介电常数导致微波相位的改变,从而实现微波相位的连续可调谐作用。
最早的液晶移相器出现在20世纪90年代初[4],当时使用Merck公司的K15液晶进行实验,在10.5 GHz下获得了5 °/cm的相移,并在随后的相关研究中将这个相移不断地放大到600 °/cm[5]。2013 年Reuter M等人[6]研究了含有端基—NCS、—F、—CN 等基团的液晶分子在高频(0.5~2.5 THz)下的双折射率和吸波系数,发现对电磁波的吸波系数大小为:CN>F≈NCS。2013年Dabrowski R等人[7]报道了苯环与三键以及端基为—NCS、—CN、—F、—OCF3时液晶分子的性质变化情况,结果表明末端基团综合性能最好的是—NCS化合物。2015年,Jost M等[8]报道了微波向列相液晶混合物和连续可调微米和毫米波成分的发展情况。2015年Szczucinski等人[9]合成了侧位含氟三联苯异硫氰酸酯类化合物,得到很多低熔点化合物,并利用这些化合物作为主要组分配置了5个液晶组合物,研究了其介电性能,发现黏度较低,但双折射率低于0.3,且缺少对介电损耗的讨论。2018 年 Kowerdziej等人[10]报道了异硫氰基含氟二苯乙炔类液晶化合物在6 GHz频段的光可调谐性随温度的变化情况,观察到共振强度并没有明显变化,说明这类液晶对微波相位可调置性(τ)和双折射率随温度变化不明显,也说明异硫氰基和乙炔基等结构单元对微波比较稳定。最近,刘豪浩等人[11]研究了侧位甲基取代和氟取代以及末端取代基对液晶材料微波性能的影响,发现末端基团是—NCS时,液晶化合物表现出较宽的向列相相态,较低的介电损耗。
异硫氰基三联苯类液晶化合物具有较大的π-电子共轭体系,不仅能提供较大的双折射率,而且能减小对微波的吸波系数;相比于常用的—CH3、—F、—CN、—OCF3等末端基团三联苯类化合物具有更优良的微波性能[9]。同时,在苯环侧位引入氟原子,可以有效扼制近晶相的形成。因此,本文合成了4种侧位含氟三联苯异硫氰酸酯类液晶化合物,并对其相态和微波频段的介电性能进行了测试,以期获得微波频段介电常数(Δεr)在0.85~1.2之间,相位调制系数(τ)≥ 0.28,最大介电损耗(tanδεr-max)≤0.01的微波用液晶化合物。
2 实 验
2.1 试剂和仪器
试剂:硫光气(CSCl2)纯度98% 为武汉格奥化学技术有限公司产品;4-乙基苯硼酸、4-正丙基联苯硼酸、4-正丁基联苯硼酸、4-正戊基联苯硼酸、3-氟溴苯、2,6-二氟-4-溴苯胺纯度均为98%,均为河北美星化工有限公司出产;碳酸钾、碳酸钙均为分析纯,来源于天津市大茂化学试剂厂;四氢呋喃、乙醇、石油醚、二氯甲烷均为分析纯,来源于天津市天力化学试剂有限公司。
仪器:Nicolet iS10型傅里叶红外光谱仪(Thermo公司)、INOVO400MHz核磁共振仪(Varian仪器公司)X-4型数字显微熔点仪(北京泰克公司)、Q-2000型差示扫描量热仪(TA公司)、XPN-100E投射偏光熔点测定仪(上海长方公司)、ZC36型高阻计(上海第六电表厂有限公司)、AR2140型电子天平(梅特勒-托利多仪器(上海)有限公司出品),N5234B型矢量网络分析仪(美国Keysight Agilent 科技公司),直流电磁铁(0.5~1.0 T)(成都恩驰微波科技有限公司)。
2.2 目标化合物合成路线
异硫氰基三联苯类液晶化合物的合成路线如图1所示。
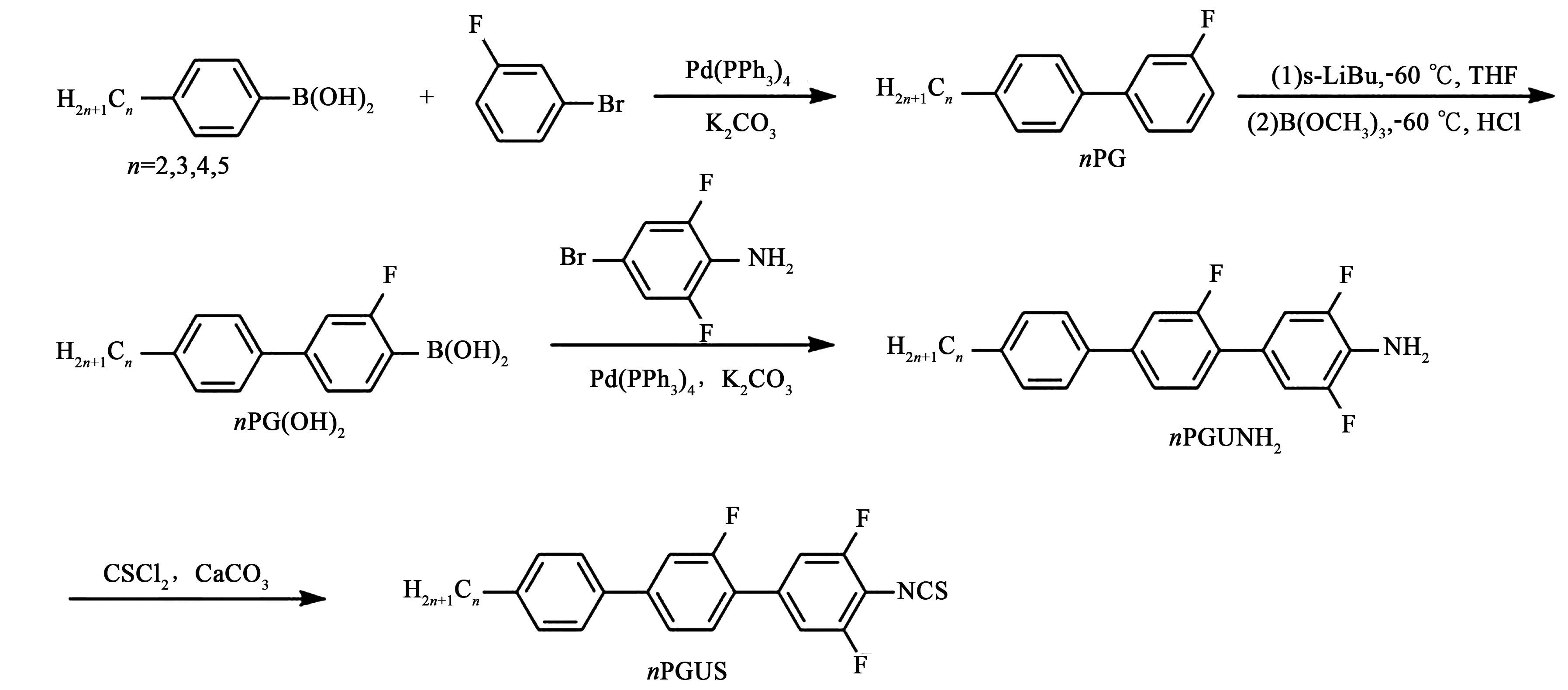
图1 目标化合物nPGUS合成路线Fig.1 Synthetic route of target compound nPGUS
2.3 目标化合物合成
2.3.1 中间体nPG合成
在氮气保护下,向装有球形冷凝管、温度计、磁力搅拌的500 mL三口烧瓶中加入4-乙基苯硼酸18 g(120 mmol)、3-氟溴苯20.87 g(120 mmol)、无水碳酸钾66.2 g(480 mmol)、去离子水40 mL、四氢呋喃200 mL和Pd(PPh3)40.7 g(0.6 mmol),加热,搅拌回流5 h后,TLC跟踪反应,待反应结束后,冷却至室温,抽滤,所得滤液脱去四氢呋喃,加入二氯甲烷100 mL,分液,水相用二氯甲烷(30 mL×3)萃取,合并有机相,水洗至中性,加入无水硫酸钠干燥12 h后,脱去溶剂,柱层析提纯,得到14.4 g无色透明液体产品2PG[12-13],收率60%。FT-IR (KBr, νmax/cm-1):3 432,2 862,1 570,1 441,1 392,1121,928,849,771,703;1H NMR(400 MHz,CDCl3)δ:7.62(d,J=12 Hz,2H),7.49~7.55 (m,2H),7.30~7.34 (m,2H),7.26~7.30 (m,1H),7.20~7.24 (m,1H),2.70~2.74 (m,2H),1.18(t,J=10 Hz,3H );13C NMR (100 MHz,CDCl3)δ:162.0,143.2,141.8,138.0,129.7,127.8,127.5,123.5,116.3,114.4,28.2,14.5;19F NMR (362 MHz,CDCl3)δ:-117.4。
同理,参考上述投料比制备3PG、4PG和5PG。
得到15.9 g无色透明液体产品3PG,收率62%。FT-IR(KBr, νmax/cm-1):3 433,2 852,1 590,1 448,1 397,1 021,918,869,731,702;1H NMR(400 MHz,CDCl3)δ:7.62(d,J=12 Hz,2H),7.49~7.55 (m,2H),7.26~7.30(m,3H),7.20~7.24(m,1H),2.62(t,J=10 Hz,2H),1.62~1.66(m,2H),0.94(t,J=8 Hz,3H);13C NMR (100 MHz,CDCl3)δ:162.0,141.8,140.9,138.1,130.1,128.0,127.5,123.5,116.3,114.4,39.7,24.1,13.7;19F NMR(362 MHz,CDCl3)δ:-117.4。
得到16.7 g无色透明液体产品4PG,收率61%。FT-IR(KBr, νmax/cm-1):3 430,2 863,1 572,1 440,1 391,1 121,928,848,761,714;1H NMR(400 MHz,CDCl3)δ:7.62 (d,J=12 Hz,2H),7.49~7.55 (m,2H),7.26~7.30 (m,3H),7.20~7.24 (m,1H),2.65 (t,J=10 Hz,2H),1.33~1.35 (m,4H),0.89 (t,J=8 Hz,3H);13C NMR (100 MHz,CDCl3)δ:162.0,141.8,141.5,138.0,130.1,127.7,127.5,123.5, 116.3,114.4,35.4,33.4,22.3,14.1;19F NMR (362 MHz,CDCl3)δ:-117.4。
得到18.3 g无色透明液体产品5PG,收率为 63%。FT-IR(KBr, νmax/cm-1):3 432,2 862,1 570,1 441,1 392,1 121,928,849,771,703;1H NMR (400 MHz,CDCl3)δ:7.62 (d,J=12 Hz,2H),7.49~7.55(m,2H),7.26~7.30 (m,3H),7.20~7.24 (m,1H),2.64 (t,J=10 Hz,2H),1.61~1.65 (m,2H),1.32~1.36 (m,4H),0.91 (t,J=8 Hz,3H );13C NMR (100 MHz,CDCl3)δ:162.0,141.8,141.5,138.0,130.1,127.7,127.5,123.5,116.3,114.4,35.7,31.4,30.9,22.7,14.1;19F NMR (362 MHz,CDCl3)δ:-117.4。
2.3.2 中间体nPGB(OH)2的合成
在氮气保护下,向装有磁力搅拌、100 mL恒压滴液漏斗、低温温度计的250 mL三口烧瓶中加入2PG 14 g,无水四氢呋喃70 mL,待体系温度降至-78 ℃后,开始滴加仲丁基锂70 mL(1.3 mol/L),控制反应温度不超过-75 ℃,滴加完毕以后,继续搅拌2 h;向反应体系中滴加硼酸三甲酯11 g(105 mmol)和无水四氢呋喃40 mL的混合溶液,滴加完毕后,自然升温至室温,反应4 h,TLC跟踪反应进程,反应结束后,向反应体系中滴加由23 mL浓盐酸(36%)和80 mL冰水组成的混合溶液水解,分液,水相用乙酸乙酯(30 mL×3)萃取,合并有机相,水洗至中性后,无水硫酸钠干燥12 h。脱去溶剂,石油醚重结晶,得到12 g白色粉末状固体2PGB(OH)2[14-15],收率70%;FT-IR(KBr, νmax/cm-1):3 347,2 995,2 357,1 616,1 545,1 391,1 340,1 126,1 038,1 002,882,820,650,528;1H NMR (400 MHz,CDCl3)δ:7.88~7.96 (m,1H),7.62 (d,J=11 Hz,2H),7.51~7.55(m,2H),7.32 (d,J=8 Hz,2H),4.20 (s,2H),2.62~2.66 (m,2H),1.18 (t,J=8 Hz,3H);13C NMR (100 MHz,CDCl3)δ:163.3,143.2,141.8,138.0,135.5,129.7,127.8,124.4,123.5,116.3,114.4,28.2,14.5;19F NMR (362 MHz,CDCl3)δ:-119.6。
同理,参考上述投料比,得到12.5 g白色粉末固体3PGB(OH)2,收率69%。FT-IR(KBr, νmax/cm-1):3 356,3 067,2 956,2 863,1 616,1 543,1 392,1 351,1 159,1 114,1 054,1 001,881,784,731,661,570;1H NMR (400 MHz,CDCl3)δ:7.88~7.96 (m,1H),7.62 (d,J=12 Hz,2H),7.52~7.54 (m,2H),7.28 (d,J=8 Hz,2H),4.20(s,2H),2.61 (t,J=8 Hz,2H),1.62~1.66 (m,2H),0.90~0.98 (m,3H);13C NMR (100 MHz,CDCl3)δ:163.3,141.8,140.9,138.1,135.5,130.1,128.0,124.4,123.5,116.3,114.4,37.9,24.1,13.7;19F NMR (362 MHz,CDCl3)δ:-119.6。
得到13 g白色粉末固体4PGB(OH)2,收率68%;FT-IR(KBr, νmax/cm-1):3 356,2 928,2 859,1 918,1 618,1 542,1 390,1 344,1 130,1 018,884,816,659,538;1H NMR (400 MHz,CDCl3)δ:7.88~7.96 (m,1H),7.62 (d,J=12 Hz,2H),7.52~7.54(m,2H),7.28 (d,J=8 Hz,2H),4.20 (s,2H),2.65 (t,J=8 Hz,2H),1.52~1.60 (m,2H),1.30~1.36 (m,2H),0.85~0.93 (m,3H);13C NMR(100 MHz,CDCl3)δ:163.3,141.8,141.5,138.0,135.5,130.1,127.7,124.4,123.5,116.3,114.4,35.4,33.4,22.3,14.1;19F NMR (362 MHz,CDCl3)δ:-119.6。
得到14.2 g白色粉末固体5PGB(OH)2,收率71%。FT-IR(KBr, νmax/cm-1):3 359,2 922,2 856,1 920,1 617,1 546,1 392,1 338,1 123,1 081,1 001,805,606,541;1H NMR (400 MHz,CDCl3)δ:7.88~7.96(m,1H),7.62 (d,J=12 Hz,2H),7.52~7.54(m,2H),7.28 (d,J=8 Hz,2H),4.2 (s,2H),2.64 (t,J=8 Hz,2H),1.60~1.66 (m,2H),1.30~1.38 (m,4H),0.88~0.94 (m,3H);13C NMR(100 MHz,CDCl3)δ:163.3,141.8,141.5,138.0,135.5,130.1,127.7,124.4,123.5,116.3,114.4,35.7,31.4,30.9,22.7,14.1;19F NMR(362 MHz,CDCl3)δ:-119.6。
2.3.3 中间体nPGUNH2合成
在氮气保护下,向装有球形冷凝管、温度计、磁力搅拌的500 mL三口烧瓶中加入2PGB(OH)210 g(41 mmol)、2,6-二氟-4-溴苯胺8.5 g(41 mmol)、无水碳酸钾22.6 g(164 mmol)、去离子水40 mL、四氢呋喃180 mL、甲苯80 mL、Pd(PPh3)40.23 g,升温回流5 h后,TLC跟踪反应进程,待反应结束后,降至室温,抽滤,脱去四氢呋喃后,加入100 mL乙酸乙酯溶解,分液,水相用乙酸乙酯(30 mL×3)萃取,合并有机相,水洗至中性后加入无水硫酸钠干燥24 h,脱去溶剂得到粗品,用甲醇和石油醚重结晶得到9.5 g浅黄色固体产品2PGUNH2[16-18],收率71%。FT-IR(KBr, νmax/cm-1):3 432,2 862,2 016,1 570,1 441,1 392,1 121,1 035,928,849,810,771,703,583,510;1H NMR (400 MHz,CDCl3)δ:7.57~7.59 (m,2H),7.41~7.47 (m,3H),7.33 (t,J=8 Hz,2H),7.18~7.20(m,2H),3.89(s,2H),2.68~2.73(m,2H),1.03~1.08 (m,3H);13C NMR(100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.0,143.9,143.5,136.2,135.4,130.2,129.1,126.8,124.1,123.1,114.5,112.4,112.2,110.0,77.4,77.1,76.7,35.6,31.6,31.1,22.6,14.1;19F NMR (362 MHz,CDCl3)δ:-116.9,-117.3。
同理,参考上述投料比,收得10 g浅黄色固体3PGUNH2,收率72%。FT-IR(KBr,νmax/cm-1):3 432,2 950,2 856,2 209,2 013,1 574,1 473,1 389,1 270,1 180,1 029,935,867,815,703,654,603,504;1H NMR (400 MHz,CDCl3)δ:7.57~7.59 (m,2H),7.41~7.47 (m,3H),7.33 (t,J=8 Hz,2H),7.18~7.20 (m,2H),3.89 (s,2H),2.68~2.73 (m,2H),1.7~1.79(m,2H),1.03~1.08 (m,3H );13C NMR(100 MHz,CDCl3)δ:161.1,158.6,156.6,143.2,135.2,129.1,126.8,123.1,114.6,112.2,110.0,76.7,37.7,29.8,22.7,13.9;19F NMR(362 MHz,CDCl3)δ:-116.9,-117.4。
得到10 g浅黄色固体产品4PGUNH2,收率69%。FT-IR(KBr,νmax/cm-1):3 424,2 933,2 879,2 217,2 121,1 633,1 479,1 395,1 182,1 140,1 030,930,861,813,654,591,520,456;1H NMR (400 MHz,CDCl3)δ:7.57~7.59 (m,2H),7.41~7.47 (m,3H),7.33 (t,J=8 Hz,2H),7.18~7.20 (m,2H),3.89 (s,2H),2.68~2.73 (m,2H),1.43~1.74(m,4H),1.03~1.08 (m,3H);13C NMR (100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.0,143.4,143.5,136.1,135.4,130.2,129.2,126.7,124.0,123.1,114.5,112.4,112.2,110.0,77.4,77.1,76.8,35.4,33.6,22.5,14.0;19F NMR (362 MHz,CDCl3)δ:-116.9,-117.3。
得到10.5 g浅黄色固体产品5PGUNH2,收率70%。FT-IR(KBr,νmax/cm-1):3 431,2 949,2 858,2 212,2 014,1 575,1 477,1 387,1 278,1 183,1 026,937,869,814,702,653,606,508;1H NMR (400 MHz,CDCl3)δ:7.57~7.59 (m,2H),7.41~7.47 (m,3H),7.33 (t,J=8 Hz,2H),7.18~7.20 (m,2H),3.89 (s,2H),2.68~2.73 (m,2H),1.66~1.74(m,2H),1.30~1.42 (m,4H),0.95 (t,3H);13C NMR (100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.7,144.0,143.9,143.4,136.1,135.4,130.2,128.6,126.7,124.0,123.0,114.5,112.2,110.0,77.4,77.1,76.8,28.6,15.5;19F NMR (362 MHz,CDCl3)δ:-116.9,-117.4。
2.3.4 目标化合物nPGUS合成
向装有球形冷凝管、100 mL恒压滴液漏斗、低温温度计和磁力搅拌的500 mL三口烧瓶中加入2PGUNH28.5 g(26 mmol)、碳酸钙6.5 g(65 mmol)、去离子水30 mL、二氯甲烷200 mL,将反应体系温度降至0 ℃,开始滴加CSCl27.5 g(65 mmol)和80 mL二氯甲烷组成的混合溶液,控制滴速确保反应体系温度不会出现剧烈上升。滴加完毕以后,保持在0~5 ℃反应2 h,自然升温至室温反应0.5 h,升温至回流反应1 h,TLC跟踪反应进程,待反应结束后,加入100 mL无水乙醇搅拌0.5 h降至室温后,抽滤,分液,水相用二氯甲烷(50 mL×3)萃取,合并有机相,水洗至中性后,加入无水硫酸钠干燥24 h;脱去溶剂后,用硅胶(200~300目)和金属吸附剂进行柱层析提纯,用石油醚(60~90)洗脱,经过重结晶后得到电阻率(ρ)=7.5×1011Ω·cm的6.7 g白色固体产品2PGUS[19-21],收率70%。FT-IR(KBr, νmax/cm-1):3 433,2 962,2 017,1 571,1 443,1 396,1 123,1 036,939,859,815,770,702,593,511;1H NMR (400 MHz,CDCl3)δ:7.57 (d,J=16 Hz,2H),7.41~7.50 (m,3H),7.35 (d,J=12 Hz,2H),7.25 (d,J=10 Hz,2H),2.73~2.79 (m,2H),1.34 (t,J=16 Hz,3H);13C NMR(100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.0,143.9,143.5,136.2,135.4,130.2,129.1,126.8,124.1,123.1,114.5,112.4,112.2,110.0,77.4,77.1,76.7,35.6,31.6,31.1,22.6,14.1;19F NMR (362 MHz,CDCl3)δ:-116.8,-117.4。
同理,参考上述投料比,得到7.2 g白色固体产品3PGUS,收率73%。FT-IR(KBr,νmax/cm-1):3 431,2 955,2 866,2 206,2 023,1 576,1 477,1 397,1 274,1 178,1 034,937,869,809,702,656,601,505;1H NMR (400 MHz,CDCl3)δ:7.56 (d,J=16 Hz,2H),7.49 (t,J=20 Hz,H),7.44(d,J=8 Hz,H),7.41 (s,H),7.32 (d,J=12 Hz,2H),7.25 (t,J=10 Hz,2H),2.68 (t,J=12 Hz,2H),1.71~1.76 (m,2H),1.04 (t,J=16 Hz,3H);13C NMR (100 MHz,CDCl3)δ:161.1,158.6,156.6,143.2,135.2,129.1,126.8,123.1,114.6,112.2,110.0,76.7,37.7,29.8,22.7,13.9;19F NMR (362 MHz,CDCl3)δ:-116.9,-117.4。
得到7.3 g白色固体产品4PGUS,收率71%。FT-IR(KBr,νmax/cm-1):3 421,2 934,2 861,2 207,2 131,1 613,1 479,1 396,1 183,1 130,1 033,934,866,812,654,592,526,459;1H NMR (400 MHz,CDCl3)δ:7.56 (d,J=16 Hz,2H),7.41~7.50 (m,3H),7.32 (d,J=12 Hz,2H),7.26 (t,J=10 Hz,2H),2.72 (t,J=12 Hz,2H),1.70 (m,2 H),1.43~1.48 (m,2H),1.02 (t,J=16 Hz,3H);13C NMR (100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.0,143.4,136.1,135.4,130.2,129.2,126.7,124.0,123.1,114.5,112.4,112.2,110.0,77.4,76.8,35.4,33.6,22.5,14.0;19F NMR(362 MHz,CDCl3)δ:-116.8,-117.8。
得到7.2 g白色固体产品5PGUS,收率68%。 FT-IR(KBr,νmax/cm-1):3 435,2 929,2 856,2 217,2 076,1 572,1 480,1 400,1 265,1 177,1 125,1 034,940,863,809,704,654,599,543;1H NMR (400 MHz,CDCl3)δ:7.55 (d,J=16 Hz,2H),7.41~7.50 (m,3H),7.32 (d,J=12 Hz,2H),7.26 (t,J=10 Hz,2H),2.69 (t,J=12 Hz,2H),1.66~1.74 (m,2H),1.30~1.42 (m,4H),0.95 (t,J=16 Hz,3H);13C NMR (100 MHz,CDCl3)δ:161.1,159.1,158.6,156.6,145.1,144.7,144.0,143.9,143.4,136.1,135.4,130.2,128.6,126.7,124.0,123.0,114.5,112.2,110.0,77.4,77.1,76.8,28.6,15.5;19F NMR(362 MHz,CDCl3)δ:-116.9,-117.4。
2.4 液晶组合物配置与高频介电性能测试
采用低熔点侧乙基三苯二炔类液晶化合物[22]按一定比例(质量分数为15%~30%)混合配制成组合物作为母体(分子结构见图2),将母体液晶分别与所合成的目标化合物nPGUS以及对比物5PP(1)US[23]和5PPUS[24]按质量分数为18%~20%比例进行混合配制,得到室温下呈向列相态液晶组合物, 如表1所示;并采用矩形谐振腔微扰法测试它们在高频(10~35 GHz)下的介电性能。
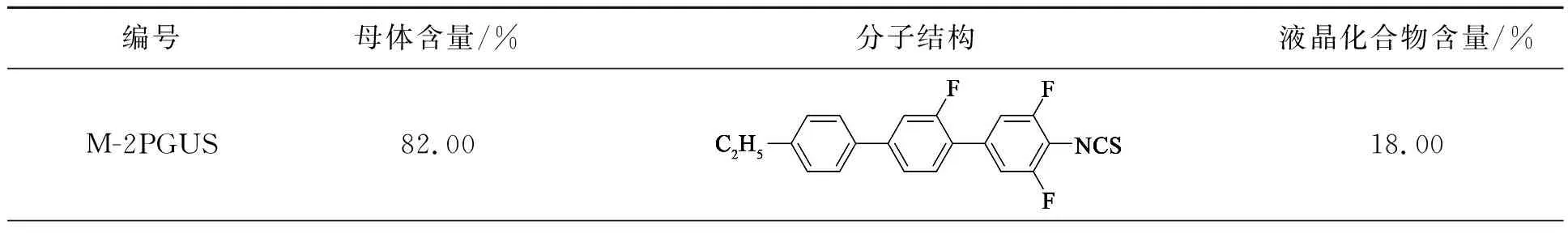
表1 混合液晶组分及含量数据Tab.1 Mixed liquid crystal composition and content
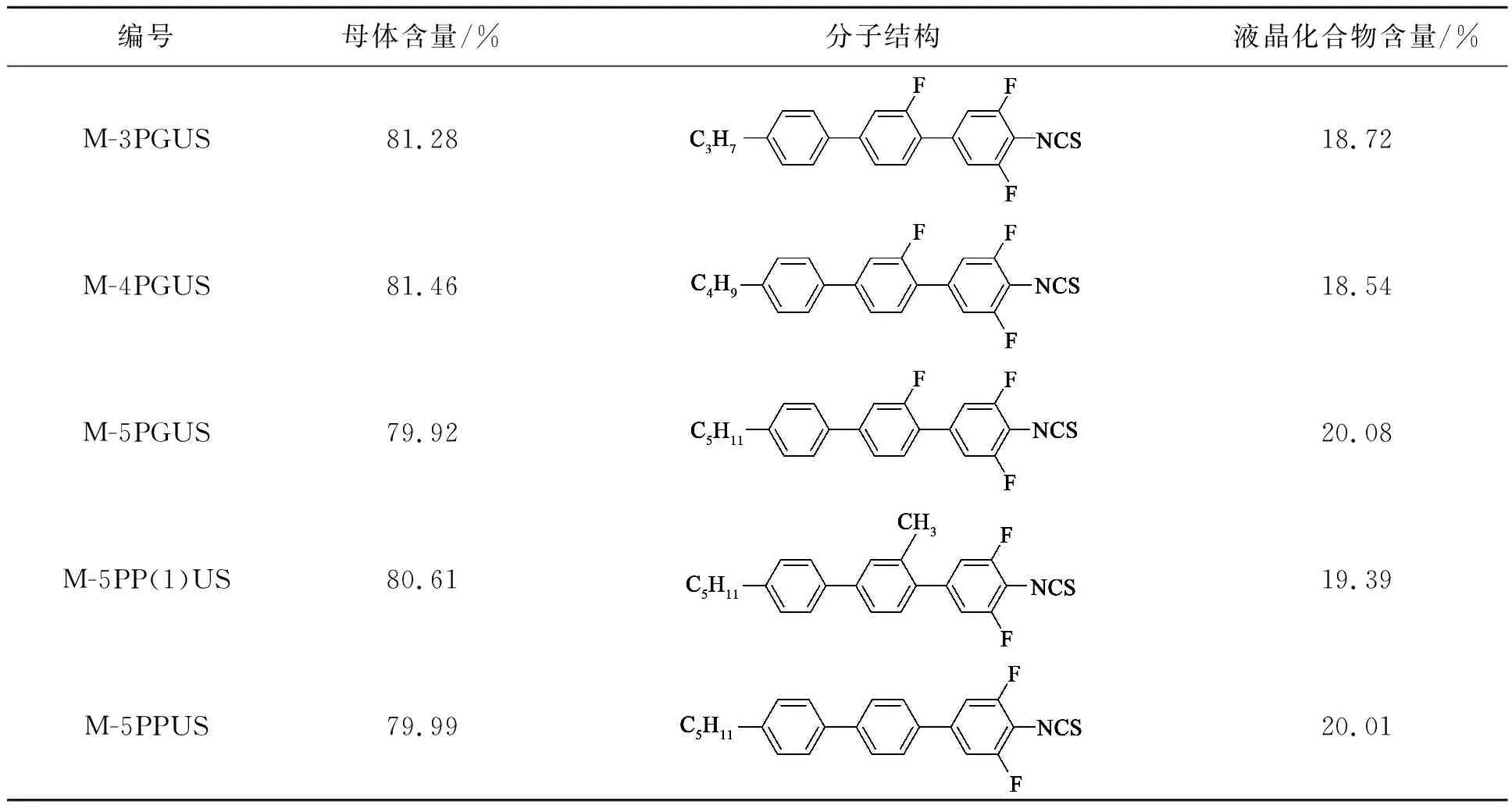
续 表

图2 母体液晶三苯二炔的分子结构通式(n,m=2~6) Fig.2 Molecular structure of triphenyldiyne(n,m=2~6) for the matrix liquid crystal
3 结果与讨论
3.1 目标化合物差热测试数据分析
目标化合物的相态温度采用TA公司Q-2000型差热分析扫描仪测定,在氮气气氛条件下,升降温速率:10 ℃/min;目标化合物的温度范围为40~190 ℃;通过上海长方公司XPE-100E投射偏光熔点测试仪(POM)测定目标化合物的相态织构,确定相态类型,采用主客体外推法测量目标化合物的Δn。
由表2和图3可知,目标化合物的熔点较低,总体上呈现逐渐下降趋势,而且它们的清亮点变化和向列相范围呈现奇偶效应,偶数碳链液晶分子的清亮点和向列相相宽低于奇数碳链液晶分子的清亮点和向列相相宽。对于这种现象,一般认为是因为烷基的排列是锯齿状的,末端的—CH3会对化合物的极化产生影响。当烷基链是奇数时,极化方向在分子长轴方向,这种情况下,会相应地增加分子的清亮点以及分子的向列相宽;当烷基链为偶数时,末端极化方向偏离分子的线性结构,这使得分子的清亮点以及向列相宽出现下降的情况[25]。如化合物5PGUS的熔点低(57.4 ℃),清亮点也较低;而化合物3PGUS的清亮点最高(169 ℃);这些化合物向列相范围都比较宽(≥84.7 ℃),平均为91.8 ℃;它们的双折射率均在0.385以上,并且随着端基烷基链碳原子数增加,其双折射率略有减小。

表2 目标化合物的相变温度与光学各向异性数据Tab.2 Phase transition temperature and optical anisotropy data of the target compound

续 表

图3 目标化合物nPGUS相变温度变化曲线Fig.3 Phase transition temperature curves of target compound nPGUS
3.2 高频介电性能测试结果与分析
图4是不同结构液晶化合物在母体液晶中的介电各向异性曲线图。从图4中可以看出,所有化合物在高频(10~35 GHz)下的介电常数均大于0.89,其中nPGUS(n=2~5)和5PPUS的介电各向异性都大于0.92,而化合物5PP(1)US的高频介电常数最小。这可能是因为5PP(1)US分子中三联苯中心环上的侧向甲基减小了分子平行轴偶极矩及其平行介电常数,使得化合物的介电各向异性降低;而化合物nPGUS中心苯环侧位氟原子可增加分子平行轴的偶极矩,导致这些化合物的平行介电常数比5PP(1)US稍大,具有较高的介电常数。
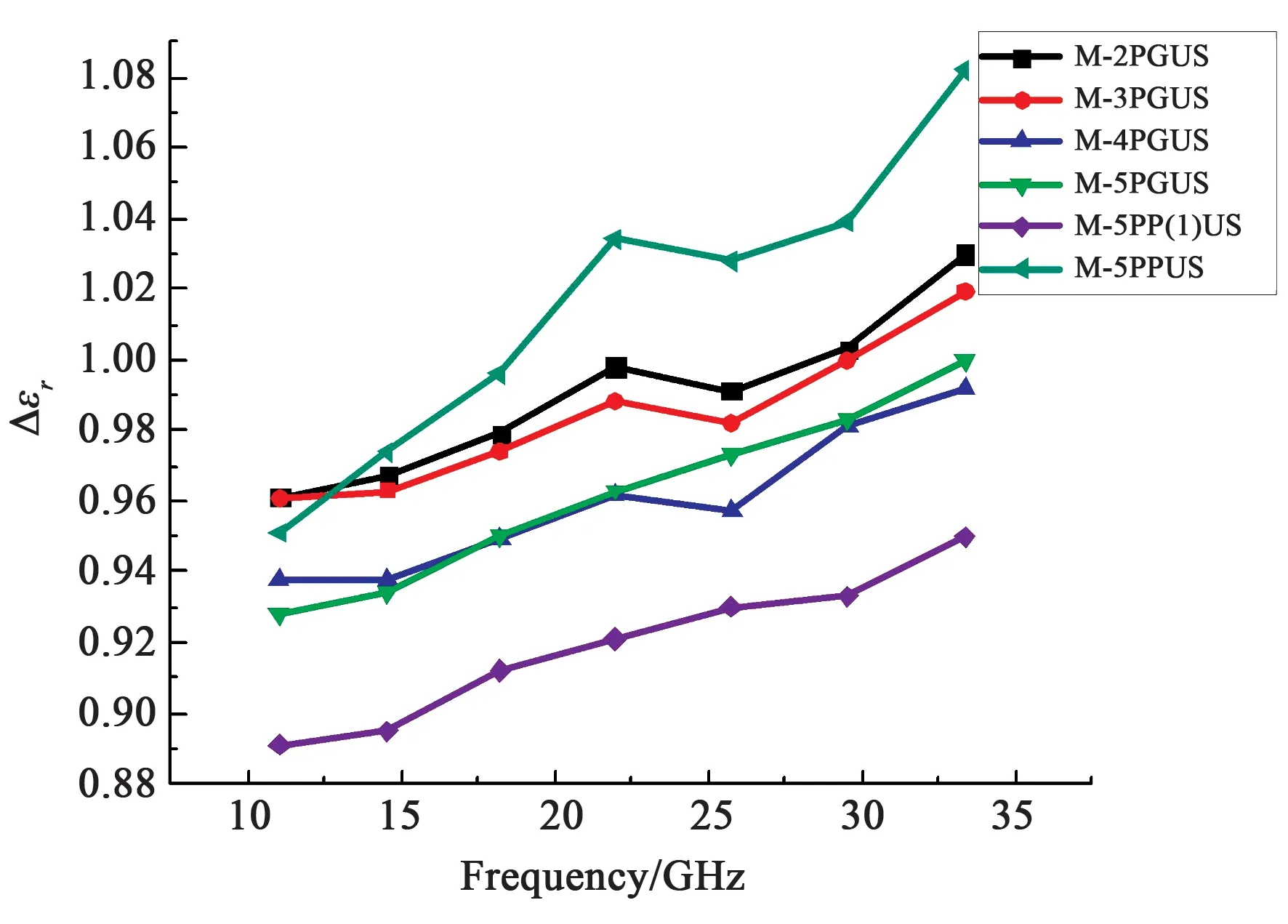
图4 不同频率下介电各向异性比较(20 ℃)Fig.4 Change curves of dielectric anisotropy with frequency at 20 ℃
由图5可知,化合物nPGUS(n=2~5)的介电损耗随着末端的烷基链的变化整体上呈现出规律性变化,烷基链长度越长,其介电损耗越小,但是5PGUS的介电损耗大于3PGUS和4PGUS,可能是因为过长的烷基链影响分子的转动,增大了其介电损耗;化合物5PP(1)US的介电损耗最小,其可能原因是其侧位的甲基使得整体的电子云密度增大,增强了分子的π-电子共轭性所导致。
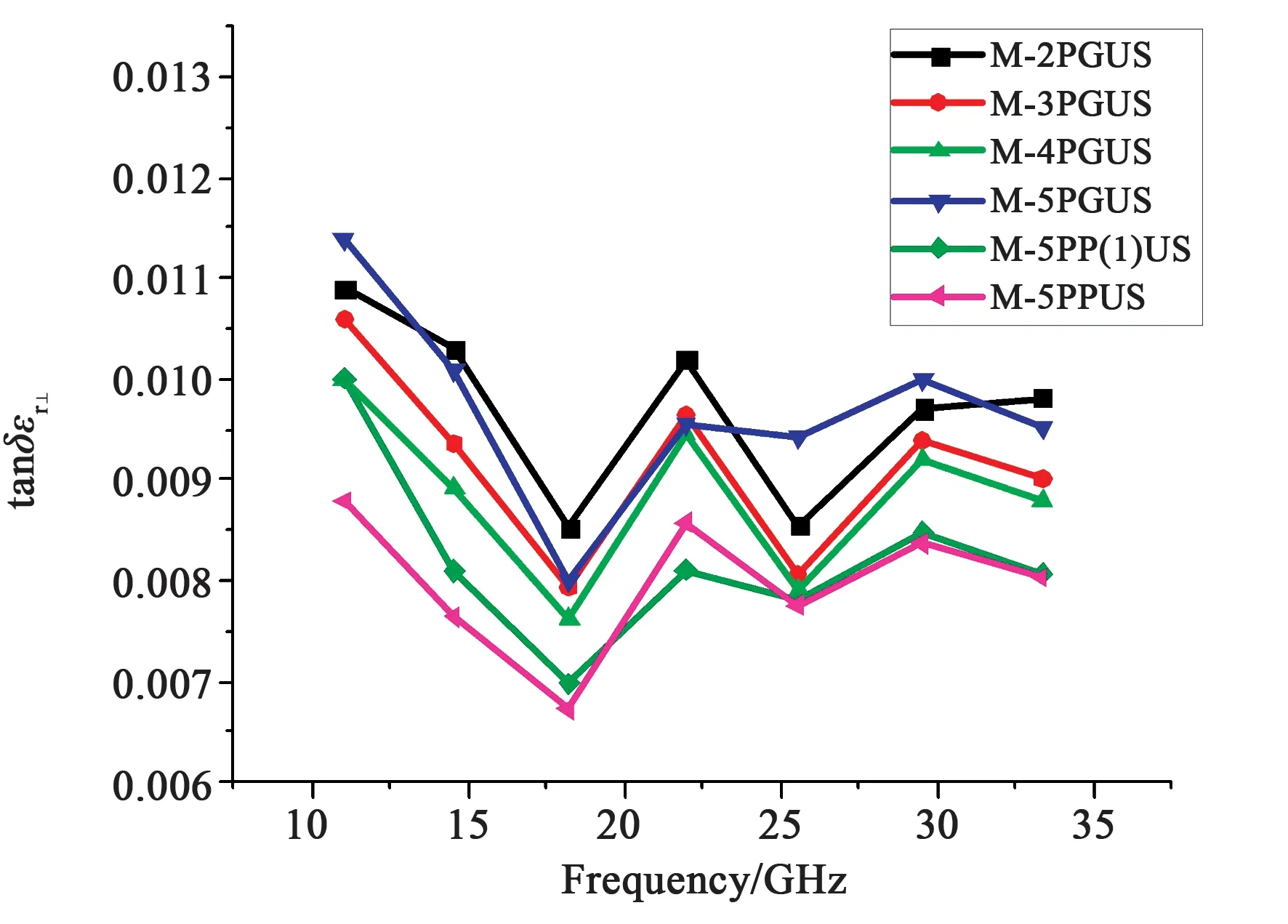
图5 不同频率下的介电损耗比较(20 ℃)Fig.5 Change curves of dielectric loss value with frequency at 20 ℃
由图6可知,随着频率增加,各个化合物的相位可调谐性(τ)都有所增加,其变化规律与介电常数变化规律一致,其中3PGUS的相位可调谐性(τ)最大,最小是5PP(1)US,这与化合物的介电常数有关,介电常数越大,相位调置系数越大。

图6 不同频率下的相位调制系数比较(20 ℃)Fig.6 Change curves of tunability with frequency at 20 ℃
图7为6种化合物在母体液晶中的品质因数折线图。由其计算公式η= τ / tanδεr⊥[26]可知,η和介电常数成正比,与介电损耗成反比。从图中可以看出,6个化合物的品质因数都大于20,当频率达到18 GHz时,nPGUS系列化合物品质因数大于30,这表明所合成的化合物适合于在微波频段使用。

图7 不同频率下的品质因数比较(20 ℃)Fig.7 Change curve of quality factor with frequency at 20 ℃
3.3 不同结构液晶化合物相态性能分析
将目标化合物相态与结构相近的两个液晶化合物5PPUS和5PP(1)US的介电性能和介晶态进行对比和分析,发现本文合成的目标化合物nPGUS的相态及在18 GHz的介电性能有一定差异,具体情况见表3所示:(a)目标化合物5PGUS熔点为57.4 ℃,低于5PPUS,但高于5PP(1)US;(b)化合物5PGUS的向列相态温度范围为101.8 ℃,而5PP(1)US没有表现出液晶相态,5PPUS的向列相宽只有76.2 ℃,说明nPGUS分子中心苯环侧位被氟原子取代有利于形成或拓宽向列相液晶态;这可能与甲基和氟原子取代改变了分子的极性及空间位阻,改变了分子间作用力有关。

表3 在微波18 GHz下不同结构液晶化合物的介电性能参数(20 ℃)Tab.3 Dielectric parameters of LC compositions at microwave 18 GHz at 20 ℃
由此可见,在微波频段(5~30 GHz)下,含氟多苯环异硫氰酸酯类液晶化合物(nPGUS)相对于其他结构类似的三联苯液晶化合物的介电损耗小,相调制量大,品质因数较高;实验表明nPGUS更有利于作为微波通信器件用液晶材料组分物。
4 结 论
本文通过 Suzuki Coupling等反应合成了目标化合物(nPGUS,n=2~5),它们的分子结构经过IR、1H NMR、13C NMR、19F NMR等谱图分析鉴定,证明分子结构正确;通过偏光显微镜和差式扫描量热法确认化合物相态;经过主客体外推法测量目标化合物的双折射率;再将目标化合物配制成液晶组合物材料,用矩形谐振腔微扰法测其微波(5~30 GHz)下介电性能。得到结论如下:4个目标化合物(nPGUS,n=2~5)熔点较低,最低为57.4 ℃,呈现出宽温向列相态(ΔTN≥ 84.7 ℃),其双折射率Δn值在0.390左右;将化合物(nPGUS,n=2~5)提纯精制后与母体液晶混合后测得在18 GHz时的介电常数(Δεr)为0.95,介电损耗为(tanδεr-max)0.00 763,相位可调谐性(τ)0.265,满足微波用向列相液晶材料性能要求,可用于液晶微波通信器件技术研究中,为研究开发我国液晶微波器件积累了实验素材。

