银屑灵片对寻常型银屑病血瘀证患者外周血单核细胞差异表达基因和miRNA芯片结果关联分析※
卢 月 亓 垚 陈曲波 韩 凌 郜恒骏 卢传坚
(广州中医药大学第二附属医院广东省中医证候临床研究重点实验室,广东 广州 510006)
寻常型银屑病是由多种遗传基因决定的、多环境因素刺激诱导的慢性增生免疫异常性皮肤病,发病率占世界人口的2%~3%[1-2]。有研究认为,微血管生成异常与银屑病的发生、持续存在及复发关系密切,在寻常型银屑病的发病机制中起重要作用[3]。
中医学称寻常型银屑病为“白疕”,中医治疗寻常型银屑病的优势在于缓解期长,病情稳定,不易反弹,毒副作用少[4]。我们前期通过对寻常型银屑病中医基本证候与疾病分期及病情的相关性进行探讨,发现寻常型银屑病患者中医基本证候分布依次为血瘀证(70.3%)>血燥证(17.3%)>热证(12.4%),且血瘀证与稳定期相关[5]。研究表明,寻常型银屑病患者存在明显的微循环障碍和血液流变学变化,组织病理检查中可见毛细血管异常,包括血管扭曲、血管通透性明显升高等表现[6-8]。银屑灵片由赤芍、莪术、肿节风、土茯苓、乌梅、紫草、当归、熟地黄、牡丹皮和甘草组成,为广州中医药大学第二附属医院制剂,制剂号Z20080123,治疗寻常型银屑病疗效确切,且安全性好[9]。
通过基因表达谱芯片和miRNA芯片技术,对银屑灵片治疗寻常型银屑病血瘀证患者前后的外周血单核细胞(PBMC)基因表达水平和miRNA表达水平进行分析,对差异表达基因和miRNA进行关联分析,从基因和miRNA水平揭示银屑灵片治疗寻常型银屑病血瘀证的微观物质基础。
1 资料与方法
1.1 病例选择
1.1.1 诊断标准 西医诊断符合寻常型银屑病的诊断[10],中医证型诊断符合白疕血瘀证诊断[3]。且3分<银屑病皮损面积及严重程度指数(PASI)评分<30分,体表受累面积(BSA)<30%。
1.1.2 纳入标准 本研究所有与人体相关的研究内容均遵循赫尔辛基宣言和中国有关临床试验研究规范、法规,所有纳入研究的研究对象均签署知情同意书,标本采集前由研究人员介绍本研究的目的和治疗。
1.1.3 排除标准 妊娠期或哺乳期妇女;近6个月内服用过类固醇药物或维甲酸类药物,或用过生物制剂;1个月内外用过类固醇制剂或维甲酸类乳膏;合并甲状腺功能亢进,心脑血管、肝、肾和造血系统等原发性疾病,精神病,长期服药患者;多种中医证型夹杂患者。
1.2 一般资料 选取2016-04—2016-07广州中医药大学第二附属医院皮肤科门诊寻常型银屑病血瘀证患者9例为银屑灵片组,均为稳定期[10]。男5例,女4例;年龄最大61岁,最小21岁,平均(42.26±11.24)岁;病程最长40年,最短7个月,平均(15.3±10.0)年;PASI评分 3.3~13.6分;瘙痒视觉模拟评分(VAS)0~7.6分。同时选取广州中医药大学第二附属医院体检中心门诊体检的健康者9人为健康组,男5人,女4人;年龄最大65岁,最小17岁,平均(39.52±10.31)岁。2组性别、年龄比较差异无统计学意义(P>0.05),具有可比性。
1.3 治疗方法 2组均予适当的生活指导,禁食牛羊肉、海鲜、芒果、榴莲等易致敏食物;规律作息,心情舒畅,戒烟限酒,适当运动,避免感染。
1.3.1 银屑灵片组 予银屑灵片5 片,每日三餐后口服,连服12 周。
1.3.2 健康组 不予任何治疗。
1.4 仪器及试剂 TRI Reagent(德国Sigma公司);miRNeasy Micro 试剂盒(德国QIAGEN公司);RNase-Free DNase Set(德国QIAGEN公司);Affymetrix表达谱配套试剂盒GeneChip®WT PLUS 试剂盒(美国Affymetrix公司);GeneChip®杂交洗脱染色试剂盒(美国Affymetrix公司);滚动杂交炉(美国Affymetrix公司);基因芯片洗涤工作站(美国 Affymetrix公司);Agilent Bioanalyzer 2100电泳仪(美国Agilent公司);芯片扫描仪GeneChip®Scanner 3000DX2(美国Affymetrix公司);GeneChip®clariom D 基因芯片、Agilent Human miRNA,Release 21.0(8×60K,Design ID:070156)芯片(美国Affymertix 公司);NanoDrop ND-2000超微量分光光度计(美国Thermo Scientific公司);数据采集Command Console Software 3.1软件、数据分析Transcriptome Analysis Console Software软件(美国Affymetrix公司)。
1.5 标本采集及处理 采集研究对象肘静脉血10 mL于含有肝素的抗凝管中,按照试剂盒说明书分离外周血PBMC,置-80℃冰箱保存。银屑灵片组治疗前后各抽血1次,健康组仅试验开始时抽血1次。
1.6 RNA的抽提与质检 根据Sigma提供的标准操作流程,采用TRI Reagent对样本总RNA进行抽提,进而使用miRNeasy Micro试剂盒和RNase-Free DNase Set纯化总RNA。在质检评断合格后,纯化后的总RNA,经Agilent Bioanalyzer 2100电泳仪评估RNA的完整性。
1.7 基因芯片实验 本实验采用Affymetrix表达谱配套试剂盒GeneChip®WT PLUS 试剂盒,按照生产厂家规定的标准操作流程对样品总 RNA中的mRNA进行体外反转录扩增,同时用生物素标记cRNA。
按照Affymetrix芯片杂交流程,将生物素标记的cRNA加入盒式芯片中,按照表达谱芯片配套提供的杂交标准流程使用配套试剂盒,在45 ℃滚动杂交炉中滚动杂交16 h,杂交完成后使用GeneChip®杂交洗脱染色试剂盒在基因芯片洗涤工作站按照标准操作流程进行芯片洗涤。
芯片结果采用芯片扫描仪GeneChip®Scanner 3000DX2进行扫描,用Command Console Software 3.1 软件读取原始数据,质控合格的数据采用Command Console Software 3.1软件进行归一化处理,使用Gene level-SST-RMA算法对数据进行质控并出具数据报告,采用Transcriptome Analysis Console软件进行初步的基因差异表达分析。筛选P<0.05,倍性变化(fold change)≥2的差异基因,利用DAVID在线数据库进行富集,选择P<0.05的通路进行分析。
1.8 miRNA芯片实验 本研究使用的芯片为Agilent Human miRNA ,Release 21.0(8×60K,Design ID:070156)芯片,样品总RNA利用NanoDrop ND-2000超微量分光光度计定量并经Agilent Bioanalyzer 2100电泳仪检测RNA完整性。RNA质检合格后,参照芯片标准流程进行样本的标记、芯片的杂交及洗脱,洗脱后利用Agilent Scanner G2505C扫描得到原始图像。采用Feature Extraction 10.7.1.1软件处理原始图像提取原始数据。接着利用Genespring 13.1软件进行标准化和后续处理。筛选P<0.05,倍性变化(fold change)≥2的上调或下调差异miRNA。然后利用3个数据库Targetscan在线数据库、microRNAorg在线数据库和pita在线数据库共同对差异miRNA进行靶基因预测,接着对靶基因进行基因本体(Gene Ontology,GO)和代谢途径(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析,以判定差异miRNA主要影响的生物学功能或通路。根据表达谱芯片的差异基因分析结果,miRNA芯片差异miRNA及靶基因预测结果,利用DIANA在线工具及其数据库对基因芯片和miRNA芯片结果进行关联分析和维恩分析。
2 结果
2.1 银屑灵片组治疗前与健康组PBMC表达谱芯片与miRNA芯片结果关联分析 根据银屑灵片组治疗前与健康组PBMC的miRNA芯片差异miRNA的靶基因预测结果,将表达谱分析的差异基因与miRNA芯片分析的差异miRNA按照差异改变负相关的关系进行关联分析,并绘制了差异miRNA与相关联的差异基因的网络图。结果表明,治疗前寻常型银屑病血瘀证患者与健康者PBMC的差异miRNA包括hsa-miR-30c-5p、hsa-miR-362-3p、hsa-miR-374a-5p等共48个。寻常型银屑病血瘀证患者与健康人PBMC的差异miRNA靶基因包括PIK3C2B、MSI2、RPS6KA1等共27个(见图1)。

图1 银屑灵片组治疗前与健康组PBMC差异miRNA与相关联差异基因网络图
2.2 银屑灵片组治疗后与健康组PBMC表达谱芯片与miRNA芯片结果关联分析 将银屑灵片组治疗后与健康组PBMC表达谱分析的差异基因与miRNA芯片分析的差异miRNA按照差异改变负相关的关系进行关联分析。结果表明,治疗后寻常型银屑病血瘀证患者与健康者PBMC的差异miRNA包括hsa-miR-23c、hsa-miR-149-5p、hsa-miR-486-5p等共47个。寻常型银屑病血瘀证患者与健康者PBMC的差异miRNA靶基因包括HIVEP2、RAB39B、RBMS1等共33个(见图2)。

图2 银屑灵片组治疗后与健康组PBMC差异miRNA与相关联差异基因网络图
2.3 银屑灵片组治疗前后PBMC表达谱芯片与miRNA芯片结果关联分析 银屑灵片组治疗前后PBMC表达谱芯片与miRNA芯片结果关联分析结果表明,治疗前后PBMC的差异miRNA包括7个:hsa-miR-146b-5p、hsa-miR-186-5p、hsa-miR-194-5p、hsa-miR-212-3p、hsa-miR-31-5p、hsa-miR-362-3p、hsa-miR-199b-5p,差异miRNA靶基因包括14个:MYADM、SLAM6、DYNLL2、PHF20L1、ZNF385A、ARID18、TJAP1、MLXIP、KLF13、NINL、BACH2、RBMS1、DDX5、SORL1(见图3)。
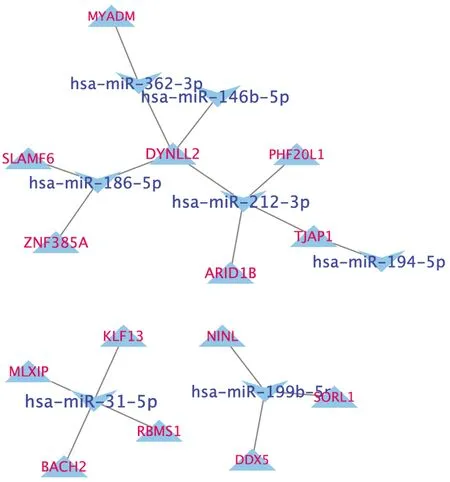
图3 银屑灵片组治疗前后PBMC差异miRNA与相关联差异基因网络图
3 讨论
本研究通过基因表达谱芯片和miRNA芯片技术,对银屑灵片治疗前后寻常型银屑病血瘀证患者与健康者PBMC中差异表达的基因和miRNA进行分析,并将结果进行关联。
寻常型银屑病血瘀证患者与健康者PBMC芯片结果存在具有靶标关系的差异miRNA 48个和差异靶基因27个。寻常型银屑病血瘀证可能是通过这些差异miRNA对靶基因进行调控,从而参与寻常型银屑病血瘀证的发生和发展。有文献报道,miR-148a-3p可靶向调控c-Jun mRNA表达,C-Jun调节炎症相关基因的表达,并影响细胞增殖、细胞周期和细胞凋亡[11]。miR-148b-3p可调节肿瘤坏死因子α(TNF-α)、白细胞介素(IL)-6和IL-8等促炎因子,影响核因子κB(NF-κB)信号通路[12]。miR-199b-5p通过PBMC中的糖原合成酶激酶3β(GSK3β)/NF-κB信号传导途径减弱了炎性反应[13]。microRNA-362-3p通过抑制Paired box基因2减轻神经痛并减少细胞外调节蛋白激酶(ERK)和分裂原激活的蛋白激酶p38(p38 MAPK)的活化抑制神经元炎症[14]。心肌再灌注损伤常引起氧化应激和炎症,miR-374a-5p可能对体内心脏缺血/再灌注(I/R)损伤和体外缺氧/复氧(H/R)损伤具有保护作用[15]。miR-148a-3p、miR-148b-3p、miR-199b-5p、microRNA-362-3p和miR-374a-5p共有靶基因磷酸二酯酶4(PDE4)通过降解环磷酸腺苷(cAMP)发挥促炎作用,而PDE4抑制剂在体内和体外均具有抗炎作用。有研究表明,与正常组比较,寻常型银屑病患者PBMC中PDE4B和PDE4D mRNA过度表达,真皮中PDE4表达上调[16]。miR-148a-3p和miR-148b-3p共有靶基因双特异性酪氨酸磷酸化调节激酶1B(DYRK1B)与T淋巴细胞中IL-2产生相关[17]。
本研究结果表明,银屑灵片组治疗前后PBMC芯片结果中有差异miRNA 7个和差异靶基因14个。有研究表明,miR-212-3p通过抑制SRY和转录因子5(SOX5),可减少类风湿关节炎成纤维样滑膜细胞(RA-FLS)增殖并促进细胞凋亡[18]。miR-31促进角质形成细胞的增殖和迁移[19],miR-31-5p的靶基因Bach2在调节辅助型T细胞2(Th2)分化和Ⅱ型免疫应答中发挥重要作用[20]。miR-31-5p的靶基因KLF13在多个阶段参与B淋巴细胞和T淋巴细胞的发育,KLF13在CD21和CD23的共调节中具有负性调节作用,并参与T细胞抗原受体(TCR)、前B细胞受体(pre-BCR)和B细胞抗原受体(BCR)的信号传递[21]。因此,我们认为银屑灵片通过调控这些差异表达的miRNA和靶基因发挥治疗寻常型银屑病血瘀证的作用。
综上所述,本研究通过对银屑灵片治疗寻常型银屑病血瘀证患者PBMC的表达谱芯片与miRNA芯片结果进行关联分析,得到寻常型银屑病血瘀证和银屑灵片治疗血瘀证的微观物质基础,并且发现hsa-miR-146b-5p等7个miRNA及其靶基因DYNLL2等14个基因有可能是银屑灵片治疗寻常型银屑病血瘀证的重要靶点,本结果还需动物和细胞实验的进一步验证。

