经导管封堵卵圆孔未闭预防卒中复发的研究进展
孙丽杰 李静
100053 北京,首都医科大学宣武医院心脏科
卵圆孔未闭(patent foramen ovale,PFO)是由于婴儿出生后心房原发隔与继发隔未能紧密闭合而形成的连接左右心房的通道,在人群的发生率大约为25%[1]。部分PFO与卒中、偏头痛、减压病、高原肺水肿等疾病有一定关系,约50%的隐源性卒中(cryptogenic stroke,CS)患者同时合并PFO[2]。来自静脉系统的栓子“逃过”肺循环的溶解,从右心系统进入左心系统继而引发体循环栓塞事件的现象称为反常栓塞(risk of paradoxical embolism,RoPE)[3],PFO增加了RoPE发生机会。以往此类患者多采用抗凝药物保守治疗。20世纪90年代首次研究PFO封堵预防卒中复发,但其治疗效果一直存在争议。最新几项大型随机对照试验(randomized controlled trial,RCT)结果公布,肯定了PFO封堵预防卒中复发的有效性。本文通过对几项RCT的简单分析进一步讨论PFO封堵的有效性和安全性,结合RCT和其他研究对PFO封堵获益人群的特征、术后管理等方面简要综述。
1 PFO封堵安全性和有效性
1.1 阴性结果试验
CLOSUREⅠ试验[4]纳入990例CS或短暂性脑缺血发作(transient ischemic attack,TIA)患者,将其随机分入封堵治疗组和药物对照组(使用华法林或阿司匹林由医师视情况决定),术后平均随访2年。但该试验存在两方面问题,一方面封堵组使用的Star Flex封堵器导致手术成功率较其他类型封堵器低(89.4%),术后6个月存在明显残余分流患者偏多(14%),术后房颤发生率较对照组也明显偏高(5.7%比0.7%,P<0.001)[5];另一方面在入组患者筛选上,两组患者高血压(34%比28%)和高血脂(47%比41%)患病率偏高,对卒中复发患者分析发现,反映动脉粥样硬化的指标明显升高,如体质指数、高血压、糖尿病、缺血性心肌病[6]。这引发了对此类患者卒中的原因是否与PFO相关的怀疑。最终,该试验并未证实封堵治疗和药物治疗预防PFO患者卒中再发效果的差别。
PC试验[7]纳入414例CS、TIA和系统性栓塞患者,对照组设置与CLOSUREⅠ试验类似,平均随访4年。该试验使用Amplatzer封堵器,手术成功率较CLOSUREⅠ试验明显增加(95.9%),术后残余分流减少(4.1%)。该试验纳入系统性栓塞等非脑栓塞事件的PFO患者,扩大了封堵适应证范围。但纳入的患者约1/4有高血压、高血脂、吸烟等动脉粥样硬化危险因素,而且约17.6%的患者退出试验或失访[8]。最终,封堵组和药物治疗组的试验结果对比差异也无统计学意义。
RESPECT试验[9]纳入980例CS和TIA患者,对照组使用的药物包括阿司匹林、氯吡格雷、华法林或阿司匹林加双嘧达莫,封堵器也是Amplatzer封堵器。2013年进行短期总结,平均随访时间仅为2年。但封堵组和对照组失访率相差较大(9.2%比17.2%)[8]。虽然结果在统计学上无意义,但比较卒中复发人数,能明显看到封堵治疗优势。
虽然由于试验设计不周全、患者纳入标准宽松、随访时间短、失访率高等因素导致以上几项临床RCT结果阴性,但能看到封堵手术较药物治疗的长期优势(表1)。后续对以上RCT进行的荟萃分析表明,封堵治疗预防卒中复发的效果优于药物治疗(HR=0.59,95%CI:0.36~0.97,P=0.04)[10],这种优势在PC试验和RESPECT试验的荟萃分析中更明显(HR=0.54,95%CI:0.29~1.01,I2=0%)[11]。
1.2 阳性结果试验
RESPECT试验[12]将随访时间延长至平均5.9年,发现封堵组卒中复发的比例下降至45%,并且出现了统计学差异(P<0.046)[13]。而在合并房间隔膨胀瘤(atrial septal aneurysm,ASA)(1.7%比7.6%)和较大PFO(2.0%比6.9%)的患者中,PFO封堵优势更明显[14]。
REDUCE试验[15]纳入664例CS患者,按2∶1比例随机分为封堵组和对照组。该试验对患者卒中类型的筛选更严格,纳入栓塞来源导致卒中的患者,排除其他原因所致卒中的患者,加大PFO与卒中的相关性,PFO封堵的效果较单纯抗血小板治疗优势更明显。经过3年的随访,得出了封堵能显著降低卒中复发风险的结论。
CLOSE试验[16]纳入663例存在大量右向左分流(right-to-left shunt,RLS)或合并ASA的患者,平均随访5年。不同于之前的试验,该试验将纳入患者随机分为3组,首次比较了封堵联合抗血小板药物、单用抗血小板药物和单用抗凝药物的治疗效果。结果显示,封堵组预防卒中复发比单用抗血小板治疗有效,单用抗血小板治疗和单用抗凝治疗的预防效果无统计学差异,但未报道关于抗凝治疗和封堵治疗的对比结果[17]。
DEFENCE试验[18]纳入123例高危PFO患者,随机分入试验组和对照组。与之前RCT纳入患者年龄均小于60岁不同,该试验将年龄限制扩大到了80岁,很多年龄超过60岁的患者被纳入试验。与其他阳性结果试验一样,封堵组患者卒中复发率更低。
以上阳性结果试验在患者的选择方面更严格,尽可能筛选出卒中与PFO紧密相关的患者,TIA患者被排除在试验外,而且更强调PFO解剖特征,所以封堵治疗优势更明显(表1)。因此,只有选择恰当的患者才能真正发挥PFO封堵治疗的有效性。
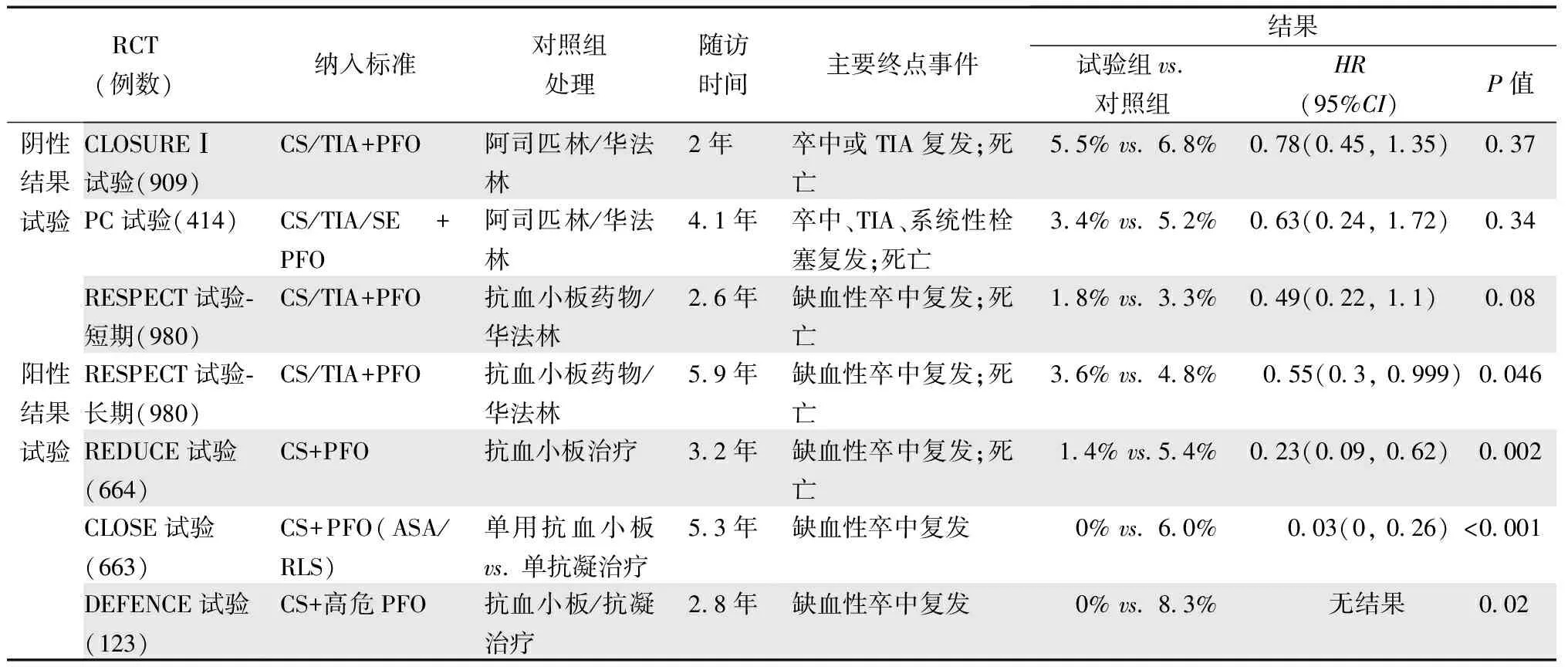
表1 PFO封堵预防卒中复发的RCT汇总
1.3 PFO封堵并发症
PFO封堵安全性高,并发症少见,严重不良事件罕见。RESPECT、REDUCE和CLOSE试验均显示封堵组和药物治疗组在术后不良事件上无统计学差异,表明封堵手术并不会比药物治疗增加风险[19]。对CLOSUREⅠ、PC、RESPECT、REDUCE、CLOSE和DEFENCE试验进行荟萃分析发现,封堵组患者新发房颤的比例明显高于药物治疗组,使用Amplatzer封堵器组的房颤发生率低于其他设备(3.65%比5.61%)[20-22]。大部分新发房颤在术后1个月发生,仅短暂存在,并且复发率低。房颤的发生与封堵器的类型、患者年龄等有一定关系[23]。但封堵术后房颤的长期意义尚不明确,相关研究目前较少。
其他封堵并发症包括封堵器血栓、封堵器脱落或移位、腹股沟血肿、心包积液或心脏压塞、心脏穿孔、感染性心内膜炎、空气栓塞、封堵器过敏等,对58项观察性研究的荟萃分析显示,封堵器栓塞或移位的发生率为0.4%,心包积液或心脏压塞的发生率为0.3%,其他相关并发症的报道较少[24]。
2 PFO封堵获益患者的特征
2017年之后的试验能明确证实封堵优于药物治疗,很重要的改进是患者的严格筛选。只有对由PFO导致的卒中患者进行封堵,手术预防卒中复发的效果才最大。因此,术前对患者进行详细的评估至关重要。
2.1 解剖特征
经食道超声心动图能清楚呈现房间隔解剖结构,既是诊断PFO的“金标准”及首选方法[25],又能辨别高危PFO。高危PFO的特征包括大PFO、PFO合并ASA、中到大量RLS。对于长PFO(>10 mm)、PFO合并下腔静脉瓣或希阿里式网、PFO和下腔静脉瓣的角度关系及其他解剖特征与CS的关系仍需探讨。
PFO大小指静息状态或Valsalva动作时原发隔和继发隔的最大距离,PFO大小范围在1~19 mm之间,平均4.9 mm[24],超过2 mm即为大PFO[26]。根据RoPE机制PFO宽度越大,越有利于栓子通过。RESPECT和DEFENCE试验均显示封堵效果在大PFO患者中效果更佳。纳入9项研究PFO解剖特征与CS关系试验的荟萃分析显示,卒中组患者与对照组相比,静息时PFO的大小无明显差异[2.4(1.5, 3.3)mm比1.8(1.4, 2.2)mm],但Valsalva动作时卒中组的PFO大小明显大于对照组[6.4(5.1, 7.8)mm比3.1(1.8, 4.4)mm][27]。
ASA是指房间隔从中线向左右两侧偏移幅度过大,不同研究幅度定义值不同,一般在11~15 mm之间[27]。REDUCE、DEFENCE和CLOSE试验均发现,PFO封堵预防卒中复发的治疗效果在PFO合并ASA更明显。RESPECT试验的亚组分析也得到了类似的结论。而且CLOSE试验表明,PFO合并ASA也会增加卒中复发的风险[17, 28]。ASA使PFO通道开放频率增加,为栓子及血管活性物质通过提供更多的机会。由此,有些研究将房间隔高活动度也归为高危PFO类型[29]。欧洲立场文件明确指出,ASA会增加卒中复发的风险[30]。
PFO分流情况通过经胸或经食道超声心动图声学造影观察,使用静息时或Valsalva动作后左心房的微泡数来反映分流的严重程度。但不同研究定量标准不一,我国专家指南标准[24]左心腔内≥30个微泡/帧提示大量RLS。大部分试验均认为大量分流患者封堵受益更大。在RESPECT试验中,大量RLS患者封堵带来的益处更明显(HR=0.26,95%CI:0.10~0.71,P<0.005),而没有RLS的患者则相反(HR=0.96,95%CI:0.44~2.61,P<0.93)[17]。
不同于以上解剖特征存在RCT研究证据,支持PFO长度、合并下腔静脉瓣或希阿里式网、PFO和下腔静脉瓣的角度关系等解剖特征的研究多为回顾性研究。PFO长度指原发隔与继发隔重叠的长度,一般为3~18 mm,平均8 mm[24]。Nakayama等[26]研究指出,当PFO长度超过10 mm时,PFO导致卒中的危险性增加。长隧道型PFO容易因为血液湍流及停滞而成为微栓子的形成场所。残余的下腔静脉瓣不仅阻碍血流,而且会引导血流RLS。希阿里式网的存在大多合并ASA。PFO和下腔静脉瓣的角度过低,更容易形成RLS。这些解剖特征是否与卒中相关需要更多高质量试验验证。原发隔与继发隔的厚度、PFO与主动脉瓣、心房游离壁的位置关系等其他解剖特征是否与卒中相关有待探索。
2.2 临床特征
PFO患者导致卒中的原因,不仅与PFO本身的解剖形态相关,还与患者的临床状态相关。RoPE评分通过年龄、有无血管疾病危险因素、影像梗死类型等因素预测CS与PFO的相关性。患者职业影响PFO封堵选择。对于高凝状态、静脉栓塞及肺栓塞等病史具有抗凝指征的患者,PFO封堵带来的益处仍有待探讨。
RoPE评分[31]评估PFO在缺血性脑卒中的作用。该评分中年龄因素占较大比例。患者越年轻,脑血管病危险因素越少,PFO导致卒中的可能性越大。上述提及的RCT,除了DEFENCE试验纳入了60岁以上的患者,其他试验都只纳入60岁以下的患者,PFO封堵在60岁以下除外其他病因的卒中患者获益明显。Wintzer-Wehekind等[32]对年龄超过60岁PFO封堵患者进行回顾分析,发现PFO封堵对于老年患者是安全的,并且长期随访缺血性事件的发生率较低。但对年龄较大患者,术前更应充分评估除外其他卒中因素[33]。RoPE评分也考虑高血压、糖尿病、吸烟等脑血管病危险因素,合并危险因素越多,评分越低,提示PFO与卒中关系相关性越小。除此之外,皮层梗死也被纳入RoPE评分中。PFO所致卒中更容易发生单一皮质梗死或多发小的散在病灶[34],REDUCE、CLOSE和DEFENCE试验都排除了影像上表现为深且小梗死灶的患者,REDUCE试验结果表明PFO封堵减轻了浅表梗死灶患者的卒中复发率,但对于深而小梗死灶患者封堵效果不佳[32]。Kent等[35]研究发现,RoPE评分越高卒中复发的比例越低,这与“PFO与RoPE导致的卒中比其他血管因素导致的卒中的复发风险低”的研究契合。RoPE评分能反映PFO的致病性,但PFO封堵时仅依据该评分是不可靠的,还应考虑其他解剖特征(表2)。
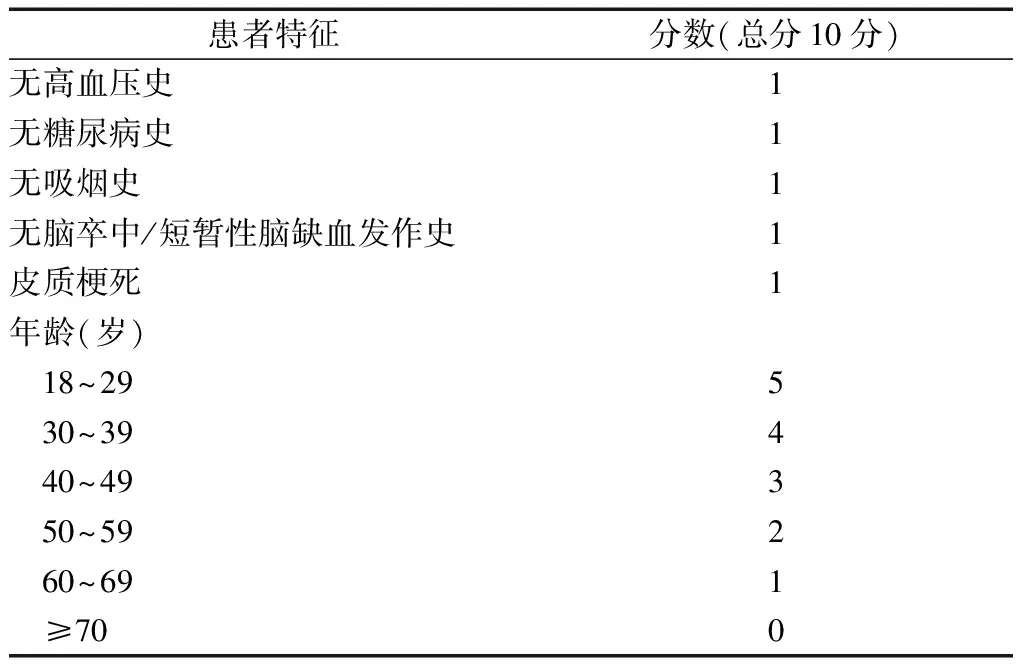
表2 RoPE评分及意义
栓塞病史和高凝状态也会增加PFO致病率。RoPE的栓子多为静脉血栓,因此对于卒中的患者应充分评估下肢静脉、盆腔静脉等。我国专家指南[24]指出,在深静脉血栓或肺栓塞之后发生卒中时,如果合并PFO,则认为PFO是“病理性”的。对于卒中患者也要完善凝血指标等生化及基因检查,确定是否存在高凝状态,因为高凝状态也会增加RoPE的可能。询问病史同样不可忽视,很多患者卒中发作前有长期旅行、外科手术后、剧烈运动、体力劳动伴类似Valsalva动作、睡眠呼吸暂停等病史,这些都会增加RoPE危险性。但这类存在抗凝指征的患者并不积极推荐进行PFO封堵[17]。REPECT试验对存在抗凝指征的患者进行分析表明,PFO封堵对其带来的益处不明显。CLOSE试验虽然将患者分为3组,但关于抗凝治疗和PFO封堵治疗的对比却无结果。关于PFO封堵对此类患者的益处仍需更多研究探讨。
在进行PFO封堵评估时,也应考虑患者的职业因素。英国专家共识[21]推荐以下职业的PFO患者应积极进行PFO封堵:深海潜水员、爬山攀岩爱好者、飞行员、宇航员、公交车司机及经常做Valsalva动作的人,如乐器演奏者和重体力搬运工。
除了患者特征,封堵器的类型也影响封堵治疗效果。目前美国FDA批准Amplatzer封堵器和GORE Cardioform封堵器用于临床[6]。由于封堵器本身与术后并发症关系密切,因此从金属合金封堵器、药物涂层封堵器到可降解封堵器,封堵器类型也不断改进和完善。目前全可降解封堵器仍处于动物实验和临床试验阶段,新型封堵器有望为患者带来更大益处。
3 PFO封堵患者术后管理
3.1 术后药物治疗
封堵术后封堵器内皮化需要一定的时间,并且存在封堵器栓塞的风险,因此术后需要口服抗血小板药。但关于抗血小板药物种类及使用时间,世界各国的标准不一。我国专家指南[24]推荐术后口服阿司匹林3~5 mg·kg-1·d-16个月及氯吡格雷75 mg/d 3个月。欧洲专家共识[30]推荐术后口服双抗3个月后,改服阿司匹林至少5年。Rigatelli等[36]通过回顾性研究分析封堵后口服100 mg阿司匹林6个月的长期安全性和有效性,证实该方法安全有效。相关的高质量RCT较少,具体的用药标准仍存争议。
封堵术后是否应用抗凝药物的研究报道较少,仅限于个别案例,具体的治疗标准仍有待公布。
3.2 术后复查
封堵后患者应常规定期复查,检查封堵器的位置、是否侵蚀其他心内结构、有无血栓、是否存在残余分流等内容。我国专家指南[24]推荐术后3、6和12个月复查超声心动图,以后每年行经胸超声心动图检查,如有其他临床症状加做心电图或Holter检查。各国各中心对术后复查的频率和时间没有统一标准,但检查手段大致相同。
最常使用的复查方法是经胸超声心动图、经食道超声心动图和经颅多普勒超声,3种方法均可结合发泡实验进行。经胸超声心动图操作方便,患者痛苦小,但对于观察封堵器及心内结构只能做大致判断,不如经食道超声心动图辨认解剖结构清楚;经食道超声心动图属于侵入性检查,大部分患者在局麻下进行操作,会因为过程痛苦而难以配合Valsalva动作,影响RLS的判断。有研究表明,经食道超声心动图结合发泡实验对RLS的检出率低于经胸超声心动图结合发泡实验[37]。判断分流情况也可采用对比增强经颅多普勒超声声学造影,但结果容易受到肺动静脉瘘等其他解剖异常影响,术后复查内容有限。
关于CT作为复查方法的报道有限。封堵术后6周进行MRI(1.5~3T)检查是安全的,但MRI用于术后复查的报道也较少。
4 指南共识
多项大型RCT已经肯定了PFO封堵治疗效果,世界各国也陆续推出专家共识规范PFO封堵治疗。欧洲医学协会专家立场文件[30]强烈建议65岁以下CS合并PFO患者进行PFO封堵治疗,英国[6]、法国[28]、波兰[20]等其他欧洲国家也积极推荐PFO封堵治疗。随着更多相关试验结果的公布,PFO封堵治疗会更加具体规范。
5 小结
随着最新RCT结果的公布,对PFO封堵预防卒中的有效性也从争议变成统一。但对于封堵治疗的决定,应经过神经内科和心脏科专家的共同评估,同时向患者告知封堵的风险和益处,再由患者和医生共同决定。
PFO封堵治疗具体的实施标准还未确定,很多细节有待研究。对于被排除在RCT之外的患者,尤其是60岁以上患者能否从PFO封堵受益?对于有抗凝指征的患者,抗凝治疗是否优于PFO封堵?封堵术后抗血小板治疗最佳持续时间?与PFO封堵相关的房颤的临床意义?房颤的发生是否会掩盖封堵带来的益处?尚需更多临床试验及研究一一解惑,指导PFO封堵治疗。
利益冲突:无

