国际FAPAS乳粉中金黄色葡萄球菌定量检测能力验证结果与分析
秦婧 王琳帆 魏思宇 陈奕杉 陈鸿剑 郑玉红
摘 要:目的:国际FAPAS能力验证旨在评估实验室对于金黄色葡萄球菌的检测能力,加强实验室质量管理。方法:依据FAPAS作业指导书及GB 4789.10—2016第二法(平板计数法)对乳粉中金黄色葡萄球菌进行定量检测,并用两种国产配套试剂进行比对。结果:采用北京陆桥配套试剂检测样品的菌落总数上报结果为1.0×105 CFU/g,且两种国产配套试剂检测结果均在能力验证结果范围内。结论:国际FAPAS乳粉中金黄色葡萄球菌定量检测能力验证结果评价为满意,Z值为0,上报结果是此次能力验证的指定值。
关键词:金黄色葡萄球菌;能力验证;定量检测;FAPAS
能力验证是利用实验室间比对,按照预先制定的准则评价参加者的能力的外部质量活动,寻求并参加能力验证是合格评定机构的责任和义务[1]。英国FAPAS分析实验室能力验证(Food Analysis Performance Assessment Scheme)是专门从事食品检测分析方面的能力评估体系,通过实验室间测试结果的比对来判定实验室能力的合格评定活动。FAPAS为世界约3 000家实验室专门提供医学、食品检测方面的能力验证活动;FAPAS建立了一套完整的能力验证提供者的评价体系。该体系在全世界各国的食品分析实验室迅速普及,它已是食品分析领域全球第一的国际评价体系[2]。FAPAS在2007年已与CNAS(中国合格评定国家认可委员会)达成互认。为提高检验检测能力和水平,本实验室参加FAPAS于2021年4月的乳粉中金黄色葡萄球菌定量检测能力验证,希望通过此次FAPAS能力验证来评估实验室检验人员的能力,维持实验室检验检测水平。依据的方法是GB 4789.10—2016第二法(平板计数法),并对北京陆桥、广州环凯两个厂家生产的检测配套培養基进行了比对。
1 材料与方法
1.1 试剂
氯化钠(分析纯)来自天津天力化学试剂有限公司;Baird-Parker琼脂平板、血琼脂平板、胰蛋白胨大豆琼脂平板(tryptic soy agar,TSA)、革兰氏染色液、脑心浸出液肉汤(brain heart infusion broth,BHI)和冻干血浆,均分别来自北京陆桥技术股份有限责任公司和广东环凯微生物科技有限公司。
1.2 仪器设备
均质器(宁波新芝生物科股份有限公司 SCIENTZ-11);生化培养箱(上海悦丰仪器仪表有限公司SPX-150B-Ⅱ);生物显微镜(奥林巴斯广州工业有限公司 CX23);可调式混匀仪(大龙兴创实验仪器北京股份有限公司 MX-S);生物安全柜(上海博讯实业有限公司医疗设备厂 BSC-1300ⅡA2)。
1.3 方法
1.3.1 能力验证样品的接收和确认
实验室收到FAPAS乳粉中金黄色葡萄球菌能力验证样品1份,样品编码是M263E14,样品为10 g乳粉,塑料瓶包装,并确认样品完整性。
1.3.2 能力验证样品的前处理和水化
根据FAPAS乳粉中金黄色葡萄球菌(M263E14)能力验证作业指导书的说明,开启样品前应先将样品放置在室温下30 min。在二级生物安全柜中以无菌操作开启样品,将样品置于提前准备好的无菌均质袋中,用少量无菌生理盐水充分冲洗样品容器并将其吸入到放有样品的均质袋中,最终使水化的生理盐水总量为90 mL,用均质器充分混匀,即为10-1样品匀液。后续依据《食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验》(GB 4789.10—2016)第二法(平板计数法)进行检测分析。
1.3.3 样品的稀释
该步骤在生物安全柜中以无菌操作进行。用1 mL无菌吸管吸取10-1样品匀液1 mL,沿管壁缓慢注于盛有9 mL生理盐水的无菌试管中(注意吸管尖端不要触及稀释液面),充分振摇试管,制成10-2的样品匀液。按以上操作程序,依次制备10-3、10-4样品匀液。后续操作分别使用北京陆桥和广州环凯生产的配套试剂进行检测分析。
1.3.4 样品的接种和培养
在3个B-P平板上分别加入0.3 mL、0.3 mL、0.4 mL样液进行涂布。由于GB 4789.10—2016第二法(平板计数法)存在涂布不均匀和B-P平板接种量较大不易吸收的情况,故同时在5个B-P平板上各加入0.2 mL样液进行涂布。注意B-P平板应提前一天配制并放于冰箱冷藏,因为新鲜配制的B-P平板表面易有水珠。涂布后,将平板静置10 min,如样液不易吸收,可将平板放在培养箱(36±1) ℃培养1 h,等样品匀液吸收后翻转平板,倒置放于(36±1) ℃培养24~48 h。
2 结果与分析
2.1 菌落计数及鉴定
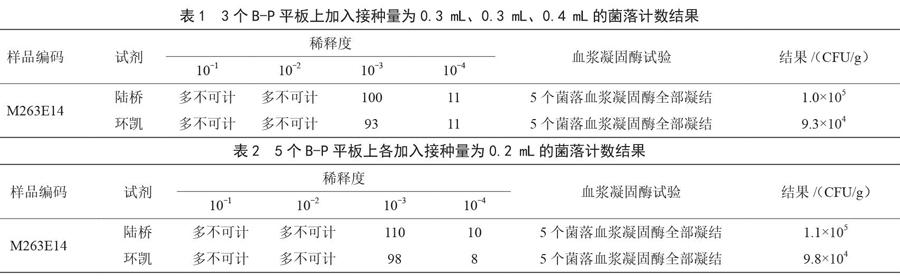
样品培养48 h后,北京陆桥和广州环凯的B-P平板上均仅有一种菌落,且菌落呈黑色、有光泽、表面光滑、凸起、湿润、有浅色的边缘,周围绕以不透明圈,其外有一清晰带,依据GB 4789.10—2016第二法确定其为典型菌落。将10-3稀释度的菌落依据GB 4789.10—2016进行血平板划线、染色镜检、血浆凝固酶试验。结果如表1、表2所示。
2.2 讨论
3个B-P平板上分别加入接种量为0.3 mL、0.3 mL、0.4 mL的样液,采用北京陆桥配套试剂检测样品的菌落总数结果为1.0×105 CFU/g,采用广州环凯配套试剂检测样品的菌落总数结果为9.3×104 CFU/g;5个B-P平板上各加入接种量为0.2 mL的样液,采用北京陆桥配套试剂检测样品的菌落总数结果为1.1×105 CFU/g,采用广州环凯配套试剂检测样品的菌落总数结果为9.8×104 CFU/g。样液接种量为0.2 mL的方法,采用北京陆桥和广州环凯试剂的样品菌落总数检测结果均要大于样液接种量分别为0.3 mL、0.3 mL、0.4 mL的方法,因为GB 4789.10—2016第二法(平板计数法)本身存在接种量较大和涂布不均匀的情况,没有接种量为0.2 mL的方法有利于菌落生长,这一点与已有陆其聪等人[3]与王洪亮等人[4]的相关研究一致。因为本次FAPAS能力验证采用方法为GB 4789.10—2016第二法(平板计数法),日常样品检测采用北京陆桥配套试剂,故上报结果为1.0×105 CFU/g。此次国际FAPAS乳粉中金黄色葡萄球菌定量检测能力验证结果评价为满意,且Z值为0,说明上报结果是为此次能力验证指定值,由此可见该实验室具备金黄色葡萄球菌定量检测分析能力。
3 注意事项
对于新取得检验检测资质的微生物实验室来说,承接能力验证前需要进行大量的准备工作,现就准备工作做一个总结,以期为新实验室或新进检测人员提供参考。
①准备工作。得知要参加能力验证后应提前准备相关试剂、器具和设备,如提前验证商品化培养基,提前准备所用三角瓶和试管,且不与日常检测相混淆,提前确定使用的培养箱是否洁净、是否在计量有效期内等。②作业指导书。收到样品后,应首先确认样品的完整性并记录收样日期,不要急于准备相关试剂,应先制定作业指导书和确定检验依据。③试剂配制。新鲜配制的B-P平板较软、不好涂布,应提前1 d配制并在第2 d使用;使用前确认B-P平板干燥、无水珠,若有水珠可提前放置在培养箱中待水珠消失;9 mL生理盐水应在使用时分装,不可分装好后再灭菌,因为灭菌过程中会使9 mL生理盐水增加或减少,影响结果准确性。④试验操作。样品应提前从冰箱中取出并恢复至室温,可安排两人同步试验,一人取样并进行10-1倍稀释,稀释好后,两人分别进行后续稀释和加样,进行人员比对;涂布时每个稀释梯度使用一根涂布棒,不可每个B-P平板用一根涂布棒,会造成样液损失,影响结果准确性;注意整个操作应在20 min内完成,因为细菌20~30 min繁殖一代[5];完成试验后,若B-P平板上样液不吸收,可将平板放在培养箱(36±1) ℃培养1 h,等样品匀液吸收后翻转平板,倒置培养。⑤计数。按照检验依据所描述的菌落形态进行典型和可疑菌落计数,并一定拍照保存,平板前后均要拍照,平板背面更方便观察典型菌落透明圈,便于识别典型菌落,照片可作为科室学习资料保存。
参考文献
[1]中国合格评定国家认可委员会.能力验证规则:CNAS-RL02:2016[EB/OL].(2016-04-15)[2021-05-21].https://www.docin.com/p-1699040362.html.
[2]陈万胜,马莉,亓潇.国际FAPAS乳粉中沙门菌属能力验证的关键点[J].河南预防医学杂志,2020,31(12):900-903.
[3]陆其聪,钟宇思,王立博,等.金黄色葡萄球菌定量检测能力验证结果与分析[J].食品研究与开发,2017,38(16):153-156.
[4]王洪亮,程艳宇,王梦晓.食品中金黄色葡萄球菌定量檢测方法的研究[J].食品研究与开发,2016,37(9):185-187.
[5]雷兰兰.食品微生物能力验证的重要因素[J].现代食品,2018(16):4-6.

