复杂内耳畸形患儿人工耳蜗植入术后疗效分析
赵天峰 陈俊 任寸寸 温立婷 查定军 邱建华
内耳畸形曾一度被认为是人工耳蜗植入的禁忌症,自上世纪90年代Albernaz开展第一例Mondini畸形患者人工耳蜗植入术以来[1],越来越多的成功病例成为证明内耳畸形患者人工耳蜗植入有效的有力证据。但学者对内耳畸形人工耳蜗植入也提出了一些不同观点,尤其是对伴蜗神经发育不良的严重内耳畸形患儿能否进行人工耳蜗植入仍然有争议。因此,本文通过分析17例行人工耳蜗植入术的复杂内耳畸形患儿的临床资料,了解其术后听觉言语发育效果,为复杂内耳畸形患儿的人工耳蜗植入提供参考。
1 资料与方法
1.1研究对象 选择2018年1月至2019年6月在西京医院耳鼻咽喉头颈外科行人工耳蜗植入的17例复杂内耳畸形患儿作为研究对象(内耳畸形组)。排除大前庭水管综合征、耳蜗分隔不全2型患儿。所有患儿均为重度或极重度感音神经性聋,均满足2013年人工耳蜗植入工作指南的患儿选择标准[2]。所有患儿均由高年资影像学医师及主刀医师依据影像学表现及临床听力检查结果给予诊断,并参照Sennaroglu内耳畸形分类标准进行分类[3],其中,IP-1畸形2例,IP-3畸形2例,共同腔2例,耳蜗发育不全11例(10例伴蜗神经发育不良,3例合并Charge综合征);双侧植入1例,右侧植入8例,左侧植入8例;植入年龄1~10岁,平均3.49岁;男6例,女11例;耳聋相关基因检测示10例患儿无常见位点已知突变,2例PDS基因突变,CHD7基因突变3例,2例未检测。经圆窗植入电极11例,鼓岬植入4例,2例共同腔畸形经骨性半规管植入。
随机选择同期18例内耳结构正常、年龄、性别、术侧与内耳畸形组无统计学差异的人工耳蜗植入的感音神经性聋患儿作为对照组,其中,双侧植入5例,左例植入3例,右例植入10例,植入年龄0.78~5.82岁,平均2.05岁。两组患儿术前听力无统计学差异。
1.2术前评估 术前听力学检查包括纯音听阈或声场测听及助听听阈、耳声发射、听性脑干反应、40 Hz相关电位和听性稳态反应等。基因筛查包括GJB2、GJB3、PDS基因及线粒体A1555G基因。术前影像学检查包括颞骨薄层断层CT扫描;内听道MRI轴位及斜矢状位平扫,用来评估面听神经发育情况。对患儿均进行言语能力评估、心理健康状态、智力及学习能力评估。
1.3术中评估 调取手术记录及手术录像,记录手术方式及术中并发症,包括乳突切开、上鼓室鼓窦面隐窝开放,人工耳蜗电极植入;脑脊液漏修补术、电极植入位置、面神经走行及术中并发症情况。调取所有患儿手术结束时即时测量相关数据,包括神经遥测反应波形及电阻值情况。
1.4术后随访 统计术后并发症的发生情况,包括皮瓣积液、血肿、继发皮瓣感染坏死等及排异反应、植入体故障、电极位置不佳或移位、面肌痉挛、刺激电极植入错位、脑脊液耳漏、继发性脑膜炎等严重并发症。
所有患儿术后均于西京医院听力中心行人工耳蜗开机和调试,调试时询问患儿家长患儿近期听力表现,术后是否进行规律的康复训练,并评估患儿听觉言语发育情况。开机时间为手术后1个月,并由听力医师评估记录相关指标结果,建立随访档案。人工耳蜗调试时间节点为开机后1、3、6、12个月及以上。
1.5术后听觉言语效果评估 分别于上述时间点进行听觉行为分级标准评分(categories of auditory performance, CAP)[4]、婴幼儿有意义听觉整合量表评分(infant-toddler meaningful auditory integration scale, IT-MAIS)、言语可懂度分级标准(speech intelligibility rating, SIR)[5]和有意义言语使用量表(meaningful use of speech scale, MUSS)评分。CAP评分是检查者根据患儿对测试声音的反应以及家属对患儿日常生活的描述进行评判,分为0~7个等级,用以评估患儿听力发育情况。得分越高,听力越好。为评判更加细致的效果,检查者采用IT-MUSS量表进行评估。同理,对于患儿言语发育情况,采用SIR言语分级和MUSS言语量表进行评估。
1.6统计学方法 采用SPSS 13.0 将IT-MAIS、MUSS评分采用重复测量方差分析,CAP、SIR评分采用Wilcoxon秩和检验、Mann-WhitneyU检验,性别、侧别等构成比资料采用卡方检验。
2 结果
2.1术中及术后并发症情况 复杂内耳畸形组术中发生井喷11例,其中共同腔1例,IP-3畸形2例,IP-1畸形2例,耳蜗发育不全6例;电极不完全植入5例,均为耳蜗发育不全伴蜗神经发育不良患儿。5例患儿术中NRT未引出或波形不佳,其中4例为耳蜗发育不全伴蜗神经发育不良,1例为IP-3畸形。无面神经损伤病例。1例出现术侧皮瓣下积液、血肿,穿刺加压包扎一周治愈。1例共同腔畸形患儿术后半年发生植入体故障,否认头部外伤史,原因不明,取出人工耳蜗,于对侧重新植入。对照组患儿术中提示解剖结构无明显异常,术中无井喷等特殊并发症,术后无皮下积液、植入体感染等并发症发生。
2.2复杂内耳畸形组和对照组言语听觉效果评估结果 17例复杂内耳畸形患儿全部完成术后6个月的随访,13例患儿完成至少1年随访。对照组18例患儿完成术后6个月随访,8例完成术后1年的随访。两组CAP、SIR、IT-MAIS、MUSS评分结果见表1~4。可见,内耳畸形组与对照组术前听力与言语发育无统计学差异。两组CAP、SIR评分在开机后1、3、6个月、1年无统计学差异(P>0.05),IT-MAIS、MUSS在开机后1、3、6个月差异有统计学意义(P<0.05)。1例耳蜗发育不全伴蜗神经发育不全患儿1岁8月龄时植入人工耳蜗,1年后听力无提高,目前该患儿考虑行听觉脑干植入方案,这表明蜗神经发育不良增加了手术预后的不确定性。另1例双侧耳蜗发育不全伴蜗神经发育不良的语前聋患儿(双侧植入),随访中一侧效果不明显,听觉及言语发育由对侧刺激产生。
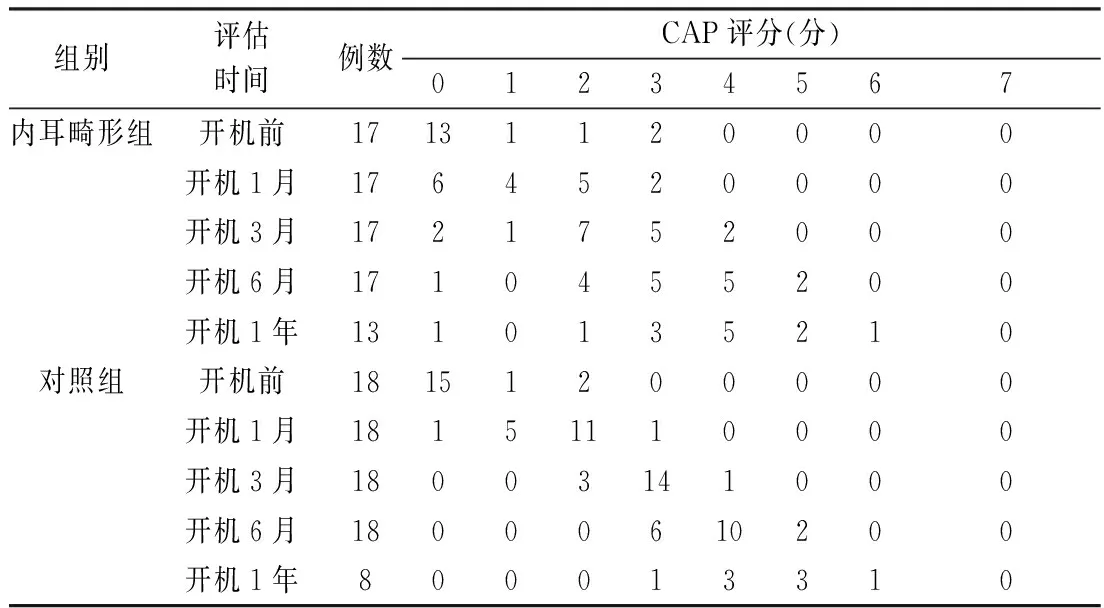
表1 复杂内耳畸形组与对照组CAP不同评分例数分布(例)
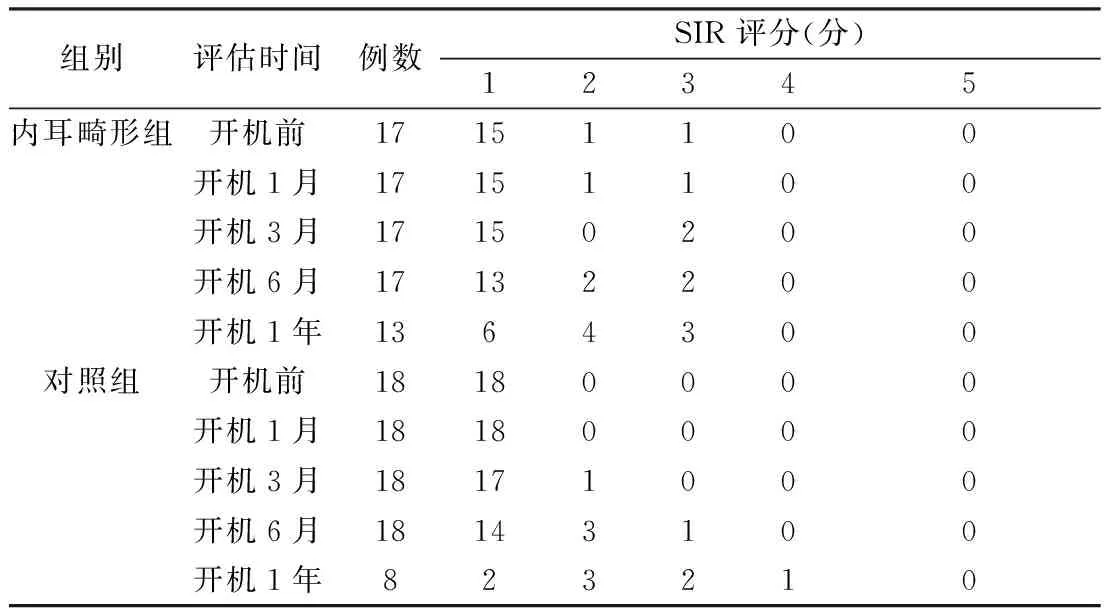
表2 复杂内耳畸形组与对照组SIR不同评分例数分布(例)

表3 复杂内耳畸形组与对照组IT-MAIS评估结果(分,

表4 复杂内耳畸形组与对照组MUSS评估结果(分,
2.3蜗神经发育不良组与对照组听觉言语效果评估结果比较 蜗神经发育不良组10例均完成术后6个月的随访,9例完成开机后1年的随访。开机一年时CAP评分0分1例,2分2例,3分2例,4分4例,5分1例;术后6个月和术后1年比较的P值见表5。蜗神经发育不良组与对照组在开机后6个月、1年CAP评分存在统计学差异(P<0.05),SIR评分无统计学差异(P>0.05)。术后6个月IT-MAIS、MUSS差异有统计学意义(P<0.05)。
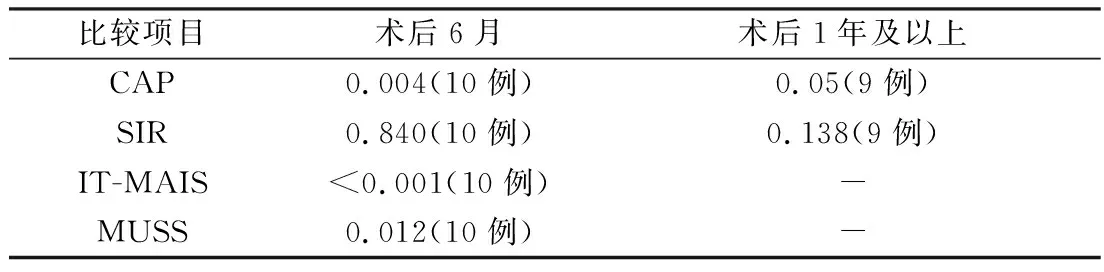
表5 蜗神经发育不良组与对照组CAP、SIR、IT-MAIS、MUSS评估比较的P值
3 讨论
内耳畸形多合并面神经异位、内听道狭窄、蜗神经发育不良,临床表现为伴或不伴全身性综合征的感音神经性聋。相对于内耳结构正常的人工耳蜗植入患儿,内耳畸形的诊断、人工耳蜗植入方式、言语康复及预后判断难度较大[6]。围手术期需考虑多种因素,包括井喷、脑脊液漏的处理,面神经异常走行,手术入路及电极选择,合适的听觉植入装置、适合的手术时机[7]。本研究17例内耳畸形中,畸形部位包含多个解剖结构,并且畸形的解剖结构会出现不同亚型的变异,因此内耳畸形的诊断及鉴别诊断至关重要,术前正确诊断对于人工耳蜗植入效果起关键性作用。
内耳畸形患者人工耳蜗植入中可能发生井喷、面神经损伤、电极不完全植入等手术并发症。Farhood[8]曾对1993~2015年发表的59篇关于内耳畸形人工耳蜗植入并发症的发生率荟萃分析显示,81.8%的病例电极可以完全植入,39.1%术中会发生井喷,34.4%面神经走行异常。
据统计,LVAS患者术中发生井喷概率为33%,复杂的内耳畸形为55%,共同腔畸形为11%;IP-3畸形因为蜗轴和蜗管内间隔完全消失,与内听道的骨性隔板消失,故理论上发生率100%[3,9~11]。本组17例内耳畸形患儿中,11例[IP-3(2/2)、IP-1(2/2)、共同腔(1/2)、耳蜗发育不全(6/12)]发生井喷。其中1例术前伴脑脊液耳漏、无复发性脑膜炎的耳蜗发育不良患儿,当开放面隐窝后大量脑脊液搏动性涌出,术中探查发现圆窗膜破裂,遂行人工耳蜗植入及脑脊液瘘修补,术后1年随访仅有面肌痉挛,无脑膜炎发生,该例患儿开机后1年CAP 4级,SIR2级。这与chen等[12]报道相似,他随访2例伴有脑脊液耳漏、复发性脑膜炎的内耳畸形患儿,开机后1年CAP、SIR评分分别为4分、2分。本组中5例耳蜗发育不全患儿发生电极不完全植入,术后1年随访CAP评分3~5分,平均3.8分。1例共同腔畸形患儿术后半年发生植入体故障,否认头部外伤史,术前CAP为3级,SIR为2级,遂行患侧植入体取出、对侧重新植入,术后随访13个月,CAP达4级水平,SIR为3级。
合并综合征的语前聋患儿需谨慎把握手术适应证,人工耳蜗植入预后与多个因素相关,如植入年龄、听神经发育情况、电极植入时是否折叠、潜在神经系统发育情况[13]。Charge综合征涉及患儿中枢神经系统发育及听力言语发育,预后具有不确定性。李万鑫等[14]随访3例Charge综合征患儿人工耳蜗植入术后3年,一例听力改善,无言语能力,一例无效,一例听力明显提高,言语能力发展良好。本组3例Charge综合征患儿,开机后9个月2例可以分辨言语声,1例仅对言语声作出反应,这3例患儿语言发育较慢,仅能通过手势及简单的词汇进行日常交流。
不同类型的内耳畸形患儿人工耳蜗植入术后疗效不同。Farhood等[8]对Mondini畸形、共同腔畸形、耳蜗发育不全的病例人工耳蜗植入术后效果进行荟萃分析发现,长期效果(随访2年)Mondini畸形患儿术后听觉言语发育效果最好,共同腔和耳蜗发育不全患儿术后效果相当,但次于前者。因为文章异质性较大,并未与内耳结构正常的人工耳蜗植入患儿进行比较。卢星等[15]随访448例患儿人工耳蜗植入术后1年,以CAP、SIR为指标,分析得出大前庭水管综合征及Mondini畸形患儿听觉及言语发育与耳蜗结构正常患儿相当,而共同腔畸形和蜗神经发育不良患儿听力及言语能力较弱。本研究通过开机后1年的随访,发现总体上复杂内耳畸形患儿术后听觉言语能力较术前显著提高,且与内耳结构正常患儿程度相似,但在细节上存在差距。因本研究各种畸形患儿数量有限,故未进行相互比较。Daneshi等[16]对IP-1畸形(19例)、IP-2畸形(31例)、共同腔畸形(17例)、耳蜗发育不全(17例)、LVAS(23例)患儿人工耳蜗植入术后随访2年,认为不同类型的内耳畸形患儿预后相似,CAP评分中位数可达5分,SIR评分可达3分。本组患儿CAP评分介于4~5分,SIR评分介于1~3分,可能是随访时间较短,而言语能力需要长时间的锻炼习得。本研究患儿术前听力无统计学差异,引起大脑皮层听觉反应至少需要5 000个螺旋神经节细胞[17],但人工耳蜗尚可提供足够有效的电刺激[18],因此可以满足听觉形成的条件。一旦听觉传导通路建立,便能形成正反馈使得患儿听力逐渐提高,除非听觉中枢存在病变。
此外,本研究中耳蜗畸形组CAP评分在开机后1、3、6个月与对照组相比均无明显差异,而IT-MAIS评分有统计学差异。Qi 等[19]在比较Mondini畸形与耳蜗结构正常患儿人工耳蜗植入术后在开机后12、24、36个月MUSS、SIR评分发现此现象,但随访至48个月时MUSS和SIR统计学结果一致,其原因可能是IT-MAIS和MUSS更细致地描述了患儿的听力学表现,它包括发声行为、对声音敏感性以及从中提取信息的能力;即便同一听力等级(CAP评分相同)的患儿,他们对声音的反应也不尽相同。由于大部分患儿尚处于语言学习起步阶段,在言语发育方面的差异还需要进一步随访观察。
本研究17例复杂内耳畸形患儿中,10例耳蜗发育不全伴蜗神经发育不良。先天性感音神经性聋约有2%为蜗神经发育不全所致。该10例患儿开机后6个月CAP、IT-MAIS、MUSS评分与对照组有统计学差异(P<0.05),提示伴蜗神经发育不良的内耳畸形患儿人工耳蜗植入术后疗效有限。据报道,合并蜗神经发育不良的内耳畸形患儿术后CAP评分一般不超过5分[20]。本组患儿开机后1年CAP评分在0~5分之间,平均3.2分,中位数4分。人工耳蜗植入疗效在开机半年至1年才初步显现,且听觉神经系统可塑性在3岁左右,此时若发现人工耳蜗对患儿疗效有限,应及时行对侧听觉脑干植入术。Yamazaki等[21]报道19例蜗神经发育不良患儿,CAP评分介于1~6分之间,5例患儿CAP得分5分或6分,并且认为MRI显示前庭蜗神经发育不良且术中EABR未引出波V,可准确判定CAP评分结果差。Bradley 等[22]报道了6例蜗神经发育不良患儿人工耳蜗植入术后随访2~6年的结果,其中5例患儿CAP评分仅2分,1例CAP评分达4分,认为人工耳蜗植入对于伴蜗神经发育不良的先天性聋患儿的获益有限,需谨慎考虑手术适应症。
综上所述,复杂内耳畸形患儿人工耳蜗植入术后听力较术前有所提高,与耳蜗结构正常患儿开机后6个月、1年相比基本相似。但蜗神经发育不良语前聋患儿人工耳蜗植入术后1年听力提高程度低于内耳结构正常的人工耳蜗植入患儿,并且术后效果差异大。人工耳蜗植入对内耳畸形患儿是可以选择的治疗方法,但术前应谨慎把握手术适应症。

