海洋肽对接受手术治疗的胃癌患者营养状况的影响观察*
赵法之,罗进,高勇,何尧,杨超,徐锐,陈小东,赵平
610041成都,四川省肿瘤医院·研究所,四川省癌症防治中心,电子科技大学医学院 胃肠外科中心(赵法之、罗进、杨超、徐锐、陈小东、赵平);628300四川 广元,剑阁县人民医院 普外二科(高勇、何尧)
恶性肿瘤是影响健康、危及生命的重大疾病负担。除肿瘤本身所致不良结局外,与之伴随的不良营养状况亦能够持续影响患者生存质量,并影响抗肿瘤治疗结局[1-2]。胃部肿瘤因其发病部位的特殊性,患者出现的早饱、纳差、呕吐等消化道症状,加剧了胃肿瘤患者的营养状态恶化及营养风险[3-4],并降低了抗肿瘤治疗的耐受性。胃癌的治疗强调以手术为主的综合治疗,而维持围术期患者良好的营养状态对患者手术安全性及术后治疗耐受性的重要意义已为多项研究所证实[5-6]。对于术前存在营养不良的胃癌患者,纠正不良营养状况能够提高患者术后生活质量并促进术后恢复[7-8]。对于术后患者早期的营养支持方式目前仍以肠外营养为主。但随着近年来加速康复外科理念的推广与普及,术前及术后早期经口营养补充在临床实践中逐步开展,安全性及有效性已为临床研究所验证[9-10]。
低聚肽是2~10个氨基酸的寡肽链,是人体吸收利用蛋白质的主要形式[11]。因其易于利用、营养改善速率快的代谢特点,肿瘤患者围术期添加低聚肽作为蛋白补充具有缩短营养支持时间,纠正负氮平衡,改善手术耐受性的优势[12]。低聚肽制剂因其具有吸收、利用迅速的特点,在需手术治疗的胃癌患者中作为营养补充制剂具有一定优势。既往的研究发现,海洋鱼皮水解低聚肽具有抗肿瘤、抗氧化、免疫调节等生理活性,适用于肿瘤患者的临床应用[13]。基于以上研究结果及本中心快速康复理念的开展,我们观察并分析了接受手术治疗的胃癌患者的临床资料,比较围术期添加海洋鱼皮水解低聚肽(以下简称为:海洋肽)对患者术后恢复及术后营养状况的影响。
1 材料与方法
1.1 纳入及排除标准
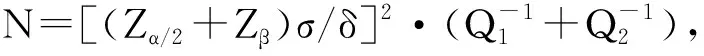
1.2 研究方法
外科治疗:纳入患者依据原发肿瘤部位确定切除范围。切除范围包括远侧胃切除术、全胃切除术或近侧胃切除术。行远侧胃切除及全胃切除手术患者淋巴结清扫范围施行标准D2淋巴结清扫术,近侧胃切除术采用D1+淋巴结清扫术。依据术中操作条件,手术方式采用全腹腔镜手术或开腹辅助腹腔镜手术方式。
1.3 营养治疗
所有患者遵循自身治疗意愿,自主选择是否围术期补充海洋肽制剂,形成观察组与对照组。入院后行营养风险筛查2002 (nutrition risk screening,NRS 2002)评分及主观整体营养状况评估量表(Patient-Generated Subjective Global Assessment,PG-SGA)评分,评估患者是否存在营养风险及合并营养不良状态。对NRS 2002评分≥3分患者和(或)PG-SGA评分≥4分患者入院后由外科医师及营养师共同评估营养支持方案,肠内营养选择口服全营养素整蛋白型营养制剂(安素,美国雅培制药有限公司,400 g/听)。肠内营养提供不足者需考虑肠外营养。患者每天能量需要量按25~35 kcal/kg估算,蛋白质按 0.8~1.5 g/kg 估算。观察组患者术前即开始使用海洋肽制剂(广东中食营科生物科技有限公司,许可证号SC10644190001078),该制剂系海洋鱼皮及鱼肉经蛋白酶解及纯化的肽粉剂,主要成分为海洋鱼皮胶原低聚肽粉(80%),辅料为赤藓糖醇、麦芽糊精、菊粉、柠檬酸钠、柠檬酸、甜菊糖苷,6 g/包。按每次12 g,3次/d剂量添加。对照组患者在保证足够能量及蛋白摄入基础上,不进行海洋肽制剂补充。两组患者术后第1日即开始少量饮水,第2日开始予口服或经营养管管喂全营养素制剂,依据肠道耐受情况控制在250~500 kcal/d。观察组患者术后第2日同时添加海洋肽,每次6 g,2~3次/d,依据肠道耐受情况增加至每次12 g,2~3次/d。对照组患者术后不进行海洋肽制剂补充。
1.4 评价指标
分别记录并比较两组患者术前临床基线资料、营养状态评分、术前及术后7日空腹体重、血红蛋白、血清白蛋白、前白蛋白及转铁蛋白水平。比较两组术后并发症(感染性并发症、吻合口漏、胃瘫、炎性肠梗阻及乳糜漏)发生率。
1.5 统计分析
采用SPSS 19.0版本进行统计检验。正态分布计量资料采用均数±标准差表示。均数的比较采用独立样本t检验,分类变量构成比的比较采用Pearson卡方检验或似然比卡方检验,以双侧P<0.05判断差异具有统计学意义。
2 结 果
2.1 一般资料
共纳入94例患者,其中观察组44例,对照组50例。观察组及对照组在年龄、性别构成、手术方式、入院时BMI指数平均值及BMI过低患者(BMI<18.5)构成比、PGS-GA评分、NRS 2002评分、血清血红蛋白、白蛋白、前白蛋白及转铁蛋白水平比较差异无统计学意义。合并营养风险患者及合并营养不良状态的患者在两组之间构成比差异无统计学意义(表1)。
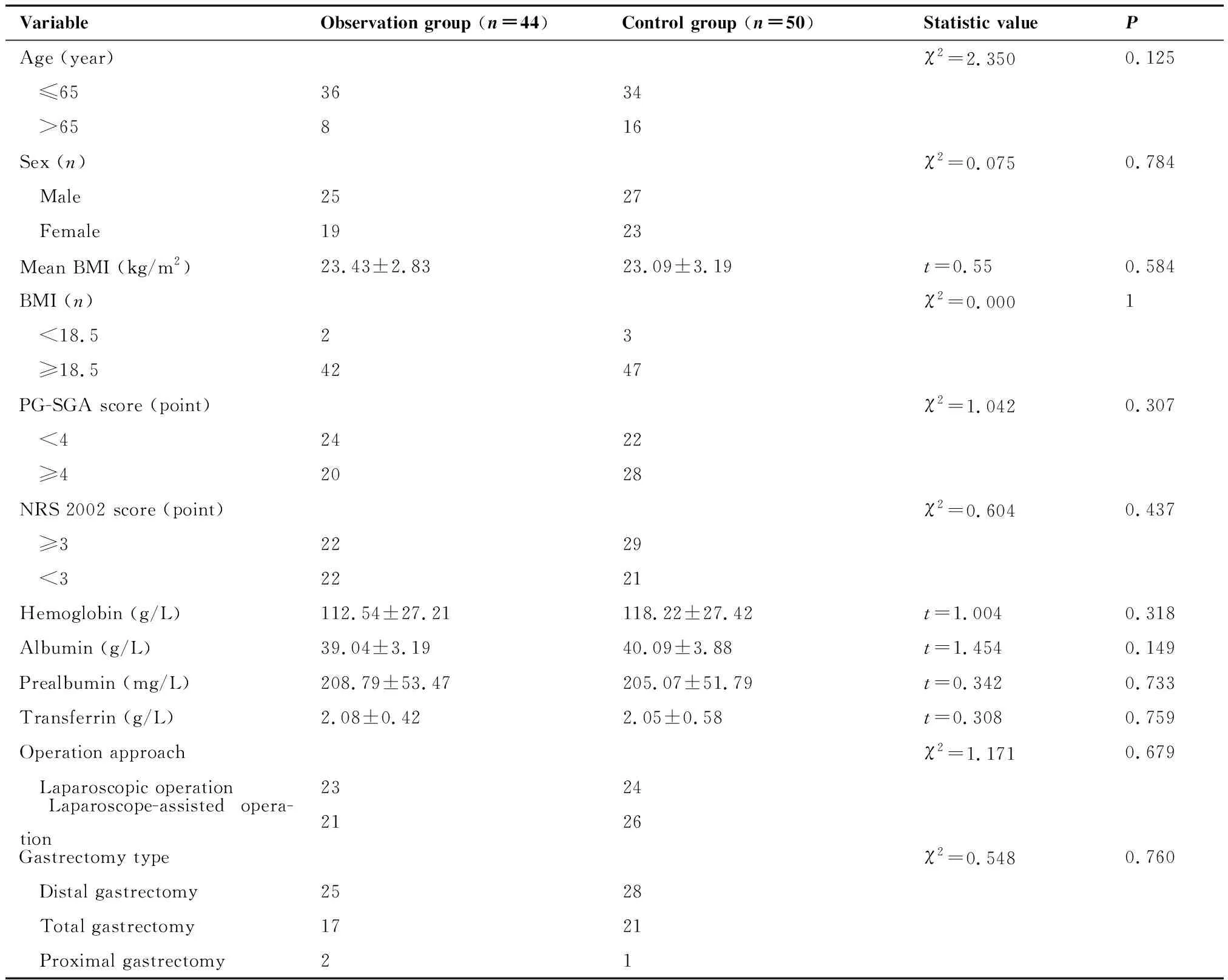
表1 两组患者术前基线临床病理资料比较
2.2 两组术后情况及营养状况比较
术后住院期间观察组共出现术后并发症6例,对照组共出现术后并发症7例,并发症发生率差异无统计学意义(χ2=0.003,P=0.959)。术后一般情况及营养状态相关观察指标的比较中,观察组较对照组患者术后肛门排气时间有缩短趋势, 但差异无统计学意义(P=0.162)。两组患者术后7日体重、血红蛋白、白蛋白、前白蛋白及转铁蛋白水平均较术前水平有下降(P<0.05)。组间比较体重、血红蛋白、白蛋白、前白蛋白及转铁蛋白水平在手术前后的变化值,观察组术后7日前白蛋白下降水平较对照组少(P=0.043),差异有统计学意义。其余血液学指标变化值在两组间差异无统计学意义。两组术后恢复及营养状况资料比较见表2。
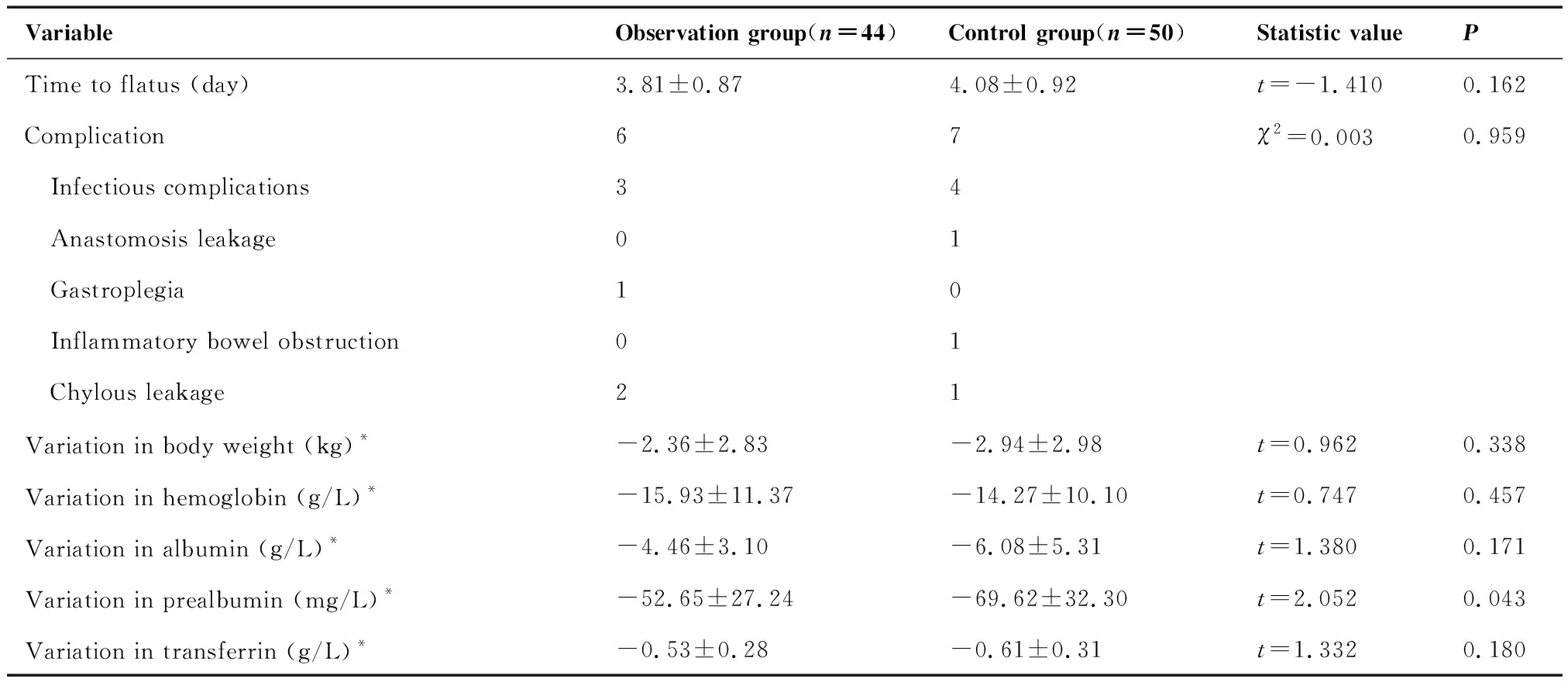
表2 两组患者术后恢复及营养状况资料比较
2.3 不良反应
本研究纳入的患者中有10例(观察组6例,对照组4例)出现消化不良、排气增多症状,两组间差异无统计学意义(P=0.583)。均通过蒙脱石散、肠道菌群制剂等对症治疗获得症状缓解,继续营养支持治疗。
3 讨 论
胃癌患者术后因受消化道重建、麻醉及胃肠神经—体液功能恢复等因素影响,术后短期需行肠外营养支持,其作为常规治疗模式的价值已为临床研究所证实[10]。肠内营养支持的恢复则依赖于牢靠的消化道外科重建以及胃肠道生理功能的恢复,加速康复外科理念在此基础上得到了推广应用。研究证实早期经口或管饲给予肠内营养,能够促进患者术后胃肠功能及机体营养状态恢复,有助胃肠蠕动恢复、缩短住院时间[5,9,15-16]。本研究中仅1例对照组患者术后因出现吻合口漏而停用肠内营养,其余患者均完成肠内营养支持至出院,显示术后早期肠内营养治疗安全可行,这与目前普遍观点一致。
胃癌患者围术期营养支持策略需满足基础营养需求并于术后开始复合营养支持,即于术前及术后分别进行评估,并及时进行营养干预。术前不良的营养状态会增加术后消化道漏等不良外科结局的发生[17]。相应的,术前的营养支持能维持患者营养状态及免疫功能,缩短住院时间,促进术后恢复[18]。这种在手术等待期即给予患者以蛋白质为主的营养补充等策略,形成“预康复”的营养支持理念,能为患者带来临床获益[19]。基于这种围术期管理模式,我们对观察组及对照组中营养摄入不足的患者均采用了术前营养补充并联合常规术后营养的治疗方案,以满足围术期生理状态热量及蛋白质营养需求,同时对观察组患者进行额外海洋肽制剂的摄入以真实反映海洋肽制剂对于术后恢复及营养相关指标的影响。在营养治疗方案中为满足肿瘤患者整体营养状态的维持,对于营养素的补充尤其强调蛋白性营养的足量摄入。对经手术治疗的患者,围术期蛋白性营养物质的补充应满足机体100%的需求[20]。除肿瘤所致负氮平衡以外,手术等急性应激条件更易造成短期内机体蛋白质营养迅速消耗,导致术后低蛋白状态。短链肽类相较整蛋白补充,更易被机体吸收、利用,直接合成蛋白质,维持患者术后蛋白水平[21-22]。本研究比较两组患者围术期体重及白蛋白在手术前后差值虽差异无统计学意义,但术后前白蛋白下降程度观察组较对照组差异有统计学意义,观察组术后前白蛋白水平下降幅度小,更接近术前水平,提示低聚肽成分对术后不良应激及负氮平衡的纠正可能具有优势。前白蛋白为肝脏合成的急性时相蛋白,其半衰期仅12 h,主要承担组织修补材料及转运蛋白的生理作用。其在恶性肿瘤、手术创伤等条件下大量消耗。多项研究表明术后前白蛋白水平低下与感染、胃肠功能恢复延迟有关[23-24]。胃肠道肿瘤患者术后早期行肠内免疫营养治疗,有助于提高患者血清前白蛋白水平[25]。既往在食管癌及肝癌患者的研究中也发现添加海洋肽制剂能提高患者术后血清蛋白水平[12,26]。结合既往文献及我们的研究结果,可以认为围术期应用海洋肽制剂有助于提高胃癌患者术后前白蛋白水平,推测与其分子量小、机体吸收利用迅速等生理特性有关。本研究中观察组患者术后肛门排气时间较对照组有缩短趋势,亦提示海洋肽对肠蠕动及肠功能恢复具有促进作用。由于这种缩短术后排气、排便时间的作用在不添加海洋肽制剂的常规加速康复外科管理患者中也可被观察到[27],因此这种促进胃肠功能恢复的效应可能来源于肠内营养途径对消化道功能的刺激调节,而不仅限于海洋肽成分的生物效应。具体机制尚需进一步的研究加以证实。术后肠内营养干预宜采用与肠功能逐步适应的进食成分,根据患者消化道症状与肠道功能耐受性调整方案 。本研究观察组患者普遍对低聚肽耐受良好,少数患者出现口服困难、腹部不适、腹泻等症状,因肽类制品及溶液具有特殊口感及气味,推测可能与其口感及肠功能不适有关。既往对海洋肽应用的报道中虽有患者出现腹泻等症状,但较常规肠内营养治疗腹泻的发生率并未明显增加[12]。表明海洋肽制剂在样本人群有较好的耐受性。腹泻、腹胀及呕吐等消化道反应属肠内营养常见的并发症。控制营养补充的量及输注速度、调整营养制剂成分配伍、使用调理胃肠活动的药物及热敷、针灸辅助治疗等措施可作为解决对策[28]。
综上所述,本研究表明胃癌手术患者围术期添加海洋肽制剂有助于患者代谢的维持及胃肠功能恢复,符合现代快速康复外科理念的应用与实践,是一种潜在安全、有效的围术期营养治疗方案。海洋肽制剂对胃癌患者的临床价值有待进一步研究探寻。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

