胰腺神经内分泌瘤的MRI征象对术前病理分级的应用价值*
温志鹏,陈晓丽,罗红兵,任静
610041成都, 四川省肿瘤医院·研究所,四川省癌症防治中心,电子科技大学医学院 影像诊治中心
起源于肽能神经元和神经内分泌细胞的胰腺神经内分泌瘤(pancreatic neuroendocrine tumors,PNETs)[1],是一种胰腺罕见肿瘤,普通人群发病率小于2/10万[2-3];近十年来由于影像检查及诊断技术的不断提高,PNETs的检出率呈逐渐上升的趋势[4-5]。国际癌症研究机构(International Agency for Research on Cancer,IARC)在世界卫生组织(World Health Organization,WHO)肿瘤分类小组支持下,于2017年11月召开了神经内分泌肿瘤(neuroendocrine neoplasm,NENs)分类共识会议,最终提出了“2018 IARC/WHO 共同分类框架”,对分化好的神经内分泌瘤(neuroendocrine tumors,NETs)及分化差的神经内分泌癌(neuroendocrine carcinomas,NECs)进行区分:PNETs根据有丝分裂计数及Ki-67标记指数分为三级(G1-3);而胰腺神经内分泌癌(pancreatic NECs,PNECs)不再进行明确分级,统一认定为高级别,明确具有高级别恶性组织学和生物学行为[6-8]。
在临床治疗手段上,分化程度较好的G1-2级PNETs,即使出现局部转移,首选治疗方案仍为手术切除; G3级却需要全身化疗,且5年生存率差异巨大[9-10]。病理穿刺活检作为临床常用的诊断方式,由于取材的局限性,所取标本的Ki-67指数可能与大体产生偏差[11-13],因此影像学诊断能够有效地协助PNETs进行术前分级。但以往PNETs的影像学研究,大部分都以2010 WHO分类标准对胰腺神经内分泌肿瘤(pancreatic neuroendocrine neoplasm,PNENs)进行术前分级[2,14-17];因此,本研究希望通过回顾性分析按照2018 IARC/WHO 共同分类框架标准进行术后病理分级的PNETs患者MRI影像学资料,评估MRI及弥散加权成像(diffusion-weighted imaging,DWI)检查对于PNETs术前分级的应用价值。
1 资料与方法
1.1 一般资料
回顾性分析2018年1月至2019年8月在本院就诊并手术确诊的PNETs患者,选取符合以下标准的患者。纳入标准:1)患者术前在我院行MRI平扫、三期增强扫描及DWI检查,图像质量好、病灶显示清晰;2)所有患者MRI检查前未进行过任何相关治疗;3)所有患者术后病理按照2018 IARC/WHO 共同分类框架标准确诊为PNETs并进行病理分级。排除标准:1)术前进行了肿瘤相关治疗;2)患者憋气不佳、运动伪影重,图像质量差,病灶显示不清;3)对比剂过敏或肾功能不全,无法坚持完成检查者。
最终共有38例PNETs患者达到标准,纳入研究,男20例,女18例,均为胰腺单发肿瘤;年龄41~73岁,平均年龄(53.58±10.02)岁;MRI检查与手术间隔不超过2周。
1.2 MRI检查方法
选择西门子公司3.0T超导磁共振扫描仪,所有患者检查前禁食禁饮8 h,行MRI平扫、三期增强扫描及DWI检查,层厚5 mm,层距1 mm。扫描序列如下:常规T1WI、T2WI序列;脂肪抑制T1WI、T2WI序列;增强扫描前行弥散加权序列扫描,b值分别为0、30、50、150、600、800 s/mm2,获得DWI及表观扩散系数(apparent diffusion coefficient,ADC)图像;增强扫描,使用Gd-DTPA,用量为0.1 mmol/kg,经静脉注射,注射后20 s、60 s、120 s采集图像,分别取得动脉期、门脉期及延迟期图像[2,17]。
1.3 图像分析
两名腹部MR诊断经验丰富的放射科医师(一名主治医师,一名副主任医师),在知晓患者为PNETs、但不知晓术后病理分级的情况下,对所有患者MRI图像进行阅片,有分歧者协商达成一致。分析的主要影像学征象包括:1)瘤体位置:胰腺头颈、体、尾部;2)有无囊变坏死;3)瘤径:(最大层面长径+短径)÷2;4)肿瘤形态是否规则;5)肿瘤边界是否清晰;6)有无主胰管扩张;7)有无转移;8)动脉期、门脉期及延迟期强化方式:与邻近正常胰腺组织相比,表现为低、等、高信号;9)DWI数据分析:在b值=800 s/mm2的图像上,避开瘤体坏死、囊变及钙化区域,选取感兴趣区(region of interest,ROI),计算平均ADC值[18]。
1.4 病理分级
采用“2018 IARC/WHO 共同分类框架”关于PNETs的病理分级标准对术后肿块进行准确病理分级[7-8]。
1.5 统计学分析
根据临床治疗手段及肿瘤预后的差异[9-10],主要对比G1-2级与G3级之间的统计学差异;采用SPSS 20.0软件:MRI征象(包括肿瘤位置、有无囊变坏死、肿瘤形态是否规则、边界是否清晰、有无主胰管扩张、有无转移、增强后各期强化方式)等级资料采用百分比及频数表示,运用Kruskal-Wallis 秩和检验方法进行分析;瘤径及不同病理级别的ADC值计量资料用(均数±标准差)表示,差异采用t检验两两对比;P<0.05视为差异具有统计学意义。
2 结 果
2.1 一般结果
经术后病理确诊的PNETs患者共38例,其中:1)G1级4例,均为男性,年龄49~62岁,平均年龄(51.75±7.97)岁;2)G2级20例,男性8例,女性12例,年龄43~70岁,平均年龄(54.25±9.58)岁;3)G3级14例,男性8例,女性6例,年龄41~73岁,平均年龄(51.71±10.18)岁。统计结果见表1。
对比G1-2级与G3级的一般情况,统计学结果分析表明G1-2级与G3级PNETs患者间的性别及年龄差异均没有统计学意义(P>0.05)。
2.2 不同病理分级PNETs的MRI图像一般特征分析
分析的一般影像学征象包括:1)瘤体位置:胰腺头颈、体、尾部;2)有无囊变坏死;3)瘤径(cm):(最大层面长径+短径)÷2;4)肿瘤形态是否规则;5)肿瘤边界是否清晰;6)有无主胰管扩张;7)有无转移。统计结果见表2。
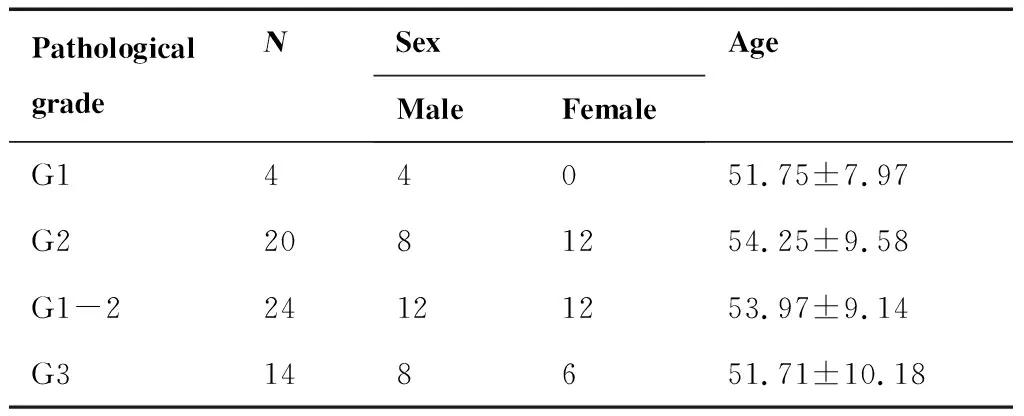
表1 G1-3级PNETs患者一般情况统计

表2 G1-3级PNETs患者MRI图像分析(一般特征)
对比G1-2级与G3级PNETs间的MRI图像一般特征:1)G1-2级患者瘤体位置大部分位于胰腺头颈部(75%),而G3级患者瘤体大部分位于胰腺尾部(71.4%),统计学分析提示两者间差异有统计学意义(P=0.002);2)G1-2级患者的肿瘤囊变坏死率(58.3%)低于G3级PNETs患者(85.7%),但两组间差异无统计学意义(P=0.084);3)在瘤径上,G1-2级(3.44±1.32)cm及G3级(5.97±2.37)cm间差异有统计学意义(P=0.010);4)G1-2级患者肿瘤形态较大部分是规则的(67.0%),而G3级PNETs患者肿瘤形态均不规则(100%),统计学分析提示两者间差异有统计学意义(P<0.001);5)G1-2级PNETs患者肿瘤边界大部分清晰(75.0%),而G3级PNETs患者肿瘤边界大部分不清晰(85.7%),两组间差异有统计学意义(P<0.001);6)在主胰管扩张上,G1-2级者占比较多(25%),G3级占比较少(14.3%);7cm大部分G3级患者伴有转移(85.7%),而G1-2级转移者很少(8.3%),两组间差异有统计学意义(P<0.001);且G3级患者的所有转移灶均位于肝脏。
2.3 不同病理分级PNETs的MRI图像强化特征及DWI分析
分析的MRI图像强化特征及DWI征象包括:1)动脉期、门脉期及延迟期强化方式:与邻近正常胰腺组织相比,表现为低、等、高信号;2)DWI数据分析:在b值=800 s/mm2的图像上,避开瘤体坏死、囊变及钙化区域,选取ROI,计算平均ADC值。统计结果见表3。
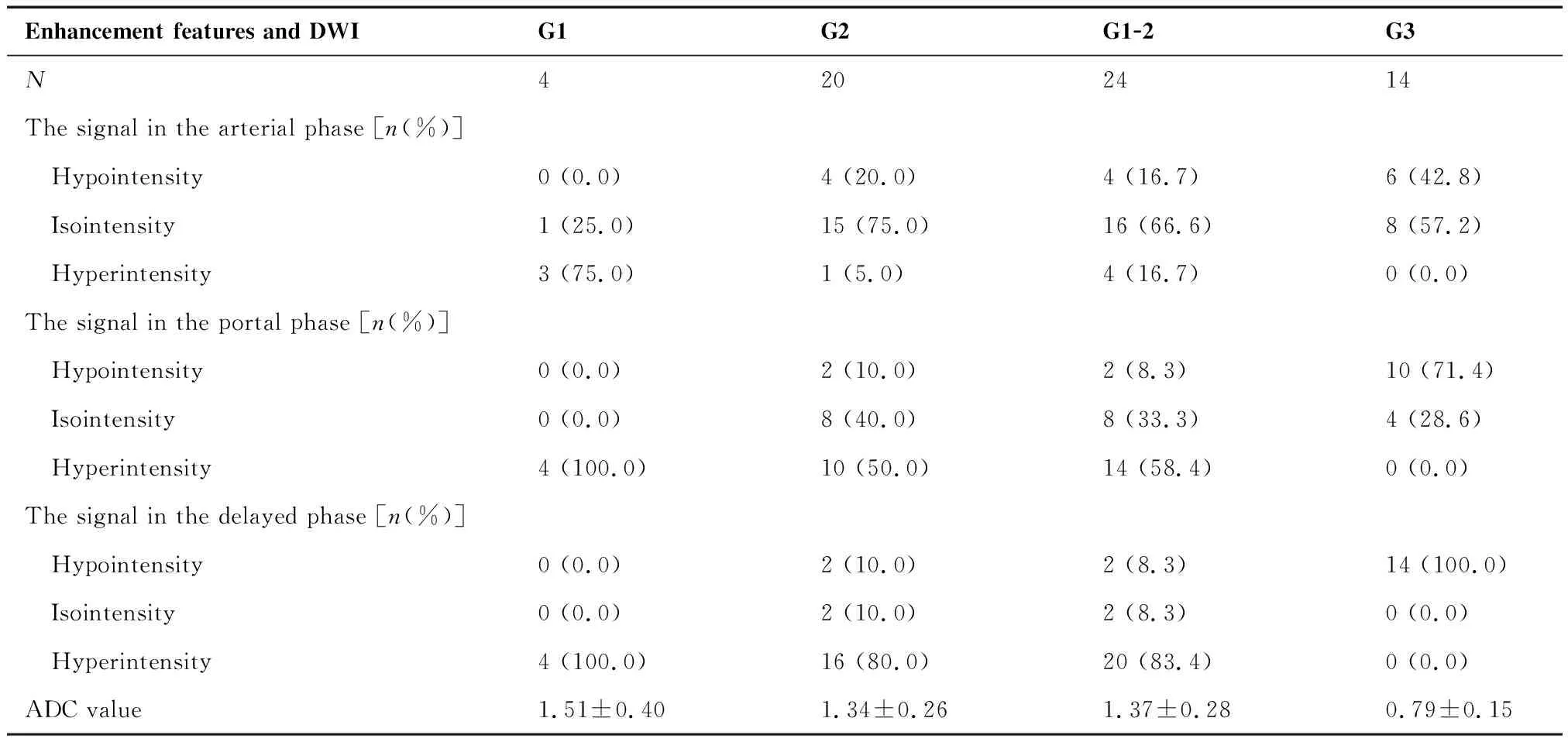
表3 G1-3级PNETs患者MRI图像分析(强化特征及DWI)
对比G1-2级与G3级PNETs间的MRI图像强化特征及DWI:1)G1-2级瘤体,动脉期部分为低信号(16.7%)、大部分为等信号(66.6%)、部分为高信号(16.7%);G3级瘤体,动脉期部分呈低信号(42.8%),部分呈等信号(57.2%),动脉期两组间信号差异有统计学意义(P=0.033);2)G1-2级瘤体,门脉期低、等信号者减少(分别占比8.3%、33.3%),高信号者增多(58.4%);G3级瘤体,门脉期低信号者增加(71.4%),等信号者减少(18.6%),两组间信号差异有统计学意义(P<0.001);3)G1-2级瘤体至延迟期呈低信号者同门脉期(8.3%),等信号者进一步减少(8.3%),大部分瘤体呈高信号(83.4%);而G3级瘤体延迟期均呈低信号,与G1-2组差异有统计学意义(P<0.001);4)G1与G2组PNETs患者MRI图像的ADC值差异无统计学意义(P=0.237);G1-2与G3级PNETs患者MRI图像的ADC值差异有统计学意义(P=0.030)。
3 讨 论
“2018 IARC/WHO 共同分类框架”对PNETs及PNECs进行了区分[7-8]。不同分级PNETs间的首选治疗方案及5年生存率差异巨大[9-10],且以往对于PNETs的研究,大部分侧重于运用CT、少有的运用MRI者也都是以2010 WHO分类标准对PNENs进行术前分级[2,13-17];因此,本研究希望通过回顾性分析按照2018 IARC/WHO 共同分类框架标准术后病理确诊的PNETs患者MRI影像学资料,评估MRI及DWI检查对于PNETs术前分级的应用价值。
本研究结果表明,G1-2级与G3级PNETs患者间的性别及年龄差异均没有统计学意义(P>0.05),与Lotfalizadeh等[2]的研究结果一致。
对于MRI图像一般特征的分析提示:1)在瘤体位置上,G1-2与G3组两者间差异有统计学意义(P=0.002);总共38例中,22例位于胰腺头颈部(57.9%),16例位于胰腺体尾部(42.1%),这与部分文献结果[17]存在差异,可能是由于G1组样本量过少导致的;2)肿瘤囊变坏死率,两组间差异无统计学意义(P=0.084);3)G1-2及G3级间在瘤径上差异有统计学意义(P=0.010),这一结果与国内外研究结果是一致的[2,19];4)在瘤体形态及边界上,G1-2级大部分规则、边界清晰,而G3级均不规则、边界大部分不清晰,统计学分析提示两者间差异有统计学意义(P<0.001),说明肿瘤级别升高、恶性程度上升、细胞增殖加快,瘤体形态变得更不规则、边界也更模糊;5)部分研究[2,17,20]表明胰管扩张在不同分级间差异无统计学意义,本次研究G1-2级瘤体多位于胰腺头颈部,因此G1-2级中主胰管扩张比例较多,而G3级较少;6)G3级患者大部分伴有转移,而G1-2级转移者极少,两组间差异有统计学意义(P<0.001);且本次研究中所有转移灶均位于肝脏,与文献描述一致[21-22]。
对比G1-2及G3级PNETs间的MRI图像强化方式,本研究发现: 1)G1-2级瘤体在动脉期低、等、高信号均有分布,G3级瘤体均为等低信号;2)随着静脉注射Gd-DTPA后时间的推移,G1-2级瘤体等低信号者逐渐减少,大部分瘤体在延迟期呈高信号(83.4%);而G3级瘤体低信号者逐渐增加,至延迟期均呈低信号。这些结果都表明G1-2与G3级PNETs间的MRI强化方式差异是有统计学意义的,肿瘤等级越高,瘤体信号强度从动脉期至延迟期呈减低的趋势,这与国内外大部分文献结果是一致的[2,23-24]。
作为MR检查中一种常用的功能成像序列,DWI能够反映水分子在瘤体中的扩散程度,肿瘤恶性程度越高,ADC值越低。对比G1与G2组PNETs患者瘤体的ADC值,虽然G2级相对于G1级均值稍低,但统计学分析提示两组间差异没有统计学意义(P=0.237);而G1-2级与G3级的ADC值差异有统计学意义(P=0.030),说明G3级PNETs恶性程度更高、水分子运动受限更明显,与文献报道基本一致[2,18]。
综上所述,不同病理分级PNETs的MRI及DWI影像具有一定的特征性,MRI及DWI检查对于PNETs术前分级具有指导价值,瘤径大、瘤体形态不规则、边界模糊、伴有转移、延迟期低信号及ADC值低均有助于高级别PNETs的诊断。当然,由于本研究属于回顾性研究,也有可能出现选择偏倚。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

