合并多支血管病变的ST段抬高型心肌梗死非罪犯血管行经皮冠状动脉介入治疗的最佳时机及其对患者预后的影响
徐艺芮 王怀根 梁焱娇 王东琦
急诊行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)开通ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)患者罪犯血管可以减少梗死面积,降低心力衰竭、心原性休克及恶性心律失常的发生率,并降低病死率[1-3]。研究发现,接近50%的STEMI患者合并多支血管病变(multivessel disease,MVD)[4]。MVD是导致这类患者预后不良的重要因素,能明显增加心肌梗死复发率及PCI术后短期死亡率[4-5]。目前,对于STEMI合并MVD患者的介入治疗主要有三种手术策略:即刻完全血运重建(immediately complete revascularization,ICR)、分期完全血运重建(staged complete revascularization,SCR)和仅行罪犯血管血运重建(culprit-only revascularization,COR)。当前的指南对于STEMI合并MVD患者除了合并心原性休克建议行ICR以外,对于血流动力学稳定的患者并不推荐行ICR[2,6]。2015年美国心脏病学会、美国心脏协会与美国心血管影像和介入学会的STEMI患者PCI指南[6]指出,对于部分血流动力学稳定的MVD患者,可在处理罪犯血管的同时,对非梗死相关血管进行干预(Ⅱb类推荐)。2017年欧洲心脏病学会急性STEMI患者管理指南[2]规定非罪犯血管的处理方案为:存在MVD的STEMI患者在出院前可对非罪犯血管进行常规血运重建(Ⅱb类推荐)。而2015年和2019年中华医学会心血管病学分会急性STEMI诊断和治疗指南[3,7]均不推荐对血流动力学稳定患者的非罪犯血管进行急诊PCI。
目前,对STEMI合并MVD的患者进行完全血运重建已基本达成共识,但是对于选择ICR还是SCR,以及对SCR策略中非罪犯血管干预的最佳时机的研究较少,结论也不尽一致[8-11]。Lee等[8]的研究指出,应在3周至1年内对非罪犯血管进行血运重建。Zhao等[9]根据首次和分期PCI之间的时间间隔,将患者分为3组(首次PCI后1周、1~2周、2~12周)。结果发现,在2周内行非罪犯血管完全血运重建与2周后相比能明显降低主要不良心脑血管事件(major adverse cardiac and cerebrovascular events,MACCE)发生率(23.0%比33.0%比40.0%,P=0.001),这一优势主要体现在较少的再次血运重建上。本研究对应用SCR策略的STEMI合并MVD患者进行随访,比较不同时期处理非罪犯血管患者的MACCE及全因死亡的发生率,从而评估不同手术时机对于患者预后的影响。
1 对象与方法
1. 1 研究对象
连续性收集2015年1月至2018年12月就诊于西安交通大学第一附属医院心脏重症监护室的STEMI合并MVD行急诊PCI术开通罪犯血管并分期开通非罪犯血管的患者共367例。STEMI的诊断依据患者的临床症状、心肌损伤标志物及12导联体表心电图。对病变血管的定义:主要冠状动脉或其主要分支狭窄程度≥50%。MVD是指左前降支、左回旋支、右冠状动脉或其主要分支至少存在两支≥50%狭窄的病变,其中左主干受累统一视为MVD。所有患者在入院后进行标准的双联抗血小板治疗并在12 h内行急诊PCI术开通罪犯血管,根据患者具体情况分期开通非罪犯血管。排除单支病变、未行急诊手术或未行SCR干预非罪犯血管的患者,同时排除预期寿命较短的患者。
1. 2 研究方法
临床基线资料、实验室检查及造影结果均通过医院电子病历系统获取,患者出院后服药及其他情况通过检索电子病历、门诊以及电话随访获得,所有患者的随访于2019年6月至7月完成。共有1486例急性STEMI患者于2015年1月1日至2018年12月31日入住西安交通大学第一附属医院心脏重症监护室接受急诊PCI术,排除不符合入组条件的患者,包括单支血管病变(420例)、急诊PCI术未成功(12例)、在院死亡或预期寿命小于1年(16例)、行ICR(25例)、未在30 d内干预非罪犯血管(633例)、资料丢失或失访(13例),最终共入选367例STEMI合并MVD患者。根据非罪犯血管的干预时机,将患者分为组1(1~3 d内干预非罪犯血管,138例)、组2(3~7 d内干预非罪犯血管,173例)和组3(7~30 d 内干预非罪犯血管,56例)。
本研究的主要终点为在中位数22(10,37)个月的随访期内患者的全因死亡及MACCE发生率,次要研究终点为MACCE的各个独立事件。MACCE包括心原性死亡、非致死性心肌梗死、再次血运重建、卒中及因心力衰竭或心绞痛再入院。其中再次血运重建包括靶病变再次血运重建、靶血管再次血运重建及非靶血管血运重建。
1. 3 统计学分析
本研究数据均使用IBM SPSS 24.0进行统计分析。对于连续型资料:若服从正态分布,使用(±s)进行统计描述,采用单因素方差分析(oneway ANOVA)进行组间比较,如果组间差异有统计学意义,进一步采用SNK方法进行两两比较;若不服从正态分布,使用中位数及四分位数间距进行统计描述,组间比较采用Kruskal-Wallis H检验。无序分类资料比较采用χ2检验。等级资料比较采用Kruskal-Wallis H检验。采用Kaplan-Meier法对生存资料进行描述,并采用log-rank检验对生存曲线进行比较。采用Cox单因素回归对MACCE的危险因素进行初筛,变量筛选的检验水准设为α=0.15,最后把年龄、肾小球滤过率、进门至球囊扩张(door to balloon,D2B)时间、左心室射血分数、是否三支血管病变及SCR时间纳入Cox多因素回归,结果报告为HR以及HR的95%可信区间。以P<0.05为差异有统计学意义。所有检验均为双侧检验。
2 结果
2. 1 基线特征
对患者的基线资料分析显示,三组患者吸烟比例(58.7%比69.4%比53.6%,P=0.044)、D2B时间[65(51,84)min比75(59,97)min比74(59,91)min,P=0.003]、三酰甘油[(1.62±0.09)mg/dl 比(1.52±0.09)mg/dl比(1.78±0.12)mg/dl,P=0.047]、同型半胱氨酸[22.75(16.20,32.60)μmol/L比18.80(13.75,29.60)μmol/L比16.45(12.55,32.00)μmol/L,P=0.034]、冠状动脉三支血管病变比例(48.6%比57.2%比75.0%,P=0.003)、非罪犯血管置入支架数[(1.49±0.06)枚比(1.61±0.07)枚比(1.89±0.13)枚,P=0.023]、非罪犯血管置入支架总长度[(38.36±1.80)mm比(40.28±1.68)mm比(48.91±3.70)mm,P=0.038]比较,差异均有统计学意义。三组其余指标比较差异均无统计学意义(均P>0.05)。患者的基线资料、实验室检查、冠状动脉造影及PCI手术结果、术后服药情况见表1~4。

表1 三组患者基本临床特征比较
2. 2 临床结局事件
2. 2. 1 MACCE 在22(10,37)个月的随访期间,组1有36例(26.09%)发生MACCE,组2有40例(23.12%)发生MACCE,组3有24例(42.86%)发生MACCE。在MACCE的发生率上,组1与组2比较差异无统计学意义(HR 1.20,95%CI 0.76~1.89,P=0.42),而组3的发生率高于组1和组2(HR 1.94,95%CI 1.08~3.46,P=0.01;HR 2.28,95%CI 1.25~4.16,P<0.001)。三组之间的累积无MACCE生存曲线(Kaplan-Meier法)显示,三组患者的无MACCE生存率差异有统计学意义(P=0.003)。三组患者随访期间无MACCE的生存曲线见图1。

图1 三组患者无MACCE的K-M生存曲线
2. 2. 2 全因死亡 在22(10,37)个月的随访期间,组1中12例(8.70%)、组2中11例(6.36%)、组3中3例(5.36%)发生全因死亡。三组之间累积无全因死亡的生存曲线显示,三组患者全因死亡发生率比较差异无统计学意义(P=0.61),三组患者随访期间全因死亡的生存曲线见图2。

图2 三组患者全因死亡的K-M生存曲线

表2 三组患者实验室检查指标比较
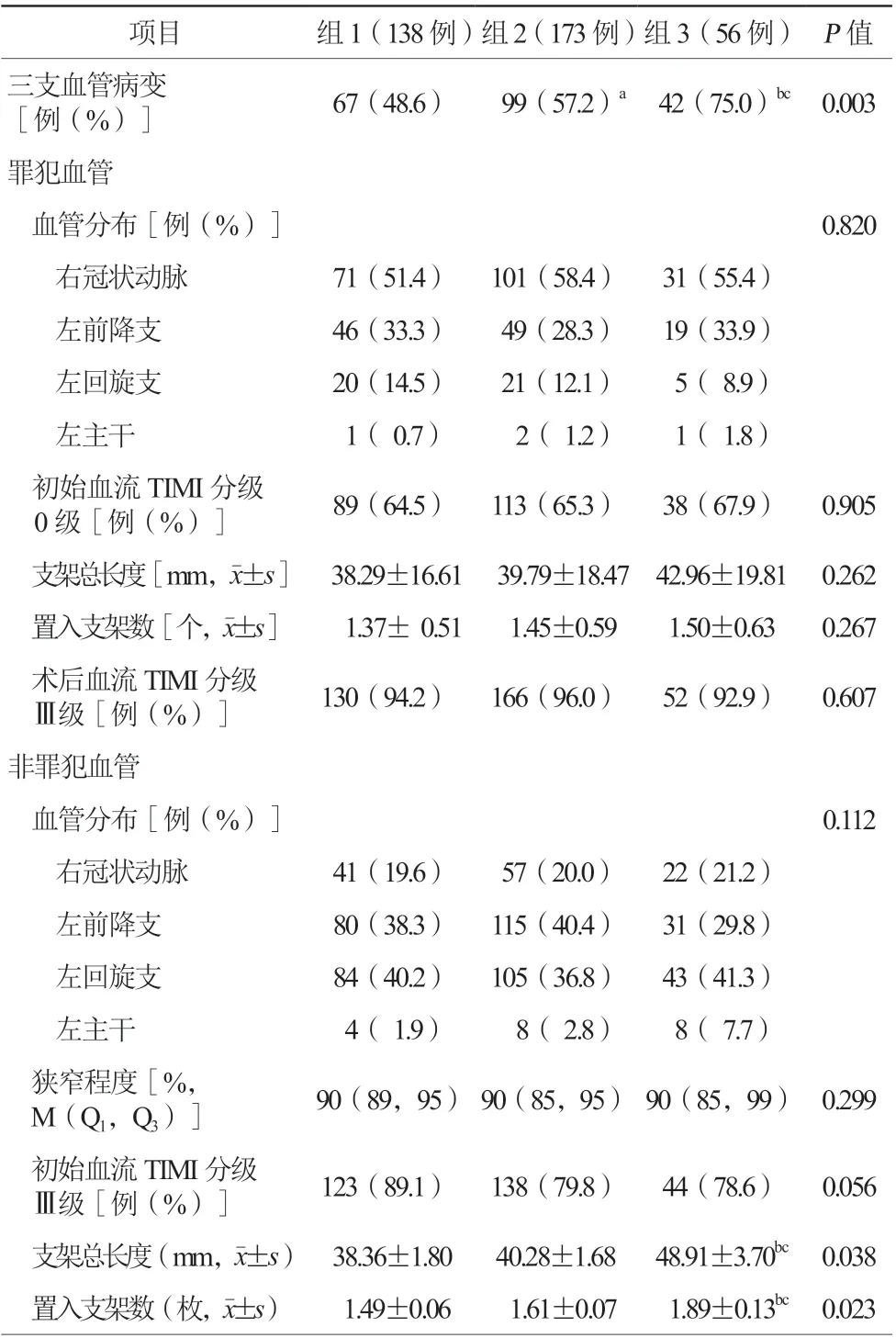
表3 三组患者造影及手术结果比较
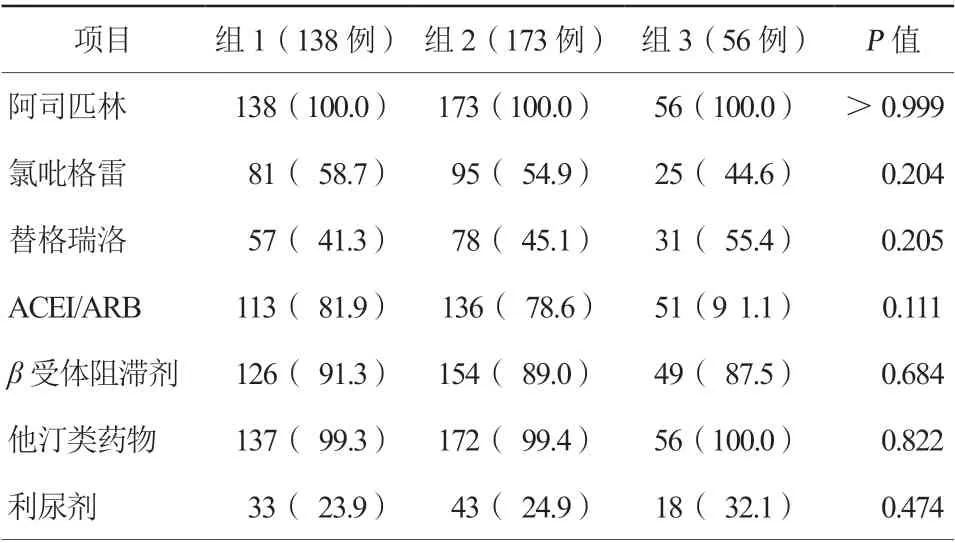
表4 三组患者术后服用药物情况比较[例(%)]
2. 2. 3 次要终点 三组患者随访期间的次要终点事件见表5。三组患者血运重建发生率(5.07%比6.36%比19.64%,P<0.001,表5及图3 A)、因心力衰竭或心绞痛再入院发生率(14.49%比13.87%比30.36%,P=0.003,表5及图3 B)比较,差异均有统计学意义。进一步进行组间比较发现,在再次血运重建发生率上,组3明显高于组1和组2(HR 4.22,95%CI 1.35~13.24,P=0.001;HR 3.49,95%CI 1.16~10.55,P=0.001),差异有统计学意义;组1和组2比较差异无统计学意义(HR 0.83,95%CI 0.37~1.82,P=0.719)。同样,在因心力衰竭或心绞痛再次入院的发生率上,组3高于组1和组2(HR 2.48,95%CI 1.11~5.54,P=0.004;HR 2.65,95%CI 1.21~5.80,P=0.002),组1和组2比较差异无统计学意义(HR 1.07,95%CI 0.62~1.84,P=0.791)。三组患者心原性死亡(3.62%比3.47%比1.79%,P=0.822)、卒中(1.45%比2.31%比3.57%,P=0.614)、非致死性心肌梗死(2.90%比2.31%比7.14%,P=0.172)发生率比较,差异均无统计学意义(表5)。
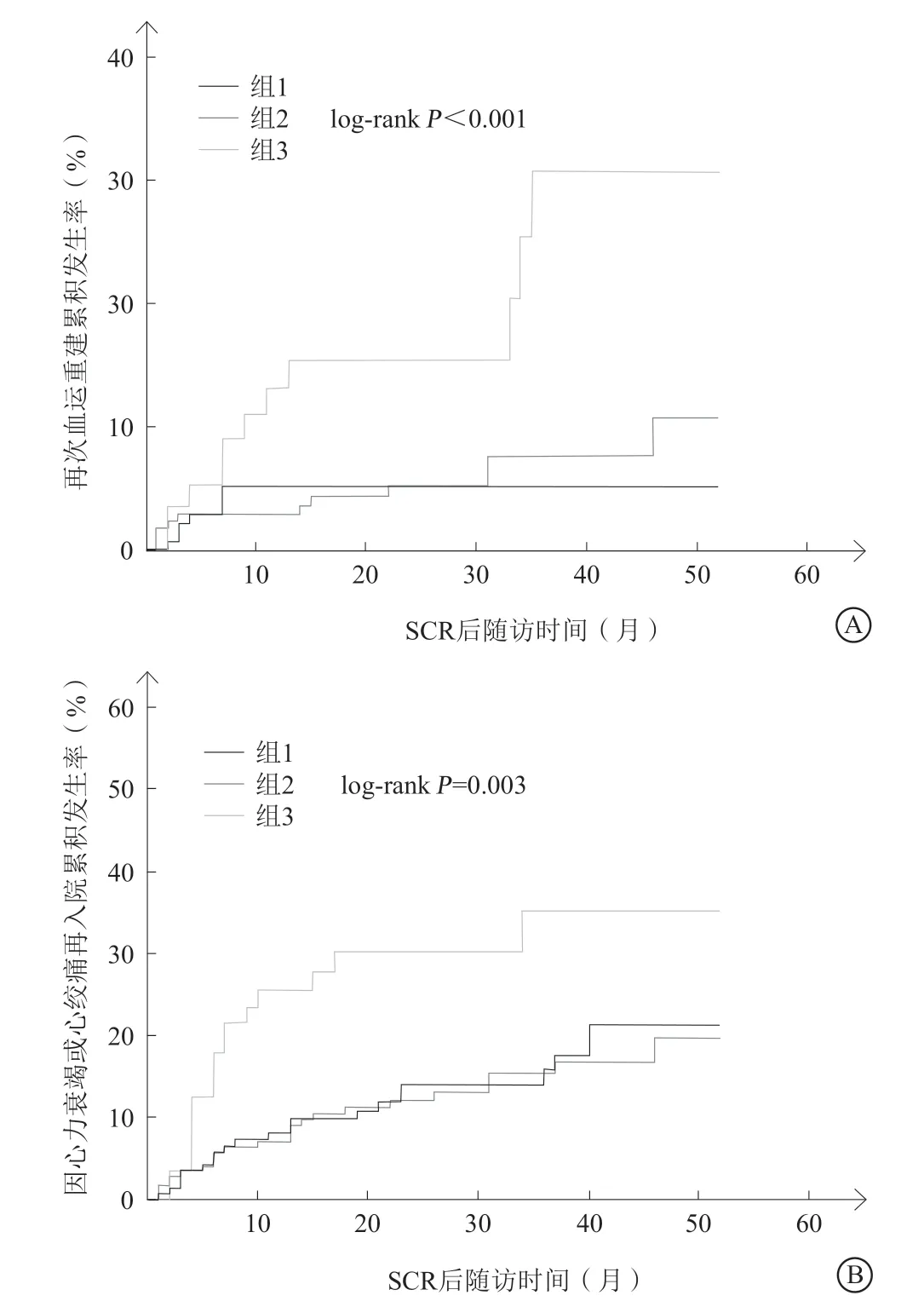
图3 部分次要终点事件累积发生率 A. 三组患者再次血运重建累积发生率; B. 三组患者因心力衰竭或心绞痛入院累积发生率
2. 2. 4 Cox回归分析 所有患者MACCE的Cox回归分析见表6。不同血运重建时机的Cox多因素回归分析见图4。在Cox多因素回归分析中,分类变量赋值情况如下:年龄>60岁=1,年龄≤60岁=0;左心室射血分数<40%=1,左心射血分数≥40%=0;三支血管病变=1,非三支血管病变=0;D2B时间>60 min=1,D2B时间≤60 min=0。经多因素Cox回归分析发现,在纳入年龄>60岁、估算的肾小球滤过率、左心室射血分数<40%、三支血管病变、D2B时间>60 min这些危险因素后,与超过1周行SCR干预非罪犯血管相比,在3~7 d内行SCR干预非罪犯血管与MACCE发生率的降低显著相关(HR 0.48,95%CI 0.28~0.80,P=0.014)。根据SCR完成的不同时间进行Cox多因素回归分析发现,在1~3 d内和3~7 d内行非罪犯血管的完全血运重建均与更低的MACCE风险(HR 0.52,95%CI 0.31~0.87,P=0.036;HR 0.44,95%CI 0.27~0.74,P=0.001)、更低的再次血运重建风险(HR 0.25,95%CI 0.10~0.64,P=0.005;HR 0.28,95%CI 0.12~0.65,P=0.010),以及更低的因心力衰竭或心绞痛再入院风险(HR 0.40,95%CI 0.21~0.76,P=0.018;HR 0.37,95%CI 0.20~0.69,P<0.001)相关(图4)。超过7 d行SCR干预非罪犯血管是MACCE的独立危险因素。

图4 组1(1~3 d,138例)及组2(3~7 d,173例)不同血运重建时机的Cox多因素回归分析(以组3为参照)

表6 MACCE的Cox回归分析
3 讨论
本研究发现,与7 d内干预非罪犯血管相比,在7 d至30 d内干预非罪犯血管会显著增加患者MACCE的发生率,主要体现在较高的再次血运重建及因心力衰竭或心绞痛再入院的发生率上。1~3 d内干预非罪犯血管与3~7 d干预非罪犯血管相比,患者的MACCE差异无统计学意义。经Cox多因素回归分析发现,在纳入年龄>60岁、估算的肾小球滤过率、左心室射血分数<40%、三支血管病变、D2B时间>60 min这些因素后,7 d内干预非罪犯血管同样能明显降低MACCE、再次血运重建及因心力衰竭或心绞痛再入院的发生风险,7 d后干预非罪犯血管是MACCE发生的独立危险因素。
早期干预非罪犯血管一直存在争议,在急性心肌梗死的早期阶段容易发生各种危及生命的并发症,如心脏破裂、支架内血栓形成及各种恶性心律失常[12]。在此期间再次行PCI术干预非罪犯血管可能增加这些风险。既往研究发现,这一时期干预非罪犯血管患者的短期预后不良,明显增加围术期并发症的发生风险,因此早期的指南也不推荐早期干预非罪犯血管[3,13-14]。但是随着介入技术的成熟及介入器械的进步,近年来研究显示,这一风险正在逐渐降低,同时,早期开通非罪犯血管有利于挽救濒死心肌,改善心肌血供,对于心脏功能恢复及患者的远期预后有利。随后的多项随机临床研究证实,同期或者早期开通非罪犯血管在不增加安全性风险的前提下能显著改善患者远期预后[15-19]。PRAMI研究[15]、CvLPRIT研究[17]、DANAMI-3-PRIMULTI研究[16]、Compare-Acute研究[18]均证实了同期或者再次开通非罪犯血管对患者远期预后有益,尤其是明显降低再次血运重建及再次心肌梗死的发生率。基于这些研究结果,2018年欧洲心脏病学会及欧洲心胸外科协会联合发布的心肌血管重建指南[20]也建议,对于这类患者无论是住院期间还是出院后,可常规行非罪犯血管的完全血运重建。2019年公布的COMPLETE研究[19]共纳入2016例行SCR以及2025例COR的STEMI合并MVD患者,在为期3年的随访中,SCR组在包含心原性死亡和再次心肌梗死的复合终点上明显优于COR组(7.8%比10.5%,HR 0.74,95%CI 0.60~0.91,P=0.004)。
由于缺乏大规模的随机对照临床研究,当前的指南中并没有明确给出这类患者非罪犯血管的最佳血运重建时机。而在既往研究中,对于非罪犯血管的最佳血运重建时机的研究结论也不尽一致[8-10,21-22]。Tarasov等[23]将STEMI合并MVD的患者分为两组,A组(39例)首次手术后60 d内行SCR,B组(148例)首次手术后60 d后行SCR,结果显示,A组的靶血管血运重建和再次心肌梗死发生率均低于B组(5.1%比27.7%,P=0.05;0比9.46%,P=0.09),但两组死亡率比较差异无统计学意义(P>0.05)。Kim等[11]一项共纳入753例STEMI合并MVD患者的回顾性研究,将患者分为三组,A组(316例)在住院期间进行完全血运重建,B组(360例)在1周内进行SCR,C组(77例)在1周后进行SCR,结果显示,在平均3.4年的随访中,包含全因死亡、非致死性心肌梗死、再次血运重建的复合终点上,C组的事件发生率高于A组(OR 1.83,95%CI 1.06~3.18,P=0.031),但A组与B组的MACE发生率比较差异无统计学意义(OR 1.01,95%CI 0.70~1.46,P=0.950),因此该研究指出,对于STEMI合并MVD患者应当进行ICR或在1周内进行SCR。Moore等[24]的研究指出,对于仅有一支非罪犯血管的患者应在49 d内对非罪犯血管进行干预,而有两支以上非罪犯血管的STEMI患者,应在10 d之内进行完全血运重建。总之,尽管当前的指南对于非罪犯血管的最佳血运重建时机没有明确建议,但目前临床上对于非罪犯血管多倾向于早期行完全血运重建,以改善患者预后。但是需要指出的是,对于非罪犯血管的干预时间需要综合评估患者的各项情况,包括治疗的有效性和安全性,从而制定个体化的治疗方案。同时,尚需大规模的临床研究来进一步明确不同时间段干预非罪犯血管对于患者预后的影响,为这类患者制定出更加适合的手术策略,从而实现个体化、精准化的治疗。
本研究主要有以下几个局限:首先,本研究为单中心、回顾性、观察性研究,存在选择偏倚,无法充分评估混杂因素对于研究结果的影响。其次,本研究未充分评估患者自身冠状动脉病变的严重程度,如应用Gensini评分或者SYNTAX评分来评价冠状动脉病变严重程度,而Gensini评分以及SYNTAX评分与患者的预后明显相关。
对于合并MVD的STEMI患者,干预非罪犯血管的最佳时机为7 d内,7 d后干预非罪犯血管与7 d内相比明显增加MACCE发生率。而在7 d的时间内,无论是急诊PCI术后1~3 d还是3~7 d行SCR干预非罪犯血管,对患者预后的影响差异无统计学意义。
利益冲突所有作者均声明不存在利益冲突

