浅议色谱-质谱分析中的内标法检测技术
马瑞欣
摘 要:通过查阅文献和实验,分析总结色谱-质谱分析中内标物的要求与作用,内标法检测技术使用注意事项、优势与不足。
关键词:内标法;同位素内标;色谱-质谱分析
内标法定量是利用待测物浓度和内标物浓度的比值与待测物响应值和内标物响应值的比值成正比进行定量分析的方法,是经典的色谱-质谱定量分析方法,广泛应用于食品安全、医学、环境等领域。
本文将对色谱-质谱分析中内标物的要求和常用类型、内标物的作用、内标法使用注意事项、内标法的优缺点进行分析总结。
1 内标物的要求及其常用类型
内标物要求其在样品中不存在,不与样品发生反应,与目标物的物理化学性质相似。根据仪器定性定量原理,色谱分析中要求内标物与样品中的其他组分有良好的分离,质谱分析中一般要求与目标物的母离子或子离子的质荷比(m/z)不同。有机质谱分析中常用2H、13C、15N、18O、34S等稳定同位素内标[1],农药、兽药残留色谱-质谱分析中最为常见的内标物是2H和13C同位素内标。
2 内标物的作用
2.1 监测仪器的稳定性
只用于监测儀器的稳定性时,一般在样品前处理的最后一步加入等量的内标[2-3],适用于样品的提取比较充分,基质干扰可以忽略的检测,内标法所得校准曲线的线性相关系数和定量结果与外标法相比无显著差异,内标法、外标法定量均可,但是通过每次进样时内标物响应值的变化,能够对仪器的稳定性进行判断,必要时对设备进行维护保养。
2.2 校正基质效应
基质效应是质谱分析普遍存在的一种现象,分为基质抑制效应和基质增强效应。内标物只用于校正基质效应时一般上机分析时在线加入[4]或上机分析前[5]加入。此种情况样品的提取比较充分,但样品的基质干扰比较大,基质标准曲线适用性比较差。由于内标价格昂贵,相比于样品提取前加入同位素内标,在线或上机分析时添加适量低浓度的内标,可以大大减少内标的使用量,节约检测成本。同位素内标因与目标物具有相同的化学性质和相同的保留时间而成为消除基质效应首选的内标物。
2.3 校正样品前处理
内标物在样品提取前[6-7]或某个步骤前加入[8-9],用于校正样品的前处理损失,同时也可以减小基质效应。样品提取前加入内标比在某个步骤前加入能够获得更好的回收率[10]。样品提取前加入内标,特别是同位素内标,能够校正前处理过程的损失,降低操作要求,减小基质效应,成为兽药残留色谱-质谱分析中非常经典的方法。
3 内标法使用注意事项
3.1 内标加入量
内标法要求内标的加入体积要准确并且浓度适当。内标加入量是影响检测结果的一个比较重要的因素[11-12],在标准曲线定量时要求标准曲线、样品中内标加入量应保持恒定。内标的加入量太低不足以校正仪器波动,对测定结果影响较大;太高不仅造成浪费,还可能造成污染。当前处理过程涉及到分体积操作且用标准曲线定量时,需注意样品上机液中内标物的理论浓度需与标准系列中内标物的浓度相一致,否则可能产生错误的结果。
3.2 内标加入后样品放置时间
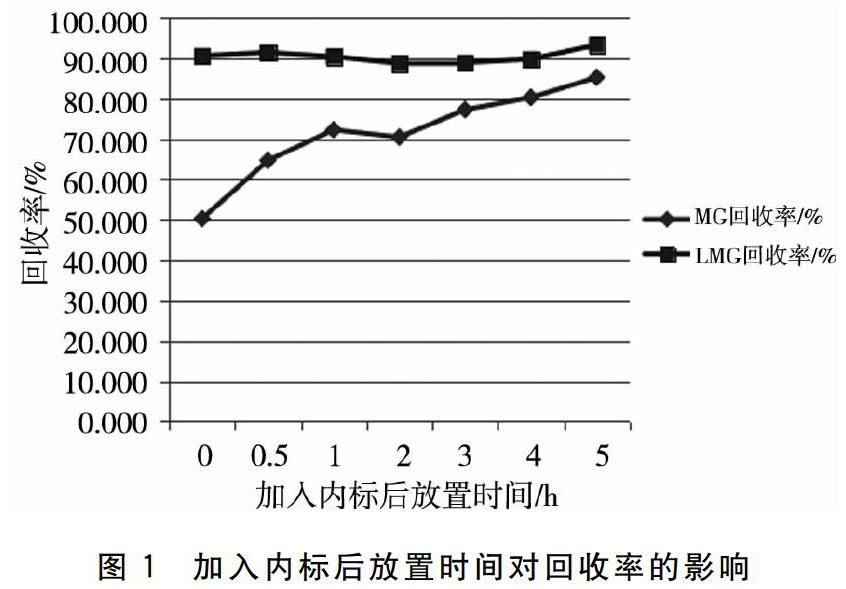
在前处理操作之前加入内标用于校正样品的前处理损失时,应注意保证内标物被样品充分吸附,否则会造成检测结果偏低。为证明加入内标后样品放置时间对检测结果的影响,设计实验如下:称取14个鲤鱼空白样品,每个样品5.00 g,同时加入孔雀石绿(MG)和隐色孔雀石绿(LMG)外标混合标准溶液,加标量均为4.0 μg·kg-1,混匀,-20 ℃放置4 d后,按照GB/T 19857-2005中鲜活水产品进行实验。14个样品分为7组,每组2个平行样品,加入内标混合液的体积完全相同,放置时间分别为5 h、4 h、3 h、2 h、1 h、0.5 h、0 h。液相色谱-串联质谱分析的实验结果见图1。
实验结果证明:孔雀石绿内标加入后的放置时间对检测结果影响较大,而隐色孔雀石绿则不受放置时间的影响。这可能与内标物的性质有关。孔雀石绿内标物为孔雀石绿-D5苦味酸盐,隐色孔雀石绿内标物为隐色孔雀石绿-D6,隐色孔雀石绿-D6极性较孔雀石绿-D5苦味酸盐弱,脂溶性强,极易被鱼肉吸附,其提取效率与放置时间无关;孔雀石绿-D5苦味酸盐极性较强,放置时间越短,吸附量越小,提取出来的越多,导致目标物回收率降低。
4 内标法的优势与不足
4.1 优势
从定性分析来看,同位素内标物峰可以作为目标峰是否发生漂移的参考依据,因为同位素内标与分析物的物理化学性质相近,在色谱-质谱分析中常常与目标物有相同的保留时间,可以通过内标物的保留时间是否发生漂移来确定目标物是否发生漂移。
从定量分析来看,内标可以校正目标物在样品前处理中的损失,降低对仪器稳定性和进样量的严格要求,降低质谱检测的基质效应,从而得到更好的准确度和精密度。
从实验操作来看,提取前加入内标物的前处理方法对实验操作的要求比外标法有所降低,对体积的准确性要求没有外标法严格。当目标物有对应的同位素内标时,可以直接使用溶剂标准溶液,不必配制基质标准溶液,从而可以减少实验操作,提高检测效率。
4.2 不足
同位素内标物价格较贵,在分析中并不是所有目标物都能找到合适的内标物,特别是对于多种物质同时检测时,由于存在极性差异,即使同类物质的内标同位素也很难抵消基质效应,仍需配制基质匹配标准溶液来进一步抵消基质效应[13-14]。
在定量分析中,我们期望不管在样品处理和分析过程中有任何变化,分析物和同位素内标物的峰面积比为常数,但实验中发现并非如此[15]。实验中使用同位素内标有时不能补偿基质效应[16],有时即使有对应的同位素内标仍不能获得满意的回收率。分析原因可能是同位素内标与目标物存在极性上的差异,会导致在样品提取时二者的提取效率有差异或者是色谱—质谱分析中二者到达离子源的时间不同,从而引起基质效应不同。
内标法做为水产品药物残留色谱—质谱分析的常用方法,样品的个体差异需引起重视。有时同种水产品同批次进行检测,不同个体之间回收率会存在较大差异。分析原因可能是不同的个体对于待测物和其对应内标的回收率造成的影响不同所致。
5 结论
内标法作为一种定量分析方法,虽然存在不足,但在色谱—质谱分析中,同位素内标法仍不失为一种降低基质效应,提高准确定性定量分析的重要方法。
参考文献:
[1] 杜晓宁,张鹏帅,雷雯,等.稳定同位素技术在我国食品安全检测领域的应用进展[J].同位素, 2019,32(3):231-243.
[2] 曹琦,张亚珍,朱正伟,等.气相色谱-四极杆/飞行时间质谱筛查确证辣椒中244种农药残留及其代谢物[J].色谱,2021,39(5):494-505.
[3] 中华人民共和国国家卫生健康委员会,中华人民共和国农业农村部,國家市场监督管理总局.食品安全国家标准 植物源性食品中208种农药及代谢物残留量的测定 气相色谱-质谱联用法:GB 23200.113-2018[S].北京,中国农业出版社,2018:1-44.
[4] 华宇,高和杨,聂兴娜,等.同位素内标-高效液相色谱-串联质谱法检测牛奶及奶粉中黄曲霉毒素M1[J].食品安全质量检测学报, 2020,11(6):1978-1984.
[5] 刘笑笑,丁辉,吴福祥,等.杂质吸附固相萃取-液相色谱串联质谱法同时测定粮食中15种真菌毒素[J].粮油食品科技, 2021,9(1):155-167.
[6] 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.水产品中孔雀石绿和结晶紫残留量的测定:GB/T 19857-2005[S].北京,中国标准出版社,2005:1-7.
[7] 张璇,杨光昕,孔聪,等.高效液相色谱-串联质谱法测定水产品中镇静剂及其代谢物残留[J].分析化学,2021,49(3):460-467.
[8] 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法:GB/T 22286-2008[S].北京,中国标准出版社,2008:1-5.
[9] 中华人民共和国卫生部,中国国家标准化管理委员会.动物食品中克伦特罗残留量的测定:GB 5009.192-2003 [S].北京,中国标准出版社,2003:520-531.
[10] 徐青萍,易水生.内标加入顺序对测定猪尿中盐酸克伦特罗残留量的影响[J].中国卫生检验杂志,2008,18(2):236-238.
[11] 王婷,王儒,赵晓野,等.液相色谱质谱法测定贝类水产品中氯霉素的不确定度评定[J].食品工业科技,2021,42(4):245-251.
[12] 韩德娟, 高艾英, 高大山.液相色谱串联质谱内标法测定猪肉中沙丁胺醇及莱克多巴胺残留量的不确定度分析[J].食品安全质量检测学报, 2020,11(1):223-230.
[13] 刘洁,佟玲,孟文婷,等.固相萃取-超快速液相色谱-串联质谱法测定当归中135种农药及其代谢物残留[J].色谱,2015,33(12):1257-1268.
[14] 杨欣,李鹏,赵云峰,等.高效液相色谱-线性离子阱三级质谱法检测花生中涕灭威及其代谢物涕灭威砜、涕灭威亚砜[J].色谱,2012,30(3):309-313.
[15] WANG S,CYRONAK M, YANG E.Does a stable isotopically labeled internal standard always correct analyte response? A matrix effect study on a LC/MS/MS method for the determination of carvedilol enantiomers in human plasma[J].Journal of Pharmaceutical and Bilmedical Analysis,2007,43(2):701-707.
[16] BUNCH D R, EI-KHOURY J M, GABLER J, et al.Do deuterium labeled internal standards correct for matrix effects in LC-MS/MS assays? A case study using plasma free metanephrine and normetanephrine[J].Clinica Chimica Acta 429(2014):4-5.
(收稿日期:2021-07-01)

