低C/N亚铁氧化硝酸盐还原菌群脱氮特性
周佳敏 ,黄廷林 *,刘 茜 ,杨尚业 ,寇莉青 (1.西安建筑科技大学,陕西省环境工程重点实验室,陕西 西安710000;2.西安建筑科技大学,西北水资源与环境生态教育部重点实验室,陕西 西安 710000;.陕西省引汉济渭工程建设有限公司,陕西 西安 710010)
目前,几乎每座水库都存在一定程度富营养化问题,严重的已经不能作为供水水源[1-2].而氮源污染是导致水体富营养化的主要原因之一.控制氮源污染成为解决微污染水体问题的重要环节[3].
生物脱氮法由于具有高效、低耗的特点,成为饮用水源脱氮处理中经济有效的方法之一[4].对于营养物质贫乏的微污染水源水体,碳源不足已成为传统生物脱氮技术的重大瓶颈[5].研究[6-8]发现,以铁、锰等无机物质作为电子供体来辅助低有机碳水体进行生物脱氮是一种高效、便捷、经济、环保的生物工艺.研究者发现,部分 Fe(Ⅱ)氧化与 Fe(Ⅲ)还原是由特定微生物驱动的酶促反应[9].这些微生物能够利用Fe(Ⅲ ) / Fe(Ⅱ )耦合其他的电子供体或者电子受体进行铁的氧化还原,从而形成了一个持续的生物调控的铁的地球化学循环.部分异养反硝化菌可以利用亚铁为电子供体进行硝酸还原,被称为亚铁氧化硝酸盐还原菌[10].此后,其他研究者陆续报道了稻田、湿地、湖泊、海洋沉积物及活性污泥中该类反硝化过程的发生,研究表明此过程是典型厌氧环境中铁、氮循环的重要步骤[11-13].
目前,关于亚铁氧化耦合硝酸盐还原过程及其微生物的研究还处于起步阶段[14-15],针对微污染水源水利于此类功能菌强化脱氮的研究工作还鲜见报道.
本文从西安市李家河和黑河水库底泥中驯化筛分出一组能够在低C/N条件下高效脱氮的亚铁氧化硝酸盐还原混合菌群命名为 Z13.利用高通量测序技术鉴定确定该菌群的种群结构,并对其反硝化特性及环境因素对反硝化效率的影响进行研究,以期为亚铁氧化硝酸盐还原混合菌群应用于工程实践提供理论依据,为微污染水源水的原位生物脱氮研究奠定基础.
1 材料与方法
1.1 样品采集
于2019年7月取自陕西省西安市李家河水库和黑河水库,采用彼得森[16]采泥器采集水库表层0~10cm 沉积物[17],装于灭菌的取样瓶中,放置在装有冰袋的泡沫箱内, 48h内运回实验室,待用.
1.2 培养基的配置[18]
富集培养基: CH3COONa 0.3g/L;NaNO30.3g/L;KH2PO40.15g/L; FeSO4·7H2O 0.45g/L; MgSO4·7H2O 0.15g/L;CaCl20.15g/L;微量元素 2mL/L; pH 6.5~6.8.
基础培养基:CH3COONa 0.1g/L;NaNO30.1g/L;KH2PO40.05g/L; FeSO4·7H2O 0.15g/L; MgSO4·7H2O 0.05g/L;CaCl20.05g/L;微量元素 2mL/L;pH 6.5~6.8.
固体培养基:除添加 10g琼脂外,其他与基础培养基相同.
微量元素主要成分:MgSO4·7H2O 0.5g/L; EDTA 1.0g/L ; ZnSO40.2g/L ; MnCl2·4H2O 0.1g/L; FeSO4·7H2O 0.5g/L; CuSO4·5H2O 0.5 g/L; CoCl2·6H2O 0.2g/L.
1.3 亚铁氧化硝酸盐还原混合菌群的筛选
取李家河和黑河水库沉积物的混合样品250mL于500mL的培养瓶中,剩余部分用已灭菌的富集培养液填满,盖上软橡皮塞,摇晃盐水瓶使瓶中样品混匀,置于恒温培养箱(30℃)中培养.以 7d为 1个培养周期更换一半的培养基,期间每天摇晃 1次盐水瓶.
驯化3周后,取1mL沉积物加入9mL的无菌水进行梯度稀释,稀释梯度分别为 10-2、10-3、10-4、10-5,取以上稀释梯度的菌悬液0.1mL涂布于固体培养基的平板上[19],再将已灭菌还未凝固的固体培养(30~40℃)覆盖在已涂布的固体平板上形成双层平板,置于恒温培养箱(30℃)中培养.3~7d后根据菌落的生长情况,将平板上的菌落挑选至基础培养基中培养.对经多次转接依旧能保持高效脱氮的反硝化混合菌群置于甘油中在-20℃保存.
1.4 亚铁氧化硝酸盐还原混合菌群结构分析
取处于对数生长期的Z13菌液500mL经已煮沸灭菌的0.22μm醋酸纤维滤膜过滤,采用上海美吉生物医药科技有限公司的细菌基因组DNA提取试剂盒(离心柱型)对反硝化混合菌群进行 DNA 提取[17].利用1%琼脂糖凝胶电泳检测DNA提取物的质量.以基因组DNA为模板,采用338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')引物进行PCR扩增,扩增体系包括(20μL):DNA模板10ng、338F引物0.8μL(5μmol/L)、806R 引物 0.8μL(5μmol/L)、dNTPs 2μL(2.5mmol/L)、DNA 聚合酶 0.4μL、缓冲液 4μL、BSA 0.2μL、ddH2O 补至 20μL.扩增条件为:95℃预变性3min,95℃变性30s,55℃退火30s,72℃延伸45s,72℃终延伸 10min,循环 27次.扩增后的 PCR产物采用凝胶回收试剂盒回收(Axygen, USA),用Tris-HCl进行洗脱,2%琼脂糖凝胶电泳检测,通过 Quanti Fluor™-ST 蓝色荧光定量系统(Promega)检测 PCR产物浓度[20].在上海美吉生物公司完成高通量DNA 测序.本研究中所有关于16S rRNA基因测序的原始数据均上传至 NCBI-SRA数据库(美国国立生物技术信息中心),其编号为SRP301306.
1.5 亚铁氧化硝酸盐还原混合菌群生长及脱氮特性研究
将处于对数生长期的Z13菌液按V/V=10%的接种量转接至装有45mL新鲜反硝化基础培养基的盐水瓶(50mL)中,拧紧瓶塞,置于恒温培养箱(30℃)中培养.另设不加菌液的作为空白对照组.为避免在单个盐水瓶中重复取样对后续实验产生影响,实验中根据取样次数培养15瓶微生物.其中接种的混合菌群 Z13来自同一批培养,基础培养基也是同一批配制.通过检测总氮、硝酸盐氮、亚硝酸盐氮、氨氮、Fe2+的质量浓度、pH值、TOC和OD600研究混合菌群Z13的生长及脱氮特性,每次样品重复3次.
1.6 不同因素对亚铁氧化硝酸盐还原混合菌群脱氮特性影响
为避免在单个培养瓶中重复取样对后续实验产生影响,实验中根据取样次数培养15瓶微生物.其中接种的混合菌群 Z13取自同一批培养,基础培养基也是同一批配制.每隔一段时间检测硝酸盐氮、亚硝酸盐氮、氨氮、OD600和Fe2+的质量浓度.
1.6.1 温度对 Z13菌群脱氮影响 依据大多数细菌的温度适应范围及水源水的实际水温条件,将不同的恒温生化培养箱的温度分别设置为 10,15,20,25,30和40℃6个梯度,将培养瓶分别置于不同的恒温培养箱中培养.
1.6.2 初始pH值对Z13菌群脱氮影响 依据大多数细菌的pH值适应范围,将反硝化基础培养基的初始pH值分别调整为5.0,6.0,7.0,8.0 4个梯度,接菌后置于30℃恒温培养箱中培养.
1.6.3 C/N对Z13菌群脱氮影响 结合实际水体情况及考虑到碳源过多会对实际水体造成污染等因素,将C/N设定为0、1.0、1.821和4.0.通过改变乙酸钠质量浓度来改变C/N(质量比),接菌后置于30℃恒温培养箱中培养.
1.6.4 Fe2+浓度对Z13菌群脱氮影响 将Fe2+浓度设置为 0,5,15,30和 50mg/L 5个梯度,接菌后置于30℃恒温培养箱中培养.
1.7 分析方法
细菌菌密度(OD600),采用紫外分光光度计测定样品在 600nm 的吸光度;总氮(TN)采用碱式过硫酸钾消解-紫外分光光度法测定;硝酸盐氮(NO3--N)采用紫外分光光度法测定[21];亚硝酸盐氮(NO2--N)采用N-(1-萘基)-乙二胺光度法测定;氨氮(NH4+-N)采用纳氏试剂分光光度法测定;二价铁离子浓度(Fe2+)采用邻菲啰啉分光光度法测定;TOC采用总有机碳测定仪测定.除菌密度(OD600)和总氮(TN)测定不过滤外,其余水样测定需经0.22μm的醋酸纤维滤膜过滤[22],每个水样重复测定3次.
1.8 Z13菌群反硝化过程动力学分析
Monod方程在水处理领域中,其表达式[23]如下:

两边取倒数得:

式中: V和Vmax分别为硝氮的比降解速率mg/(L·h)和最大比降解速率mg/(L·h);S为碳源浓度;Ks为饱和常数.
由生长曲线数据得出 1/V与 1/S关系,如图(3),代入上式(1)、(2),得出Vmax与Ks.
2 结果与分析
2.1 混合菌群Z13种群结构分析
本文通过高通量 DNA测序分析测定混合菌群Z13的群落结构及组成比例.从门水平上看,细菌群落主要分布在 Proteobacteria(83.45%)和 Acidobacteriota(14.39%)两个门类.这与文献报道[24-25]的相一致.在属水平上,混合菌群 Z13的组成如下:Zoogloea(69.25%)、Geothrix (14.39%)、Dechloromonas(5.94%)、Ralstonia (3.46%)、Curvibacter (1.16%)、Caulobacter (0.48%)和others (5.32%),其中属于亚铁氧化菌的 Zoogloea占比最大,其次是 Fe(III)还原菌Geothrix.这与陈鹏程等[26]报道的相一致.混合菌群Z13培养至末期时,90%以上的Fe(II)已经被氧化(图2),因此推测 Fe(III)的积累有可能激活了铁还原菌,发生 Fe(III)的还原溶解[26].本研究通过驯化筛选得到混合菌群 Z13,研究其脱氮特性,此过程中所得到的菌群是自然配对形成的,相比传统筛选的纯菌具有更好的适应能力[19],由不同种属的亚铁氧化硝酸盐还原菌组成的混合菌群更有利于水体中氮素的去除.
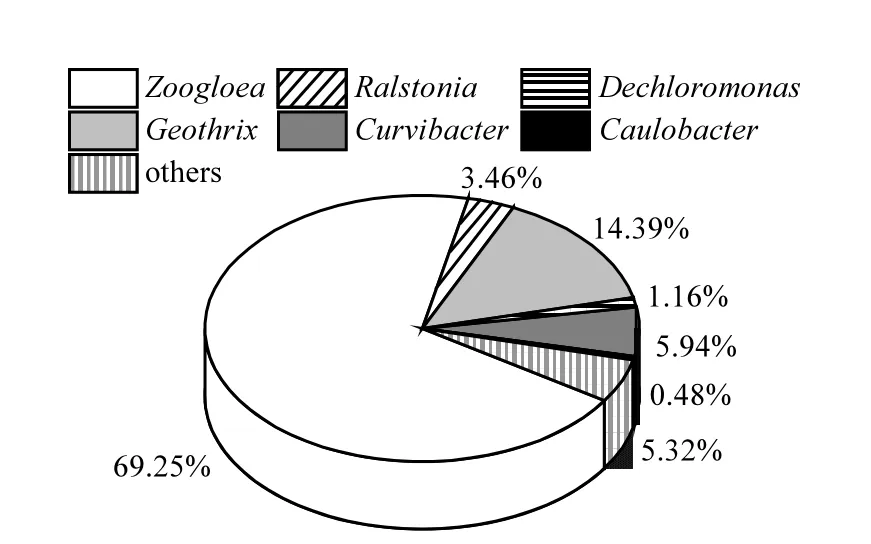
图1 亚铁氧化硝酸盐还原混合菌群Z13群落结构组成Fig.1 Community structure composition of mixed bacteria Z13 reduced by ferrous oxide nitrate
2.2 混合菌群Z13生长及脱氮特性分析
如图2所示,在0~8h阶段,混合菌群Z13处于缓慢期,培养基中乙酸钠消耗速度较慢,硝酸盐氮浓度由原来的16.310mg/L降至15.241mg/L. Fe2+加入培养基之后溶液的pH值快速下降,故0h测得pH值为5.985,之后8h内由于Fe2+继续水解使得pH值继续下降至 5.395.此阶段接菌组和空白对照组对 Fe2+的去除也比较缓慢.随着混合菌群对环境的适应,在8~22h阶段,混合菌群 Z13进入对数增长期,期间乙酸钠消耗逐渐加快,培养基逐渐由清澈变的浑浊,说明微生物在此阶段大量消耗乙酸钠进行生长繁殖,OD600急剧增加,反硝化作用明显加强,硝酸盐氮浓度由 15.241mg/L降至 0.808mg/L.对应的反应速率为1.0310mg/(L·h).亚硝酸盐氮浓度在22h达到最大值 1.684mg/L,之后随着反硝化的进行逐渐降低.因反硝化期间会产生碱度,使得pH值从5.395升至7.510.此阶段细菌表现出强烈的氧化铁能力,接菌组的Fe2+浓度快速下降,由26.610mg/L降至5.980mg/L,Fe2+氧化率明显高于空白对照组.说明培养基中Fe2+的氧化和氮素的去除与菌体生长有直接关系,且反硝化作用主要发生在对数生长期,随着菌体的快速增殖,培养液中硝酸盐氮和 Fe2+的量会迅速下降,这与郭端强等[27],康鹏亮等[28]的研究结果相一致.在22~50h阶段,混合菌群Z13进入细菌生长稳定期,此时乙酸钠消耗速率逐渐降低,亚硝酸盐氮也逐渐降低.50h后,培养基中乙酸钠和 Fe2+已经耗尽,细胞内残存的有机物不足以支撑微生物继续增长,因此数量开始下降. 78h时空白对照组的氮素并未去除,而接菌组的硝酸盐氮的去除率为 99.85%,总氮去除率和平均去除速率为89.91%和0.1888mg/(L·h).由于总氮测定中包含了微生物同化的氮,故总氮的减少主要源于微生物反硝化作用,在本研究中总氮的减少程度即代表了反硝化脱氮的效果.TOC从初始的29.150mg/L降低至2.140mg/L,去除率和平均消耗速率分别为 92.66%,0.3462mg/(L·h).TOC 浓度的变化与上述氮素浓度的变化具有类似的趋势.整个反硝化过程中,无氨氮的积累,亚硝酸盐氮在反硝化前期有个短暂的积累,但很快消失.随着 Fe2+被大量氧化,培养基中生成了许多絮状的沉淀.此现象与周志华等[29]的研究一致.因培养瓶内并不是绝对厌氧的环境,故空白对照组 Fe2+的氧化主要为化学氧化,接菌组 Fe2+的总去除率为 99.86%,其中生物氧化率为82.70%,微生物调节的 Fe2+氧化可能比非生物的Fe2+氧化进行的更快,有研究表明[30]铁氧化菌的参与可以使得Fe2+的氧化速率提高4个数量级. Straub等[31]的研究中也证明了这种机制的存在.

图2 亚铁氧化硝酸盐还原混合菌群Z13氮素、TOC、Fe2+浓度去除及pH值与生长曲线Fig.2 Removal of nitrogen, TOC, Fe2+ concentration and pH value and growth curve of mixed bacteria Z13 by reduction of ferrous nitrate
由图3可知,混合菌群Z13在生长的过程中,硝氮的最大降解速率Vmax为1.290mg/(L·h),饱和系数Ks为41.606mg/L.
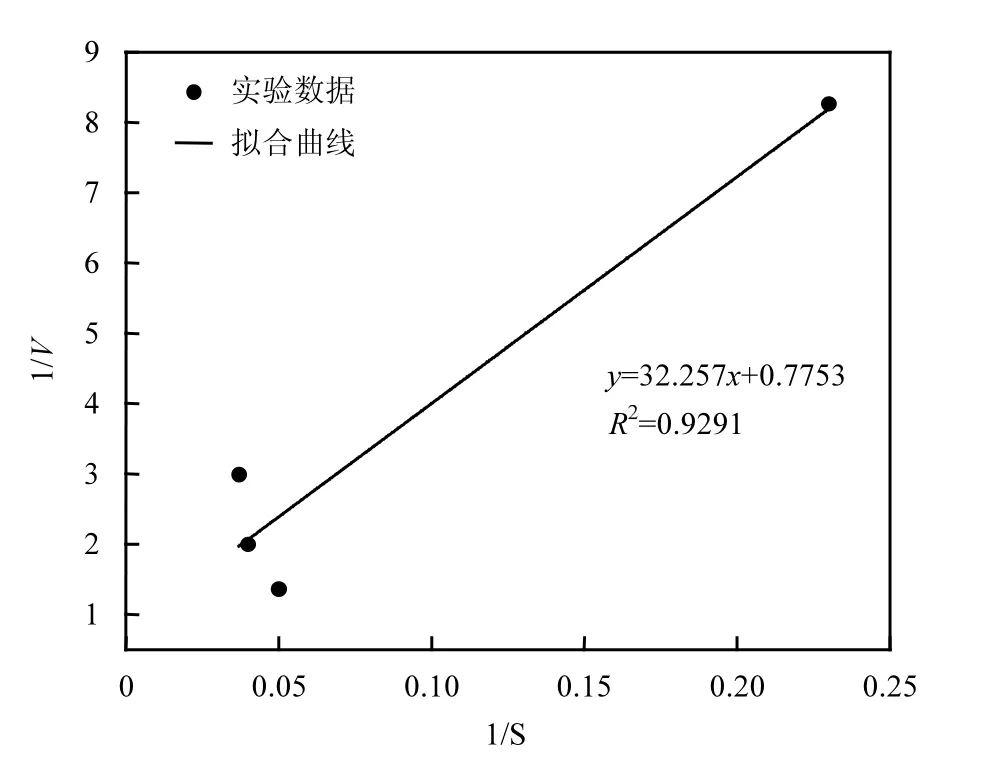
图3 1/V和1/S的关系Fig.3 The relationship between one over V and one over S
2.3 理化因素对混合菌群Z13脱氮特性影响
2.3.1 温度对 Z13菌群脱氮影响 如图 4所示,温度对反硝化混合菌群Z13的脱氮效果影响显著.10℃条件下,混合菌群 Z13反硝化进程相对缓慢,细菌活性较差,代谢速率较低,菌密度也较低,从而影响了反硝化速率和Fe2+的生物氧化效果. 78h时硝酸盐氮去除率为 19.03%,亚硝酸盐氮的累积为0.978mg/L,此时Fe2+的总去除率为40.07%,生物氧化率为 26.94%.15℃条件下混合菌群 Z13在 78h时的硝酸盐氮去除率为 54.58%,Fe2+的总去除率为57.31%.亚硝酸盐氮在44h到达最大1.180mg/L,78h时降为 0.643mg/L.20℃条件下混合菌群 Z13在78h的硝酸盐氮去除率为81.12%,Fe2+的总去除率为 96.35%,亚硝酸盐氮的累积为 0.234mg/L.菌密度和Fe2+的去除效果随温度的升高也逐渐增加,在 25~40℃温度范围内 78h时硝酸盐氮去除率均在 94%以上,且反硝化结束后也无亚硝酸盐氮和氨氮的累积.此范围内 Fe2+的化学去除率为15.96%~22.52%.混合菌群Z13在40℃的条件下亚硝酸盐氮累积量在 12h达到最大 0.354mg/L,而30℃条件下亚硝酸盐氮累积量在 22h达到最大1.684mg/L.说明不同的温度下混合菌群 Z13脱氮速率差异明显,且在一定范围内,温度越高,微生物的活性越高,增殖速度越快[23]. 10~40℃温度范围内,整个反硝化过程中都未检测到氨氮的生成,由菌密度可看出40℃条件下的混合菌群Z13比其他组更早进入对数期,但稳定期明显缩短,提前进入衰亡期,说明在较高温度之下虽然有助于细菌的分裂生殖但也会导致细菌迅速进入衰亡期,细胞活性迅速下降.相比而言 30℃时混合菌群 Z13既能够迅速进入对数期快速分裂生殖,并且最终培养基中也能够获得较高的细菌密度.因此,所有混合菌群Z13的预培养及活化过程均在30℃恒温生化培养箱中进行.故本文中混合菌群Z13最佳的培养温度为30℃.
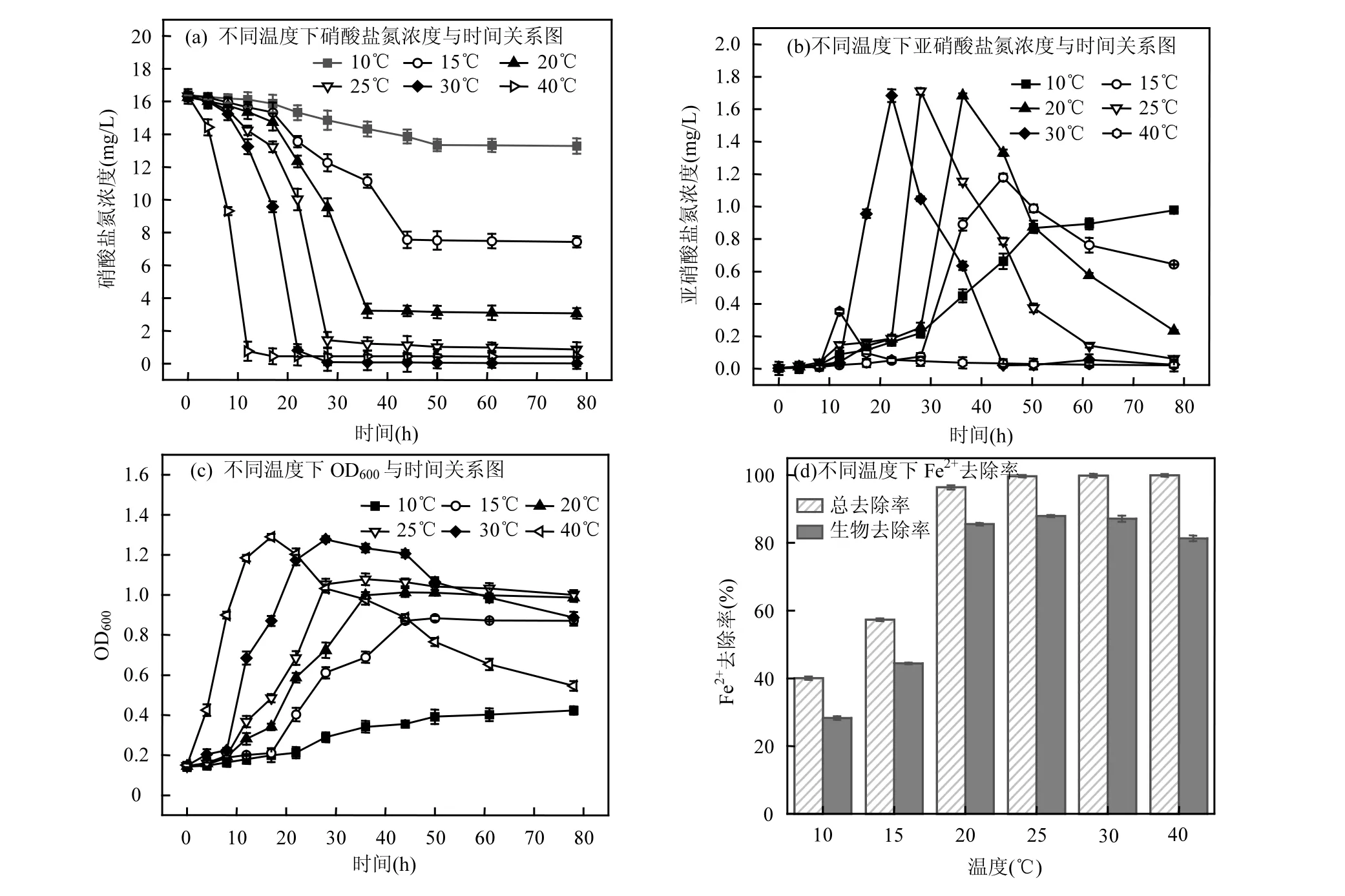
图4 温度对Z13菌群脱氮影响Fig.4 Effect of temperature on denitrification of Z13bacteria
混合菌群 Z13对温度的适应范围较宽,在 25~40℃温度范围内脱氮性能良好,这与已报道的其它亚铁氧化硝酸盐还原菌相类似[32],这样的宽温度范围有利于菌体在环境中的竞争与存活,并能够有效地发挥该菌的反硝化能力.
2.3.2 初始pH值对Z13菌群脱氮影响 由图5可知,培养基的初始pH值对混合菌群Z13脱氮有显著的影响,在初始pH值为5的酸性环境中,Fe2+溶解性良好且稳定,但大多数反硝化生物活性会被抑制.故菌体生长缓慢,脱氮速率也较低,由菌密度可看出细菌适应期较长.50h后,混合菌群 Z13才适应环境开始进入生长对数期.78h时硝酸盐氮去除率为93.80%,亚硝酸盐氮的累积量为 1.123mg/L,在初始pH值为6的条件下,混合菌群Z13在44h时亚硝酸盐氮的累积量达到最大为 1.785mg/L,78h时降为0.428mg/L,同时硝酸盐氮的去除率为 93.80%.由实验数据可看出初始pH值为5和6的情况下,混合菌群Z13生长缓慢,78h时反硝化进程还未结束.
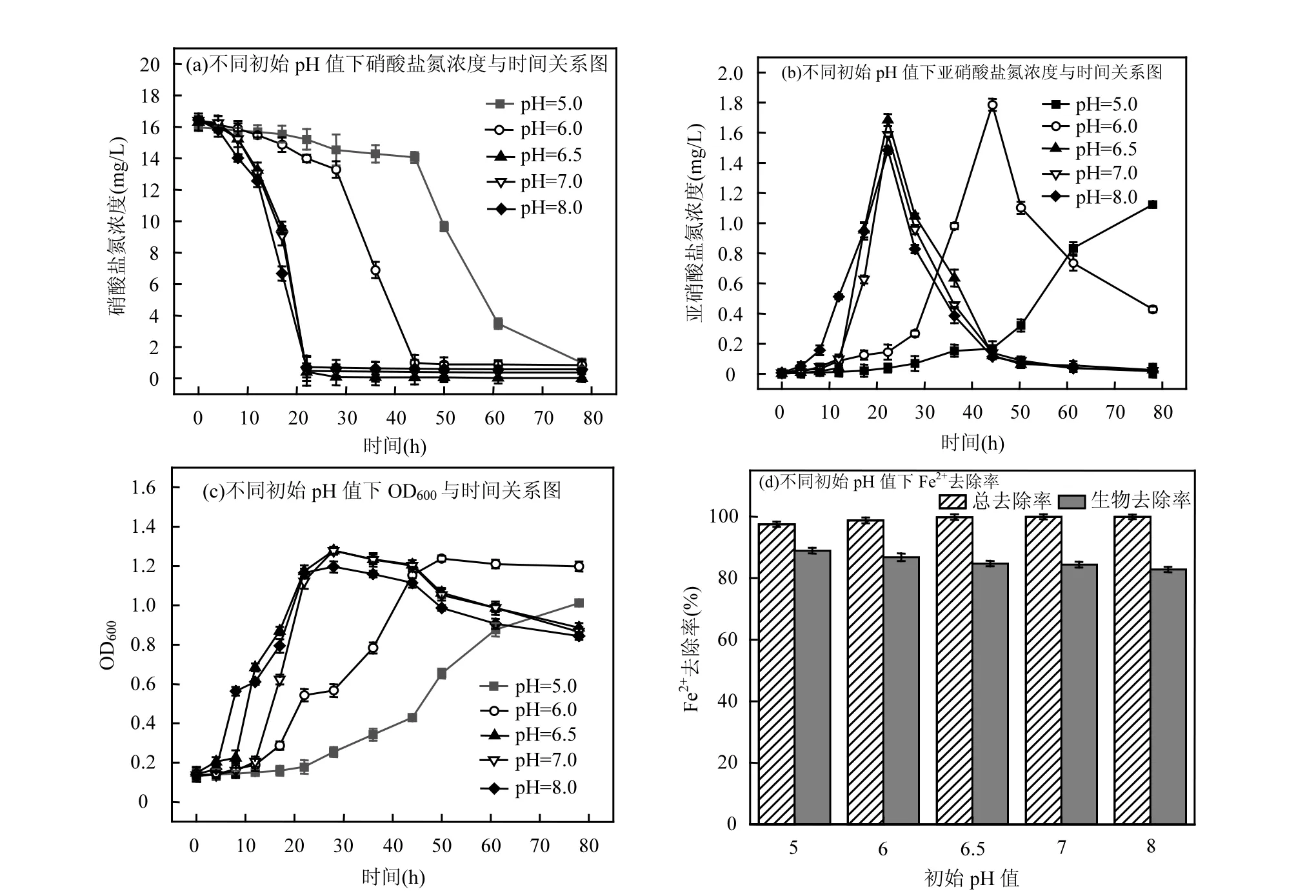
图5 初始pH值对Z13菌群脱氮影响Fig.5 Effect of initial pH on denitrification of Z13 bacteria
当初始pH值为7和8时,混合菌群Z13活性较高,脱氮速率更迅速,微生物对营养物质的吸收和酶的活力都较高[33].22h时,硝酸盐氮去除率达到94.57%和 95.62%.Fe2+总去除率达到 99.95%和99.93%.生物去除率为84.42%和82.83%,化学去除率为15.53%和17.10%.pH值在7~8范围内时Fe2+易被氧化,混合菌群Z13必须与非生物铁氧化过程竞争二价铁源.由实验结果可知,混合菌群Z13对中性和弱碱性环境适应性较强,相应的反硝化效果也较好.
pH值在5~8范围内时混合菌群 Z13均可进行反硝化,说明混合菌群Z13能够适应的pH值范围很宽,对 pH 的耐受能力很强,且整个反硝化过程中并未监测到 NH4+的生成.实验结果表明混合菌群 Z13的菌体生长及亚铁氧化和反硝化速率都与pH值呈较强的相关性.在一定的范围内,随着 pH 值的升高,菌密度也逐渐增加,反硝化速率逐渐加快.22h时,混合菌群Z13在pH=8时的硝酸盐氮去除率是pH=6时的 6.54倍.文献[34-35]中提到已发现的不同类型的亚铁氧化硝酸盐还原菌适宜生长的pH值范围具有一定的差异,最适的培养 pH值范围也并不统一,有的在pH值为6.5~7.5之间具有最佳的生长速率.本文中的反硝化菌群Z13的最适初始pH值范围为6.5~8.其中最佳初始pH值为6.5.
2.4.3 C/N对Z13菌群脱氮影响 在一定质量浓度范围内作为能源的有机碳源质量浓度越高,反硝化菌群的反硝化速率就越快[36].
由图6可知C/N为0时,78h时硝酸盐氮去除率为 19.30%, Fe2+的总去除率为 36.83%.由此可见,在不提供有机碳源的情况下, Fe2+作为唯一的电子供体,所提供的能量并不能满足菌体的生长,混合菌群Z13生长缓慢,活性和菌密度较低,脱氮性能及氧化Fe2+的能力也较低.当C/N增加为1时,78h时硝酸盐氮去除率为53.72%, Fe2+的总去除率为77.55%,生物去除率为 61.30%.表明添加少量的有机物作为共同电子供体时,相比仅使用 Fe2+做为电子供体,反硝化菌群的脱氮性能有所提升且亚铁氧化率也显著提高.这与文献[10,12]中的研究结果相一致.继续提高C/N为1.821,78h时硝酸盐氮去除率为99.85%, Fe2+的总去除率为 99.86%,其中生物氧化率为 88.30%,且亚硝酸盐氮的累积量达到最大值的时间也比C/N为1时提前,菌密度也有所增加.由实验数据可知,在C/N小于1.821时,混合菌群Z13脱氮效率随着C/N的增加而快速增长,这主要是因为初始的碳源越充足,反硝化菌群的生长速度越快.为进一步探究高C/N对混合菌群脱氮效率的影响以及考虑到资源浪费的问题,本实验将 C/N最高定为 4.此时混合菌群Z13的脱氮效率及Fe2+去除率基本不再增加而是处于平稳的状态,相比其他情况,脱氮速率有所增加,反硝化过程中亚硝酸盐氮的累积量也逐渐减少, 22h时最大累积量仅为0.244mg/L之后又快速消失,菌体的稳定期延长.因此,当C/N在0~4之间变化时,混合菌群Z13的亚铁氧化率及脱氮效率随有机碳源的增加而增加,但当提供的碳源远高于混合菌群的需求时,此时碳源已非限制性因素,混合菌群的生长和代谢活性处于稳定阶段,反硝化脱氮效率则不再增加而是处于基本稳定状态,此现象与文献[37]报道的相一致.且整个反硝化过程中并未检测出NH4+的生成,从实验结果可以看出,最佳的C/N为1.821.混合菌群Z13的贫营养特性为其将来应用于水源水生物脱氮创造了有利条件.

图6 C/N对Z13菌群脱氮影响Fig.6 Effect of C/N on denitrification of Z13 bacteria
2.3.4 Fe2+浓度对Z13菌群脱氮影响 图7中,不加Fe2+时,78h时硝酸盐氮的去除率为87.31%,亚硝酸盐氮的累积量为 3.721mg/L.此时乙酸钠作为唯一的有机碳源供菌群生长利用,其中硝酸盐氮的去除主要是通过反硝化完成[38],由于未加亚铁,电子供体不足使得当乙酸钠被消耗完之后微生物无可利用的物质,反硝化进行不完全,故会有亚硝酸盐氮的累积.混合菌群Z13在初始Fe2+浓度为5mg/L条件下,78h时硝酸盐氮的去除率为 91.95%,亚硝酸盐氮累积量为 2.25mg/L.Fe2+浓度为15mg/L时混合菌群Z13在78h时硝酸盐氮的去除率为 95.96%,亚硝酸盐氮累积量为1.603mg/L.说明Fe2+浓度为0~15mg/L时,还是不足以使反硝化进行完全.但是随着 Fe2+浓度的增加,硝酸盐氮的去除率也逐渐增大,亚硝酸盐氮累积量逐渐减小.这表明,微生物很可能利用了 Fe2+作为电子供体进行硝酸盐的还原,这与 Liu等[39]人文献中所报道的相一致.虽然 Fe2+与亚硝氮可发生化学反应,但是已有研究证明[40]在亚铁氧化硝酸盐还原过程中, 亚硝氮的还原过程存在生物和非生物共同作用,具体机制有待进一步研究.当Fe2+浓度为30和50mg/L时, 78h时混合菌群Z13反硝化作用完全,无亚硝酸盐氮的累积.这表明混合菌群Z13对硝酸盐还原时,亚硝酸盐氮是中间产物而不是最终产物,并且过程中未出现较高浓度的积累,生成后很快被继续还原[41],且全程并未检测出NH4+的生成.加入的 Fe2+浓度在 5~50mg/L 时,混合菌群Z13在78h内对Fe2+总去除率可达到98.0%以上,生物去除率能够保持在82.70%以上.由此可见混合菌群Z13对Fe2+去除效果表现出稳定而高效的能力,这与周志华等[29]的研究结果相一致.考虑到经济性问题,本实验Fe2+最佳加入量为30mg/L.

图7 Fe2+浓度对Z13菌群脱氮影响Fig.7 Effect of Fe2+ concentration on denitrification of Z13 bacteria
3 结论
3.1 本文从李家河和黑河水库底泥中驯化筛选出在低C/N条件下能够高效脱氮的亚铁氧化硝酸盐还原混合菌群 Z13.经高通量测序技术进行分析表明Z13菌群主要含有 Zoogloea、Geothrix、Dechloromonas、Ralstonia、Curvibacter、Caulobacter等菌属,为微污染水源水的原位生物脱氮提供菌源保障.
3.2 亚铁氧化硝酸盐还原混合菌群 Z13在低 C/N条件下能够高效脱氮, 78h时硝酸盐氮去除率和平均去除速率为99.85%和0.2087mg/(L·h),总氮去除率和平均去除速率为89.91%和0.1888mg/(L·h).Fe2+的总去除率为99.86%,其中生物氧化率为82.70%,无亚硝酸盐氮和氨氮的累积.
3.3 在温度 30℃,pH 6.5,C/N 1.821, Fe2+浓度30mg/L时,亚铁氧化硝酸盐还原混合菌群Z13对亚铁氧化和氮素的去除效果最好,为亚铁氧化硝酸盐还原混合菌群Z13在微污染水体生物脱氮提供科学依据.

