基于标准加入法的改进计算公式测定苹果中毒死蜱、戊唑醇残留量
武 源,覃慧丽
(柳州市质量检验检测研究中心,广西柳州 545006)
毒死蜱、戊唑醇常用于苹果病虫害的防治,属于苹果病虫害化学防治中的高频农药[1]。戊唑醇主要用于枝干轮纹病、干腐病、斑点落叶病、褐斑病等病害的防治[2],毒死蜱常用于桃小食心虫、苹果绵蚜等虫害的防治。农药在保障作物生长、提高作物产量的同时,也会对环境和人体产生一定副作用,例如戊唑醇属于难降解农药,在土壤、水体中的降解半衰期大于180 d[3],容易引发农药再残留问题。中高毒农药毒死蜱在苹果上的检出率高,在残留风险等级中属于高风险农药[4]。合理有效的检测手段有助于农药残留日常监督管理,从而提升食品安全生产质量,降低存在的残留和安全风险。
质谱法可提供化合物的分子质量和结构信息,由于质谱属于通用型检测器,在多农残快速筛查领域的应用越来越广泛[5-7]。食品中农药残留GC分析领域常见基质效应,是指待测组分受基质共流物的影响而导致响应增强或抑制的现象[8-12]。基质标准溶液替代溶剂标准溶液可以很好地解决基质效应带来的定量不准确的影响[13-15],但不是所有的样品都能找到不含待测物的空白基质[16],尤其面对能力验证实验样品或者待测物为内源性物质等复杂多样的样品[17-19]。
标准加入法是在待测样品中加入不同浓度的标准物质,保证了样品溶液和基质标准溶液在基质效应上的一致性,消除了基质共流物对分析物的影响,是目前解决基质效应最为可靠有效的定量方法[20-22]。查阅大量文献发现,标准加入法定量通常将标准工作曲线反向延长至与横坐标延长线相交,交点与原点之间的距离即为待测物的质量浓度[23-26]。基于标准加入法测定样品溶液浓度,传统计算公式视待测组分的响应值为曲线截距,且忽略了曲线截距与待测组分的响应值之间的距离对定量结果带来的偏差影响,所得浓度是不够准确的。笔者基于标准加入法,对比了传统计算公式和改进计算公式所得样品含量结果的差异,以“z-比分数”评价测得结果的满意度,为样品的准确定量提供新的解决方案。
1 材料与方法
1.1 材料与试剂
提取包5982-5650CH:4 g MgSO4,1 g NaCl,1 g柠檬酸钠,0.5 g三水合二柠檬酸二钠及1颗陶瓷均质子;净化试剂管5982-5256:885 mg MgSO4,150 mg PSA,15 mg GCB,美国安捷伦公司。
乙腈(色谱纯),德国Merck公司;丙酮(色谱纯),上海安谱实验科技股份有限公司;乙酸乙酯(色谱纯),上海安谱实验科技股份有限公司;毒死蜱(纯度99.89%)、戊唑醇(纯度99.30%)、环氧七氯B(纯度98.70%),德国Dr.Ehrenstorfer公司。
1.2 仪器与设备
7890B-7000D气质联用仪、VF-1701MS色谱柱(30 m×0.25 mm×0.25μm),美国安捷伦公司;XP26微量电子天平,瑞士Mettler Toledo公司;IKA VORTEX 4 basic涡旋振荡器,德国IKA公司;IKA VXR basic圆周振荡器,德国IKA公司;TTL-DCⅡ型氮吹仪,北京同泰联科技发展有限公司;SIGMA 3-30K离心机,德国SIGMA公司。
1.3 方法
1.3.1 标准溶液的配制
待测物储备液:精密称取毒死蜱、戊唑醇标准品于10 mL容量瓶中,丙酮溶解并定容至刻线。
内标储备液:精密称取环氧七氯B标准品于10 mL容量瓶中,乙酸乙酯溶解并定容至刻线。
混合标准溶液(10μg/mL):精密吸取适量的毒死蜱、戊唑醇标准储备液于20 mL容量瓶中,用乙酸乙酯定容,配制成混合标准溶液。
内标工作液(5μg/mL):精密吸取一定量的内标储备液,用乙酸乙酯配制成内标工作液。
系列混合标准工作液:根据实验需求,精密吸取不同体积混合标准溶液,用乙酸乙酯稀释定容,配制成所需混合标准工作液。
标准加入法标准曲线:准确称取若干份10 g不含待测物的空白样品于50 mL离心管,根据1.3.2样品前处理步骤制备好回收样品溶液(0.02、0.05、0.1 mg/kg 3个添加水平)氮吹近干,加20μL内标工作液并加入1 mL从0开始递增的一系列混合标准工作液复溶。以复溶加入标准工作液的质量浓度为横坐标,待测组分定量离子与内标定量离子响应值之比为纵坐标绘制标准曲线。
1.3.2 样品前处理
准确称取10 g待测样品于50 mL塑料离心管中,加10 mL乙腈并加入提取包5982-5650CH,盖上离心管盖,振荡器剧烈振荡1 min后于4 200 rpm离心5 min,吸取8 mL上清液至净化试剂管5982-5256中,立即摇散,涡旋混匀1 min,4 200 rpm离心5 min,准确吸取1 mL上清液于10 mL试管中,40℃水浴中氮吹至近干,加入20μL的内标工作液,加入1 mL乙酸乙酯复溶,0.22μm滤膜过滤后上机测定。
1.3.3 GC-MS/MS条件
1.3.3.1 色谱条件
1.3.3.2 质谱条件
电子轰击源:70 eV;离子源温度:280℃;传输线温度:280℃;溶剂延迟:3 min;多反应监测MRM模式。化合物采集离子对信息见表1。
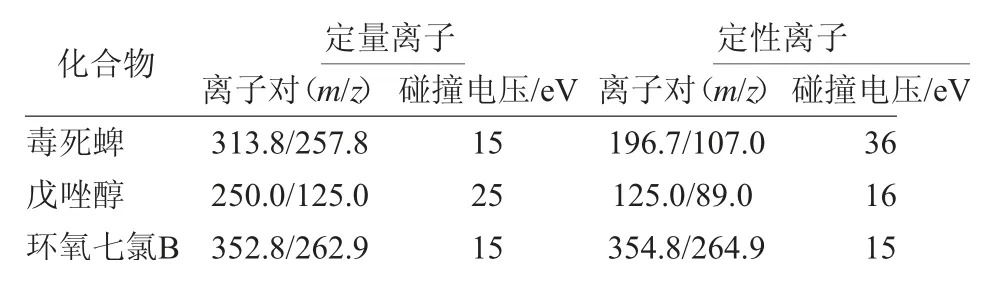
表1 化合物定量离子对、定性离子对和碰撞能量
2 结果与分析
2.1 质谱条件的优化
化合物质谱分析的子离子选自其在质谱离子源轰击中形成的碎片离子,不同子离子抗干扰能力也有差异。优化电压,选择抗干扰能力强、丰度值高的离子对有助于提高定量的准确性和灵敏度,提高化合物在仪器上的响应。取1μg/mL溶剂标液进样,优化化合物离子对参数。
毒死蜱常见的离子对有313.8/285.5、313.8/257.8、196.7/107.0、313.8/193.8,其中313.8/285.5和313.8/193.8离子对响应弱,信噪比远远低于其他2对离子对的信噪比。通过优化电压得到最强丰度响应,313.8/257.8最适电压为15 V,196.7/107.0最适电压为36 V,选择响应最高的313.8/257.8为定量离子对。
戊 唑 醇 离 子 对 有252.0/127.0、250.0/125.0、125.0/99.0、125.0/89.0。4对离子对中,252.0/127.0和125.0/99.0响应较弱,不利于定量分析,故选择250.0/125.0、125.0/89.0为确定离子对。进一步优化得到250.0/125.0、125.0/89.0的最佳电压分别是25 V和16 V,选取丰度值最高的250.0/125.0为定量离子对。
同理优化得到环氧七氯B定量离子对为352.8/262.9,电压为15 V,定性离子对为354.8/264.9,电压为15 V。
2.2 线性关系和基质效应
准确称取空白样品若干份,根据1.3.2样品前处理步骤制备得空白基质溶液。精密吸取1 mL净化后的空白基质溶液于40℃水浴氮吹近干,加入20μL的内标工作液,并准确加入1 mL系列浓度的混合标准溶液复溶,以待测组分与内标响应值之比(y)对复溶加入标准溶液的质量浓度(x)做基质标准曲线。毒死蜱在21.86~874.4 ng/mL线性范围内线性良好,线性方程y=0.021 7x-0.259 1,相关系数为0.999 0;戊唑醇在24.16~966.4 ng/mL线性范围内线性良好,线性方程y=0.041 8x-0.236 2,相关系数为0.999 2。
以基质标准曲线与溶剂标准曲线斜率的比值考察基质效应(ME)[27]。由于仪器浮动的影响,当斜率比值为0.9~1.1,基质效应忽略不计;当斜率比值>1.1,为基质增强效应;当斜率比值<0.9,为基质抑制效应[28]。本实验结果显示,毒死蜱ME值为7.4,戊唑醇ME值为25.9,毒死蜱和戊唑醇均为基质诱导增强效应,且戊唑醇基质增强效应大于毒死蜱。苹果基质共流物对毒死蜱和戊唑醇的诱导影响较大,基质标准溶液可消除内源性和外源性共流物对分析物的影响,定量更准确。对于无法得到空白基质的样品,标准加入法结合本实验改进计算公式可准确获得阳性样品溶液浓度。
2.3 回收率、精密度和定量限
准确称取若干份10 g空白苹果样品,分别加入不同浓度的混合标准溶液(0.02、0.05、0.1 mg/kg 3个添加水平),静置30 min后,按照1.3.2样品前处理步骤制备样品溶液,不同添加水平样品制备6份平行样以考察方法可行性及稳定性。结果表明,3个添加水平下苹果中毒死蜱回收率在99.3%~106.0%,精密度在3.6%~4.9%;苹果中戊唑醇回收率在96.3%~103.8%,精密度在3.3%~4.2%,回收率和精密度均符合实验室质量控制的要求[29](表2)。
水利枢纽工程安全监测系统在设计开发中,不仅涉及多个学科,还会涉及多个专业,因而在设计过程中能够集中多个领域的优势。从专业知识的角度来说,水利枢纽工程安全监测系统设计主要设计的专业有传统的水利专业、现代的微电子专业、通信专业以及自动控制专业等。水利枢纽工程安全监测系统开发是一项整体的工程,且建成后会发挥重要的作用。
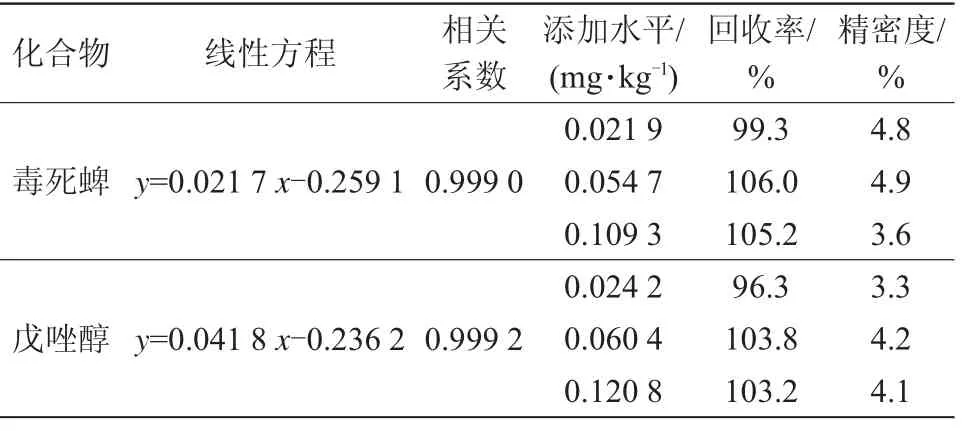
表2 毒死蜱、戊唑醇线性方程及添加回收结果(n=6)
以10倍信噪比对应的添加水平确定方法定量限。根据前处理稀释倍数及样品称样量,得到苹果中毒死蜱和戊唑醇方法定量限分别为0.003 mg/kg、0.001 mg/kg,满足日常检测的需要[30]。
2.4 标准加入法改进计算公式推导
对阳性待测样品采用标准加入法进行定量时,以加入样品中标准溶液的质量浓度为横坐标(x轴),待测组分响应值为纵坐标(y轴)绘制阳性样品的基质标准曲线(图1a)。常规的标准加入法计算方式[23-26]是将标准曲线反向延长至与x轴相交,交点与原点间的距离对应的质量浓度即为待测组分的质量浓度(y′=0时所对应的x值),详见常规式(1)。
式中:C为从基质标准曲线得到的待测组分溶液浓度,单位与横坐标一致;b′为标准加入法基质标准曲线的截距;k′为标准加入法基质标准曲线的斜率。
假设存在与测定样品匹配的空白基质,则以此空白基质溶液同法可配制得阴性样品的基质标准曲线(图1b)。比较2条标准曲线可知,同类样品基质效应相同,阴性基质标准曲线与阳性基质标准曲线各点的加标质量浓度相同,各点响应值差别只有阳性样品本底值A′。由于同一阳性样品溶液中质量浓度水平恒定,则本底浓度在相同仪器条件下的响应值A′保持恒定,因此理论上2条标准曲线是斜率相等,截距不同的平行线段,截距差值即为阳性样品的响应值带来的本底增量A′。故2条标准曲线关系有k′=k0,b0=b′-A′。
色谱分析中,空白基质应未检出目标物质,即阴性基质标准曲线0点的响应值A0=0。在阳性样品溶液中加入从0开始递增的一系列混合标准溶液,阳性基质标准曲线0点的测得响应值为A测=A′+A0=A′+0=A′。采用基质标准曲线法定量,将待测物质在仪器上的响应A测带入阴性基质标准曲线y=k0x+b0即可得出待测组分溶液浓度[31-32]。根据上述推导关系得改进的式(2)。未知量k0、b0均转化至已知k′、b′、A测,阳性样品含量可解。
式中:A测为标准加入法阳性基质标曲0点的测得响应值(内标法则为待测组分与内标响应值之比)。
根据“最小二乘法”原则确定回归方程,A测为标准加入法阳性基质标曲0点的测得响应值,与直线方程存在一定的偏离度[33-34],A测往往与b′并不重合,即|b′-A测|≠0。传统计算公式以b′/k′计算样品浓度,直接用截距b′代表阳性样品响应值A测,从而忽略了b′与A测之间差值对定量结果带来的误差,导致所得浓度不够准确。改进计算公式克服了上述不足,更好地诠释了浓度与响应值之间的定量关系,由此得到更准确的待测组分溶液浓度。
2.5 标准加入法的2种计算公式对结果的影响
按照1.3.2样品前处理步骤,以回收样品溶液为测定溶液,氮吹近干后加入20μL的内标工作液,加入1 mL从0开始递增的一系列混合标准溶液,以复溶加入标准溶液的质量浓度为横坐标,待测组分定量离子与内标定量离子响应值之比为纵坐标绘制标准曲线。用“z-比分数”评价标准加入法的2种计算公式定量结果的准确性,详见式(3)。
式中:x为样品测定值;X为指定值(本实验为添加水平),σ为标准差。当|z|≤2时,测得结果满意;当2<|z|<3时,测得结果有问题(可疑);当|z|≥3时,测得结果不满意(离群)。
从表3看出,2种计算公式得到的毒死蜱、戊唑醇样品含量结果的z值均小于2,测试结果均满意;2种组分根据改进计算公式得到的z值均小于传统计算公式得到的z值,改进算法优于传统算法。2种计算公式得到的z值在低浓度添加水平下(0.02 mg/kg)差异不显著,但在中高浓度添加水平下(0.05、0.1 mg/kg)z值差异显著。改进的计算公式得到的z值远远小于传统计算公式计算的z值,与真值更接近。基于标准加入法采用改进公式计算样品含量,得到的样品结果准确性更高,可靠性更强,为样品准确定量提供了新的解决方案。
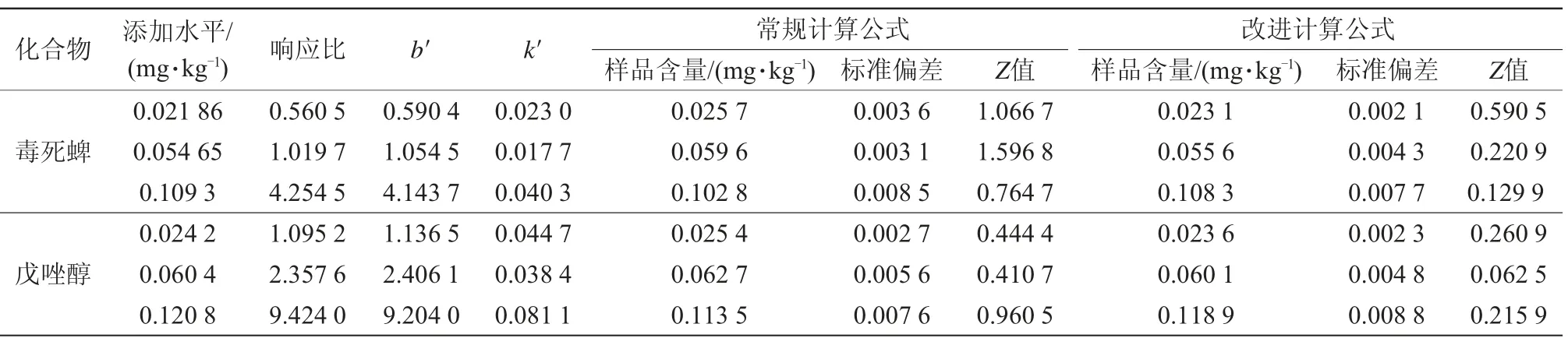
表3 标准加入法不同计算方式对定量结果的影响(n=6)
3 结 论
本试验前处理在食品安全国家标准GB 23200.113的基础上,基于标准加入法建立了苹果中毒死蜱、戊唑醇残留量的分析。在标准加入法定量方式上,采用2种计算公式计算样品含量。结果显示,常规和改进计算公式均能满足常规定量使用,但改进计算公式得到的样品含量准确性和可靠性更高,适用于果蔬基质中农残的准确定量。当前处理方法回收率满足测定要求,操作稳定性好。样品中待测物质溶液浓度在仪器上有较好的响应时,基于标准加入法结合改进计算公式,也可用于能力验证样品、特殊基质样品和内源性物质样品的准确定量。

