碳点的合成、光学性能及生物应用
陈 一,朱雪儿,周沁雨,马文君,曾德柳,张和凤
(汕头大学理学院化学系,广东 汕头 515063)
0 引 言
2004 年Scrivens 等[1]在单壁碳纳米管电泳纯化过程中偶然发现了碳点(Carbon Dots,CDs),与传统半导体量子点及有机染料相比[2-3],碳点具有低毒性、良好的生物相容性、较强的化学惰性、高抗光漂白性、易改性和优异的电子性能等优点,在传感[4-5],发光器件[6],光催化[7],特别是在生物应用方面如生物传感[8-9],生物成像[10-11],药物负载[12-13]和光诊疗[14-15]等领域得到了广泛的研究和关注.人们对碳点的原始材料、制备方法和潜在应用进行了大量的研究,合成出了各种各样的碳点[16],极大地丰富了碳材料家族.根据碳核的不同,碳点主要可分为三种类型:石墨烯量子点(Graphene Quantum Dots,GQDs)、碳纳米点(Carbon Nanodots,CNDs)和聚合物点(Polymer Dots,PDs)(图1a).其中,单层石墨烯点(Single-layered GQDs,s-GQDs)以一层石墨烯碎片作为碳核,多层石墨烯点(Multi-layered GQDs,m-GQDs)具有石墨化的纳米晶结构特征;碳纳米点是一种没有明显晶格的准球形碳纳米粒子,主要由sp2/sp3碳或非晶态碳嵌入sp2杂化的纳米晶区组成;聚合物点是由线性聚合物或单体经聚集或交联衍生的聚合物纳米粒子[17-20].碳点的多样性主要归因于碳源与合成方法的不同,目前碳点的合成策略主要有“自上而下”和“自下而上”两种.“自上而下”的合成策略是通过直接剥离石墨、石墨烯、碳纤维等较大的碳源产生纳米级碳点,并进行一定的表面处理;“自下而上”的合成过程是小分子或聚合物前驱体经过脱水或自组装再经过碳化形成碳点[17-18].需要说明的是,“自上而下”的合成策略有利于合成结晶度高、结构完整的石墨烯点或碳纳米点[21-22],而“自下而上”的合成策略通常会产生具有非晶态碳核、掺杂位点丰富和表面官能团多的碳点[23-24].碳点材料的形貌特征、性能及应用与其合成方法密切相关.发展高效的合成方法,有利于解决碳点领域长期存在的难题,如碳点的精确控制、大规模制备和发光机理与发光基团精细结构等.

图1 a)碳点的分类;b)碳点的主要制备方法
碳点通常被定义为尺寸小于10 nm、表面经过钝化并拥有明亮荧光的碳纳米粒子[25].其独特的光物理和化学性质促进了成像探针、高性能纳米传感器和多重纳米复合材料的发展.优异的生物相容性和体内清除性理想地满足了体内应用的要求,成为了生物应用研究的理想材料[26].表面钝化是它们荧光性质的关键[19],所制备的碳点具有许多反应基团,可以被其他化学基团修饰,而表面功能化或钝化的碳点可以提高其量子产率和荧光发射[27](图2),进而满足生物应用的要求.Xie 等[28]通过激光烧蚀合成碳点时发现,得到的样品及其悬浮液并没有光致发光行为,但是进行表面钝化即将有机物种附着在酸处理后的碳颗粒上之后,就会展现出明亮的荧光.Liu 等[29]发现原始碳点会引起细胞氧化应激,降低细胞活力,但用聚合物修饰后便没有显示任何异常的细胞周期. 这些结果表明,碳点的表面化学对其荧光性质及生物相容性起着至关重要的作用.另外,丰富和可调谐的官能团,如氨基、羧基或羟基等,赋予了碳点携带治疗剂和靶向剂的能力,与适当的分子和治疗药物链接能够产生热敏纳米医学效应.同时,碳点的荧光性能提供了动态和实时监测药物分布和反应的机会[30].因此,使用“量身定制”的分子对所合成碳点进行合适的表面修饰过程是实现碳点生物应用的关键[31].本文将在第三节对近几年来通过碳点表面功能化以促进生物应用方面的研究进行综述,并总结研究人员通过碳点表面工程提高其量子产率和稳定性同时降低细胞毒性以拓展碳点在生物应用领域的进展.

图2 不同的表面修饰过程导致的不同荧光发射
此外,发光机理一直是碳点领域的研究前沿,碳点的多样性以及表征方法的缺失,揭示碳点发光基团精细结构还存在较大的挑战.尽管近年来取得了一些进展,但碳点的实际发光机制仍存在争议,发光基团的精细结构依然不甚清晰.本文第二节将系统总结现有的碳点发光机理.
1 合成策略及方法
1.1 “自上而下”合成策略
“自上而下”的合成策略是通过剥离或刻蚀较大的碳材料(石墨、石墨烯、碳纳米管、炭黑、煤等),形成较小尺寸的纳米粒子.该合成策略简单高效,但在具体合成过程中,难以对实验条件精准控制,从而导致得到的碳点往往具有较宽的尺寸分布.虽然透析等方法可以对得到的碳点产物进行分级,但分级过程费时费力,在一定程度上限制了该合成策略的广泛应用.目前,用于“自上而下”合成策略的方法主要有电弧放电、激光刻蚀、电化学和化学剥落等方法.
1.1.1 电弧放电法
碳点最早发现于电弧放电法.Xu 在利用电泳法分离由电弧放电法制备的单壁碳纳米管过程中首次发现了碳点[1].作者发现在365 nm 光激发下其发出明亮的荧光,进一步的洗脱将混合荧光带分离为蓝绿、黄、橙亚发射带(图3a 和图3b).元素分析表明,这些纳米点仅含有C(55.93%)、H(2.65%)、N(1.2%)和O(40.33%).Zhang 等[32]以电弧放电法制备碳纳米管得到副产物石墨杂质,离心分级后得到了粒径分布较窄的石墨碳点.经混酸氧化后,产物的荧光性能得到显著提高,发射强绿色荧光.有趣的是,荧光表征结果表明,所制备的碳量子点最大发射波长约为502 nm,与激发波长无关,且显示出荧光双转换的特性(图3c 和3d),作者将其上转换荧光归因于碳点的多光子活性过程.
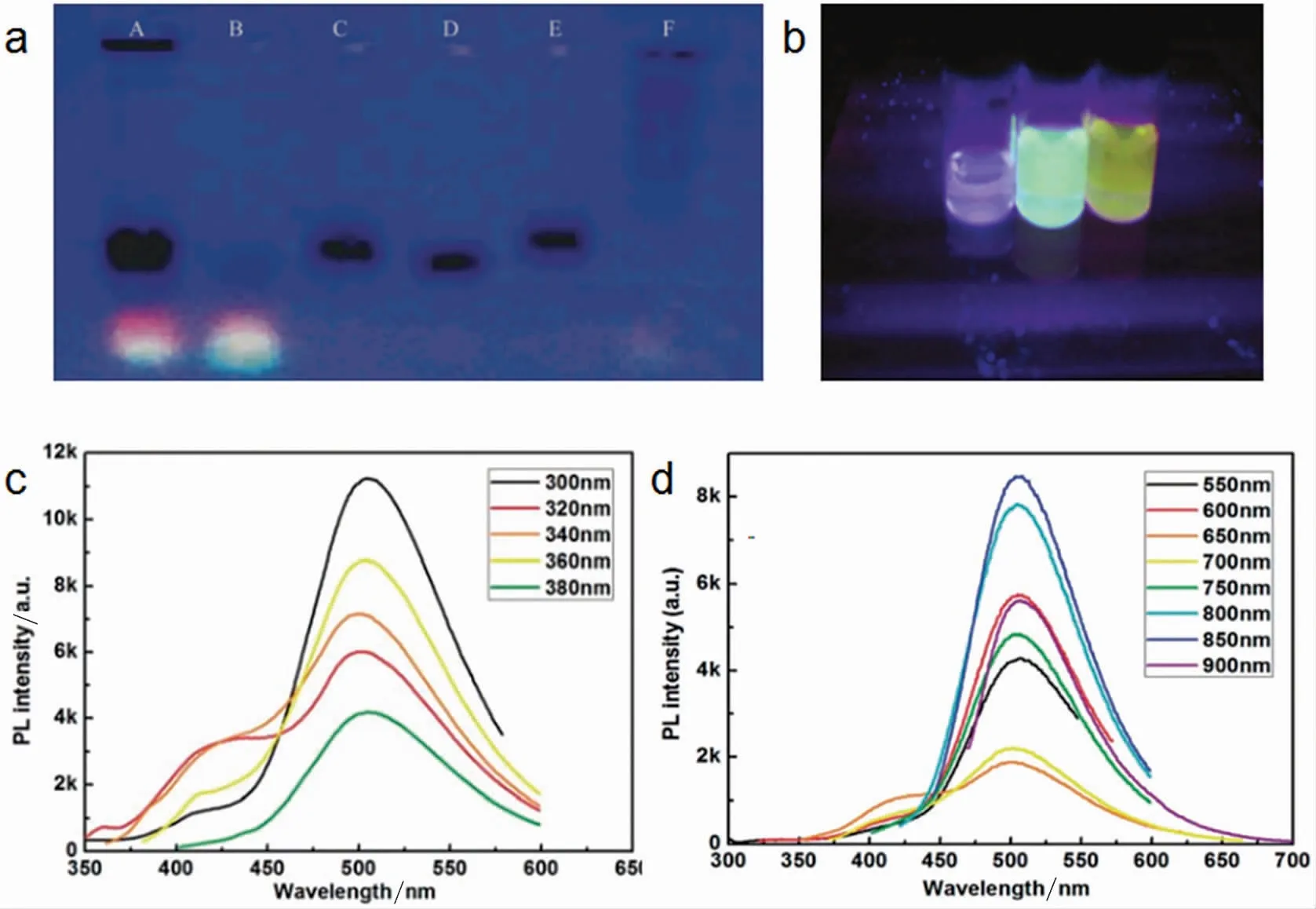
图3 a)在365 nm 紫外光下1%琼脂糖凝胶中的电泳图谱;b)在365 nm 紫外灯下不同组分图片;c)不同激发波长的荧光光谱;d)不同激发波长的上转换荧光光谱
1.1.2 激光刻蚀法
2006 年,Xie 等[28]以石墨和水泥热压制备的碳靶为碳源,利用激光烧蚀制备得到碳纳米颗粒,并利用硝酸对其进行表面钝化.结果表明,在简单有机物附着碳点表面后,原不发光的样品经光激发后发射出明亮的荧光,并将这种荧光纳米粒子命名为碳量子点.作者发现碳点的光致发光光谱通常较宽,其最大发射波长取决于激发波长,并将这种激发波长依赖性的荧光行为归因为样品尺寸的宽分布和碳点内荧光基团的分布不同.随后,研究人员对上面的方法进行了改进,将激光烧蚀和表面改性在一步反应中完成[33],改进了合成碳点的方法.
1.1.3 电化学方法
2007 年Ding 等[34]首次提出了从多壁碳纳米管中合成蓝光碳点的电化学方法. 作者以四丁基高氯酸铵为电解质,在脱气乙腈溶液中对多壁碳纳米管进行电化学处理后得到碳点材料.Zhang 等[35]在采用电化学方法合成碳点时发现电解质环境对碳点的形成起着重要的作用,当采用碱性电解质时(NaOH/EtOH),可以成功合成碳点,而酸性电解质(例如H2SO4/EtOH)则无法生成碳点.Liu 等[36]采用电化学氧化方法以石墨电极为碳源在碱性醇溶液中制备得到较高量子产率(QY=11.2%)且结晶度高的碳点.电化学方法为荧光碳点制备提供快捷、温和的途径[37],通过调整外加电位和电流密度,可以控制碳点的尺寸、组成和荧光性能[38].
1.1.4 化学剥落法
2007 年,Mao 等[39]首次发展了化学剥落法,以酸性氧化物处理蜡烛燃烧的烟尘合成了碳点.随后,人们以碳水化合物[40],炭黑[41],活性炭[42]等材料为碳源,通过化学剥落法成功制备了相应碳点材料.Ajayan 和Zhu 等[43]报道了从化学剥落碳纤维中成功合成碳点的研究方法,将碳纤维加入浓酸中进行2 h 超声处理,然后剧烈搅拌并将混合物加热24 h 后,得到了尺寸分布较窄(直径在1-4 nm 之间)的碳点.结果表明,通过控制反应温度,可以制备不同尺寸的碳点,并可以调节碳点的光学性质.Huo 等[42]利用化学剥落法合成碳点(QY=1.5%)后,使用胺端化合物作为表面钝化剂对碳点表面进行改性,有效提高了其荧光量子产率,量子产率达到12.6%.需要说明的是,现有化学剥落法合成效率往往较低,并且通常需要通过表面钝化过程提高碳点荧光量子产率.
1.2 “自下而上”策略
1.2.1 热解法
一些热力学不稳定的小分子可以在高温下直接碳化形成碳点,因此被成功发展成为一种快速有效合成荧光碳点的方法.2008 年,Giannelis 等[44]首次通过热解法合成得到碳点,通过不同柠檬酸铵盐或4-氨基安替比林在溶液中的热分解,一步合成得到功能化的碳点材料. 制备的碳点平均尺寸小于10 nm,具有明显的激发波长依赖性. 之后,作者较为系统地探索了碳点的热解过程[45],发现随着温度从180°C 升高至400 °C,碳点的碳化程度升高,但荧光亮度和荧光量子产率明显下降.近年来,含杂原子碳点的制备得到较多关注. Huang 等[46]采用两步碳化法制备了L-半氨酸修饰的手性碳点LC-CQDs,首先在200°C 下热解柠檬酸20 min,制备得到具有羧基的碳点之后,利用L-半氨酸的氨基在200 °C 下对碳点表面进行化学修饰,得到了具有手性和高荧光性能的碳点(QY=68%).
1.2.2 微波辅助法
微波具有加热效率高、消耗时间少和成本低等优点,在碳点合成中得到越来越多的应用.2009 年,Yang 等[46]利用微波辅助加热合成了碳点.作者将聚乙二醇(PEG-200)和糖类(葡萄糖、果糖等)溶于去离子水中形成透明混合物,经微波炉加热后,透明溶液被碳化生成碳点产物,并且加热时间被成功用于调控碳点的尺寸.X 射线光电子能谱表明,碳点的主要成分是碳和氧,丰富的亲水官能团赋予了该类碳点良好的水溶性.Cui 等[47]报道了量子产率为44.9%的蓝光发射碳点.Guo 等[48]利用微波辅助法制备出固态的Si-CDs,量子产率达到65.8%.Lau 等[49]和Lin 等[50]通过微波方法分别实现了碳点的深紫外和近红外发射.
1.2.3 溶剂热合成法
小分子可以在水或有机溶剂中通过缩合、聚合、碳化和钝化过程形成碳点,特别是水热法已经成为应用最为广泛的碳点合成方法.2011 年,Wang 和Li 等[51]报道了通过水热法合成碳点的方法.在磷酸单钾存在下,作者对葡萄糖进行水热处理合成得到荧光碳点,并且可以通过简单地调节磷酸单钾的浓度来调节碳点产物的荧光行为.Chang 等[52]发现含有氨基和羧酸基团的有机分子有利于碳点的形成,并且氢键在分子组装过程中起着关键的作用,他们将碳点的形成过程归为脱水、聚合、碳化和钝化四个步骤.Sun 等[53]以柠檬酸和乙二胺为碳源和氮源,利用溶剂热合成法成功制备出高亮荧光碳点,其在水中的荧光量子产率高达94%.Qu 等[54]以叶酸为前驱体,制备了高荧光叶酸改性的碳点,其在水中的量子产率高达94.5%,更重要的是,碳点表面残留的叶酸对癌细胞有良好的靶向能力,为肿瘤的诊疗提供了可能性.溶剂热法中溶剂的性质、反应温度和时间对碳点的形成及碳化程度有显著影响,直接决定了碳点的发光效率和光学性能.
1.2.4 模板法
虽然多种方法已经被发展出来,但碳点结构的精准控制,特别是碳点的“按需合成”仍存在较大挑战.近年来,模板法被成功应用于纳米材料的精确合成.硬模板或软模板都可以作为具有受限空间的纳米反应器,用于“自下而上”合成所需尺寸的纳米结构.相应地,选择合适的模板可以有效地抑制聚集问题,形成具有较窄尺寸分布的碳点,使用模板法可以实现碳点尺寸和形貌的可控性.Li 等[55]以介孔二氧化硅球为硬模板,柠檬酸为碳源,高温碳化后,经过刻蚀二氧化硅,得到尺寸为1.5~2.5 nm 的亲水性碳点. 随后,Liu 等[56]首次提出了一种软硬模板方法,即以共聚物Pluronic P123 为软模板,有序介孔二氧化硅SBA-15 为硬模板,制备了多种结构规整且具有上转换光致发光行为的碳点,其中尺寸较窄的分布为CDDAB:(3.0±0.4)nm,CD PHA:(4.4±0.4)nm.Zhang 等[57]利用不同孔径的金属- 有机骨架材料(MOFs)作为模板,经过葡萄糖碳化和MOFs 刻蚀,合成一系列具有高度规整结构的碳点(图4).

图4 碳点尺寸与相应的MOFs 模板孔径对比
2 光学性能
虽然碳点具有较好的光稳定性和激发波长依赖性等特殊的荧光行为,但现有碳点发光亮度和荧光效率仍普遍较低,且荧光多为蓝绿光.另外,碳点材料的微观结构仍不清晰,发光机理还存在一定争议.由于碳点微观结构和发光机理的复杂性,系统整理总结现有碳点的光学性能和可能的发光机理将有力推动高荧光性能碳点的制备和应用的进展.
碳点的光致发光通常呈现宽峰发射,并且最大发射波长取决于采用的激发波长,具有明显的激发波长依赖性.Xie 等[28]利用激光烧蚀法制备碳点时发现了碳点这种与其硅对应物[58]相似的荧光行为,即同一样品在不同的激发波长下会发出不同颜色的荧光,他们将其归为样品中不同粒子尺寸的影响和每个钝化碳点上发射位点的分布不同的影响.目前,对于碳点荧光行为的激发波长依赖性形成了多种解释:表面缺陷机制[59-61],尺寸效应[62],碳核的形成[63]及溶剂驰豫[64].一般认为,碳点的激发波长依赖性行为是由以上一种或几种因素作用导致的.碳点的这种激发波长依赖性行为使碳点可以在不同的激发波长下实现细胞和组织的多色成像,且在长波长激发下使其发射波长能够位于近红外区域,为体内较深层组织成像及肿瘤诊疗提供了可能性[65-66].
除了具有激发波长依赖性,现有报道中少量碳点还表现出与激发波长无关的荧光发射行为.Veca 等[67]通过向碳点中引入氧化锌和硫化锌,得到了具有上转换荧光特性的产物,即在波长为800 nm 的激发光下,碳量子点发出绿色荧光.Zhang 等[32]以电弧放电法制备碳点时发现,其制备的碳点具有荧光双转换特性(图3c 和3d),即当激发波长从300 nm 变化到380 nm 时,相应的荧光光谱几乎保持不变,在502 nm 处呈现出较强的发射峰,作者将其解释为碳点表面相对均匀且官能团种类较少;当激发波长从550 nm变化到900 nm 时,展现出上转换荧光,荧光图谱与其下转换荧光图谱类似.作者将上转换荧光归因于碳点的多光子活性过程,即两个或多个光子的同时吸收导致的反斯托克斯型发射.Callan 等[68]设计了一种与敏化剂原卟啉IX 相连的碳点,通过荧光共振能量转移(FRET)介导的方式,在800 nm 激发波长下发出上转换荧光,使敏化剂敏化,进而产生大量的单线态氧以杀死较深层组织的肿瘤细胞.
另外,光稳定性是指在长时间持续激发时荧光发射强度维持稳定的能力.与有机荧光染料相比,碳点具有较高的光稳定性,即使在激发光源或者氖灯的持续照射下,也无光漂白现象,依旧能保持原有的荧光强度.
2.1 发光机理
碳点的发光机理是碳点领域的核心科学问题,清晰的机理对调节其光学性能以及高性能碳点的合成具有重大的意义.虽然碳点的发光机理长期以来一直是人们探索的重点,然而,由于碳源的多样性和碳化方法的不同,众多因素在不同类型的碳点荧光发射过程中起着不同的作用,导致碳点结构多样,且对碳点微观结构的探索手段还不完善.迄今为止,碳点的发光机理仍存在较大挑战,主要体现为荧光来源及精细结构依然不甚清晰和发光机制仍存在争议.目前,得到较为普遍认可的机理主要有:量子尺寸效应,表面态效应,分子态和碳核态,交联引起的荧光增强效应(CEE 效应),多种荧光机理同时存在,又相互影响.
2.1.1 量子尺寸效应
目前,多种由不同碳源和碳化方法制备的碳点均表现出与尺寸相关的荧光行为,即量子尺寸效应.Lee 等[69]利用电化学方法结合分级纯化,制备了尺寸为1.2~3.8 nm 的碳点.荧光结果表明,碳点荧光性质随碳点尺寸的变化而不同.如图5a 所示,随着碳点尺寸从1.2 nm 增加至1.5-3 nm 和3.8 nm,其荧光最大发射波长从紫外光区红移至可见光区和近红外区.另外,如图5b 所示,Yang 等[70]通过采用不同的前驱体和碳化时间,合成出了尺寸分别为1.95 nm,2.41 nm,3.78 nm,4.90 nm 和6.68 nm 的碳点,其发射峰分别是430 nm,513 nm,535 nm,565 nm 和604 nm.然而,Rhee 等[71]通过模板法合成碳点时,发现随着尺寸从1.5 nm 增大到2.5 nm 后,碳点的荧光发射波长不增反降.因此,合理控制碳点尺寸和优化其化学结构可以使其荧光发射发生红移,有利于制备长波长发射碳点.

图5 a)不同尺寸碳点的荧光行为;b)适当调控反应前驱体和碳化时间以合成不同尺寸和荧光发射的碳点
此外,碳点的尺寸也会影响其荧光寿命. Lau 等[72]制备了水溶性单分散晶体(GQD),直径在(1.5±0.55)~(3.9±0.55)nm 之间,其中GQD 的直径越大,平均荧光寿命越短.
2.1.2 表面态效应
碳点具有丰富的表面官能团,不仅可以有效增加其能级分布,同时也可以导致一定程度的表面缺陷,经光激发后,表面态的发射阱将主导发射.较高程度的表面氧化或其他有效的表面修饰可以产生更多的表面缺陷,从而为调控碳点的荧光行为提供可能.如图6a 所示,表面态的荧光基团由化学基团和碳核间的相互作用形成.虽然碳点中荧光的来源尚不清楚,但越来越多的证据表明,荧光发射既来自碳核内部受限的sp2共轭产生的能隙变化,也来自表面状态产生的外部荧光,这种表面状态既可以由碳核能隙的能量转移直接激发,也可以由能量转移激发. Tang 等[73]探索了碳点在不同温度下的荧光行为,发现碳点表现出双发射带且具有相似的温度依赖性,作者将双荧光带归因于碳核和表面状态发射(图6b). 随后,Tang 等[74]提出,碳点的双发射带是由本征态和表面态所致,其中带I 起源于碳核内部受限的sp2共轭产生的能隙,能隙由sp2共轭结构的大小和形状决定,而带II 起源于表面态,表现出较宽的荧光发射范围.在此基础上,通过控制sp2共轭结构的尺寸或对碳点表面进行修饰,实现了碳点的可调谐荧光发射.

图6 碳点表面态发光机理图
2.1.3 分子态和碳核态效应
分子态效应与表面态不同,如上所述,表面态的荧光中心由化学基团和碳核的相互作用形成,而分子态完全由有机荧光团形成荧光中心,其荧光团连接在碳骨架的表面或内部,可以直接实现荧光发射.如图7 所示,通过小分子碳化(“自下而上”路线)制备碳点过程中,低温下形成小的荧光团分子(分子态)随着碳化温度的升高,初始分子脱水或由所形成的荧光团进一步碳化形成碳核,荧光团具有较强的荧光发射和较高的量子产率,而碳核态具有较弱的荧光行为和较高的光稳定性.Giannelis 小组[75]以柠檬酸(CA)和乙醇胺(EA)为模型对碳化过程进行了较为系统地探索,首次从分子态和碳核态两个方面探索了碳点的形成机理.作者发现,在180°C 下热解得到一种分子前驱体,荧光量子产率达50%.在较高的温度(230°C)下,碳核开始形成,荧光发射来源于分子荧光团和碳核.然而,这些CNDs 的量子产率只有15%,显著低于上述50%,表明大量的荧光团被用作碳核的构建.特别是在更高的温度(300 °C 和400°C)下,得到了主要或仅由碳核组成的碳点,量子产率进一步明显下降.碳核结构的荧光淬灭促进了相邻分子态的发射,这也在一定程度上解释了在高温下制备的碳点具有较低的荧光性能.类似的,Yang 等[76]以CA 和乙二胺(EDA)为模型分子研究了分子和碳核态.他们发现在反应温度小于150°C时,形成了一种高QY 的荧光团;在150~250 °C 的反应温度下,CA 和EDA 既形成了荧光分子,又形成了交联聚合物骨架,荧光主要是由CNDS上连接的形成的荧光团引起的;在高温下(超过300°C),由于进一步碳化,部分荧光团被消耗以进一步形成碳核,荧光性能降低.

图7 碳点碳核态发光机理过程
2.1.4 聚合物碳点中交联结构促进荧光发射效应(CEE)及蓝光起源
由热力学不稳定的碳源通过脱水、缩合、碳化或组装路线制备的非共轭聚合物点,具有高度交联的化学结构.高度交联的拓扑结构强烈限制了碳点内各基团的运动,也就抑制了各种非辐射跃迁,从而实现荧光增强,这种现象即交联导致的荧光增强效应(CEE).目前,CEE 效应得到了较为广泛的认可.与荧光共轭聚合物通过组装形成的共轭聚合物点和具有大共轭结构的石墨烯点不同,非共轭聚合物点是具有高度交联和致密结构的聚合物,其荧光中心来源于其重复单元荧光团,并且荧光团的荧光性能被CEE效应有效放大.Liang 等[77]通过分段共聚物的自组装制备了两亲性的PDs,PDs 的刚性和致密结构在激发波长依赖性和增强的荧光行为中起着至关重要的作用.PDs 的pH 依赖性荧光进一步证实,酸性环境导致更刚性和致密的构象,并诱导独特的荧光效应.Yang等[78]以支化聚乙烯亚胺(PEI)为非共轭聚合物模型,研究了一系列聚合物点(PD 1-4)的发光机理.PEI 基聚合物点潜在的荧光团是仲胺和叔胺,交联PEI 基聚合物点振动和旋转的减少导致了其荧光增强.从PEI 及PDs 的电子能级(图8a)可得,对于PEI,激发电子主要通过非辐射振动/旋转过程下降到基态;而对于PD 1 和PD 2,由于交联骨架,氨基荧光团的振动和旋转受到限制,辐射过程的百分比增加(CEE 效应);对于PD 3,PEI 链固定在非晶态碳核上,PEI 链的固定和碳核的天线效应(Antenna effect)都增强了荧光性能;对于PD 4,虽然PEI 链是固定的,胺基中心被CEE 效应增强,但具有多层晶格的碳核具有非辐射结构和陷阱(如层间猝灭),CEE 效应被非辐射过程抵消,辐射过程受到影响和限制.
明亮蓝色荧光发射是由羧酸和胺前驱体制备的各种聚合物碳点的一个显著特征,然而,这类聚合物点难以确定其精确的化学结构,极大地阻碍了对其发光机制的理解.Maser等[79]通过低温合成途径,从柠檬酸和乙二胺中制备出具有明亮蓝色荧光行为的聚合物点.密度泛函理论计算结果表明,PDs 的最高占据(HOMO)和最低未占据(LUMO)分子轨道分别位于酰胺和羧基上,基团之间的光诱导电荷转移导致了强发光行为(图8b).此外,由氢键介导的链间超分子相互作用有利于形成刚性网络结构,从而进一步增强辐射过程.

图8 a)PEI 及PDs 的电子能级;b)光诱导电荷转移过程
3 生物应用
3.1 毒性评估
与荧光有机染料和荧光蛋白相比,碳点本身具有较高的光稳定性、生物相容性和抗代谢降解等显著优势,在生物成像和光治疗中具有光明的应用前景.碳点的毒性评估是碳点实现生物应用的前提.Sun 等[80]利用激光烧蚀石墨粉和水泥合成碳点,以PEG1500N为表面钝化剂,对人乳腺癌MCF-7 细胞和人结直肠腺癌HT-29 细胞的生物相容性进行了探索.对两种细胞的增殖、死亡率和活力等观察表明,即使碳点的质量浓度达到50 μg/ml,也表现出优异的生物相容性(图9),这远远高于实际应用需求.最近,一些研究[81-82]通过体外(正常和各种癌细胞)和体内(大鼠、斑马鱼、小鼠)研究来评价各种纳米尺寸(零维CDS、GQDs、炭黑、一维碳纳米管、二维石墨烯和氧化石墨烯)的细胞毒性.碳纳米材料的体内毒性研究表明,碳纳米材料的细胞毒性取决于其浓度、表面电荷和时间.另外,对包括浮游动物、斑马鱼和浮游植物在内的各种物种进行的碳点体外毒性研究表明,经表面功能化的碳点对上述物种并没有明显的损伤或毒性.总的来说,碳点对许多细胞和物种表现出无毒的性质,不仅如此,通过利用生物相容性分子(聚合物、蛋白质和氨基酸)修饰碳点表面,可以进一步降低其可忽略的毒性.

图9 a)小鼠静脉注射不同当量(黑:对照组;灰:8 mg/kg;白:40 mg/kg)碳点一段时间(上:1 d;中:7 d;下:28 d)后血清生化结果;b)毒性评估结果(黑:碳点;白:PEG1500N)
3.2 表面功能化设计以便生物应用
现有部分碳点中,“原始碳点”一般不发或只发射很弱的荧光,而表面经过功能化或钝化的碳点往往可以提高其量子产率,改变荧光发射行为[28].此外,原始碳点与生物系统的相互作用较差,会阻碍其在生物方面的应用,但是碳点表面丰富的反应基团,可以被其他化学基团修饰,进而满足生物应用的要求.
生物相容性及毒性在一定程度上决定了碳点在生物领域的应用,而碳点表面工程为提高其稳定性提供了有效途径.Liu 等[83]对人支气管上皮细胞进行了原始荧光碳点的细胞毒性评价,发现原始碳点位于细胞表面,会引起氧化应激,从而降低细胞活力.之后,他们用聚乙二醇和聚乙烯亚胺等聚合物对原始碳点的表面进行了修饰.体外研究表明,经过表面功能化之后的碳点没有显示任何异常的细胞周期.因此,一般需要对原始碳点进行表面修饰以将能够增加其生物相容性的分子或者聚合物链接或钝化到碳点表面.研究人员于此做出了巨大的努力,目前,聚乙二醇[84]、聚乙烯亚胺[85]、聚丙烯酸[86]、丙基乙烯胺- 乙烯胺共聚物[87]等多种聚合物被成功用于改善碳点的生物相容性.
3.3 生物成像
由于碳点优异的光学性能、低毒性及生物相容性,其在体内外成像领域有着清晰的应用前景.2009 年,Sun 等首次报道了碳点在体内的光学成像[10],结果表明,多种方式注入小鼠的碳点在体内仍保持强烈的荧光(图10).如图11a,作者在使用碳点标记体外人类乳腺癌MCF-7 细胞时[87]发现,MCF-7 细胞的细胞质和细胞膜发出荧光,而细胞核未发荧光,以此推测出碳点难以进入细胞核内,在其他报道中也得出了类似的结论[88-90].然而,Yin 等[91]研究发现,以多巴胺和乙二胺为氮源所合成的氮掺杂碳点可以进入细胞核,以实现细胞核染色,并且使用多种细胞如PC12、A549、HepG 2 和MD-MBA-231 为模型验证了该碳点染核的通用性(如图11b).作者认为大量氨基的存在导致碳点表面带正电荷、较小的尺寸(平均粒径:2.34 nm)以及模拟多巴胺分子的结构和性质,是该碳点不同于其他碳点进入细胞核的原因.此外,Qu 等[92]以柠檬酸和间氨基酚为前体分子设计合成了含罗丹明类亲脂阳离子结构的碳点,所得到的碳点产物不仅具有罗丹明类亲脂阳离子的线粒体靶向性(图11c),而且呈现出优异的抗光漂白性能,使其具有长期线粒体成像和监测线粒体变化的潜力,这为探索线粒体和诊断线粒体相关疾病方面提供了强力的手段.

图10 a)皮间注射;b)静脉注射;c)皮下注射

图11 a)能检测到荧光的细胞膜和细胞液;b)能检测到荧光的细胞核;c)靶向线粒体的荧光碳点
3.4 药物负载
碳点优良的生物相容性和易降解的特点可以理想地满足生物应用的要求,另外,碳点表面丰富和可调谐的官能团,如氨基、羧基或羟基等,赋予了碳点携带治疗剂和靶向剂的能力,与适当的分子和治疗药物链接能够产生热敏纳米医学效应.同时,碳点的荧光性能提供了动态和实时监测药物分布和反应的机会.Zheng 等[93]以牛血清白蛋白为原料通过溶剂热反应制备了空心的碳点(图12),负载了具有荧光活性的阿霉素作为模型抗癌药物,形成了双发射给药系统.结果表明,该给药系统能被细胞迅速吸收并通过调节pH 释放阿霉素. Lin 等[94]以叶酸为原料采用“一锅法”原位制备了荧光介孔硅- 碳点(MSNs-CDs),该策略结合叶酸基团对癌细胞的靶向作用和介孔硅纳米颗粒大的比表面积与孔体积的独特性质,形成了一种很有应用潜力的给药系统.Sun 等[95]利用柠檬酸和聚烯多胺热解合成的碳点负载奥沙利铂(一种抗肿瘤药物),注射到被异种移植的小鼠体内,以蓝光为激发源,利用体内光学成像系统成功观察到了药物的动态分布.如图13所示,通过碳点的荧光成像,可以清楚地看到异种移植模型地肿瘤不断变小.

图12 空心碳点TEM 图谱

图13 碳点负载抗癌药物及其在小鼠中治疗效果
3.5 探针检测
生物体内某些特定物质与生命活动息息相关,可以作为标志物用于评估生物体的健康水平.过氧化氢(H2O2)是活性氧家族的重要成员,在生物体中起着至关重要的作用,因此,检测H2O2并阐明其生物学功能已成为生物和生物医学研究的重要领域.Wu等[96]通过共价连接线粒体靶向配体(三苯基膦,TPP)和H2O2识别基团(PFL)到碳点上,制备了基于FRET 的靶向线粒体H2O2比率的荧光纳米探针,用于活细胞中线粒体的成像并检测H2O2的含量.
细胞的氧化还原态在生命活动中发挥着重要的作用,调节着细胞功能的各个方面.谷胱甘肽(GSH)是影响细胞内氧化还原态的重要因素,细胞内的GSH 浓度反映出细胞的氧化还原状态.Yang 等[97]设计了一种基于碳点的复合微球探针,基于GSH 与二硫键的交换反应和碳点聚集淬灭效应,通过调节二硫键的交联密度可改变碳点释放所需的GSH 浓度,从而制备出一系列具有不同GSH 浓度响应的复合微球探针,成功实现了细胞内GSH 浓度的测量.
在生物系统中,特别是对活细胞来说,极性是建立和维持活细胞正常生理功能的重要参数.极性的异常变化通常与生物体的疾病有关,表明了细胞的生理状态.但极性的测量需要计算一系列的非共价相互作用,包括偶极/极化率和氢键,存在较大挑战.除此之外,细胞自噬是由称为自噬体的细胞器介导的过程,在饥饿或应激过程中,细胞质中折叠不当的蛋白质和功能失调的细胞器会被分解为氨基酸和脂肪酸,进而进行代谢.这一过程涉及多种功能和人类疾病,迄今为止,还缺乏能够以无毒和原位的方式实时监测自噬活动的方法.最近,Huang 等[98]开发了一种具有高灵敏度的聚合物碳点,在不干扰细胞状态的前提下,成功实现了细胞极性的可视化,且能够实时监测细胞自噬变化.如图14 所示,富营养素(正常)细胞红、绿通道的荧光图像和荧光强度在不同时间保持不变(图14a-e),表明细胞极性在这种情况下保持相对稳定.然而,细胞中的红色荧光分布随时间(图14f-j)减少,伴随着饥饿细胞绿色荧光强度的增加,提示自噬过程中活细胞极性的降低.在自噬抑制组中,这些细胞的荧光强度基本保持不变(图14k-o).结果表明,自噬过程中活细胞的极性会降低.

图14 a-e)富营养细胞(对照组);f-j)饥饿细胞(自噬组);k-o)自噬抑制组
3.6 血脑屏障的穿过及脑部疾病诊疗
体外研究表明,某些碳点能有效抑制胰岛素颤动,这与神经系统疾病有关[99].然而,由于血脑屏障(BBB)的存在,内皮细胞之间紧密连接会抑制治疗药物进入大脑病理组织,因此将药物输送到大脑仍然是一个较大的医学挑战.幸运的是,BBB 中的紧密连接区域具有4-6 nm 的间隙.因此,尺寸为4 nm 左右的纳米粒子,如碳点,可能通过这些间隙穿过BBB[100].另外,纳米粒子进行BBB 穿透的另一个重要因素是其静电电荷,阳离子分子可能占据BBB 内皮的阴离子区域,从而增加内皮细胞通透性[101].因此,通过设计合适尺寸且含有阳离子的碳点,有望实现突破血脑屏障,为脑部疾病的诊断和治疗提供了便利.
作为一种阳离子大分子,聚乙烯亚胺可以使碳点表面在生理条件下具有正电荷,从而提高生物膜的渗透性.在此背景下,Lu 等[102]以聚乙烯亚胺和柠檬酸为碳源,通过水热法合成了氮掺杂碳点(N-CDs,平均粒径~2.6 nm).在紫外光照射下,N-CDs发出强烈的蓝色发光,量子产率高达51%.对BBB 穿透的模型研究结果表明,N-CDs可以成功穿透BBB,但存在一定的浓度和时间依赖性(图15).

图15 N-CDs 合成路线及其形貌信息
缺血性脑卒中发作时会形成血栓,需要进行各种治疗,以解开闭塞的血管.然而,溶栓再灌注后,由于BBB 完整性的损害,可能发生颅内出血.通过将溶栓剂与荧光材料结合,为评估缺血性脑卒中后BBB 的早期损伤提供一种简便的方法.最近,Qu 等[103]报道了一种新型的蛋白质- 碳点纳米杂化物,通过共价键将溶栓剂掺入到碳点上,用于大脑中动脉闭塞小鼠的脑成像(图16).结果表明,CDs 可以成功用于评估BBB 损伤和出血风险,从而指导进一步的治疗,并且碳点可作为载体提供溶栓剂实现对缺血性脑卒中的治疗.

图16 碳点在缺血性脑卒中的应用
3.7 光诊疗
光诊疗有望成为一种新兴并拥有极大应用前景的肿瘤诊疗手段,可以在精准靶向癌细胞的同时,完成肿瘤细胞的杀灭,光诊疗主要包括光动力疗法(PDT)和光热疗法(PTT).在PDT 过程中光敏剂被特定波长的激光照射并激发,激发态的光敏剂可以产生对癌细胞具有毒性的单线态氧,从而实现对肿瘤的治疗.PTT 过程中,光热剂吸收特定波长的光产生局部热量,杀伤癌细胞.
在体内光诊疗过程中,通过体内组织的光的穿透能力与其波长相关,较长波长的光能够穿透更深组织并能有效屏蔽生物自身荧光的干扰.Callan 等[68]设计了一种与光敏剂原卟啉IX 相连的碳点,通过FRET(荧光共振能量转移)介导的方式,在800 nm 激发波长下发出上转换荧光,激发光敏剂,进而产生大量单线态氧,从而杀死较深层组织的肿瘤细胞(图17a).Zhang 等[104]合成出一种新的近红外荧光剂,同时掺杂氮和硼的石墨烯量子点(N-B-GQDs). 该碳点具有较小的尺寸(~5 nm),在血清中高度稳定,并且在1 000 nm 处有峰值荧光发射和高的光稳定性.除了近红外区成像能力之外,N-B-GQDs在外部NIR 光源照射下能够有效吸收NIR 光并将其转化为热能,这表明其拥有光热治疗的潜力.结果表明,N-B-GQDs 能够在体外杀死癌细胞并完全抑制异种移植小鼠模型中的肿瘤生长(图17c),同时该碳点在小鼠体内具有安全性、延长血液半衰期和快速排泄等特点,有利于在体内生物医学的应用.
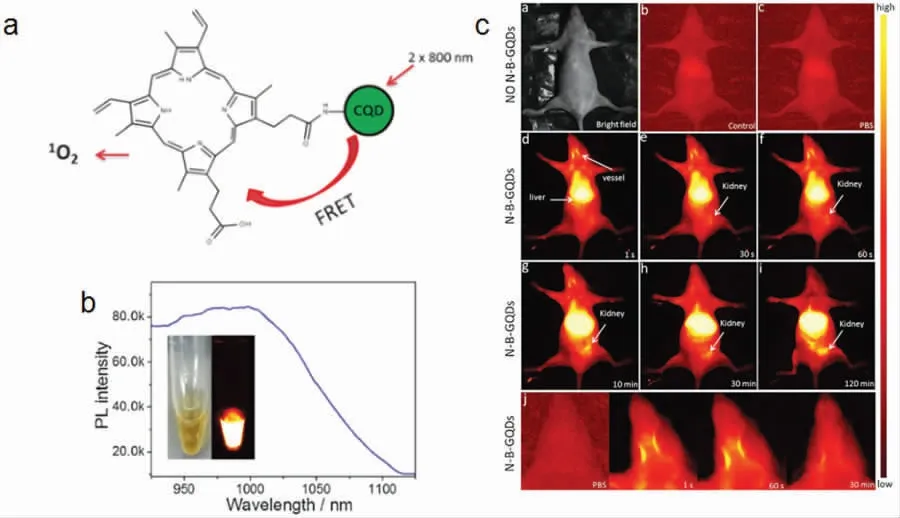
图17 a)携带光敏化剂的碳点;b)荧光图谱;c)肿瘤移植小鼠光热治疗效果
4 结 论
作为一种新型的碳纳米材料,碳点具有优良的光学特性、良好的生物相容性和低毒性等优点,在生物领域的应用得到了广泛的研究,是一类极具发展潜力的碳基质材料.未来工作中,碳点领域仍存在以下几个方面需深入探索:1)分门别类探索不同碳源和合成方法得到碳点的微观结构和发光机制;2)不同结构碳点荧光行为的共性研究及其光物理学探索;3)发展高亮度和高荧光效率的碳点材料;4)发展具有红色和红外光发射的荧光碳点;5)碳点结构的精确控制;6)碳点材料的大规模合成及其在聚合物加工等领域的应用探索;7)碳点材料在生物成像和肿瘤诊疗中的应用及其生物毒性等性质的深入探索.

