内路房角镜辅助经管腔内小梁切开术治疗多次手术开角型青光眼患者的疗效观察△
李海军 任静 杨潇远 董良 刘茜
开角型青光眼(OAG)是一类以房角开放、多因眼压增高致使特征性视神经萎缩而严重致盲的疾病。临床上在最大降眼压药物剂量使用无效的情况下,常常采取小梁切除或其他房水引流物植入等手术,以创建非生理性外引流通道而控制眼压。然而,仍有约30%OAG患眼需要行多次滤过手术,甚至转为难治性青光眼,严重影响视功能,治疗较为棘手[1]。目前认为,Schlemm临管组织区域(JCT)是房水流出的阻力区域,改善JCT阻力有利于OAG的治疗[2]。近年来,内路房角镜辅助经管腔内小梁切开术(GATT)是一种通过切开小梁网和Schlemm管内壁,使房水直接流入Schlemm管而降低眼压的手术,已被证明不仅对儿童青光眼有效,而且对OAG也有效[3-5]。然而对多次外滤过失败的OAG患眼疗效报道较少,本文回顾性分析GATT治疗初次手术与多次手术OAG患眼的有效性与安全性,现将结果报告如下。
1 资料与方法
1.1 一般资料收集2016年4月至2018年9月河南省人民医院行GATT治疗OAG患者57例(57眼),根据有无滤过手术史分为初次手术组与多次手术组。其中,初次手术组患者18例(18眼),多次手术组患者39例(39眼);两组患者年龄分别为(50.44±10.58)岁、(52.35±10.68)岁 (t=0.028,P=0.878),人工晶状体眼占比分别为44.44%与33.33%(χ2=0.653,P=0.419),基线眼压分别为(32.12±4.14)mmHg(1 kPa=7.5 mmHg)与(33.49±4.78)mmHg(t=-1.011,P=0.316),抗青光眼药物使用种类分别为3.00[3,4]种、2.75[3,4]种(Z=0.296,P=0.768),病因以原发性开角型青光眼(POAG)为主,占比分别为88.9%、82.1%(P=0.704),房角不全切开占比分别为27.8%、 53.8%(χ2=3.374,P=0.006),切开范围分别为(266.01±45.05)°与(262.85±49.41)°(Z=-0.033,P=0.974)。纳入标准:(1)OAG患者;(2)使用2种及以上降眼压药物情况下患者眼压仍>21 mmHg。排除标准:(1)原发性或继发性闭角型青光眼;(2)先天性青光眼;(3)随访周期<1年。所有患者均常规行裂隙灯、眼底镜及房角镜检查,利用Goldmann眼压计测量眼压。本研究遵循赫尔辛基宣言,经河南省人民医院伦理委员会审核批准,所有患者均知情同意并签署知情同意书。
1.2 手术方法全身麻醉或爱尔卡因表面麻醉状态下,患者侧头30°~45°,透明角膜切口,黏弹剂支撑前房,微管经透明角膜入路,房角镜辅助下切开Schlemm管内壁,经切口插入微导管(iTrackTM-250A,美国ellex iScience公司),闪光灯示踪经管腔内走行,对侧管口穿出,牵拉头尾两端,切开小梁网;若遇管内阻塞不能穿行眼,范围<180°,反向穿行或分段切开至范围>180°。冲洗前房黏弹剂及积血、水密闭透明角膜,妥布霉素地塞米松眼膏涂眼,术毕。术后妥布霉素地塞米松眼液滴眼,4次·d-1,共1周,10 g·L-1硝酸毛果芸香碱眼液滴眼,3次·d-1,共3个月。所有手术均由青光眼专家完成。
1.3 观察指标记录术前及术后1 d、1周、1个月、3个月、6个月、12个月两组患者眼压及抗青光眼药物种类、术中及术后并发症。眼压疗效判断标准:完全成功:术后在不使用降眼压药物条件下,眼压<21 mmHg;条件成功:术后不使用降眼压药物时眼压>21 mmHg,使用降眼压药物时眼压<21 mmHg;失效:术后最大剂量使用降眼压药物条件下,眼压>21 mmHg。
1.4 统计学方法使用SPSS 24.0软件进行数据分析。计量资料采用正态性检验,符合正态分布各时间点眼压采用重复测量数据方差分析,非正态分布小梁网切开范围、降眼压药物种类及总体治愈率使用非参数秩和检验,手术累积成功率采用Kaplan-Meier生存分析及Log-Rank两两检验。检验水准:α=0.05。
2 结果
2.1 两组患者治疗前后不同时间点眼压比较初次手术组患者随访(12.35±3.30)个月,多次手术组患者随访(13.78±3.45)个月。术后12个月时,初次手术组患者眼压为(18.23±2.88)mmHg,多次手术组患者眼压为(18.51±6.62)mmHg。两组患者术前及术后不同时间点眼压比较,差异均无统计学意义(均为P>0.05);两组患者组内术后各时间点眼压同基线眼压比较,差异均有统计学意义(均为P<0.01)(见表1)。末次随访时眼压达18 mmHg的靶眼压,初次手术组7眼(38.8%),多次手术组19眼(48.7%),差异无统计学意义(χ2=0.480,P=0.574)。末次随访时,初次手术组患者平均使用降眼压药物种类降为0.00[0,2]种,多次手术组降为1.10[1,2]种,均较术前显著下降(均为P<0.01),且初次手术组患者较多次手术组患者使用降眼压药物种类更少(Z=2.080,P=0.037)。

表1 两组患者手术前后不同时间点眼压比较
2.2 两组患者手术成功率比较术后12个月,初次手术组与多次手术组患者完全成功率分别为 55.6%、38.5%,条件成功率分别为22.2%、20.5%,失效率分别为22.2%、41.0%,两组间成功率比较,差异无统计学意义(Z=-1.404,P=0.160)。初次手术组、多次手术组患者完全成功累积生存率分别为44.4%、38.5%(χ2=0.364,P=0.546),中位生存时间分别为11.2个月、10.4个月(P=0.334)(见图1),条件成功累积生存率分别为77.8%、57.1%(χ2=1.534,P=0.215)(见图2)。

图1 两组患者完全成功累积生存率曲线图

图2 两组患者条件成功累积生存率曲线图
2.3 两组患者并发症比较术中两组患者均发生前房积血,术后以持续性或反复发生前房积血为主,眼压一过性升高次之,超过30 mmHg者给予醋甲唑胺口服,多次手术组2只外伤性眼发生前房积血伴眼压升高且持续>35 mmHg,行前房冲洗,眼压仍失控,行房水引流物植入术治疗。睫状体脱离眼常伴有低眼压、浅前房,并分别予以记录,局部维持给予妥布霉素/地塞米松眼液滴眼,4次·d-1,用药时间>2周,稳定后改用普拉洛芬眼液滴眼,4次·d-1,用药时间>2周,或联合全身用药,口服醋酸泼尼松片3~5 d。两组患者均未见严重并发症发生(见表2)。
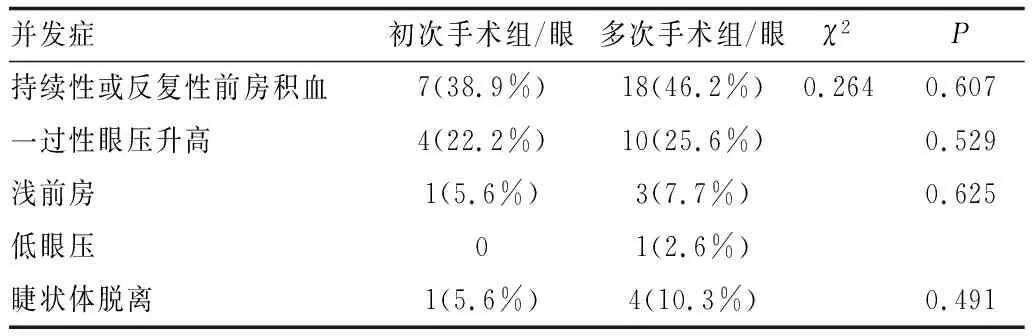
表2 两组患者术后并发症比较
3 讨论
外路小梁切除或房水引流物植入术通过创建非生理性通道、构建功能性滤过泡实现眼压的降低。然而,多次外滤过手术常因滤过通道或滤过泡瘢痕致使眼压失控,严重影响视功能的康复[6]。近年来,通过切开JCT解除房水流出阻碍部位,重建房水经由Schlemm管流出的生理性通道的内路小梁网切开术得以重视[7]。GATT属于内路小梁网切开术式之一,在儿童青光眼与青少年型青光眼研究中证实,与传统的外路小梁切除术相比,更安全有效,且具有微创性[8-9]。本研究主要对比GATT对初次及多次治疗OAG患眼的疗效与安全性。
本研究GATT治疗初次手术组与多次手术组OAG患眼结果提示,术后组内各时间点眼压与术前比较均下降,但组间比较差异均无统计学意义(均为P>0.05)。术后12个月,初次手术组、多次手术组患者完全成功率分别为55.6%与 38.5%,条件成功率分别为22.2%与20.5%,失效率分别为22.2%与41.0%,提示初次手术组成功率较多次手术组更高,但总体比较无明显差异(Z=-2.08,P=0.160),同时,1年的完全成功累积生存率分别为44.4%、38.5%,中位生存时间分别为11.2个月、10.4个月,条件成功累积生存率分别为77.8%、57.1%,尽管两组比较均无明显差异,但初次手术组具有更高的条件成功率,术后初次手术组降眼压药物使用种类较多次手术组更少(Z=2.08,P=0.037);按18 mmHg的靶眼压标准,初次手术组有7眼(38.8%)、多次手术组有19眼(48.7%)末次随访时达到靶眼压,组间比较差异无统计学意义(χ2=0.480,P=0.574)。袁志兰等[10]在观察改良的黏弹剂Schlemm管切开术和小梁切除术治疗POAG的疗效和安全性研究中报道,Schlemm管切开术后1年眼压为(14.50±3.22)mmHg,手术成功率为87.5%,认为Schlemm管切开术较小梁切除术成功率高。但潘伟华等[11]在缝线植入Schlemm管开口部成形联合小梁切除术治疗POAG结果提示,Schlemm管成形术并未较单一的小梁切除手术成功率提高。美国青光眼协会问卷调查提示,尽管针对OAG的初始治疗仍以小梁切除术为主,占比达59%±30%,然而术后3~5年随访发现,单一小梁切除术后眼压有效控制率仅为48%与40%;同时,问卷调查结果提示,患者多选择以内路小梁切开及其他系列微创手术减少结膜损伤或滤过泡依赖术式,以GATT优选(20.3%),其次为XEN、istent引流器植入术(占比分别为18.6%、14.3%),小梁切除或Ahmed阀植入等仅分别为14.1%、6.9%[12-14]。尽管文献报道多次小梁切除或房水引流物植入术联合丝裂霉素C(MMC)处理,可提高多次手术OAG患眼成功率,但增加术源眼表损害及MMC毒副作用[15-17]。本研究结果发现,GATT治疗初次手术患眼完全成功率为55.6%,与传统小梁切除手术约48%有效率较为相近,同时减少多次手术患眼术源性眼表的损伤,且其完全成功率也达38.5%,较房水引流物植入术也减少了植入物潜在的生物学安全性问题。Babighian等[18]在准分子激光辅助内路小梁切开术治疗难治性开角型青光眼(r-OAG)的研究中报道,末次随访完全成功率为40.5%,条件成功率为38.1%,末次随访时 90.5% 降眼压幅度>20%,眼压为(16.9±2.1)mmHg,且减少了降眼压药物使用的种类,结果显示激光辅助小梁切开术是r-OAG患眼的有效治疗方式,术后达到理想靶眼压,降低视功能持续损害风险。本研究结果发现,比较术后<18 mmHg靶眼压占比,多次手术组占比48.7%,较初次手术组(38.8%)占比高,但无统计学差异,与Sarkisian等[19]在GATT治疗r-OAG术后1年的随访研究中结果类似,术后眼压<18 mmHg患眼占比59%,且降压幅度>20%。由此可见,GATT术式切开JCT,重建房水经由Schlemm管流出生理性通道,可作为OAG患眼有效的治疗方式之一,与小梁切除术及房水引流物植入术比较,减少了术源性及抗代谢药物眼表损伤,以及降低了植入物的生物安全性风险,尤其是多次手术r-OAG患眼,尽管仍有不低的失效率,但达到靶眼压有效率更高。
本研究结果发现,初次手术组以全周切开率高,多次手术以次全切开率高,但次全切开范围两组并无差异。推测因Schlemm管腔狭窄或发育不良,以及多次手术区域瘢痕或术后炎症致使Schlemm管腔断裂或闭锁所致,术中注入黏弹剂扩张管腔也难以保障微导管全周贯通并切开。周龙芳等[3]在内路Schlemm管成形术治疗POAG研究中,也证实Schlemm管腔狭窄或发育不良影响微导管全周穿行。荧光素造影显示Schlemm管呈节段性扩张解剖形态,临床上基于解剖结构因素行不全切开小梁网或跨越JCT的小梁网引流器植入也可有效控制眼压,但降眼压幅度有限,多建议用于早期青光眼治疗[20-21]。本研究结果中降眼压幅度相对较大,可能归因于较大范围的切开小梁网,但多次手术后失效率仍高达41.0%,初次手术组仅为 22.2%,可见切开范围并不是影响术后有效眼压控制的单一因素,尤其是多次手术治疗患眼,不排除反复术后炎症、原发病因等多重因素的影响。国外多位学者[4-5,22]对初次或多次手术后先天性青光眼患眼采取Schlemm管切开术治疗系列研究中报道,即使初始治疗患眼也仅约85%的全周切开率,若次全切开范围>180°,术后降眼压有效率也几乎无影响。由此可见,切开范围多受Schlemm管腔本身结构影响,多次手术尽管增加不全切开与眼压失控风险,但眼压失控并不完全取决于切开范围;同时,GATT治疗更易获得较大降眼压幅度的理想靶眼压,但需要进一步研究证实。
本研究中两组均可见前房积血,因Schlemm管切开静脉回血所致,多数在3~5 d内可自行吸收。初次手术组7眼(38.9%)发生持续性或反复前房积血,其中4眼(22.2%)伴有眼压增高,多次手术组18眼(46.2%)发生持续性或反复前房积血,10眼(25.6%)伴有眼压增高,给予局部或全身辅助降眼压药物控制,此外,多次手术组2只外伤性患眼发生持续性前房积血,且眼压>35 mmHg,行前房冲洗治疗后积血改善,眼压仍然失控后植入Ahmed阀处理。初次手术组1眼(5.6%)发生浅前房,多次手术组3眼(7.7%)发生浅前房、1眼(2.6%)发生低眼压,均因发生睫状体脱离所致,睫状体脱离可归因于术中导管迷路,经Schlemm管腔至睫状体腔隙的医源性损伤,或因Schlemm管内壁切开后产生了对原有血-眼屏障的潜在影响,以及术后低眼压性相关改变。全身或局部辅助激素类药物治疗后改善,组间比较差异均无统计学意义(均为P>0.05),无其他(如角膜内皮脱离或失代偿、感染等)严重并发症发生。本研究中患者术中常伴前房积血,前房冲洗及黏弹剂填充维持术野清晰,以减少医源性角膜内皮或晶状体损伤风险,并准确经Schlemm管切口穿入微导管后予以切开,若持续大量积血,应更换术式或延期手术。尤其是外伤性OAG出血量大,且术后出血不易吸收,存在眼压持续增高与潜在角膜血染风险。术后睫状体脱离也较为常见,多同时伴有浅前房、低眼压,但激素类药物可有效控制。Sarkisian等[19]利用GATT治疗r-OAG研究中,也证实短暂性前房积血是最常见的并发症。Ahuja等[23]在内路小梁切开术研究中报道,部分患者迟发性出血最可能的机制是由于术眼巩膜静脉压升高或眼球压迫而突然的减压和血液回流,延迟发作的前房积血可能与间歇性眼压升高有关。由此可见,前房积血是GATT术后常见并发症,多次手术患眼更易发生,多伴有眼压一过性升高,无其他严重并发症发生,但对外伤性OAG应谨慎采取GATT治疗。
另外,需要进一步指出的是,本研究中尽管存在其他继发性OAG类型,如色素性青光眼、激素性青光眼,但占比较小,大多数患者为POAG,难以完全代表全部OAG。本研究具有样本量少、随访时间短、单中心、回顾性研究等不足,需要后续设计前瞻性、多中心、大样本的随机对照临床研究予以进一步证实。
综上所述,GATT是治疗初次或多次手术后OAG患眼有效方式,除短暂性前房积血与一过性眼压升高外,无其他严重并发症发生,且更加符合房水的生理性流出方式,对已行多次滤过手术的OAG失效患眼,GATT术式可作为一种可选择的治疗手段。

