不同剂量右美托咪定对紫绀型先天性心脏病患儿术后肾功能的保护作用
魏碧玉,刘 伟,高明龙,孙 立,刘永哲
随着产前诊断、微创导管技术、围术期重症监护及外科手术技术的进步,紫绀型先天性心脏病(cyanotic congenital heart disease, CCHD)患儿的存活率显著提高[1]。但是,由于心脏手术期间低体温、低流量非搏动性灌注、血管活性药物的使用,以及术后低心排量综合征、左心功能不全和严重心律失常的发生[2],易造成患儿术后急性肾损伤(acute kidney injury, AKI),其发生率为15%~52%,尤其是体外循环(CPB)时间大于140 min的CCHD患儿AKI发生率更高。大量研究表明,AKI与高并发症发生率和病死率密切相关[1,3],严重影响患儿预后。右美托咪定(Dex)是一种选择性的α2肾上腺素受体激动剂,可通过抗炎、抗交感、减少细胞凋亡作用减轻患儿肾损伤[4],但是以往国内外研究仅比较对照组和干预组AKI的发生率,并未关注患儿早期肾功能变化。本研究通过比较不同剂量Dex组CCHD患儿敏感肾损伤标志物尿中性粒细胞明胶蛋白酶相关脂质运载蛋白(uNGAL)、血半胱氨酸蛋白酶抑制剂C(bCys-C)和尿肾损伤分子-1(uKIM-1)的变化,探究不同剂量Dex对CCHD患儿早期肾功能的保护作用,以期为改善患儿预后提供理论基础。
1 资料与方法
1.1一般资料 选择2018年5月—2019年2月解放军总医院第七医学中心接受CPB下心脏手术的CCHD患儿90例为研究对象。①纳入标准:年龄≤1岁;体质量≥2.5 kg;所有入选对象监护人均签署知情同意书。②排除标准:早产儿;肝、肾、肺、脑等重要器官疾病;术前肌酐>40 μmol/L[5];术前有抢救病史;术中及术后出现重大并发症,如死亡、心搏骤停、CPB脱机困难等。根据随机数字表法将患儿分为对照组、低剂量组和高剂量组,每组30例。3组性别、年龄、体质量和先天性心脏病类型比较差异无统计学意义(P>0.05),具有可比性。见表1。本研究由解放军总医院第七医学中心伦理委员会批准,已在中国临床研究注册中心注册,注册号为ChiCTR1800019190。
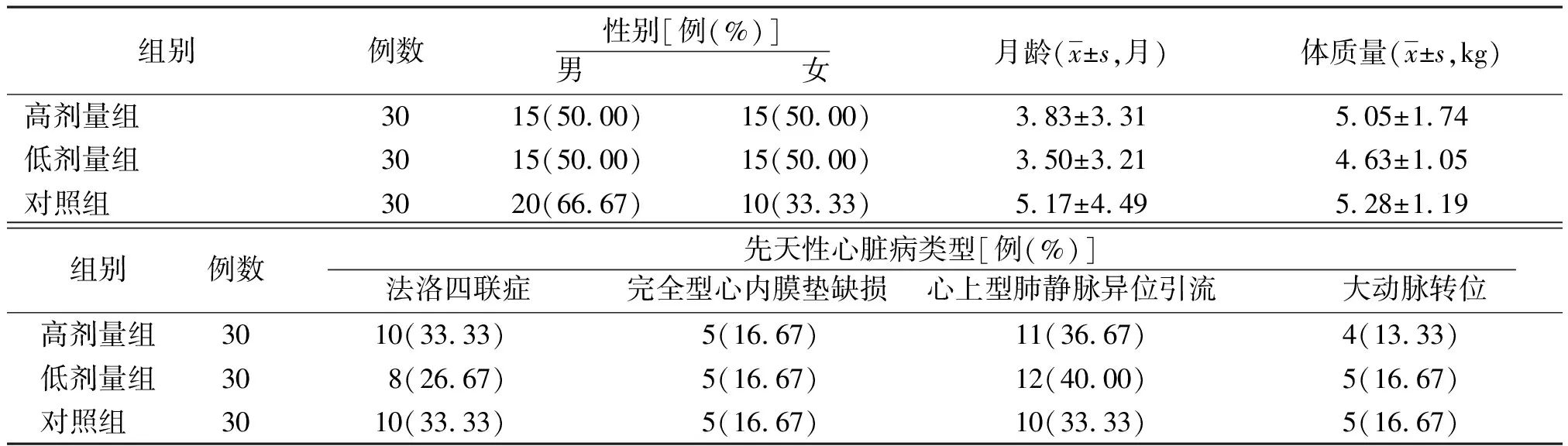
表1 应用不同剂量右美托咪定紫绀型先天性心脏病3组一般资料比较
1.2麻醉方法 CCHD患儿在病房建立静脉通路,入手术室后连接监护仪,常规监测心率、平均动脉压、血氧饱和度和脑电双频指数。对照组静脉泵注0.9%氯化钠注射液,低剂量组和高剂量组于麻醉诱导前10 min静脉泵注Dex 1 μg/kg负荷剂量,随后分别以0.5和1 μg/(kg·h)速度泵注。麻醉诱导药物为咪达唑仑0.1 mg/kg、芬太尼10 μg/kg、罗库溴铵1 mg/kg,患儿气管插管后调节呼吸参数为:新鲜气体流量2 L/min,潮气量8~10 ml/kg,呼吸频率35~40/min,吸呼比为1∶1.5,吸入氧浓度50%~90%,动脉血二氧化碳分压35~45 mmHg。超声引导下行桡动脉或股动脉穿刺测定动脉压、右侧颈内静脉或股静脉穿刺置入4.5Fr三腔中心静脉导管测定中心静脉压。术后Dex按照术中剂量持续泵注至患儿血流动力学平稳、准备气管拔管前,若用药过程中出现心动过缓(心率<100/min)则静脉注射阿托品0.02 mg/kg,必要时停止泵注Dex。麻醉维持采用静吸复合麻醉,吸入1%~2%七氟烷,根据手术进程与血流动力学情况追加咪达唑仑、芬太尼和罗库溴铵。围术期根据血压水平,泵注肾上腺素和多巴胺。手术结束后进一步监护治疗。手术由同一组医生负责,并采用相同的CPB管道及药物。术后给予0.2~0.3 μg/(kg·h)的芬太尼止痛。
1.3观察指标 比较3组手术相关指标,包括CPB时间、手术时间、术中最低体温、术中尿量情况。在气管插管后(T1)、超滤结束后(T2)、CPB结束后3 h(T3)、CPB结束后8 h(T4)、CPB结束后24 h(T5)收集血液、尿液标本,采用酶联免疫吸附试验检测并记录各组uNGAL、bCys-C、uKIM-1水平,以及术后7 d的血肌酐值。2岁以下儿童血肌酐正常范围35~40 μmol/L,根据改善全球肾脏病预后组织推荐的标准,符合以下情况之一即可诊断为AKI:①48 h内血肌酐增高≥26.5 μmol/L;②确认或推测7 d内血肌酐的增高值为基础值的1.5倍。根据上述诊断标准计算各组术后AKI的发生率,术后随访和标本采集由同一位麻醉医生进行。

2 结果
2.1手术相关指标比较 3组CPB时间、手术时间、术中最低体温比较差异均无统计学意义(P>0.05)。但低剂量组术中尿量显著高于对照组和高剂量组(P<0.05)。见表2。
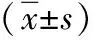
表2 应用不同剂量右美托咪定紫绀型先天性心脏病3组手术相关指标比较
2.2不同时间点uNGAL水平比较 重复测量方差分析结果显示,不同组别和时间的交互效应对CCHD患儿uNGAL水平的影响有统计学意义(P<0.01)。组内比较显示,对照组uNGAL水平在T3~T5时显著高于T1和T2(P<0.01);低剂量组和高剂量组uNGAL水平在T1~T5时比较差异均无统计学意义(P>0.05)。组间比较显示,低剂量组和高剂量组uNGAL水平在T1、T2时与对照组比较差异无统计学意义(P>0.05),在T3~T5时均较对照组显著降低(P<0.05);高剂量组uNGAL水平在T1~T5时与低剂量组比较差异无统计学意义(P>0.05)。见表3。
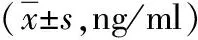
表3 应用不同剂量右美托咪定紫绀型先天性心脏病3组不同时间点uNGAL水平比较
2.3不同时间点bCys-C水平比较 重复测量方差分析结果显示,不同组别和时间交互效应对CCHD患儿bCys-C水平的影响有统计学意义(P<0.01)。组内比较显示,对照组bCys-C水平在T3~T5时显著高于T2,在T4和T5时显著高于T1和T3(P<0.05,P<0.01);低剂量组和高剂量组bCys-C水平在T4时高于T2和T3(P<0.05,P<0.01);低剂量组bCys-C水平在T5时低于T4(P<0.01);而高剂量组bCys-C水平在T5时高于T2(P<0.05);3组内其余不同时间bCys-C水平比较差异均无统计学意义(P>0.05)。组间比较显示,低剂量组和高剂量组bCys-C水平在T1~T3时与对照组比较差异无统计学意义(P>0.05);低剂量组bCys-C水平在T4和T5时较对照组均显著降低(P<0.05);高剂量组bCys-C水平在T5时较对照组显著降低(P<0.05),在T4时与对照组比较差异无统计学意义(P>0.05)。见表4。
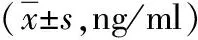
表4 应用不同剂量右美托咪定紫绀型先天性心脏病3组不同时间点bCys-C水平比较
2.4不同时间点uKIM-1水平比较 重复测量方差分析结果显示,不同组别和时间相互效应对CCHD患儿uKIM-1水平的影响有统计学意义(P<0.01)。组内比较显示,对照组uKIM-1水平在T3~T5时均显著高于T1和T2,在T4和T5时显著高于T3(P<0.01);3组其余不同时间uKIM-1水平比较差异均无统计学意义(P>0.05)。组间比较显示,低剂量组和高剂量组uKIM-1水平在T1和T2时与对照组比较差异均无统计学意义(P>0.05),在T3~T5时较对照组均显著降低(P<0.05);高剂量组uKIM-1水平在T1~T5时与低剂量组比较差异无统计学意义(P>0.05)。见表5。
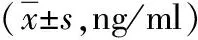
表5 应用不同剂量右美托咪定紫绀型先天性心脏病3组不同时间点uKIM-1水平比较
2.5AKI发生率比较 对照组发生AKI 10例,发生率为33.33%;低剂量组发生AKI 3例,发生率为10.00%;高剂量组发生AKI 3例,发生率为10.00%。低剂量组、高剂量组AKI发生率显著低于对照组(P<0.05),而低剂量组与高剂量组比较差异无统计学意义(P>0.05)。另外,3组在围术期均未观察到Dex相关的心血管并发症,如心动过缓等。
3 讨论
AKI是CCHD患儿CPB术后的常见并发症,能够显著延长患儿机械通气时间和住院时间,严重影响预后,尚无有效的治疗方法[6-8]。有研究表明,围术期使用Dex的CCHD患儿在术后24 h内尿量增加,血肌酐显著下降[9],但是CCHD患儿围术期使用Dex对早期肾损伤标志物影响的报道少见,本研究通过比较不同剂量Dex对0~1岁CCHD患儿uNGAL、bCys-C、uKIM-1水平的影响,发现CCHD患儿心脏手术围术期持续静脉泵注Dex 0.5 μg/(kg·h)时,uNGAL、bCys-C、uKIM-1水平在CPB结束后24 h内显著降低,早期肾功能损伤明显减轻,且术后7 d内AKI的发生率明显降低。
以往研究表明,年龄小于1岁的先天性心脏病患儿手术风险等级≥4,CPB时间>140 min是术后AKI的独立危险因素[9]。本研究控制术中主要危险因素,研究Dex对肾功能的影响,发现低剂量组尿量显著高于对照组和高剂量组。Dex可抑制抗利尿激素释放、抑制交感神经使肾动脉扩张增加肾小球滤过率,从而增加尿量,减轻患儿肾损伤[9]。而以往对180例先天性心脏病患儿持续输注Dex 0.5 μg/(kg·h),结果发现患儿术中尿量显著增加[10],本研究与该研究结果相似。
血肌酐和尿量是传统的肾损伤标志物,但不是敏感、可靠的肾功能指标,血肌酐浓度受性别、年龄、体质量及饮食的影响,且肾小球滤过率下降50%才会出现升高,尿量受内分泌及利尿剂的影响较大[11]。目前,uNGAL、bCys-C、uKIM-1是敏感的早期肾损伤标志物,可用于AKI预测及诊断[12]。本研究结果发现,CCHD患儿术后24 h内低剂量组、高剂量组uNGAL、bCys-C、uKIM-1显著低于对照组。
肾小管上皮细胞分泌少量NGAL,缺血性肾损伤发生后2 h,肾脏大量表达NGAL,并被释放到尿液和血液中,uNGAL升高可作为AKI的诊断标志物[13]。以往多项研究表明,持续泵注Dex 0.5 μg/(kg·h)至术后24 h能够对早期肾功能起到保护作用,Dex组uNGAL水平在术后24 h显著降低[14]。本研究结果发现,对照组uNGAL水平在T3时显著高于T1时,在T5时达到最高;低剂量组和中剂量组uNGAL水平在T3~T5时显著低于对照组,与以往研究得出了一致的结果。
血液循环中Cys-C仅经过肾小球滤过在近曲小管重吸收后被完全代谢分解,且不受性别、年龄及饮食的影响,是反映肾小球滤过率变化的理想内源性标志物,在缺血性肾损伤后2~4 h升高[15]。本研究结果发现,3组bCys-C水平在T4时均显著升高,但是低剂量组和高剂量组在T5时回到基线值,而对照组在T5时则显著升高;低剂量组和高剂量组bCys-C水平T5时显著低于对照组。
KIM-1是近曲小管上皮细胞的一种跨膜糖蛋白,在近曲小管受损后表达明显增强,uKIM-1在肾脏损伤4~6 h可出现升高[16]。本研究发现,对照组uKIM-1水平在T3~T5时显著高于基线值,但是低剂量组和高剂量组T3~T5时与基线值相比无统计学差异;低剂量组和高剂量组uKIM-1水平T3~T5时均显著低于对照组。
上述结果显示,Dex可以有效降低早期肾损伤标志物,减轻CCHD患儿的早期肾损伤,本研究比较3组AKI发生率发现,低剂量组和高剂量组AKI发生率显著低于对照组,且没有出现心动过缓等并发症。
肾脏血流丰富,侧支循环少,需氧量高,肾功能储备少,CPB、手术失血、麻醉使肾脏成为易受缺血/再灌注损伤的器官[17]。氧化应激和炎症反应是肾缺血/再灌注损伤的重要环节,大量研究表明,Dex通过抗氧化应激、抗炎、抑制细胞凋亡和抗交感神经活性等多种途径发挥肾保护作用[9,18],降低了早期肾损伤标志物,对CCHD患儿的肾脏保护及预后改善具有重大意义。
AKI是小儿心脏手术的常见并发症,能够增加病死率,目前尚无有效的治疗方法。本研究结果表明在CCHD患儿围术期持续静脉泵注Dex 0.5 μg/(kg·h)可对术后AKI起到良好的预防作用,是改善患儿预后的重要措施。

