吸附伏安法对辅酶Q10的测定研究
刘昱宏,郭 斌,屠一锋
(1.锦州医科大学 药学院,辽宁 锦州121000;2.苏州大学 材料与化学化工学部,江苏 苏州215123)
辅酶Q10(CoQ10),又名癸烯醌、泛醌,分子量863.36,是辅酶Q的一种。辅酶Q拥有一条由6~10个异戊二烯所构成的侧链,而辅酶Q10的此侧链的聚合度为10[1]。辅酶Q10分别以泛醌(氧化形态)和泛醇(还原形态)分布在细胞膜上,主要负责电子、质子运输,在三磷酸腺苷的合成上起着至关重要的作用[2],也是为心肌细胞提供能量的主要成分。大量医学研究证明心脏疾病与辅酶Q10的缺乏有关[3-5],其在医学和保健品领域主要用于强化心肌功能,是预防动脉硬化形成的最有效的抗氧化成分,也是各类心血管疾病的主要协同用药。因此,体内辅酶Q10的定量分析对上述疾病的防治具有重要作用。
目前,常用的辅酶Q10检测方法有高效液相色谱(HPLC)、液相色谱-串联质谱(LC-MS/MS)、紫外-可见分光光度(UV-Vis)等方法,现行的《中华人民共和国药典》2015版采用色谱法[6-11],近年来也报道了一些新的、高效的检测方法。Temova等[12]使用HPLC-UV方法测定药物和补剂中的辅酶Q10含量,首次实现同步测定辅酶Q10和其他5种脂溶性维生素。Schou-Pedersen等[13]研究了相同条件下HPLC-ECD和LC-MS/MS两种方法对辅酶Q10的测定灵敏度,HPLC-ECD表现出色,定量检出限(LLOQ)低至10 nmol/L。但所有联用HPLC分离的检测方法所需时间普遍较长,仪器成本和使用成本均较高,不利于普及应用。
本文使用吸附伏安法对辅酶Q10进行测定,发现利用辅酶Q10在玻碳电极上的吸附作用,可有效提高其测定灵敏度。在单因素分析基础上使用Box-Behnken实验设计对测定条件进行优化,获得检出限为19.0 nmol/L,接近HPLC法水平。在达3个数量级的浓度范围内,吸附伏安电流和辅酶Q10浓度的对数呈线性相关,可用于辅酶Q10的定量分析。
1 实验部分
1.1 仪器与试剂
ALS/DY2325 Bi-potentiostat电化学工作站(日本比·艾斯公司),三电极体系:工作电极为玻碳电极(φ=3 mm),对电极为铂电极,参比电极为饱和甘汞电极。
辅酶Q10标准品(USP,>98.5%,上海麦克林生化科技有限公司),使用乙醇溶解,并根据需要稀释配制标准溶液;甲醇、乙醇、硫酸(分析纯,江苏强盛功能化学股份有限公司);甲醇、乙醇按一定比例混合并加入0.12 mol/L硫酸作为支持电解质;用于溶解辅酶Q10的乙醇和电解质溶液使用前均通氮气除氧5 min,以防止还原态辅酶Q10被氧化;实验用水均为去离子水。
1.2 实验方法
1.2.1 吸附伏安测试条件在-0.2~0.6 V范围内,以不同扫描速率进行循环伏安(CV)扫描,以所得峰电流和扫速之间关系判断辅酶Q10电化学反应的控制步骤,依据研究结果优化相关测试参数(如预富集时间、温度、支持电解质溶液组成以及样品制备条件等)。
1.2.2 实际样品的处理测试样品为辅酶Q10胶囊和软胶囊,由药店随机购得。辅酶Q10胶囊颗粒状内容物用乙醇超声溶解并定容,辅酶Q10软胶囊内油状内容物使用乙醇超声提取,8 000 r/min离心15 min后吸取黄色上清液,反复数次直至残渣完全呈白色,合并提取液并定容。
2 结果与讨论
2.1 辅酶Q10电化学反应机理及主要影响因素
以玻碳电极为工作电极,在-0.2~0.6 V范围内,考察不同扫描速率(0.01、0.02、0.05、0.1、0.2、0.5、1 V/s)时0.5 μmol/L辅酶Q10的循环伏安曲线,以探讨辅酶Q10的电化学行为。结果显示,峰电流(I)随扫描速率的增大而增大,且与扫描速率(v)呈线性相关,其线性方程为:I=0.216+13.1 v,r2=0.997,符合Laviron理论:Ip=nFQν/4RT,可判断辅酶Q10在玻碳电极上的电化学反应受吸附控制[14-18],因此可通过预富集提高测定灵敏度。进一步考察不同预富集时间(0~45 min,间隔时间5 min)对辅酶Q10循环伏安电流的影响,显示辅酶Q10在玻碳电极上的循环伏安峰电流值随富集时间的延长而增强,且在富集25 min时获得最大电流,该结果支持吸附控制电化学过程的观点。但预富集时间过长则电流逐步下降,其原因可能是还原态的辅酶Q10被溶解氧部分氧化。
对多项测定条件进行筛选后,发现在制备辅酶Q10样品溶液时宜采用超声振荡以加快其溶解速度并提高溶解效率,在测定时,温度、支持电解质溶液溶剂组成有显著的影响,采用单因素分析法可分别对上述因素进行优化。样品制备时进行超声振荡可快速溶解辅酶Q10,但时间过长可能导致其形态变化,由图1A可知,超声溶解时间以不超过2 min为宜。由图1B可知,测定电流值随温度升高呈先增加后降低的趋势,温度为25℃左右时,辅酶Q10的循环伏安电流响应值最高。其原因可能是,随着温度升高,辅酶Q10的传质速度加快,有利于其在电极表面的吸附富集,而温度过高则可能加快辅酶Q10在电极表面的脱附,从而导致电流值下降[19]。已有研究多使用乙醇作为溶剂对辅酶Q10进行测定[6-13],由图2C可知,支持电解质溶液中溶剂构成对辅酶Q10的电化学响应有较为显著的影响,本实验以甲醇∶乙醇配比为1∶1时,获得的电流响应值较高。
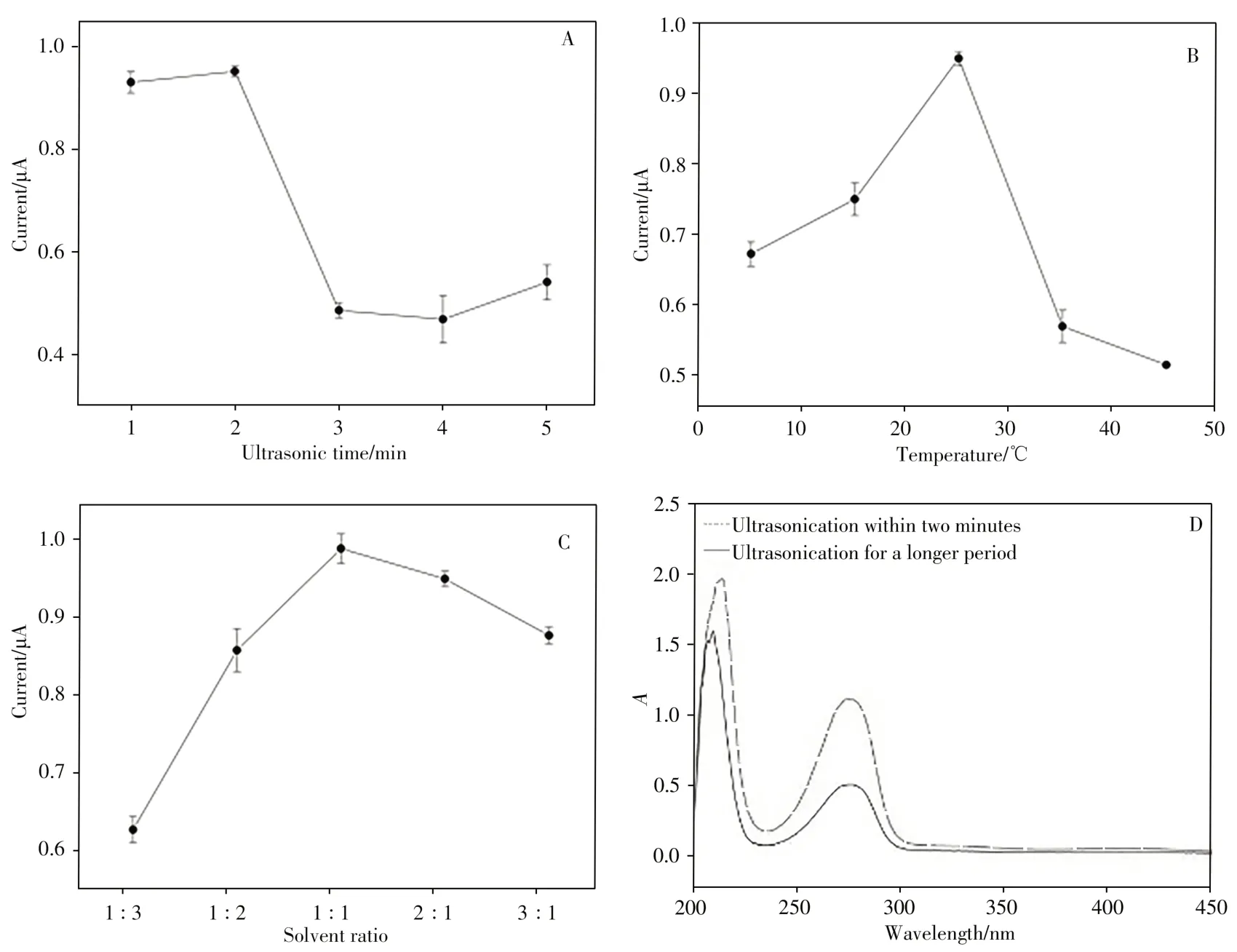
图1 样品超声时间(A)、测定温度(B)、溶剂比例(C)对循环伏安电流的影响;样品超声时间不同时所得溶液的紫外吸收光谱(D)Fig.1 Effects of ultrasonic time(A),detection temperature(B)and solvent composition(C)on CV current;UV spectra of CoQ10 solution under different ultrasonic time(D)CCoQ10=0.5 μmol/L
2.2 测定条件优化设计及结果
以上单因素试验初步揭示了相关因素的影响规律,使用Box-Behnken响应面分析法[20-22]以考察各因素的影响及交互作用,可进一步优化上述测定条件,因此进行3因素3水平实验设计和数据分析。设置样品超声时间、测定温度、溶剂配比分别为因素A、B、C,以3次平行测定平均值计数,得出回归方程为:y=2.10-0.210A-0.232B+0.206C+0.239AB+0.256AC-0.170BC-0.295A2-0.795B2-0.441C2。
方程预测相关系数(Predicted R2=0.753)与修正相关系数(Adjusted R2=0.948)差值小于0.2,说明该模型的拟合程度良好,方程相关系数R2=0.977,说明模型成立。方差分析结果见表1,表明A、B、C均为显著影响因素,且显著性A>B>C。
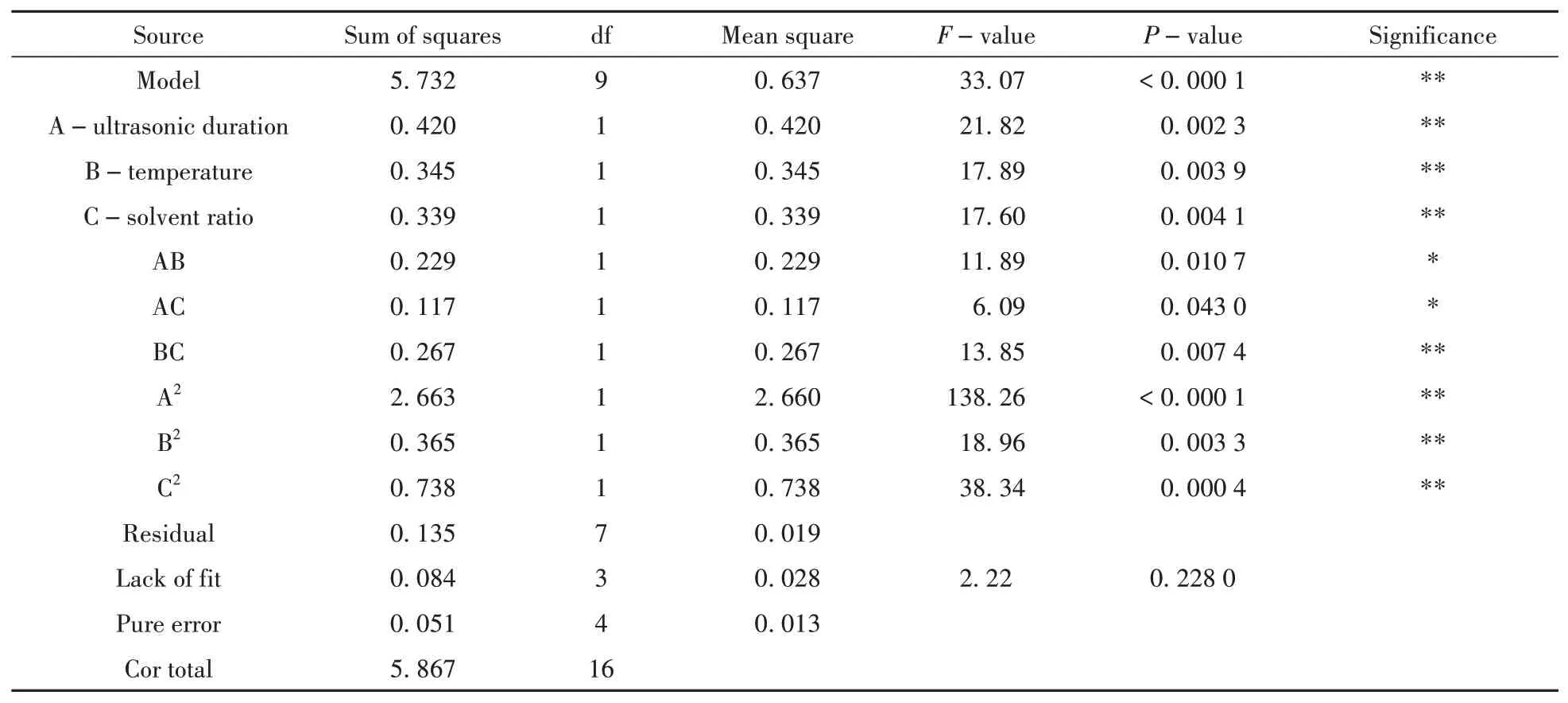
表1 回归模型及方差分析Table 1 The variance analysis of regression equation
对方差分析结果进行分析,可见A因素对结果有更大的显著性影响,而A因素参与的交互作用的显著性较小,说明A因素是一个较为独立的因素,但与其它因素间并非完全无交互作用。参考图1A所示实验结果,超过2 min的超声时间将导致辅酶Q10的检测电流显著降低,原因应与其形态变化有关,如图1D所示,过长的超声时间会导致其UV吸收降低,这可理解为超声时间过长会促使更多氧气溶解进入样品溶液中而使部分样品逐步被氧化,这一过程会持续到检测过程,从而与因素B、C发生交互作用。另一方面,超声振荡引起声空化过程导致的局部温度升高使样品以蒸发方式损失一部分也可能是原因之一[23]。
在此基础上,通过响应面分析(图2)可以获得更为精确的优化结果。
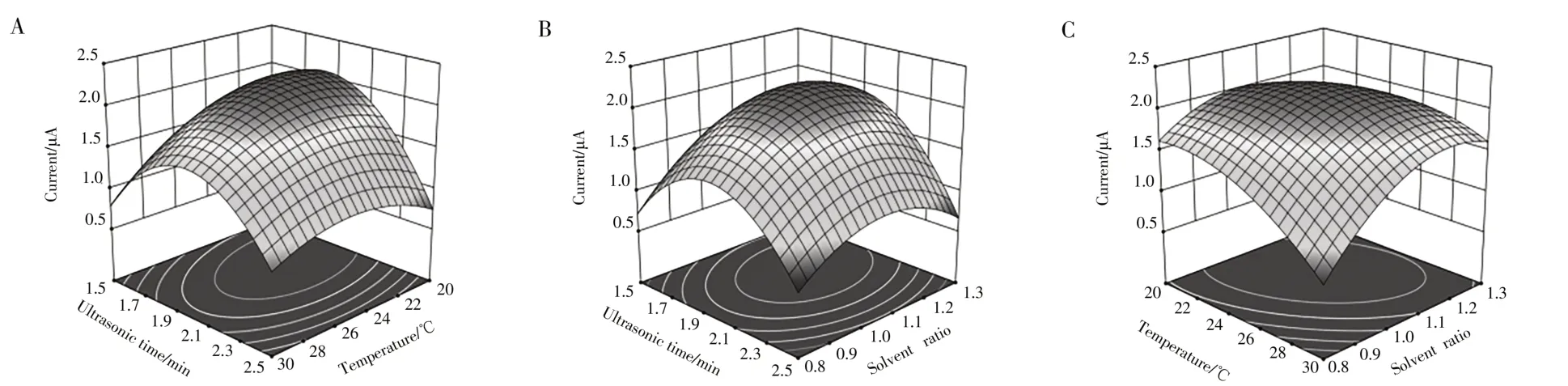
图2 超声时间与温度(A)、超声时间与溶剂比例(B)、温度与溶剂比例(C)对辅酶Q10电流值影响的响应面分析Fig.2 RSM analysis of the current response toward ultrasonic time and temperature(A),ultrasonic time and solvent ratio(B)and temperature and solvent ratio(C)
以上优化得到的最佳条件为:超声时间1.88 min,温度23.3℃,甲醇∶乙醇溶剂配比为1.1∶1,电流值的预测值为2.176 μA。结合实际情况,调整超声时间为1 min 50 s,温度为25℃,溶剂配比为1.1∶1,重复4次平行测定的平均值为2.054 μA,与由回归方程给出的理论值相吻合。证实该模型能精准地反映各因素对电流值的影响,可作为玻碳电极上CV测定辅酶Q10的最优条件。
2.3 辅酶Q10的吸附伏安响应与分析性能
在优化条件下测定不同浓度(0.025、0.25、0.5、1.25、2.5、12.5、25.0 μmol/L)辅酶Q10标准溶液的CV电流并进行回归分析,以进行辅酶Q10的定量测定,并根据回归方程计算检出限(LOD)。结果显示,其氧化峰电流随辅酶Q10浓度的增大而增大(图3),且与辅酶Q10浓度的对数呈线性相关,线性范围为0.025~25.0 μmol/L,线性方程为I=2.554+1.479lgC,相关系数(r2)为0.997,LOD([lgLOD=(3SD-a)/b])为19.0 nmol/L。取0.5 μmol/L辅酶Q10标准溶液,重复测定5次,RSD为1.1%,证明该方法的精密度良好。实验结果表明吸附伏安法可灵敏地测定辅酶Q10,与其他检测辅酶Q10的方法相比,本方法表现出很好的分析性能,其线性范围及检出限均达到较高水平(见表2)。

表2 辅酶Q10测定方法的性能对比Table 2 Comparison for the detection performances of CoQ10 with different methods
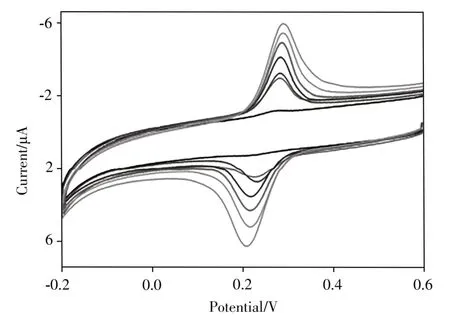
图3 不同浓度辅酶Q10的循环伏安图Fig.3 Cyclic voltammograms for different concentration of CoQ10
2.4 实际样品的测定
在优化条件下,采用CV法对3种胶囊样品中的辅酶Q10进行测定,同时进行3种不同浓度水平的加标回收率实验,结果见表3。测得回收率为85.9%~109%,相对标准偏差(RSD)为1.0%~11%。该结果在可接受的范围内,说明该方法测定辅酶Q10是一种切实有效的方法。
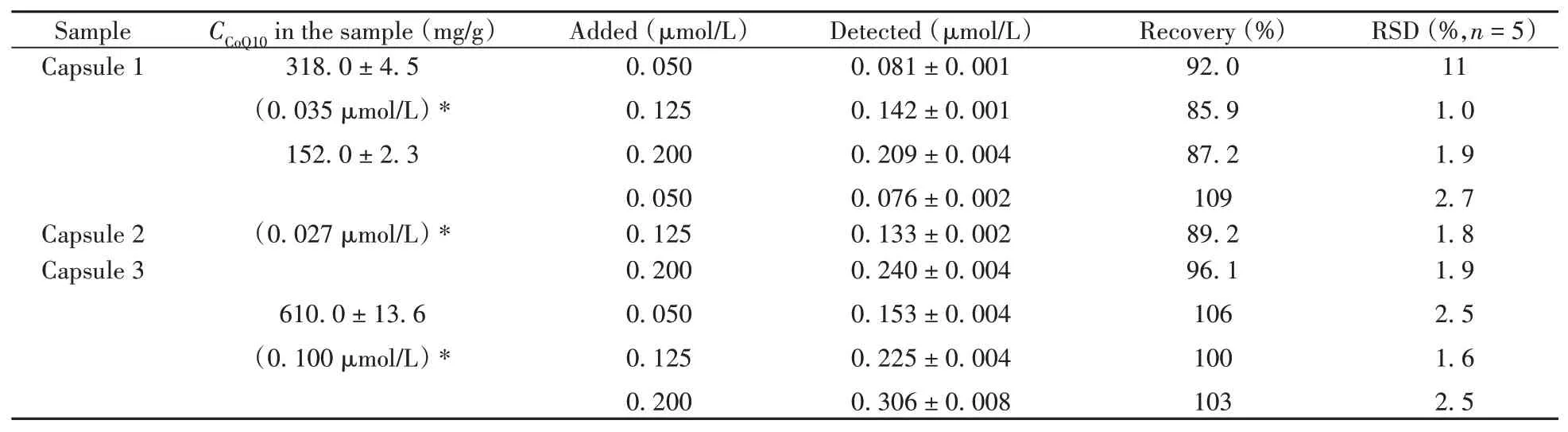
表3 样品中辅酶Q10的测定结果及回收率Table 3 The detected results and recoveries of CoQ10 in real samples
3 结论
本研究实现了辅酶Q10的吸附伏安法测定,并采用Box-Behnken响应面方法优化了样品处理及测定条件为:样品提取超声时间为1 min 50 s,测定温度为25℃,电解质溶剂配比为1.1∶1的甲醇-乙醇。上述条件下,循环伏安电流与辅酶Q10浓度的对数在0.025~25.0 μmol/L范围内呈线性相关,LOD为19.0 nmol/L,可对辅酶Q10进行精确的定量分析。

