基于多壁碳纳米管增敏的电化学传感器检测萘乙酸
杜科志,杜海军,王世彬,张 艳,李玉美
(贵州民族大学 化学工程学院,贵州 贵阳550025)
黄芪是中医里最重要的补气药材之一,含有大量药用成分和多种氨基酸[1],对人体具有良好调养作用。为了提高黄芪产量,在种植中使用植物生长调节剂是主要的手段之一。萘乙酸(NAA)作为一种植物生长调节剂,能够促进植物生根和细胞分裂[2],被广泛应用于果蔬和中药材的种植中[3-4]。刘建霞等[5]研究发现萘乙酸在黄芪种植中,能够缓解盐胁迫作用,增加黄芪的环境适应能力,对于提高土壤盐渍化严重地区黄芪产量提供了一种新的方法。但萘乙酸的过度使用易导致药材中残留物超标,不仅影响中药材的品质,而且对人体健康存在潜在威胁[6]。目前,对于中药材中萘乙酸的检测主要有气相色谱法[7-8]、液相色谱法[9-10]、电化学法[11-13]。其中电化学法因样品前处理简单,检测快速,仪器轻便以及适合现场快速分析,而受到研究者的广泛关注。
多壁碳纳米管(MWCNTs)是一种具有高比表面积的新型导电碳纳米材料[14],在电子信息、能源和传感器等领域应用广泛。由于范德华力与π-π共同作用容易引起纳米材料团聚,导致MWCNTs分散性差[15]。十二烷基苯磺酸钠(SDBS)作为一种常见的表面活性剂,将其加入到碳纳米管中,不仅能够提高其分散性[16],防止材料团聚,还能提高电极灵敏度[17]。因此,将其应用到电化学传感领域值得研究。本文将MWCNTs和SDBS制成复合物,然后将其修饰至玻碳电极表面构建高灵敏度的电化学传感器,对萘乙酸进行电化学分析,并利用差分脉冲伏安法实现了黄芪中萘乙酸的快速电化学检测。
1 实验部分
1.1 仪器与试剂
蔡司SIGMA 500扫描电镜(德国卡尔蔡司公司);CHI660E型电化学工作站(上海辰华仪器公司),工作电极为玻碳电极(GCE),辅助电极为铂电极,参比电极为Ag/AgCl电极(3 mol/L KCl);pHS-3C型酸度计(上海雷磁仪器厂);KQ-3200DB型数控超声波清洗器(郑州豫华仪器制造有限公司)。
多壁碳纳米管(≥95%)、萘乙酸(分析纯)购自国药集团化学试剂有限公司;SDBS(98%,上海阿拉丁生化科技股份有限公司);氯化钠(98%,天津市优谱化学试剂有限公司);浓硫酸、无水乙醇(分析纯,重庆川东化工有限公司);硫酸钠(分析纯,江苏强盛功能化学股份有限公司);实验用水均为超纯水;黄芪(云南帅润科技有限公司)。
1.2 实验方法
1.2.1 电极预处理与活化将玻碳电极(GCE)在抛光绒布上依次用0.3、0.05 μm Al2O3粉末打磨至镜面。用水冲洗后,依次在无水乙醇、硝酸溶液(1:1,体积比)和水中超声清洗3 min。利用循环伏安法在5 mmol/L铁氰化钾溶液中检验电极可以使用后,用水冲洗后烘干待用。
将电极置于0.5 mol/L硫酸溶液中静置5 min,在电位区间为-0.2~2 V,扫描速度为0.05 V/s的条件下循环伏安扫描20圈,用水冲洗后烘干待用。
1.2.2 SDBS-MWCNTs修饰电极的构建取4 mg MWCNTs和1 mg SDBS于2 mL水中,超声分散1.5 h得到SDBS-MWCNTs复合物。取5 μL SDBS-MWCNTs复合物滴涂于GCE表面,自然风干。将制备好的SDBS-MWCNTs/GCE置于pH 6.0的PBS溶液中,利用循环伏安法在扫描速度为0.1 V/s,电位区间为0.6~1.3 V条件下扫描至图像稳定后,烘干待用。
取6 mg MWCNTs置于3 mL水中,按上述方法制备MWCNTs/GCE,烘干待用。
1.2.3 黄芪中萘乙酸的提取参考文献的一步超声提取方法并稍作改进[18]:30 g干燥黄芪粉碎,过100目筛后,取5 g黄芪粉和2 g NaCl于10 mL水中浸泡3 h,加入20 mL乙醇,超声提取40 min,加入适量无水硫酸钠静置1 h,离心后取上层清液旋转蒸发至1 mL,溶于5 mL无水乙醇溶液中,待测。
1.2.4 电化学测量利用循环伏安法对50 μmol/L NAA进行电化学行为探究和实验条件的选择(电位区间为:0.6~1.3 V,扫描速度为0.1 V/s);利用线性扫描伏安法探究了扫描速度的影响(电位区间为:0.6~1.3 V,扫描速度区间为:0.02~0.4 V/s);利用差分脉冲伏安法对NAA进行检测,且探究了该电极的稳定性和抗干扰能力(电位区间0.6~1.3 V,电位增量0.004 V,振幅0.05 V,脉冲宽度0.05 s)。
2 结果与讨论
2.1 碳纳米管的结构表征
为了解SDBS与MWCNTs的复合程度,使用扫描电镜观察了MWCNTs和SDBS-MWCNTs材料的表面形貌。从图1A中可以看出,MWCNTs材料中有明显的管状结构,其特殊结构能增加电极的有效面积。图1B为加入SDBS后MWCNTs的表面形貌,依旧有较为明显的管状结构,可见SDBS的加入并未破坏MWCNTs的本身结构[15],且其包覆在MWCNTs周围,可使MWCNTs更好地分散在溶剂中[19],进一步将MWCNTs修饰至电极表面可提高检测灵敏度。
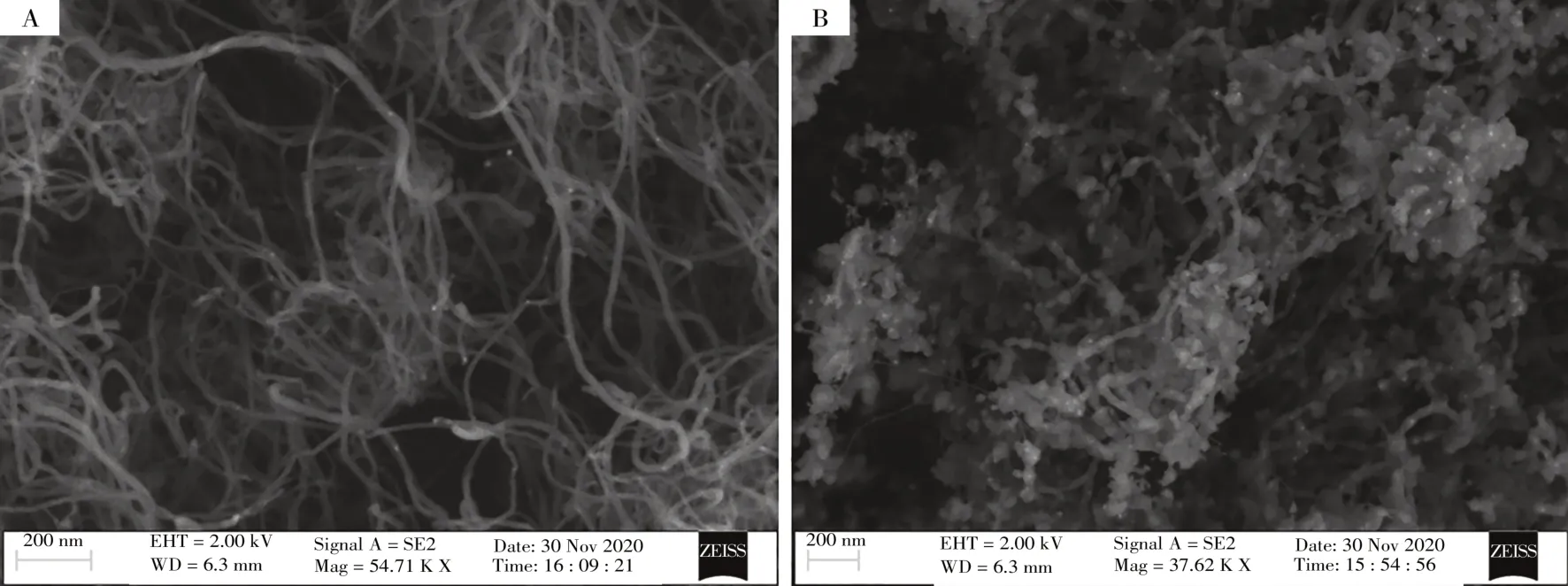
图1 MWCNTs(A)和SDBS-MWCNTs(B)的SEM图Fig.1 SEM images of MWCNTs(A)and SDBS-MWCNTs(B)
2.2 NAA的电化学行为
为了探究NAA在不同修饰电极上的电化学行为,分别使用GCE、MWCNTs/GCE和SDBS-MWCNTs/GCE对50 μmol/L NAA进行循环伏安扫描。实验结果如图2所示,在3种电极上均出现了单一的阳极氧化峰。由于无修饰材料,GCE的测试结果(曲线1)表明,NAA仅出现一较弱的阳极氧化峰,其峰电位为1.065 V,峰电流为0.795 3 μA。MWCNTs/GCE的测试结果(曲线2)表明,NAA的峰电位(1.028 V)负移,峰电流(7.506 μA)明显增强,说明MWCNTs对NAA有一定的电催化活性。利用SDBS-MWCNTs/GCE探究NAA的电化学行为(曲线3),显示NAA的峰电位(1.029 V)无明显变化,但峰电流(18.42 μA)进一步增强,这是由于SDBS的加入提高了MWCNTs的分散度,增大了电极的有效面积,有效提高了电子传输效率,增加了玻碳电极检测的灵敏度。
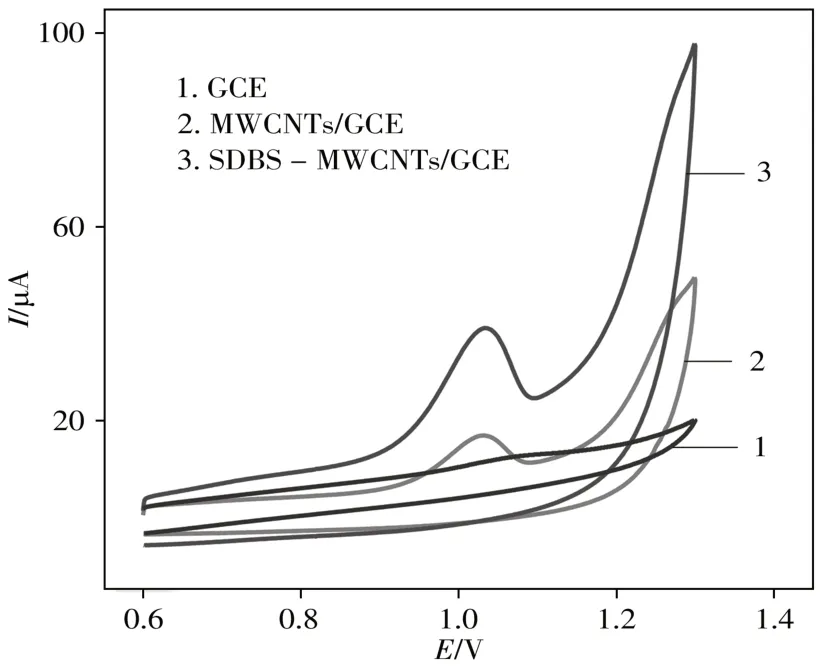
图2 GCE、MWCNTs/GCE和SDBS-MWCNTs/GCE在50 μmol/L NAA中的循环伏安图(CV)Fig.2 CV curves of GCE,MWCNTs/GCE and SDBS-MWCNTs/GCE
2.3 实验条件的优化
2.3.1 SDBS浓度的影响为了考察SDBS浓度对电化学检测的影响,在MWCNTs溶液中分别加入质量浓度为0.125、0.25、0.375、0.50、0.65、0.75 mg/mL的SDBS用于制备SDBS-MWCNTs/GCE,将修饰电极置于含有50 μmol/L NAA的PBS溶液中,利用循环伏安法考察了SDBS浓度对SDBS-MWCNTs/GCE电化学信号强度的影响。实验结果如图3所示,随着SDBS质量浓度的增加,该修饰电极的检测灵敏度不断增强,这是由于SDBS的加入提高了多壁碳纳米管的分散程度,增大了电极的有效面积。但当SDBS质量浓度增大到一定程度后,峰电流值无明显增强。因此,SDBS质量浓度以0.5 mg/mL为最佳。

图3 SDBS浓度对NAA氧化峰电流的影响Fig.3 Effect of SDBS concentration on oxidation peak current of NAA
2.3.2 滴涂量的影响滴涂量的选择也会影响传感器的检测效果。本实验将固定浓度的SDBS-MWCNTs修饰材料滴涂在玻碳电极表面,考察了滴涂量在3~8 μL范围内NAA在修饰电极上的峰电流响应。发现随着滴涂量的增大,峰电流强度先增强后下降。这是由于随着SDBS-MWCNTs滴涂量的增加,电极的比表面积增大,提高了电极检测灵敏度,但滴涂在电极表面的材料过多时,则减少了电极活性点位与目标物的接触,从而使得峰电流不断下降[20]。本实验选择最佳滴涂量为5 μL。
2.3.3 pH值的影响为了考察pH值对修饰电极测量NAA电化学信号的影响,在pH 2.0~11.0范围内,利用SDBS-MWCNTs/GCE对50 μmol/L NAA进行循环伏安扫描。结果表明在pH 2.0~6.0范围内,随着pH值的增加,峰电位负移,表明有质子参与NAA在SDBS-MWCNTs/GCE表面的反应。在pH 6.0~11.0范围内,峰电位变化不明显。如图4所示,在pH为4.5~6.5范围内,Epa与pH值呈良好的线性关系,线性拟合方程为Epa=-0.052pH+1.422(r2=0.999)。由能斯特方程知,斜率k=∂Epa/∂pH=0.059m/n(式中,m为质子转移数,n为电子转移数),m/n≈1,可见NAA在电极表面发生氧化反应过程中的电子转移数和质子转移数相等。在pH 4.5~6.5范围内,峰电流则随着pH值的增大呈先增大后减小趋势。因此,本研究选择最佳pH值为6.0。
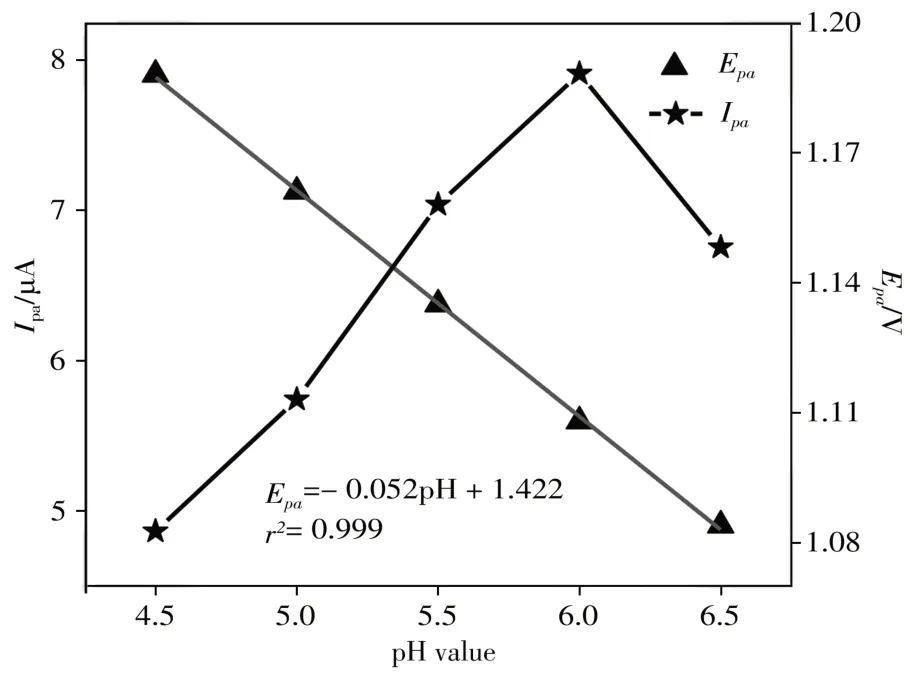
图4 pH值对NAA氧化峰电流的影响Fig.4 Effect of pH value on oxidation peak current of NAA
2.4 扫描速度的影响
为了考察扫描速度(v)对NAA检测的影响,在pH 6.0的PBS缓冲溶液中,分别以不同扫描速度(0.02、0.05、0.1、0.2、0.3、0.4 V/s)对50 μmol/L NAA进行线性伏安扫描,结果如图5所示。随着扫描速度的增加,背景电流增大,峰形逐渐变窄,峰电位正移,氧化峰电流(Ipa)不断增强。图5插图中Ipa与v呈良好线性关系,线性拟合方程为Ipa=96.91v+3.41(r2=0.993),表 明NAA在SDBS-MWCNTs修饰电极上的氧化反应受吸附控制[12]。

图5 扫描速度的影响Fig.5 Effect of scan speed
由于反应受吸附控制,根据峰电流吸附方程[21]:Ip=n2f2vAГ0*/4RT=nFQv/4RT。式中,F为法拉第常数,Q为氧化峰面积,R为气体摩尔常数,T为热力学温度。可求得该电极反应中电子转移数n=1.85≈2。由“2.3.3”中得到电子和质子的转移数相同,因此,判断NAA在电极表面发生了2个质子和2个电子参与的电化学氧化反应。
2.5 线性范围与检出限
为了更好地实现对NAA低浓度检测,采用修饰电极分别利用循环伏安法、线性扫描伏安法和差分脉冲伏安法(DPV)对低浓度NAA进行测定。发现当NAA处于较低浓度时,DPV法能够得到较为灵敏的氧化峰峰形。因此,本实验在最优条件下,利用DPV法考察了不同浓度(0.4、1、3、5、7、9、15、20、25、30、35、40、45 μmol/L)NAA的氧化峰电流响应情况。从图6可以看出,随着NAA浓度的增加,氧化峰电流增大,且峰电流与NAA浓度在0.4~45 μmol/L范围内呈良好的线性关系,线性方程为Ipa=0.103c+0.114(r2=0.991),检出限(S/N=3)为0.07 μmol/L。

图6 SDBS-MWCNTs/GCE对不同浓度NAA的差分脉冲伏安图Fig.6 DPV curves of SDBS-MWCNTs/GCE in different concentrations of NAA
将本方法与其他NAA传感器进行比较(如表1),相较于其他NAA传感器,本方法具有更低的检出限,且制备方法简单,更适于实现NAA的现场快速检测。
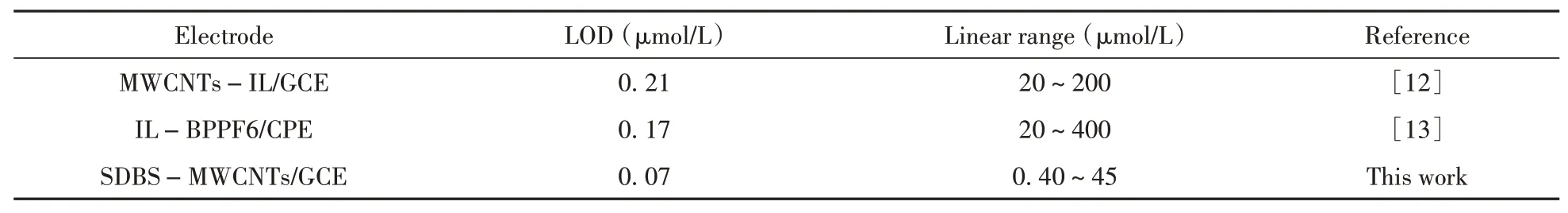
表1 不同NAA电化学传感器的比较Table 1 Comparison of different NAA electrochemical sensors
2.6 稳定性、重现性与选择性
在pH 6.0的PBS缓冲溶液中对50 μmol/L NAA使用同1根SDBS-MWCNTs/GCE进行重复检测,测量次数达7次时峰电流的相对标准偏差(RSD)为1.3%。将该电极置于5℃冰箱中密封保存1周后,用同样的方法测得氧化峰电流响应值下降5.7%,测量7次的RSD为1.3%。说明该电极具有较好的稳定性。同时制备5根SDBS-MWCNTs/GCE电极对50 μmol/L NAA进行检测,其氧化峰电流的RSD为9.9%,表明该电极的重现性良好。
控制相对测量误差在5%以内,利用DPV法探究了常见干扰物对SDBS-MWCNTs/GCE检测NAA的影响。实验结果表明,25倍的Na+、K+、Ca2+、PO3-4、Cl-和SO2-4,50倍的葡萄糖、淀粉和氨基酸,以及常见的植物生长调节剂如吲哚乙酸、吲哚丁酸、2,4-D、激动素均不干扰测定。表明所制备的SDBS-MWCNTs/GCE具有较强的抗干扰能力。
2.7 黄芪中萘乙酸的检测
利用“1.2.3”方法提取黄芪中的残留物,通过DPV法进行测量,未发现NAA残留物的存在。采用GB/T 37500-2019中的高效液相色谱法[22]验证上述结果,样品同样未检出NAA。采用标准加入法进行加标回收率实验,利用SDBS-MWCNTs/GCE传感器对加标量分别为5、15、30 μmol/L的NAA进行测定,测得回收率为97.8%~102%,RSD小于5.0%(见表2),表明该传感器可用于实际样品的检测。

表2 黄芪中NAA的含量及其回收率测定(n=3)Table 2 Content of NAA and its recoveries in Astragalus(n=3)
3 结论
本研究利用SDBS和MWCNTs制成复合物修饰玻碳电极,对萘乙酸进行了电化学分析。并利用DPV法对黄芪中的萘乙酸进行检测,效果良好。该传感器的制备方法简单,成本较低,且具有较好的稳定性和重现性,有望应用于中药材现场的快速检测。

