煤焦油渣热解特性及动力学分析
常秋连
(中煤科工清洁能源股份有限公司,北京 100013)
煤焦油渣(简称焦油渣)是煤在气化或焦化过程中,由机械化焦油氨水澄清槽底部排出的黑色或黑褐色黏稠膏状固体。焦油渣成分复杂,主要含有苯系物、多环芳烃、含氮和含硫杂环化合物、重金属等多种污染物,目前被国家列为HW11类危险废物[1-2]。
焦油渣的处理方式主要包括萃取离心-油渣收集、做烧砖燃料、制备活性炭等[1]。虽然焦炉加热制度、装煤程序和配煤工艺等操作条件的改进,可大幅度降低废渣的生成量,但废渣的处理问题仍然存在。目前中国焦油渣回收利用的主要方式是将其作为塑性添加剂直接加入炼焦配煤中或用作型煤的黏结剂。但是,在混配过程中受原料黏稠性和组分波动的影响,存在因配料难以精准,造成焦炭质量不稳定、焦炉的热负荷增加等问题;同时,由于焦油渣黏度大,在混配过程中极易与皮带粘黏造成管路堵塞。因此,随着焦油渣年产量的不断递增,清洁高效利用方式的研发迫在眉睫。
研究发现,焦油渣中碳含量高(优质渣中碳质量分数不小于80%),灰含量低,是制备活性炭的优质原料;但是焦油渣又具有结构致密、结晶度高的特点,缺乏活化所需的初孔,活化困难,这限制了其在活性炭领域的应用。然而,笔者所在课题组前期研究发现[3],若将焦油渣进行高温热解,其中的非碳元素被高温分解,以气体形式释放,剩余碳元素则形成不规则排列的石墨微晶结构,这些微晶之间留有空隙,被热解过程中析出的焦油等无定形碳填充,这些无定形碳则为后续活化过程提供了丰富的活性位。热解是炭化过程的初始和伴随反应,是活性炭制备过程中最重要的工艺。热解可以改变化学键的断裂和重组,获得不同理化结构的活性炭前驱体。巩志强等[4]研究发现油泥与微藻生物质掺混可以有效降低油泥热解反应活化能。Wu等[5]研究认为,在热解过程中,最大质量损失率和气体组分释放率随升温速率的提高而增大。Valdes等[6]认为热解过程中煤焦化学结构的变化取决于生成气体的二次反应。全翠等[7]认为热解终温对煤焦强度和孔结构均有较大影响。Wang等[8]研究发现升温速率是生物质热解过程中的一个重要因素,它通过生物质颗粒的传热传质影响热解过程。Choi等[9]观察煤焦油沥青(CTP)热解过程的结构变化,从室温至600℃左右,微晶结构逐渐形成,尺寸增加;但在700℃时,微晶结构无序程度突然增大;在800~1000℃范围内,微晶结构有序性又继续增加。因此,热解条件的变化本质上改变了化学键的重组和断裂,从而得到具有不同理化结构的活化前驱体。
焦油渣主要是由高沸点有机物夹带煤粉、固体颗粒等物质冷却形成,与煤不同,焦油渣具有石墨化度更高、灰分低、活性低的特点,热解炭化机理与煤具有显著的区别。虽然关于褐煤、水煤浆等煤基材料热解炭化机理的研究已经很多,但是关于焦油渣热解炭化机理的相关研究仍鲜有报道。
将焦油渣热解分离成焦油和热解焦,将其中的焦油进行回收,剩余热解焦用作制备活性炭的原料。该方法对焦油渣成分的适应能力强,几乎不会造成二次污染,是实现焦油渣清洁、高效利用的有效手段。因此,焦油渣热解可以作为单独的燃前预处理工艺,对于控制环境污染具有重要意义;同时,热解条件对炭化物的孔隙、比表面积和活性产生直接影响。而热解过程升温速率和热解终温则对炭化物的反应活性产生重要影响。因此,对热解过程进行深入研究,可确定活性炭制备的最佳工艺条件,提高产品质量。
笔者对焦油渣的热解行为进行深入研究,利用热重-傅里叶红外(TG-FTIR)联用,将TG的定量分析和FTIR的定性分析相结合,探索热解过程挥发分及能量的释放规律,并选取适宜的热解函数计算其动力学参数,为实现焦油渣的综合、清洁、高效利用提供理论依据。
1 实验部分
1.1 材料
实验用焦油渣选自某焦化厂鲁奇加压气化工艺,为机械化焦油氨水澄清槽沉降在底部椎体中的半流动状膏体。100~110℃下干燥2 h,经破碎、球磨、过筛处理,得到粒径为100~200目的焦油渣样品,装袋密封备用。
1.2 热解实验和计算方法
焦油渣热解实验采用德国NETZSCH公司的STA 449 F3型热重-差热分析仪和德国Bruker公司的TENSOR 27型傅里叶变换红外光谱仪,以程序升温法自动记录升温过程中样品的热失重数据,利用红外光谱仪在线检测从热重分析仪释放出来的热解气体。分别考察升温速率8、25和50℃/min,热解终温950℃条件下样品的热失重和热解气体释放情况。实验开始前,先以50 m L/min的流量通入高纯氮气(体积分数99.999%)进行吹扫,以预先设定的升温速率升温,并记录此工况下的热重-微商热重曲线(TG-DTG)和红外光谱扫描数据。TGA与FT-IR气室温度均设定为200℃,由仪器自动控温,FT-IR光谱测量范围4000~600 cm-1,分辨率优于4 cm-1,波数精度优于0.01 cm-1,信噪比高于50000∶1,检测器为DLa TGS监测,光程长为128 mm,气体池容积8.3 m L,载气流量为80 m L/min,特征停留时间为气体池容积与载气流量的比值,接近6.225 s,扫描次数为8次。FT-IR光谱数据的处理采用NIST谱库来解析光谱图,然后提取产物的实时析出规律。由于热解产物中甲烷所在谱带与饱和烃的光谱交叉重叠,难以辨别,因此在提取甲烷特征波数的实时析出曲线时,采用相对参考强度和基线校正归零后的强度进行选取,并结合参考文献[10-14]进行辨别。
焦油渣热解反应为固定升温速率条件下的不可逆气-固非均相反应,关于气-固两相的反应模型较多,相关文献已进行详细总结[15-18],笔者采用差减微分法利用Freeman-Carroll模型计算焦油渣热解过程的动力学参数。
2 结果与讨论
2.1 焦油渣的物性及红外光谱跟踪分析
2.1.1 工业及元素分析
对制得的焦油渣样品的物性进行分析,结果见表1、表2。

表1 煤焦油渣基本性质及组成Table 1 Basic properties of coal tar residue w/%

表2 脱水后煤焦油渣和固体物的主要组成对比Table 2 Composition comparisons between coal tar residue and solid after dehydration
由表1可知,焦油渣中正己烷可溶物(可溶解油组分)质量分数为48.78%,含油量高;而甲苯不溶物、四氢呋喃不溶物、正己烷不溶物质量分数相差不大,说明沥青类物质含量低。由表2看到,焦油渣中固体物(即甲苯不溶物)的灰分质量分数更高,是焦油渣原料灰分的2倍,为11.13%;而固体物中氢质量分数仅为2.26%,其H/C原子比较原料更低,仅为0.34。由表2结果推断该焦油渣中固体物组分的反应活性较低。
2.1.2 红外光谱跟踪分析
图1为不同升温速率下焦油渣热解气体产物析出的三维图。图1中,焦油渣热解过程在4000~3500 cm-1、2000~1500 cm-1处的吸收峰对应于水蒸气的特征峰;在2180 cm-1和2330 cm-1处对应于CO和CO2的特征峰,其中CO2的吸收峰主要是由于羰基和羧基的断裂和振动造成的,CO的吸收峰主要是由醚键和羧基的断裂造成的;1520~860、1900~1600、3000~2700 cm-1等处出现了强吸收峰,分别对应于C—O和C—C骨架振动;芳香族C=O伸缩振动、—CH3对称变角振动和不对称变角振动,以及C—H(甲氧基、亚甲基、甲基)的断裂和伸缩振动,分别对应于各类有机气体,如醇和酚类、羧酸类、酮类及烷烃类等大分子物质。
由图1看到,在整个热解过程中,不同升温速率下焦油渣样品的红外吸收峰的强度产生了非常明显的差异,说明热解速率改变了挥发分的释放情况,焦油渣在不同升温速率下热分解时,其相对含量发生明显改变。由图1可知,升温速率不同,气体产物的相对浓度随温度的变化趋势有所差别,但是释放气体的种类和相对比例基本相同,表明在该实验条件下,升温速率的变化未改变焦油渣的分解机理。
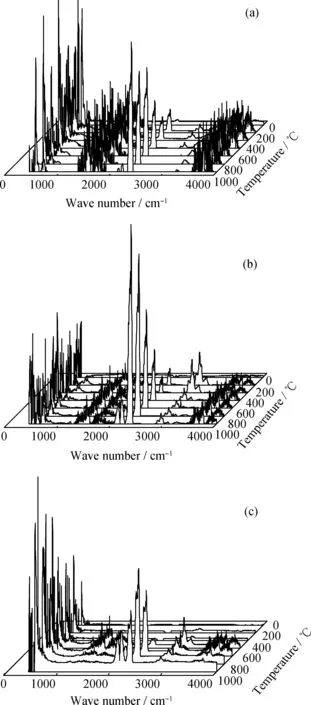
图1 不同升温速率下焦油渣热解气体产物析出红外三维谱图Fig.1 Three dimensional infrared spectra of pyrolysis gas products at different heating rates
2.2 升温速率对焦油渣热解过程影响分析
图2为不同升温速率下焦油渣热解过程的TG-DTG曲线。图2中,焦油渣热解过程主要包括3个阶段:第1阶段(初温~140℃)为自由水、结合水析出过程,失重质量分数约占总失重的1.86%;第2阶段(140~650℃)为活泼热分解阶段,样品快速失重,DTG曲线出现最大失重峰,红外谱图(图1)中出现强烷烃、羧酸、甲烷、CO2的吸收峰,有机物在此阶段出现大量分解,失重率达到峰值,失重质量分数约占总失重的86.60%;第3阶段(650~1000℃)为高温缩聚阶段,DTG曲线出现第2失重峰,失重质量分数约占总失重的11.54%,结合图1可知,该阶段析出物以CO2、CO和少量CH4为主。

图2 不同升温速率下煤焦油渣的TG-DTG曲线Fig.2 TG-DTG curves of coal tar residue at different heating rates
热解特性参数是反映热解过程挥发分析出难易程度以及析出量多少的重要指标。笔者借鉴文献[14-15]提出的表征挥发分析出难易程度的综合释放特性指数k来分析焦油渣的挥发分析出特性。结合图2,焦油渣在热解过程中,分别在低温段(0~630℃)和高温段(630~1000℃)出现2个明显的DTG峰值,因此,将计算过程分低温段和高温段分别考虑,计算结果见表3和表4。
根据图2和表3,在低温段,随着升温速率的提高,焦油渣的起始热解温度、最大失重速率、最大失重速率对应温度均增加,图2中曲线整体向高温端移动。这是因为提高升温速率,样品在某一温度处的停留时间变短,又因为样品装填在坩埚内,存在传热阻力,导致样品内外温差增大,在相同温度下的分解量减少。此外,提高升温速率意味着焦油渣挥发分的析出形式从长时间缓慢析出变为短时间快速析出,这也导致DTG曲线的失重峰明显增大[15-16]。
由表3和表4看到,焦油渣低温段的最大失重速率均大于高温段的,表明挥发分释放主要集中在低温段。在整个温度段内,随着升温速率的增大,半峰温度宽度ΔT1/2及热解产物释放特性指数k增大,表明提高升温速率使热解产物释放更加集中,挥发分释放更加剧烈,从而提高了热解速率。结合图2分析,随着升温速率的增加,煤焦产量增大,这是因为挥发分的短时间集中释放,增大了颗粒内挥发分与高温煤焦的接触几率,促使其发生二次反应,使挥发分的析出受到抑制,焦油发生再沉积和再聚合反应,二次裂解产生更多的小分子化合物,二次反应产物在煤焦表面沉积,使得煤焦产量增大[17-18]。

表3 不同升温速率条件下焦油渣的低温段(0~630℃)热解特性参数Table 3 Pyrolysis parameters at low-temperature stage(0-630℃)of coal tar residue at different heating rates

表4 不同升温速率条件下焦油渣的高温段(630~1000℃)热解特性参数Table 4 Pyrolysis parameters at high-temperature stage(630-1000℃)of coal tar residue at different heating rates
2.3 焦油渣热解产物释放特性分析
焦油渣热解过程中非碳元素(氧、氮、氢)被分解成气体排出,而剩余碳原子则形成类石墨微晶。不规则排列的微晶之间留有各种不同形状的空隙,这些空隙便是活性炭产品孔道结构的主要来源。因此,对焦油渣热解过程气体产物的释放进行研究,可以帮助分析热解对焦油渣基活性炭孔结构形成过程的影响。
焦油渣热解过程检测到的热解气体产物主要有CO2、CO和CH4,释放曲线如图3所示。
2.3.1 CO2释放特性
由图3(a)看到,随着升温速率的增加,CO2的初始析出温度升高,在400℃开始出现析出峰,第1个析出峰值出现在480℃左右,并且在700~800℃处出现最大析出峰值;且随着升温速率的增加,峰面积增大,析出峰值向高温方向移动。这是由于焦油渣中含有一定量的含氧羧基官能团,在温度小于500℃时发生分解;在700℃之后的析出峰主要来源于醚键、醌键、高热稳定性的羧基官能团(如苯甲酸)等的分解。
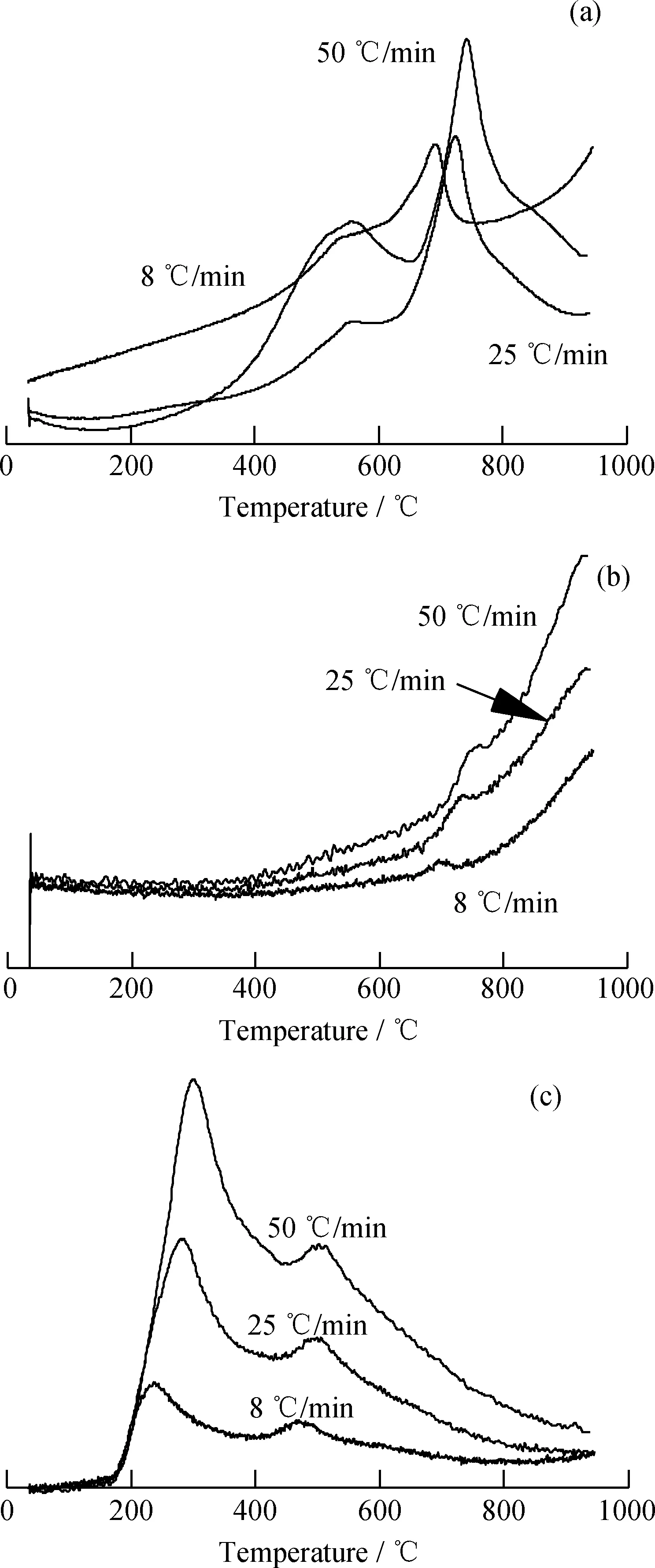
图3 不同升温速率下焦油渣热解产物析出曲线Fig.3 Precipitation curves of pyrolysis products of coal tar residue at different heating rates
研究人员通过对煤热解的研究发现[19],CO2一般来源于煤中的羧基、酯等含氧化合物。其中CO2的初始释放温度一般为200℃,释放峰温一般为500℃左右。但是笔者把CO2的初始释放温度提高至400℃,释放峰温增大至700~800℃,且随着升温速率的增加,释放峰温向高温方向移动。研究发现[3-6],羧基的热解温度小于500℃;当温度大于500℃时,样品中已经没有羧基。因此,焦油渣中CO2主要来源于醚键及高热稳定性的羧基官能团(如苯甲酸)等。当升温速率较慢时,焦油渣内高热稳定性的羧基官能团可以充分吸收热量而发生完全反应,但是当升温速率加快,在达到同等温度时,羧基官能团无法在短时间内获得反应需要的足够热量,进而使反应温度向高温方向移动;另外,热解过程中的O大部分以含氧官能团热分解的形式释放(如CO2、CO等),但仍有一部分进入焦油中,形成含氧化合物(如酚等),而快速升温会使焦油大量释放,这也改变了CO2的析出量。因此,改变升温速率可以影响含氧官能团的存在及释放形式,进而影响煤焦的孔道结构。
2.3.2 CO释放特性
由图3(b)看到,随着温度的增加,CO的析出量迅速增大。CO来源复杂,一般认为低温(350~500℃)下的CO主要来源于羰基裂解;500~800℃范围内的CO主要来源于酚类的裂解,而700~800℃的CO主要来源于反应活性弱、稳定性好的羟基、甲氧基等含氧官能团的裂解,同时,CO2与剩余碳发生反应也会产生CO;而大于800℃高温区的CO的释放主要与酚类物质、醚键、含氧杂环结构有关[20]。随着升温速率的增加,CO的析出速率增大。这是因为,增大升温速率,热解速率增加,可以使焦油渣样品在相同时间内获得更多热能,分子结构受到更加强烈的能量冲击,导致在达到相同温度时,在慢速升温条件下不能断裂的化学键发生裂解,进而引发更多含氧结构发生快速断裂,从而促进CO的快速释放。
2.3.3 CH4释放特性
由图3(c)看到,CH4在165℃开始析出,随着温度的升高,析出速率逐渐增大。CH4的释放呈现明显的双峰形状,在250℃附近出现第1个最大峰值;继续升高热解温度,在500℃附近出现第2个较小的峰值。低温条件下(≤300℃)释放的CH4主要来自原料颗粒中物理吸附的CH4产生的脱附行为;500℃附近出现的第2个峰主要来自位于3000~2700 cm-1区间的含有甲氧基、亚甲基和甲基官能团的脂肪链、芳香侧链的断裂[12]。
由图3(c)还看到,随着升温速率的增加,CH4的峰面积增大且最大析出峰值向高温方向移动,这主要是由于快速升温条件导致游离相中的长链正构烷烃的部分裂解所致;此外,快速升温条件下,能量的大量聚集导致高温区释放的挥发分出现了明显的二次反应,如焦油破裂等,进而促进了CH4的释放。
2.4 焦油渣热解反应动力学分析
焦油渣热解过程属于程序升温下旳非等温热重实验,由固体物质热解为固态和气态物质的过程,可以使用多重扫描速率法或等转化率法进行表观活化能的计算,该方法可以避免因为不同模型的选择而带来的误差。采用差减微分法Freeman-Carroll模型计算焦油渣热解过程的动力学参数,计算公式见式(1)[3]。

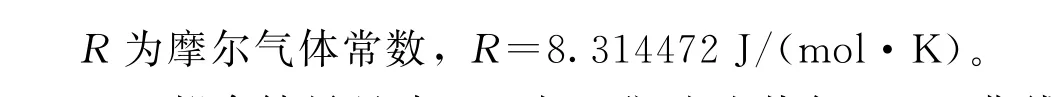
拟合结果见表5。由于焦油渣热解DTG曲线(图1)呈现出位于不同温度区域的单峰,故需分段进行动力学参数的计算,其中r2是线性相关系数。

表5 焦油渣热解动力学参数Table 5 Pyrolysis kinetic parameters of coal tar residue
根据表5,以Freeman-Carroll模型对实验数据进行拟合,线性相关系数r2的值均较高,说明所选的函数可以用来描述焦油渣的热解反应特性。
对比表5中各升温速率下焦油渣的反应活化能可以看出,低温段的活化能、指前因子均低于高温段;对于高温段,在较低的升温速率下热解活化能略有下降,但是当升温速率增大至50℃/min时,活化能迅速增大,说明适宜的升温速率有利于焦油渣挥发分的析出和二次裂解反应的发生,过高的升温速率则抑制了二次裂解的发生,这从图3的气体释放向高温端偏移也可以看出。
为考察活化能和指前因子的关系,以活化能E对指前因子的对数lnA作图,结果如图4所示。由图4可看出,活化能和指前因子之间存在着相互补偿的关系,即存在动力学补偿效应,线性相关系数r2为0.987。因此,如果在实验中发现反应速率越快,样品的活化能越大,则可能是由动力学补偿效应引起的[21]。
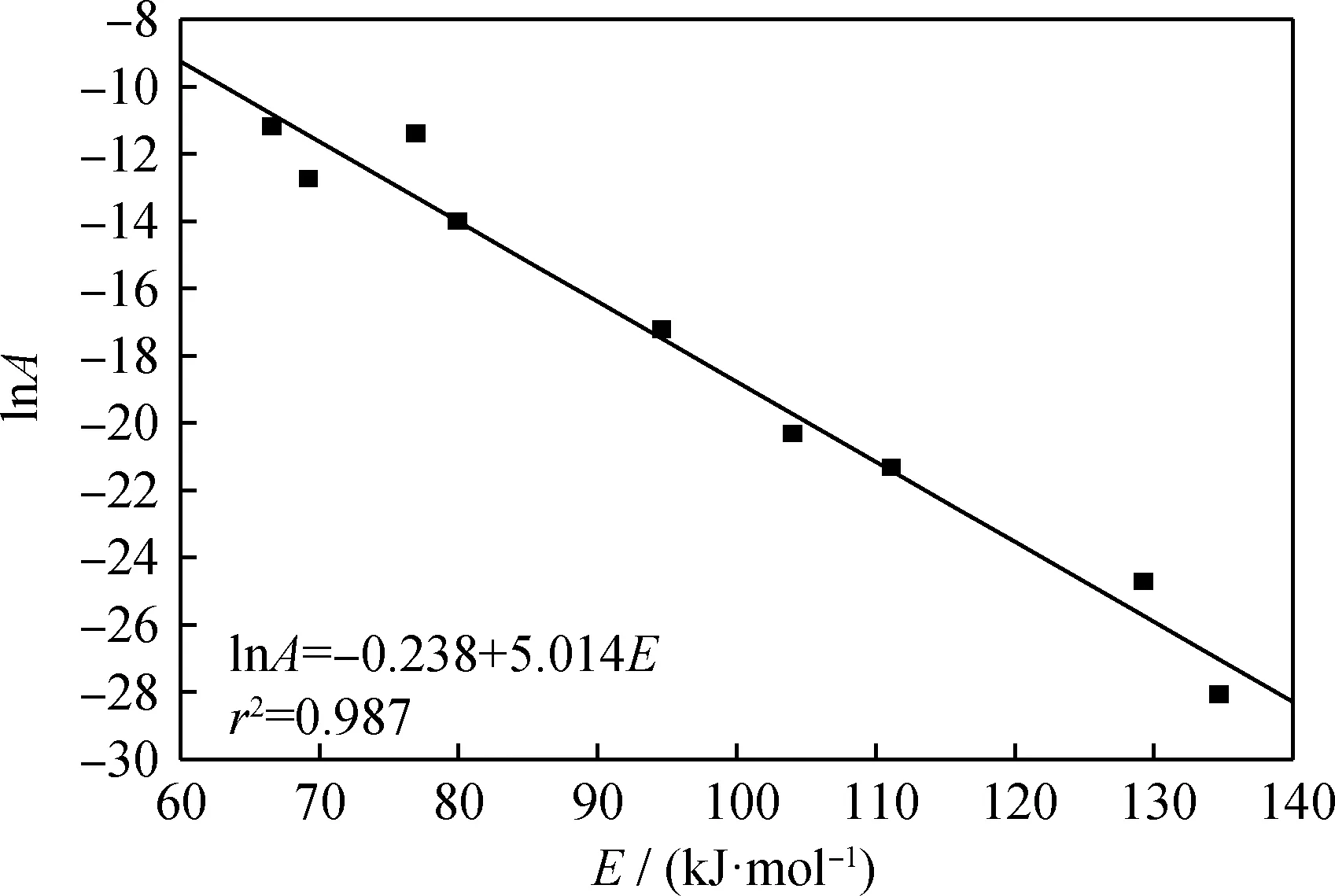
图4 活化能(E)与指前因子(A)的对数关系Fig.4 Logarithmic relationship between activation energy(E)and pre-exponential factor(A)
3 结 论
(1)不同升温速率下焦油渣的热解可分为3个阶段:低温干燥脱气阶段、活泼热分解阶段和热解缩聚阶段。在低温段,起始热解温度、最大失重速率和最大失重速率对应温度均随升温速率的增加而增大;高温段最大失重速率均低于低温段的。
(2)随着升温速率的增加,焦油渣TG和DTG曲线均向高温端移动,热解产物释放特性指数增大,升温速率对热解反应特征参数具有正相关的影响;活泼热分解阶段的失重率基本保持不变,提高升温速率对该阶段挥发分的析出量影响不大。但是,提高升温速率有利于二次裂解反应的发生,使挥发分释放受到抑制,二次反应产物沉积在煤焦表面,导致煤焦产率增大。
(3)焦油渣热解过程产物中的CO2主要来源于醚键及高热稳定性的羧基官能团;CO来源于反应活性弱、稳定性好的羟基、甲氧基等含氧官能团的裂解;低温下CH4的释放主要来自原料颗粒中物理吸附的CH4产生的脱附行为,高温下释放的CH4主要来自含有甲氧基、亚甲基和甲基官能团的脂肪链、芳香侧链的断裂。热解反应活化能在低升温速率下变化不大,但是随着升温速率的提高,活化能迅速增加,说明适宜的升温速率有利于挥发分的析出和二次裂解反应的发生,过高的升温速率抑制了二次裂解的发生;在不同升温速率下活化能和指前因子存在较好的动力学补偿效应。

