Ag纳米粒子在TiO2四棱柱阵列上的可控生长及其SERS效应
陈韶云,张行颖,刘 奔,田 杜,李 奇,陈 芳,胡成龙,陈 建
(1.江汉大学光电化学材料与器件教育部重点实验室,化学与环境工程学院,武汉 430056;2.中山大学测试中心,广州 510275)
表面增强拉曼散射(SERS)是最灵敏、功能最强大的分析技术之一,可以将分子的散射截面提高到十亿倍,从而进行单分子检测[1~3].SERS具有很高的选择性和无损检测能力,因此广泛用于分析化学[4,5]、生物医学[6,7]和材料科学[8,9]等领域.常见的高灵敏度SERS基底主要由金(Au)或银(Ag)组成,Ag微纳结构的制备成本较低且形貌容易调控,如纳米粒子[10,11]、纳米线[12,13]、纳米棒[14,15]、纳米花[16,17]、立方体[18,19]、三角板[20,21]、树枝状[22,23]和3D层级结构[24,25]等,其中Ag纳米粒子(AgNPs)具有良好的表面效应和量子尺寸效应、尺寸可控且合成工艺简单,可以作为一种通用型SERS基底.但AgNPs具有高的表面能,单个AgNPs极易发生聚集,从而对其SERS活性和保存周期等产生不良影响.因此,在制备AgNPs时需要对其进行表面修饰以防止粒子团聚[26,27].目前,设计合成支撑AgNPs的基体是有效防止AgNPs聚集的一种方法.
在众多支撑材料中,半导体材料如二氧化钛(TiO2)[28]、氧化锌(ZnO)[29]和碲化镉(CdTe)[30]由于制备过程简单、易阵列化而被广泛用作支撑模板.TiO2因其良好的光催化性能、化学稳定性和无毒性,广泛应用于清洁能源、光催化和环境修复及检测领域.在SERS应用领域,TiO2阵列作为贵金属(Au,Ag)生长的支撑模板具有如下优势:(1)TiO2阵列可以轻易地在碳纤维、导电玻璃及聚合物柔性基体上生成,使SERS基底的应用多样化;(2)由于入射光与贵金属中电子之间的强相互作用,贵金属纳米粒子不仅可提高可见光照射下TiO2的光催化效率,同时充当捕获光致电子和空穴的陷阱,减少了光催化过程中电子-空穴的重新结合,使检测分子与基底之间因电荷转移引起的化学作用增强,从而提高基底的增强因子,同时有助于提高SERS基底的循环可回收性[31];(3)TiO2阵列结构能有效减少贵金属纳米粒子之间的大量聚集,提高纳米粒子之间电磁场耦合作用,使检测分子与基底之间因电磁场引起的物理作用增强.Zhang等[32]在TiO2纳米孔阵列上化学沉积Ag纳米粒子,制备了一种新型TiO2-Ag纳米孔阵列SERS基底,该基底对有毒有机物具有良好的微量检测能力.Wang等[33]针对实际水体中多种抗生素残留的检测,采用Ag同步沉积并掺杂TiO2制备了Ag-TiO2SERS基底,实现在复杂环境中不同抗生素的识别.Yang等[34]利用静电纺丝和煅烧法制备了TiO2纳米纤维,并通过沉积制备出不同Ag粒径分布的Ag-TiO2SERS基底,用于细胞的高效SERS检测.
本文在前期研究[35~38]的基础上,以钛酸四丁酯为前驱体,通过水热法在FTO玻璃的导电面上生长一层致密的TiO2四棱柱阵列,然后分别通过聚乙烯基吡咯烷酮(PVP)还原银氨溶液(Tollens试剂)以及柠檬酸三钠(TSC)还原硝酸银2种方式在TiO2四棱柱阵列上沉积Ag纳米粒子,实现AgNPs在TiO2四棱柱阵列上的可控生长,并以罗丹明6G(R6G)和三聚氰胺为探针分子进行了SERS检测研究.
1 实验部分
1.1 试剂与仪器
硝酸银(AgNO3)、氨水、柠檬酸三钠、浓盐酸、钛酸四丁酯和聚乙烯基吡咯烷酮(K-30,Mw=40000)均为分析纯,购于国药集团化学试剂有限公司;罗丹明6G和三聚氰胺购于上海阿拉丁试剂公司;Tollens试剂为自制;掺氟二氧化锡(FTO)导电玻璃购于深圳华南湘城科技有限公司.
Renishaw inVia型激光显微拉曼光谱仪(英国雷尼绍公司);JEOL-2010型透射电子显微镜(TEM,日本电子株式会社);SU8010型冷场发射扫描电子显微镜(SEM,日本日立公司);K-alpha+型X射线光电子能谱仪(XPS,美国赛默飞公司);D-MAX 2200型X射线衍射仪(XRD,Panalytical公司).
1.2 实验步骤
1.2.1 TiO2四棱柱阵列的制备 采用典型的水热法制备TiO2四棱柱阵列.将尺寸约为1.5 cm×5 cm的FTO导电玻璃置于丙酮/2-丙醇/乙醇(体积比为1∶1∶1)混合溶液中超声洗涤,用去离子水冲洗干净,置于真空干燥箱中干燥,备用.在50 mL烧杯中先后加入24 mL去离子水和24 mL浓盐酸(去离子水与浓盐酸的体积比为1∶1),搅拌10 min,加入0.8 mL钛酸四丁酯,继续搅拌约10 min.将配好的溶液倒入100 mL水热反应釜中,将清洗后的FTO斜置于反应釜中,导电面朝下,将反应釜置于鼓风干燥箱中,在150℃下反应5 h.反应结束后,将制备好的TiO2四棱柱阵列用去离子水冲洗数次,干燥待用.
1.2.2 PVP还原Tollens试剂制备TiO2@AgNPs结构 将生长TiO2四棱柱阵列的FTO玻璃置于不同浓度的Tollens试剂(1.5 mL,0.4~1.6 mol/L银氨溶液中加入20 mL乙醇)中于常温保持10~12 h;将0.5 g PVP加入至20 mL乙醇中配制0.225 mol/L的PVP-乙醇溶液,并将其倒入银氨溶液中,于60℃鼓风干燥箱中保持2 h.反应结束后,取出生长TiO2@AgNPs的FTO玻璃,用去离子水冲洗数次后,真空干燥待用,产物记为TiO2@AgNPs-PVP,如图1所示.
1.2.3 TSC还原AgNO3制备TiO2@AgNPs结构 将生长TiO2四棱柱阵列的FTO玻璃置于50 mL 0.0025 mol/L的AgNO3溶液(0.20 g AgNO3溶于50 mL H2O)中,用保鲜膜密封,于100℃鼓风干燥箱中煮沸10 min;将0.3 g TSC溶于10 mL去离子水中,移取1.75 mL TSC水溶液注入上述反应溶液中,继续加热10~80 min.反应结束后,取出生长TiO2@AgNPs的FTO玻璃,用去离子水冲洗数次后,真空干燥待用,产物记为TiO2@AgNPs-TSC,如图1所示.
1.2.4 SERS效应测试 选择R6G作为SERS探针分子,R6G水溶液的浓度为10-5~10-12mol/L.将TiO2@AgNPs-TSC和TiO2@AgNPs-PVP 2种基底浸入R6G水溶液(50 mL)中静置2 h,然后用N2气吹扫干燥.选择三聚氰胺作为SERS检测小分子,三聚氰胺水溶液的浓度为0.01~1.0 mg/mL.将2种基底浸入三聚氰胺水溶液(50 mL)中静置2 h,然后用N2气吹扫干燥.采用激光显微拉曼光谱仪(532 nm激光线,50倍物镜)测量SERS光谱,单个光谱以谱带中心1150 cm-1处的静态测量模型进行测量,采集时间为1 s,累积次数为1次.
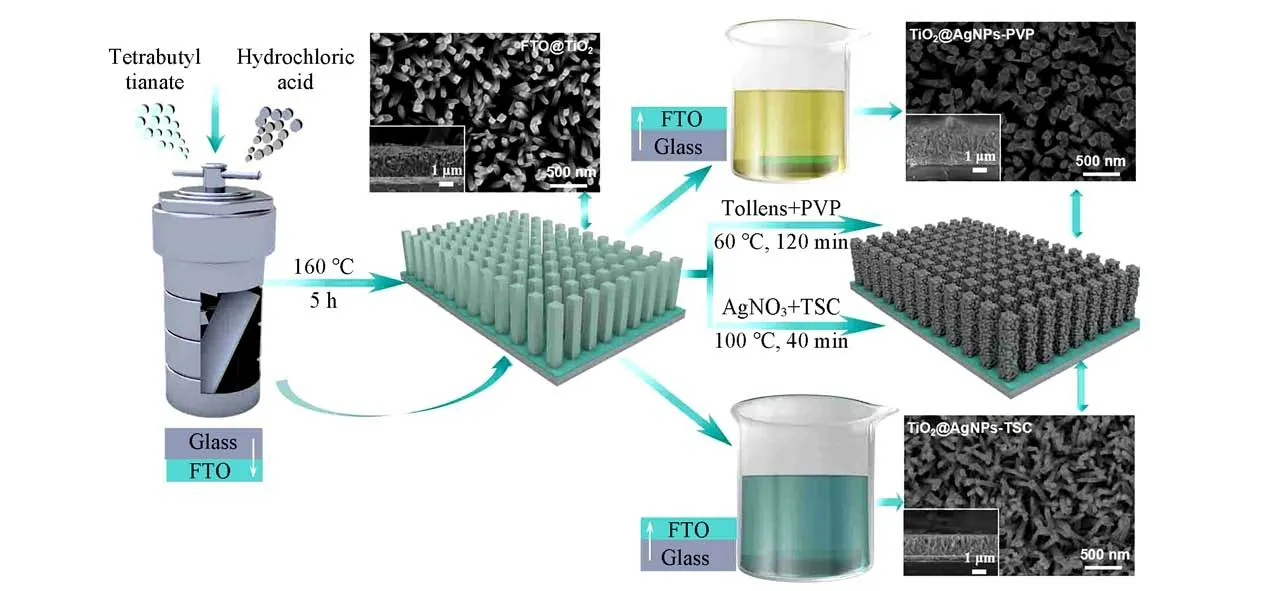
Fig.1 Process for fabrication of TiO2@AgNPs-PVP and TiO2@AgNPs-TSC micro-nano structures
2 结果与讨论
2.1 Ag纳米粒子在TiO2四棱柱列上的可控生长及其结构分析
采用传统的水热法,以FTO导电玻璃上的导电层为沉积位点,在高温、高压条件下将钛酸四丁酯分解为TiO2柱状阵列,制得的TiO2纳米棒呈四棱柱状[图2(A)],平均边长约为100 nm[图2(B)],高度约为1.5μm[图2(C)],棱柱呈相对分布均匀状态,相互之间有足够的空间以供Ag纳米粒子生长.采用PVP还原银氨溶液制备了TiO2@AgNPs-PVP微纳结构[图2(D)~(F)],大量粒径为10~20 nm的Ag纳米粒子紧密规整地生长在TiO2纳米棒上[图2(D)],而且附着Ag纳米粒子的TiO2棱柱仍呈现四棱柱状结构,其边长和高度[图2(E)和(F)]无明显变化.采用TSC还原硝酸银溶液制备了TiO2@AgNPs-TSC微纳结构[图2(G)~(I)],大量粒径为5~10 nm的Ag纳米粒子紧密规整地生长在TiO2纳米棒上[图2(G)],四棱柱状TiO2纳米棒形貌也未发生明显改变[图2(H)和(I)].采用PVP还原Tollens试剂或TSC还原AgNO3溶液都均将Ag纳米粒子原位生长在TiO2纳米棒上,Ag纳米粒子的大小取决于还原剂的种类.

Fig.2 SEM(A,D,G),TEM(B,E,H)and cross section SEM(C,F,I)images of TiO2 tetragonal prism nanoarray(A—C),TiO2@AgNPs-PVP(D—F)and TiO2@AgNPs-TSC(G—I)
2.1.1 PVP还原法制备TiO2@AgNPs-PVP微纳结构分析 已有研究表明,贵金属纳米粒子的间隙在2~10 nm之间可产生“热点”,而“热点”的分布直接影响基底的SERS活性[39,40].因此,为控制Ag纳米粒子在TiO2四棱柱上的分布、疏密程度及粒子的间距,通过调节Tollens溶液的浓度(0.4,0.8,1.2和1.6 mol/L)研究了Ag纳米粒子在TiO2四棱柱的生长情况.当Tollens溶液浓度为0.4 mol/L时,TiO2四棱柱上负载的Ag纳米粒子分布较为稀疏、粒子间距过大,粒径不均一[图3(A)];当Tollens溶液浓度升至0.8 mol/L时,TiO2四棱柱上负载的Ag纳米粒子分布相对均匀,粒子尺寸均一,并且密集地分布在TiO2四棱柱表面[图3(B)];进一步增大Tollens溶液的浓度(1.2和1.6 mol/L),Ag纳米粒子粒径增大,并且完全覆盖了TiO2四棱柱,使其失去了原有的形貌结构[图3(C)和(D)].由此可知,Ag纳米粒子的尺寸及其在TiO2四棱柱的分布与Tollens溶液的浓度紧密相关,这为Ag纳米粒子在TiO2四棱柱上的生长调控提供了思路.

Fig.3 SEMimages of prepared TiO2@AgNPs-PVP with different concentrations of Tollens(A)0.4 mol/L;(B)0.8 mol/L;(C)1.2 mol/L;(D)1.6 mol/L.
图4 为TiO2@AgNPs-PVP微纳结构的EDS谱图.4种不同浓度Tollens溶液制备的TiO2@AgNPs-PVP均含有N,O,Ti和Ag 4种元素,其中N元素来源于PVP,Ti元素来源于TiO2,Sn元素来源于导电玻璃,Ag元素在复合体系中的含量随Tollens溶液浓度的增加而增大.由图4(A)可知,当Ag纳米粒子的含量较少时,Ti元素和Sn元素的含量较高,这是因为Ag纳米粒子在TiO2四棱柱的分布比较稀疏;当Ag纳米粒子的含量增加和粒径增大时[图4(D)],Ag纳米粒子完全覆盖在TiO2四棱柱上,Sn元素的含量几乎为零,而Ti元素的含量也有所下降,这与SEM分析结果一致.
2.1.2 TSC还原法制备TiO2@AgNPs-TSC微纳结构分析 TSC还原AgNO3制备TiO2@AgNPs微纳结构是通过控制反应时间(20,40,60和80 min)来调控Ag纳米粒子在TiO2四棱柱的生长及分布,不同反应时间下的SEM照片如图5所示.通过控制反应时间,Ag纳米粒子均能很好地生长在TiO2四棱柱上:当反应时间为20 min时,Ag纳米粒子较小,尺寸为10~20 nm,个别大粒径Ag粒子(40~50 nm)生长在TiO2四棱柱的顶部[图5(A)];随着反应时间增加到40 min,Ag纳米粒子逐渐生长在TiO2四棱柱侧面且粒径增大[图5(B)];当反应时间为60 min时,Ag纳米粒子均匀地生长在TiO2纳米柱上[图5(C)]时;当反应时间为80 min时,Ag纳米粒子生长成大粒径粒子,密集地分布在TiO2四棱柱上,棱柱之间的缝隙也被Ag纳米粒子填满.由此可知,Ag纳米粒子的尺寸及其在TiO2四棱柱的分布与反应时间紧密相关,这为Ag纳米粒子在TiO2四棱柱上的生长调控提供了思路.图6为TiO2@AgNPs-TSC微纳结构的EDS谱图.不同反应时间下制备的4种TiO2@AgNPs-TSC均含有O,Ti,Ag和Sn 4种元素,Ti元素来源于TiO2,Sn元素来源于导电玻璃,Ag元素在复合体系中的含量随反应时间的增加而增大.当Ag纳米粒子完全覆盖在TiO2四棱柱上时,Sn元素的含量几乎为零,而Ti元素的含量也有所下降,这与SEM分析结果一致.
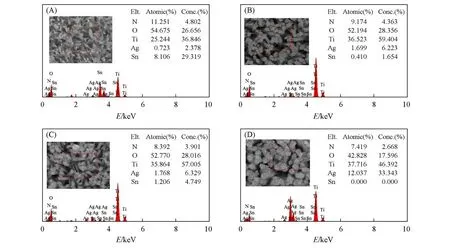
Fig.4 EDS of prepared TiO2@AgNPs-PVP with different concentrations of Tollens(A)0.4 mol/L;(B)0.8 mol/L;(C)1.2 mol/L;(D)1.6 mol/L.

Fig.5 SEMimages of prepared TiO2@AgNPs-TSC at different reactive time(A)20 min;(B)40 min;(C)60 min;(D)80 min.
2.1.3 Ag纳米粒子生长在TiO2四棱柱阵列上的晶体结构分析 FTO,FTO@TiO2,TiO2@AgNPs-PVP(Tollens-0.8 mol/L)和TiO2@AgNPs-TSC(Time-60 min)的XRD谱图如图7所示.TiO2四棱柱阵列与FTO相比多出2个特征衍射峰,其2θ值分别为36.1°和62.8°,归属于四方晶系金红石型TiO2(JCPDS No.78-2485)的(101)和(002)晶面衍射峰;TiO2@AgNPs-PVP和TiO2@AgNPs-TSC与FTO@TiO2相比多出3个特征衍射峰,其2θ值分别为44.3°,64.4°和77.5°,归属于面心立方晶系(FCC)单质Ag(JCPDS No.04-0783)的(200),(220)和(311)晶面衍射峰.TiO2衍射峰位置未发生变化,即TiO2的结晶相没有改变,表明Ag纳米粒子仅沉积在TiO2四棱柱的表面形成纳米复合结构[41].
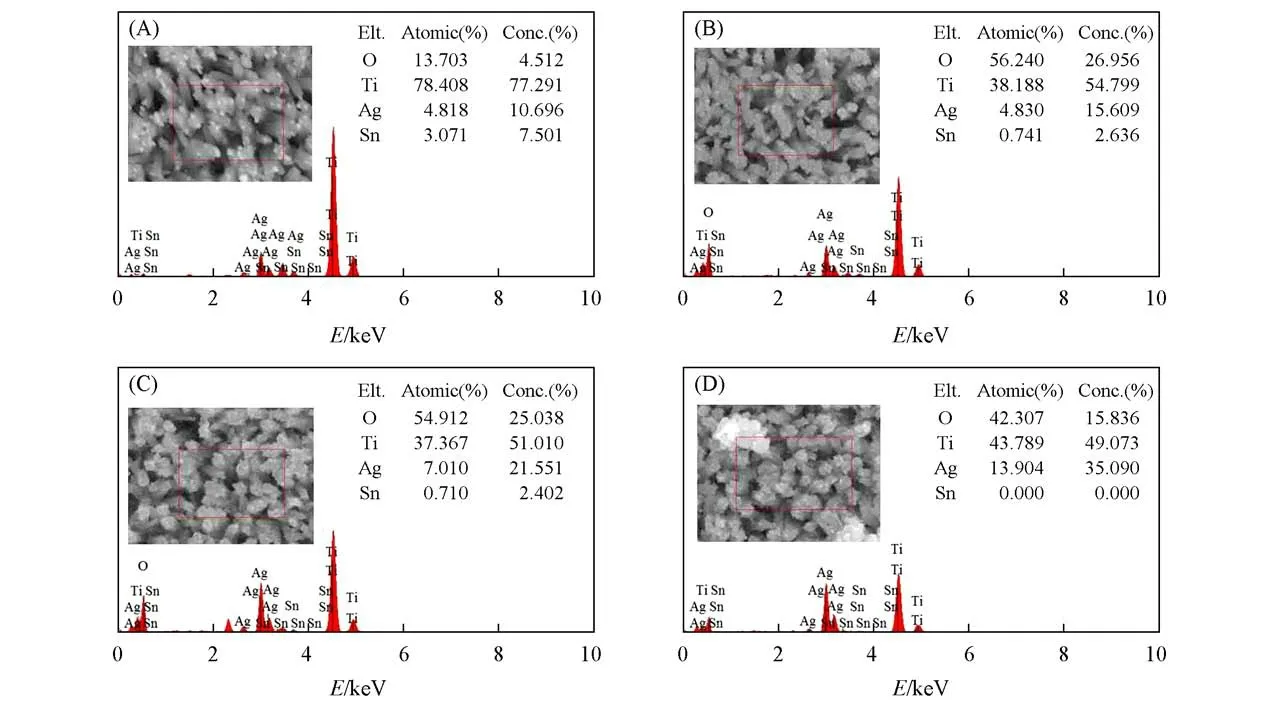
Fig.6 EDS of prepared TiO2@AgNPs-TSC at different reactive time(A)20 min;(B)40 min;(C)60 min;(D)80 min.
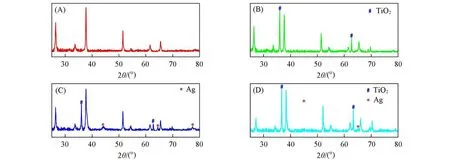
Fig.7 XRD patterns of FTO(A),TiO2 tetragonal prism nanoarray(B),TiO2@AgNPs-TSC(Time-60 min)(C)and TiO2@AgNPs-PVP(Tollens-0.8 mol/L)(D)
2.1.4 Ag纳米粒子生长在TiO2四棱柱阵列上的XPS分析 为了进一步探讨各阶段产物的表面化学组成变化,分别测定了FTO@TiO2,TiO2@AgNPs-PVP和TiO2@AgNPs-TSC纳米结构的XPS谱.如图8所示,TiO2@AgNPs-PVP和TiO2@AgNPs-TSC中都存在C,Ag,Ti,O和N 5种元素[图8(A)],其中在TiO2@AgNPs-PVP中检测到N元素,来源于还原剂PVP,通过拟合得到N1s的核心能级谱图[图8(A)插图],与EDS能谱表征结果一致.如图8(B)和(C)所示,TiO2@AgNPs-PVP的Ag3d3/2和Ag3d5/2的核心电子结合能分别为374.35和368.35 eV;TiO2@AgNPs-TSC的Ag3d3/2和Ag3d5/2的核心电子的结合能分别为374.40和368.40 eV,且每个峰都可以拟合为分别对应于Ag0和Ag+离子的2个独立峰[42],TiO2@AgNPs-PVP的Ag3d结合能374.7 eV(TiO2@AgNPs-TSC为374.6 eV)和368.7 eV(TiO2@AgNPs-TSC为368.6 eV)的峰值可以归属于Ag0[43],而374.2 eV(TiO2@AgNPs-TSC为374.4 eV)和368.2 eV(TiO2@AgNPs-TSC为368.4 eV)的峰值可以归属于Ag+离子[44].峰发生位移的主要原因在于制备TiO2@AgNPs-PVP过程中加入的PVP既是还原剂又是表面活性剂,反应完成后覆盖于Ag纳米粒子表面,PVP与Ag纳米粒子之间存在微弱的相互作用,当PVP配体包裹在Ag纳米表面时,羰基与Ag结合形成Ag—O键[45].
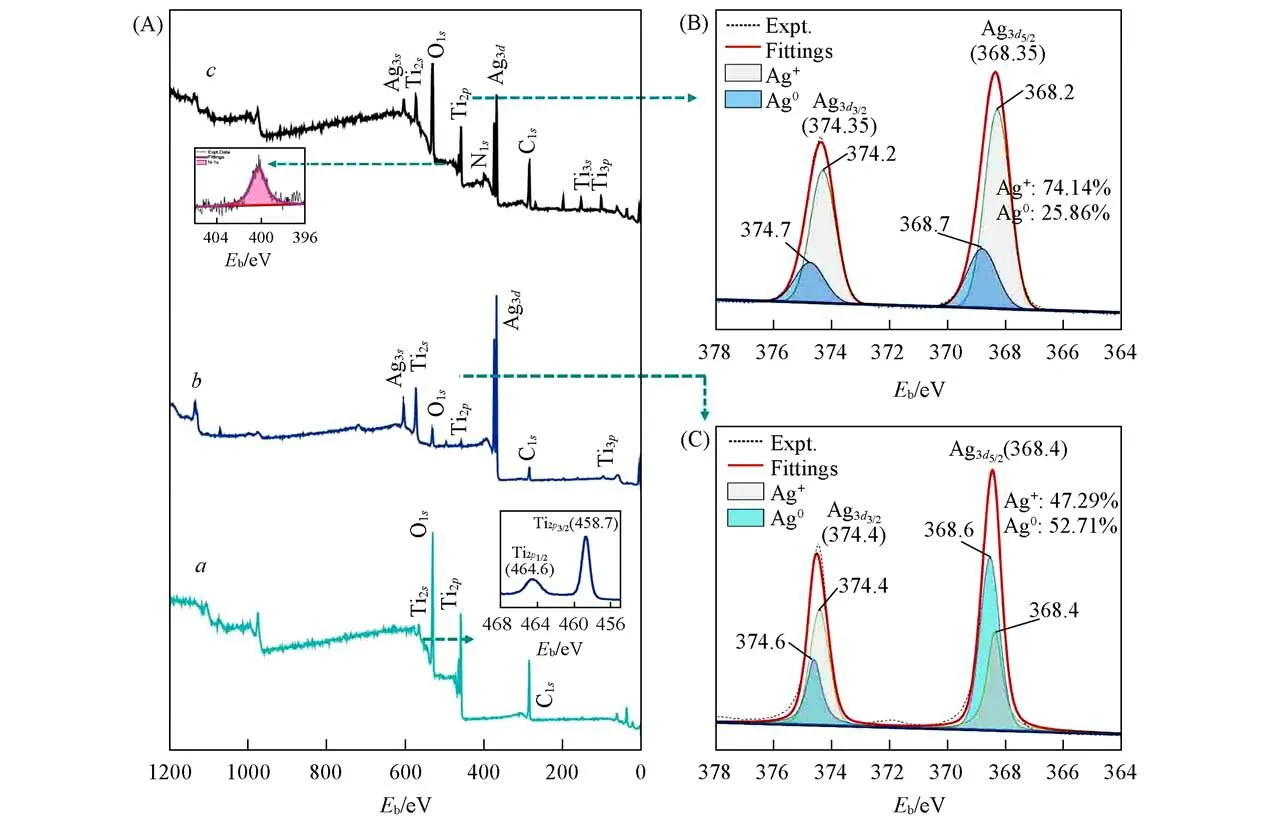
Fig.8 XPS of prepared TiO2 tetragonal prism nanoarray(a),TiO2@AgNPs-TSC(Time-60 min)(b)and TiO2@AgNPs-PVP(Tollens-0.8 mol/L)(c)(A),Ag3d core-level spectra of TiO2@AgNPs-PVP(B)and TiO2@AgNPs-TSC(C)
2.2 基底的SERS效应
使用由不同Tollens溶液浓度制备的TiO2@AgNPs-PVP微纳结构作为SERS基底,以染料分子R6G作为探针分子进行SERS检测,结果如图9所示.当R6G负载在4种SERS基底上时,均检测到R6G的特征光谱,其中612 cm-1处的峰归属于C—C—C环面内变形,773 cm-1处的峰归属于C—H面外变形;1365和1650 cm-1处的峰归属于氧杂蒽环的C—C伸缩振动[46].当Tollens溶液浓度为0.4和0.8 mol/L时,制备的TiO2@AgNPs-PVP微纳结构基底对R6G的检出限低至10-12mol/L[图9(A)和(B)].当Tollens溶液浓度增大至1.2和1.6 mol/L时,制备的TiO2@AgNPs-PVP微纳结构基底对R6G的检出限为10-8mol/L[图9(C)和(D)],这是因为大量的Ag纳米粒子堆积在一起,Ag纳米粒子之间的电磁场耦合作用减弱,导致基底的SERS活性下降.
使用不同反应时间制备的TiO2@AgNPs-TSC微纳结构作为SERS基底检测了R6G分子,结果如图10所示.当反应时间为20 min时,TiO2@AgNPs-TSC基底对R6G的检出限为10-7mol/L[图9(C)和(D)],这是因为反应时间较短,生长在TiO2四棱柱上的Ag纳米粒子较少[图5(A)],粒子间距较大,缺乏足够的活性“热点”,导致TiO2@AgNPs-TSC的SERS活性较低;随着反应时间的增加(40,60 min),生长在TiO2四棱柱上的Ag纳米粒子数量增多,粒子间距减小,TiO2@AgNPs-TSC微纳结构基底对R6G的检出限为10-9mol/L[图10(B)]和10-10mol/L[图10(C)];进一步增加反应时间(80 min),Ag纳米粒子数量的增多导致粒子之间发生团聚,降低了基底的SERS活性,此时TiO2@AgNPs-TSC微纳结构基底对R6G的检出限为10-7mol/L[图10(D)].
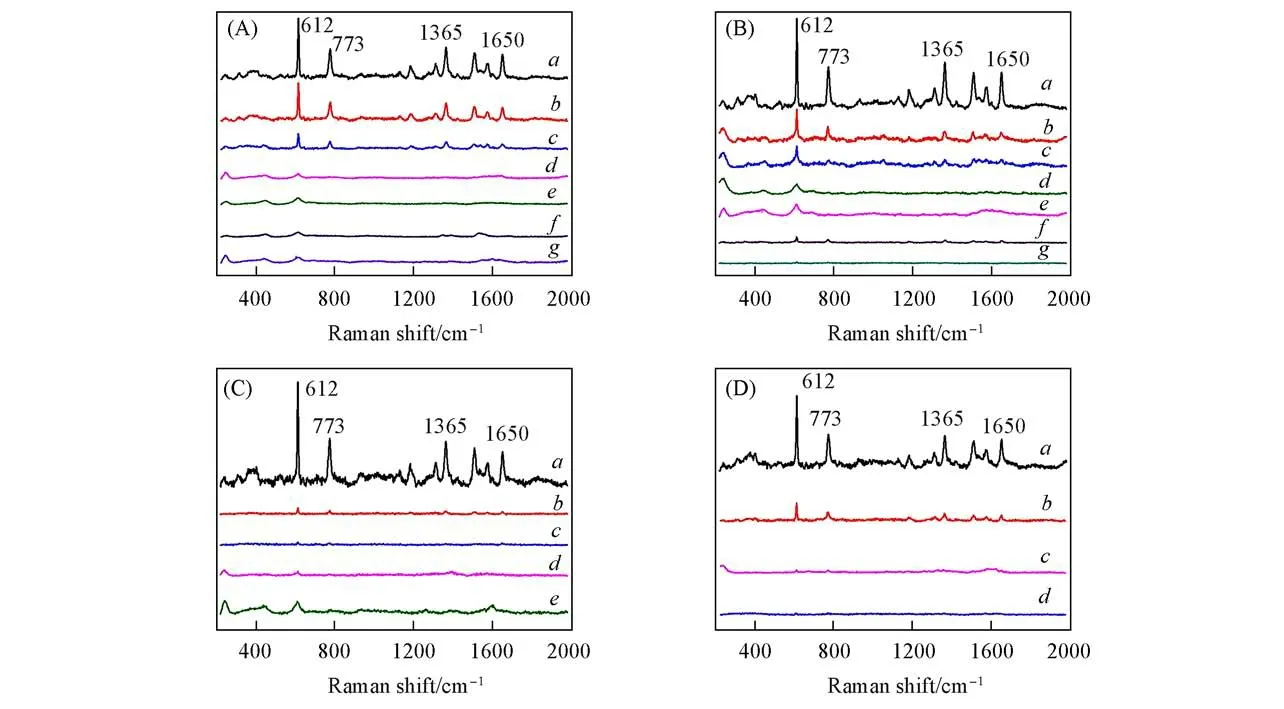
Fig.9 SERS spectra of R6G(concentration range in 10-5─10-12 mol/L)adsorbed on TiO2@AgNPs-PVP substrates prepared with different concentrations of Tollens(A)0.4 mol/L;(B)0.8 mol/L;(C)1.2 mol/L;(D)1.6 mol/L.c(R6G)/(mol·L-1):a.10-5;b.10-6;c.10-7;d.10-8;e.10-9;f.10-10;g.10-12.
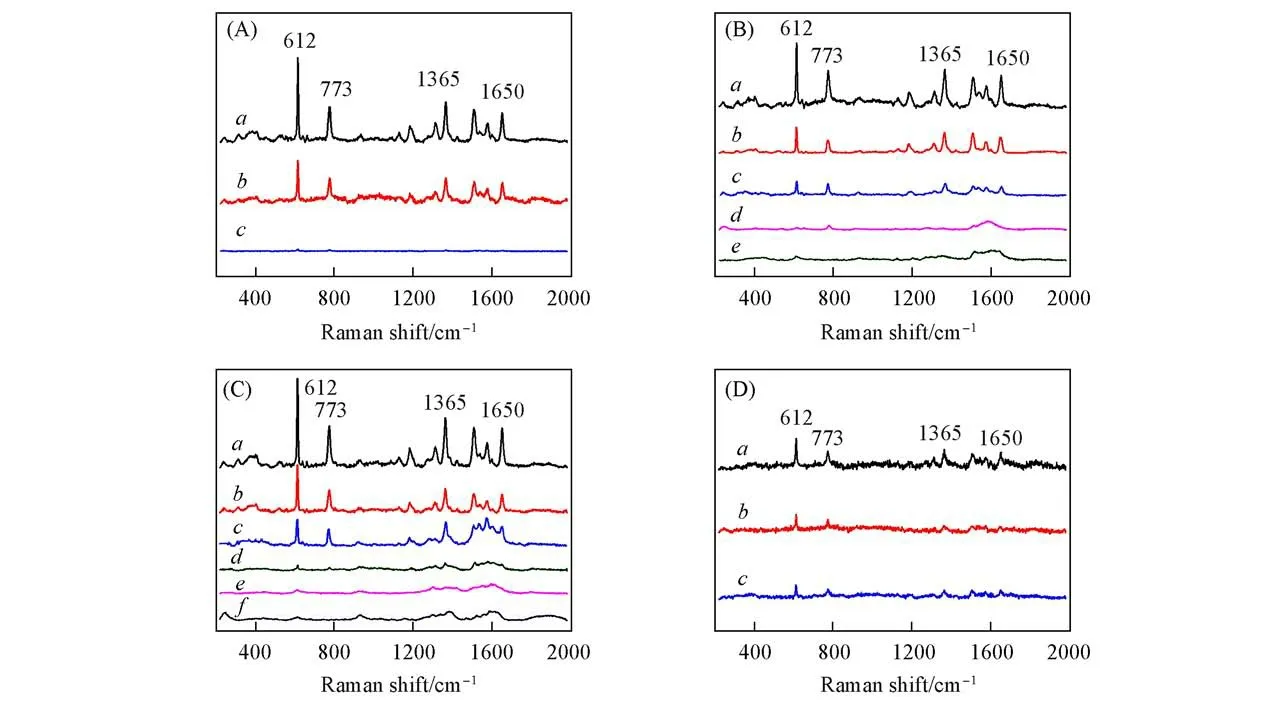
Fig.10 SERS spectra of R6G(concentration range in 10-5—10-12 mol/L)adsorbed on TiO2@AgNPs-TSC substrates prepared at different reaction time(A)20 min,(B)40 min,(C)60 min,(D)80 min.c(R6G)/(mol·L-1):a.10-5;b.10-6;c.10-7;d.10-8;e.10-9;f.10-10.
由上述结论可知,TiO2@AgNPs-PVP微纳结构的SERS活性高于TiO2@AgNPs-TSC微纳结构,主要原因在于:PVP是一种水溶性高分子聚合物,用PVP还原Tollens溶液后,PVP包覆在Ag纳米粒子上形成了隔离层(如EDS和XPS化学元素分析所示),当Ag纳米粒子靠近或发生聚集时,PVP隔离层可以避免Ag纳米粒子直接接触,从而有效防止电磁场耦合作用减弱,保证有足够的活性“热点”来捕捉探针分子[38];而TiO2@AgNPs-TSC没有PVP隔离层,Ag纳米粒子直接接触会导致SERS活性降低.根据增强因子公式:EF=(ISERS/Ibulk)×(Nbulk/NSERS)[47]和图11所示数据可计算出TiO2@AgNPs-PVP的增强因子为2.06×104,TiO2@AgNPs-TSC的增强因子为1.1×104,可见TiO2@AgNPs-PVP的SERS灵敏性优于TiO2@AgNPs-TSC,与上述讨论结果相一致.
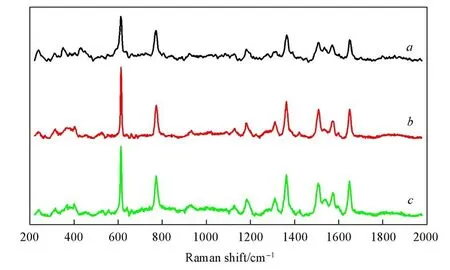
Fig.11 Raman spectra of 10-2 mol/L R6G aqueous solution(a),10-5 mol/L R6G adsorbed on TiO2@AgNPs-PVP(b)and TiO2@AgNPs-TSC(c)substrate
2.3 基底的可回收性
通过蒸馏水连续冲洗的方式探究了TiO2@AgNPs-PVP(Tollens-0.8 mol/L)和TiO2@AgNPs-TSC(Time-60 min)的可回收性.在负载相同量(10-5mol/L)的R6G分子后,基底进行不同时间的冲洗(小水量冲洗,防止基底被冲洗掉)考察了基底对R6G分子的吸附能力,从而确定基底的可回收性.如图12所示,对于TiO2@AgNPs-TSC微纳结构基底,经过24 h的冲洗后,几乎检测不到R6G分子的SERS光谱[图12(A)];对于TiO2@AgNPs-PVP微纳结构基底,经过24 h的冲洗后,仍然可以检测到明显的R6G分子的SERS光谱[图12(B)].水冲洗可以有效去除TiO2@AgNPs-TSC及TiO2@AgNPs-PVP表面的R6G分子[图12(C)],但对于PVP还原法制备的TiO2@AgNPs-PVP纳米结构而言,由于Ag纳米粒子表面负载着一层PVP隔离层,基底捕捉R6G分子时一部分R6G分子浸入PVP层中,很难被清除,因此经过长时间的冲洗该基底仍然保持着较强的SERS信号.另外,对2种基底进行了接触角测试,测得TiO2@Ag-NPs-TSC接触角为86.23°[图12(D)],明显大于TiO2@AgNPs-PVP接触角(47.71°)[图12(E)].因此当基底浸入R6G溶液中后,对于TiO2@AgNPs-TSC微纳结构基底,一方面捕获R6G分子的Ag纳米粒子较少,导致其检测灵敏度减弱,另一方面溶有R6G分子的水分子无法完全浸入TiO2四棱柱的内部,因此更容易被清洗干净;而对于TiO2@AgNPs-PVP微纳结构基底,其亲水性强,致使溶有R6G分子的水分子可以浸入到TiO2四棱柱的内部,清洗难度较大,导致部分R6G分子残留在基底上.基于我们前期的研究工作,可利用硼氢化钠((NaBH4)清洗PVP包覆层[38]或利用高温水热反应将PVP包覆层碳化[24]来提高基底的循环可回收性,但基底的SERS灵敏度会下降.
为了进一步研究TiO2@AgNPs-PVP(Tollens-0.8 mol/L)和TiO2@AgNPs-TSC(Time-60 min)2种基底在小分子检测方面的应用,以浓度为0.01~1 mg/mL的三聚氰胺作为目标小分子,进行了SERS检测研究.如图13所示,2种基底对三聚氰胺分子均表现出相似的检测活性,当基底负载低含量的三聚氰胺分子时(0.01 mg/mL),均能检测到三聚氰胺在677 cm-1处的特征拉曼散射峰(归属于三嗪环呼吸模式),且其强度随着三聚氰胺负载浓度的减小而减弱.这是因为三聚氰胺中三嗪环中的N原子与Ag之间存在相互作用,电荷发生转移,致使电荷重新分配,引起极化率的变化,导致低浓度小分子负载在Ag基底上时,其拉曼信号也会增强[48].由此可见,所制备的基底可用于一些小分子的实际应用痕量检测.
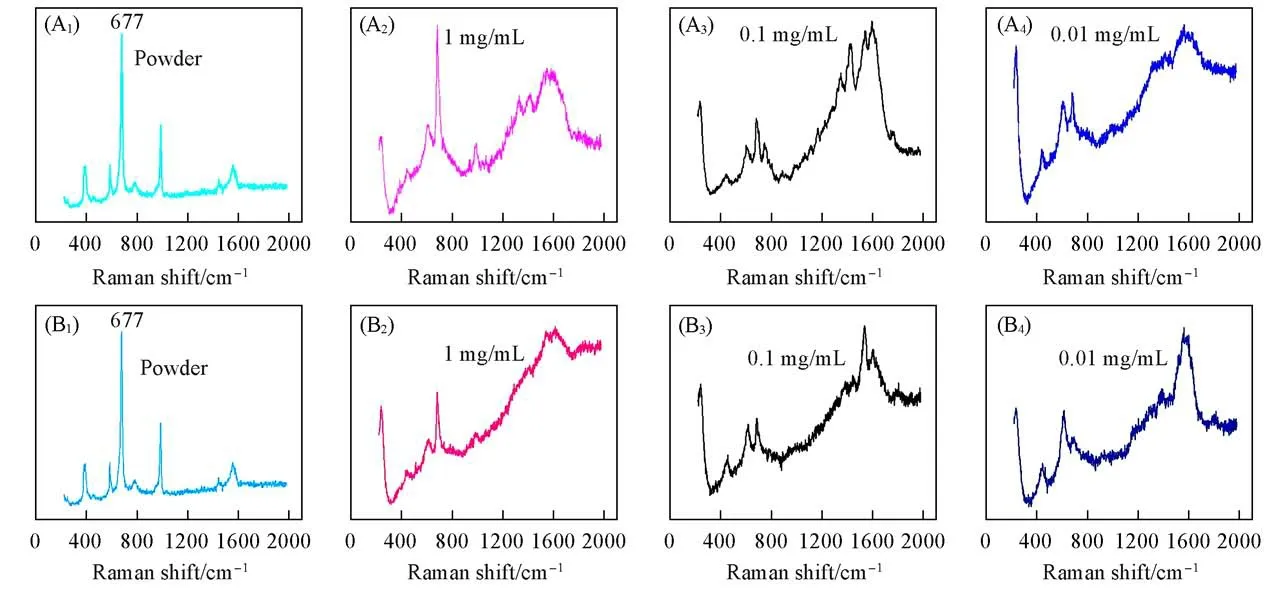
Fig.13 Raman(A1,B1)and SERS spectra(A2—A4,B2—A4)of melamine(0.01—1 mg/mL)adsorbed on TiO2@AgNPs-PVP substrate(Tollens-0.8 mol/L)(A1—A4)and TiO2@AgNPs-TSC substrate(Time-60 min)(B1—B4)
3 结 论
以钛酸四丁酯为前驱体,采用水热法在高温条件下在导电玻璃FTO导电面上沉积TiO2四棱柱阵列结构.以TiO2四棱柱阵列为基体,采用PVP还原Tollens试剂或TSC还原硝酸银溶液,将Ag纳米粒子沉积在TiO2四棱柱阵列上制备TiO2@AgNPs-PVP和TiO2@AgNPs-TSC微纳结构作为SERS基底.实验结果表明,Ag纳米粒子在TiO2四棱柱阵列的尺寸和分布与Tollens试剂的浓度和TSC还原硝酸银的反应时间密切相关,说明Ag纳米粒子在基体上的生长可通过改变溶液的浓度和反应时间来调控,进而得到SERS效应最优的基底.对于TiO2@AgNPs-PVP,通过调控Tollens试剂浓度得到的最优SERS基底对R6G的检出限为10-12mol/L,对低活性小分子三聚氰胺的检出限为0.01 mg/mL;对于TiO2@AgNPs-TSC,通过调控TSC还原硝酸银的时间得到的最优SERS基底对R6G的检出限为10-10mol/L,对三聚氰胺的检出限为0.01 mg/mL.TiO2@AgNPs-PVP的SERS活性优于TiO2@AgNPs-TSC的原因在于:PVP隔离层可以避免Ag纳米粒子直接接触,从而有效防止电磁场耦合作用减弱,保证有足够的活性“热点”来捕捉探针分子.TiO2@AgNPs-TSC的循环可回收性优于TiO2@AgNPs-PVP的原因在于:TiO2@AgNPs-TSC的亲水性差,R6G分子无法完全浸入TiO2四棱柱的内部,容易被清洗,而TiO2@AgNPs-PVP的亲水性较强,清洗难度较大.

