上海市临床实验室13个常规化学检测结果互认项目检测质量分析
蒋玲丽,朱 俊,娄 娇,杨 雪,王 青(上海市临床检验中心质量管理部信息科,上海200126)
为进一步贯彻落实上海市医药卫生体制改革工作要求,减轻群众就医负担,上海市卫生健康委员会推出《关于全面推进本市医疗机构间医学影像检查资料和医学检验结果互联互通互认工作的实施意见》(沪卫医﹝2019﹞27)[1](简称意见)。2019年10月上海市卫生健康委员会提出首先试点在37 家市级公立医疗机构间实现部分项目互联互通互认,其中常规化学检测项目13 个。同时意见指出所有医疗机构均应纳入质控范围,通过实施室间质量评价(IQC)和室内质量控制(EQA)使检验结果达到互认的合格标准。上海市临床检验中心(Shanghai Center for Clinical Laboratory,SCCL)负责实施上海市临床实验室IQC 和EQA。为了了解实验室互认项目的检测质量,本文统计实验室上传的2019年IQC 和EQA 数据,分析互认和非互认实验室的差异,为进一步推进上海地区医疗机构检验结果互认工作提供科学依据。
1 材料和方法
1.1 研究对象 所有参加SCCL 组织的IQC 和EQA 的上海地区医疗机构实验室。以2019年10月上海市卫生健康委员会提出的试点互联互通互认的37 家市级公立医疗机构实验室为互认组,其余实验室为非互认组。
1.2 方法
1.2.1 IQC 数据收集与计算 :SCCL 组织IQC 计划,实验室可自愿参加并自由选择相应浓度的质控品。每年年底SCCL 发放统一代购的室内质控品,包含低中高3 个浓度水平,分别用L1,L2 和L3 表示,实验室将IQC 数据上传至上海市临床检验中心质控及预警信息系统。以各实验室该项目全年的室内质控数据,剔除4 倍标准偏差(standard deviation,SD)后,分别计算13 个常规化学项目年度累计CV,用百分比表示。以WS/T 403-2012 临床生物化学检验常规项目分析质量指标[2]中CV标准,所有浓度水平均小于该CV标准判定实验室该项目CV合格,分别计算13 个项目2019年CV合格率。
1.2.2 EQA 数据收集与计算 :SCCL 每年组织两次EQA,一次5 个批号样本。EQA 评价采用的允许总误差(allowable total error,Tea),按WS/T 403-2012 临床生物化学检验常规项目分析质量指标推荐的Tea,每次EQA 有2 或2 个以上样本结果错误判定实验室该项目不合格;分别计算13 个项目2019两次EQA 的合格率。
1.3 统计学分析 采用MedCalc 19.1 软件进行分析,数据通过Shapiro-Wilk test 检验,呈偏态分布的数据采用中位数(四分位数)[M(P25~P75)]表示,组间比较采用Mann-Whitney 检验;两个率之间的比较采用χ2检验,以P<0.05 为差异有统计学意义。对互认组和非互认组数据进行分析。
2 结果
2.1 IQC 分析结果 见表1 和表2。13 个项目中,互认组和非互认组TG,Fe,UA,URE,CRE 和Mg项目IQC年度CV在L1 浓度水平差异有统计学意义(U=2.014,2.136,2.747,2.987,3.094 和3.253,P=0.044 0,0.032 7,0.006 0,0.002 8,0.002 0 和0.001 1,均P﹤0.05)。

表2 13 个常规化学项目年度CV 结果分析
按WS/T 403-2012 标准规定的不精密度要求,互认组13 个项目合格率在44.44%~100%之间,其中TP,ALB,GGT 和URE 4 个项目合格率低于80%;非互认组13 个项目合格率在43.58%~89.86% 之间,其中TP,ALB,ALT,GGT,CRE,URE,TBIL,TC,TG 和Mg 合 格率低于80%。GGT, TG,Mg,UA,AST,URE,TC 和CRE 项目CV合格率在互认组和非互认组实验室比较差异有统计学意义(χ2=5.197~13.636,均P<0.05)。
2.2 EQA 分析结果 见表3。13 个互认项目中,互认组合格率在97.22%~100%之间,仅URE 项目在第一次EQA 中有1 家实验室出现了不合格,其余项目两次合格率均为100%;非互认组合格率在96.62%~100%之间,除Fe 项目EQA 两次合格率均为100%外,其余项目两次合格率均未都达到100%。互认组和非互认组合格率比较差异无统计学意义(均P>0.05)。
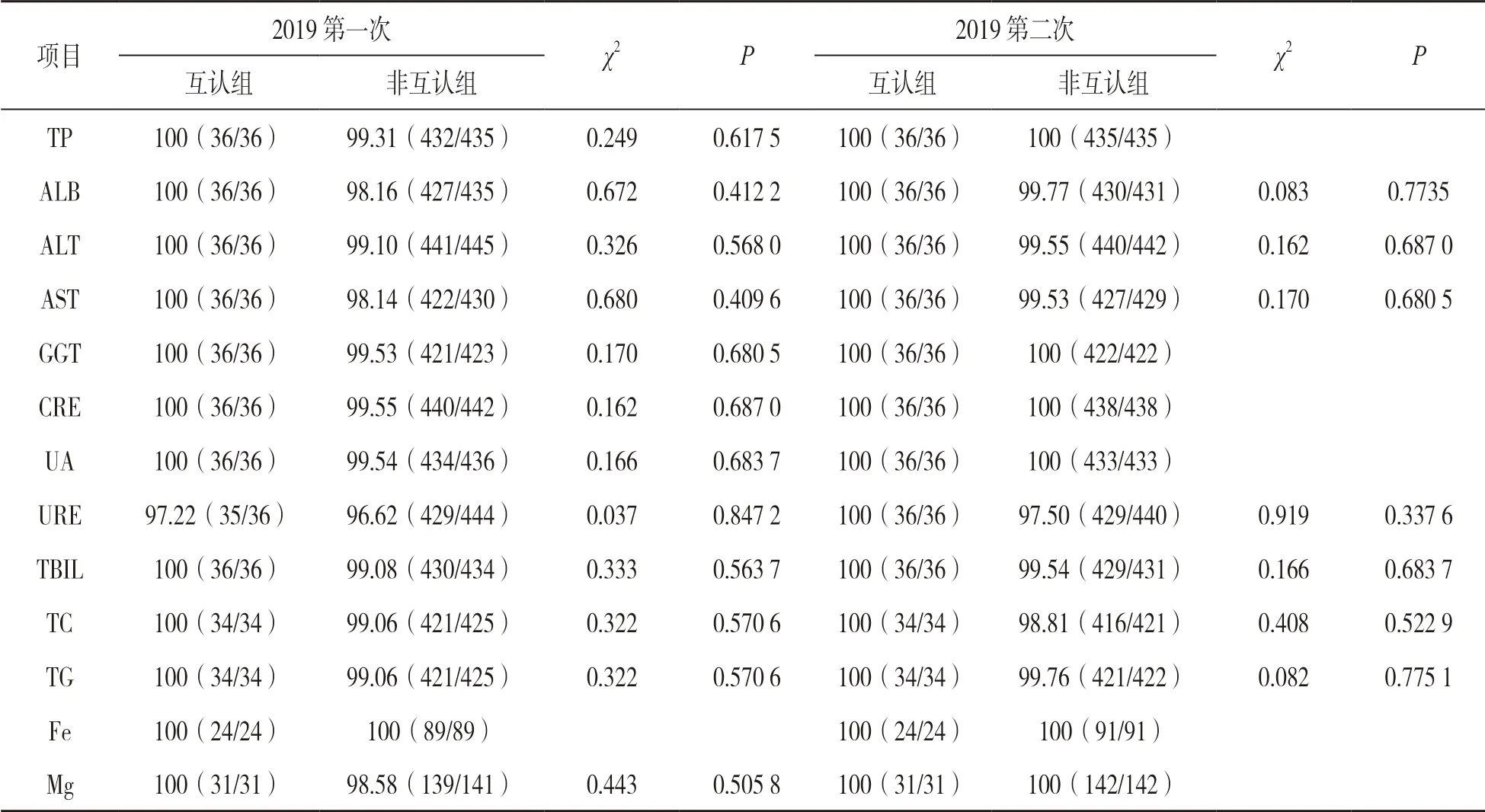
表3 13 个项目室间质评合格率[%(n)]
3 讨论
医学检验结果互认作为病人避免重复检查、促进医疗服务共享机制、增强医疗机构之间协同性的重要举措,得到了各部门的强力推行,并在历次深化医药卫生体制改革方案中被一再强调。但是检验结果互认在具体实施过程中仍然困难重重,排除临床疾病变化的影响,究其原因还是取决于各项目的检验结果在不同的检测机构中是否一致,或者说不同医疗机构的检验结果是否具有相同的临床意义。已有不少研究者通过飞行检查[3]、新鲜血比对[4]、新鲜血校准[5]等方式分析不同实验室之间检测结果的一致性。
但是以上方式费时费力常用于在纳入互认项目前了解检测项目现状,不能作为常态化的监控手段。《医疗机构临床实验室管理办法》[6]规定开展临床检验项目必须实施IQC 和EQA,故可作为互认项目长期监测的手段,李婷婷等[7]在对京津冀地区检验结果互认的建议中提出动态监测也包括IQC 和EQA 数据。SCCL 组织上海地区IQC 以及EQA 工作,可收集和了解实验室IQC 和EQA 数据。分析上海地区医疗机构实验室IQC 数据提示各项目互认组和非互认组年度CV没有明显差异,仅在CRE,UA,URE,TG,Fe 和Mg 项目低浓度水平差异有统计学意义,但这也提示参与互认的实验室在选择室内质控品浓度的时候,是否一定要选择低浓度水平的质控品;进一步与行业标准规定的CV比较,互认组合格率明显高于非互认组(表2),其中GGT, TG,Mg,UA,AST,URE,TC 和CRE 8 个项目合格率在互认组和非互认组比较差异有统计学意义。但是尽管如此,互认组还是有TP,ALB,GGT 和URE 4 个项目满足要求的实验室数低于80%,说明尽管37 家医疗机构试点互认,但是在实施过程中还有部分实验室的CV不能满足行业标准的要求;而非互认组AST,UA 和Fe 3 个项目满足要求的实验室数大于80%,说明部分项目可以扩大互认范围。分析上海地区医疗机构实验室EQA数据(表3)提示上海地区实验室13 个项目EQA合格率在95%以上,互认组合格率优于非互认组。从数据分析看出互认组IQC 的CV和EQA 的合格率均优于非互认组,说明在结果互认实施初期,从检验质量较好的市级公立医疗机构试点结果互认应该是个很好的举措;但是数据分析也提示两组中均有满足要求和非满足要求的实验室,因此实施动态监控,在互认工作实施后出现临床检验质量不符合互认要求情形的医疗机构,可根据情况督促其进行整改或取消检验结果互认医疗机构资格,同时逐步将满足要求的其他医疗机构实验室纳入结果互认。目前在实施动态监管过程中,SCCL 面临着有些实验室不上传或者不实时上传其IQC 数据的问题,可能需要卫健委出台相关政策强制实验室将数据上传至SCCL。
需要指出的是由于仪器、试剂、校准品等种类繁多,各实验室的检测系统不完全一致[8],导致不同检测系统结果存在差异,SCCL 组织的常规化学EQA 也是按检测系统分组评价的;另外参考区间上下限不一致给不同医疗机构间检测结果互认带来很大障碍[9-10]。虽然通过监测IQC 和EQA 可以动态监控结果互认,但是系统本身的差异目前还不能解决,故建议在实施检验结果互认时应标注各实验室的检测系统,并允许相同检测系统的检测结果可以互认。
综上所述,上海地市医疗机构实验室检测质量还不尽相同,要实现更大范围内的检验结果互通互认还有很长的路要走,动态监测体现检测质量的IQC 和EQA 数据支持结果互认能够使互认之路行进地更为顺畅。

