一例无毒力白喉棒状杆菌携带者的临床特征和病原学诊断分析
沈丹丹,刘 妍,胡 娟,袁应华(同济大学附属第十人民医院检验科,上海 200072)
白喉是由白喉棒状杆菌引起的传染性较强的急性呼吸系统传染病,以局部灰白色假膜和全身毒血症为临床特征,严重感染者可能会扩散至心脏和神经系统[1],病死率较高。人类是白喉棒状杆菌的唯一宿主,携带毒力菌株的患者是唯一的传染源,主要通过密切的身体接触和呼吸飞沫传播发生人际传播[2]。
随着扩大免疫接种实施和社会经济的改善,白喉发病率已稳步下降。尽管如此,在某些疫苗覆盖率低、卫生条件差和人群密集地区白喉仍然在流行暴发,根据世界卫生组织(WHO)的一份报告,全球接种疫苗后白喉病例的80%以上来自印度和印度尼西亚[3]。中国自1978年实施计划免疫后,白喉的发病率得到了极大控制,2007年后全国就没有白喉病例报告[4],截止2019年上海市连续41年无白喉病例报告[5]。近年来国内文献报道了[6-8]部分地区发现非产毒力白喉棒状杆菌携带者病例,提示我们在计划免疫当下仍要重视白喉的存在。本文针对我院2020年6月2日收治入院的1 例白喉棒状杆菌携带者的病例特点及病原学诊断做一简要的分析。
1 材料与方法
1.1 研究对象
1.1.1 病例来源:病例来源于上海市第十人民医院神经外科住院患者,该患者于2020年6月4日采集痰液标本分离培养,结果经鉴定为白喉棒状杆菌。
1.1.2 流行病调查:按照要求上报院感染与控制办公室,对患者进行现场个案调查和样本采集,同时收集病例资料和流行病学史,对密切接触者进行调查。由于患者入院时即为昏迷状态,询问其家属完成相关的流行病接触史、接种防疫史。
1.2 仪器与试剂 VITEK MS 质谱仪(法国生物梅里埃公司),WalkAway 96 Plus 微生物分析系统(德国SIEMENS 公司),mNGS 及16S rDNA 测序(北京博奥医学检验所),Veriti 96 Well PCR 热循环仪(Applied Biosystems),毒力基因toxA 和toxB 引物(上海生物工程公司),头孢曲松药敏条(郑州安图),白喉棒状杆菌标准菌株DNA(上海疾病预防控制中心)。
1.3 方法
1.3.1 普通培养鉴定及药敏试验:6月4日和8日分别采集痰液标本进行培养及鉴定。痰液标本接种血平板、麦康凯及巧克力平板,35℃,5ml/dl CO2培养箱中培养18~24h,挑取可疑菌落涂片镜检观察形态。挑取单个菌落涂于靶板,参照VITEK MS 梅里埃质谱仪操作规程进行蛋白峰分析。药敏试验采用WalkAway 96 Plus 微生物分析系统,结果按照美国临床实验室标准化委员会标准判读[9]。
1.3.2 基因测序:采集痰液标本送检北京博奥医学检验所进行宏基因测序(metagenomic sequencing,mNGS),对该标本中所有微生物DNA 或RNA 进行全基因组分析,送检分离培养的白喉棒状杆菌纯菌株行16S rDNA 测序,获得该菌株的属信息。
1.3.3 毒力基因检测:采用普通PCR 对该病例菌株样本进行toxA 和toxB 毒力基因检测,toxA和toxB 毒力基因引物参照文献[10]。扩增条件为94℃ 5min,94℃ 30s,50℃ 30s,72℃ 30s,循环30 次,72℃延长5min。同时采用超纯水做阴性对照,白喉棒状杆菌标准菌株DNA 为阳性对照。
2 结果
2.1 病例诊治及调查结果 患者于2020年6月2日凌晨4 时在家中起床后突发呕吐后昏迷倒地,入院后诊断为动脉瘤破裂伴蛛网膜下腔出血,急诊行脑血管造影备颅内动脉瘤栓塞术,术后见脑室铸型,立即给予脑室外引流术。患者入院后整个病程一直处于昏迷状态,术后予以气管插管并呼吸机辅助通气中,6月4日通过吸痰方式获取少量脓性稀痰送检,检出白喉棒状杆菌(1+)和流感嗜血杆菌,患者入院后无发热,其余咳痰、胸闷、咽痛等症状未知,追问家属患者昏迷前无发热、乏力、咽痛、胸闷、头痛等症状。查体患者咽部未见白色假膜,鼻咽部未见明显异常。患者6月8日再次送检痰液,检出肺炎克雷伯菌(4+),本次培养未见白喉棒状杆菌和流感嗜血杆菌。患者入院后立即给予积极治疗,包括手术、呼吸机辅助通气、镇静镇痛、抗血管痉挛、抗炎补液等支持对症治疗等,但患者蛛网膜下腔出血严重,于6月9日09:40 宣布临床死亡。
追问其家属流行病学史,患者近期无白喉病人接触史,无旅行史,白喉疫苗接种史不详,家属中未有类似白喉棒状杆菌感染情况发生。
2.2 细菌培养鉴定及药敏结果 患者6月4日送检痰液标本培养24 h 在血平板上呈灰白色、圆形突起,单一菌落(图1),麦康凯及巧克力平板未见相应的菌落生长,巧克力平板可见流感嗜血杆菌。将该血平板上菌落涂片革兰染色,镜下可见革兰阳性杆菌(图2)。挑选单个菌落经VITEK MS 梅里埃质谱仪蛋白分析提示99.9%为白喉棒状杆菌。白喉棒状杆菌药敏结果显示所有测试结果均敏感,见表1。患者6月8日再次送检痰标本培养检出肺炎克雷伯杆菌(4+),未出现白喉棒状杆菌和流感嗜血杆菌菌落。
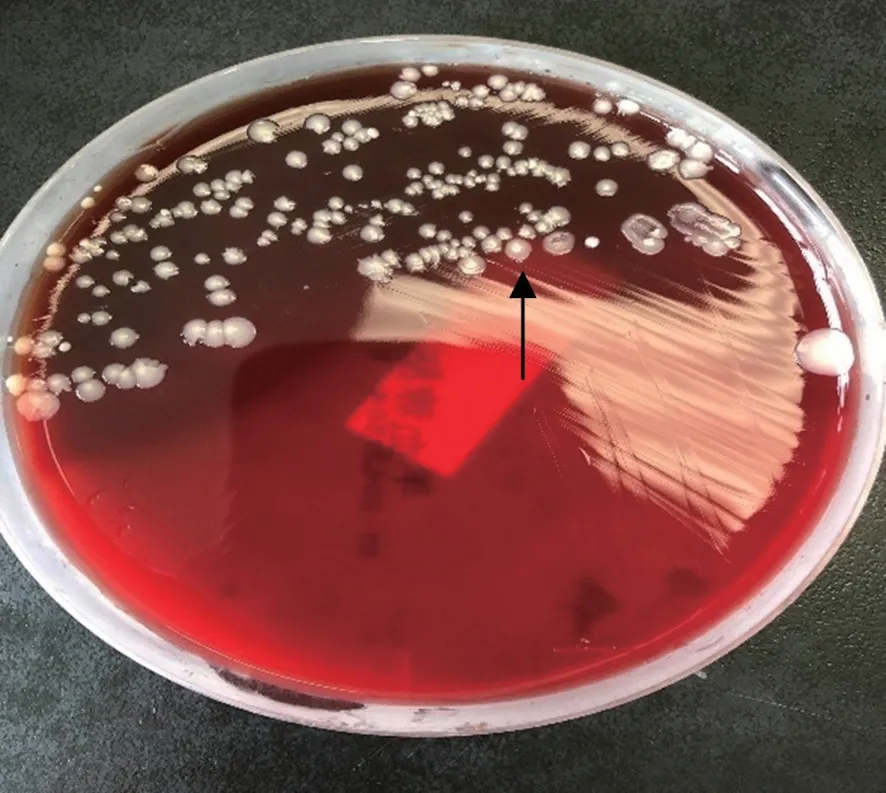
图1 血平板菌落形态
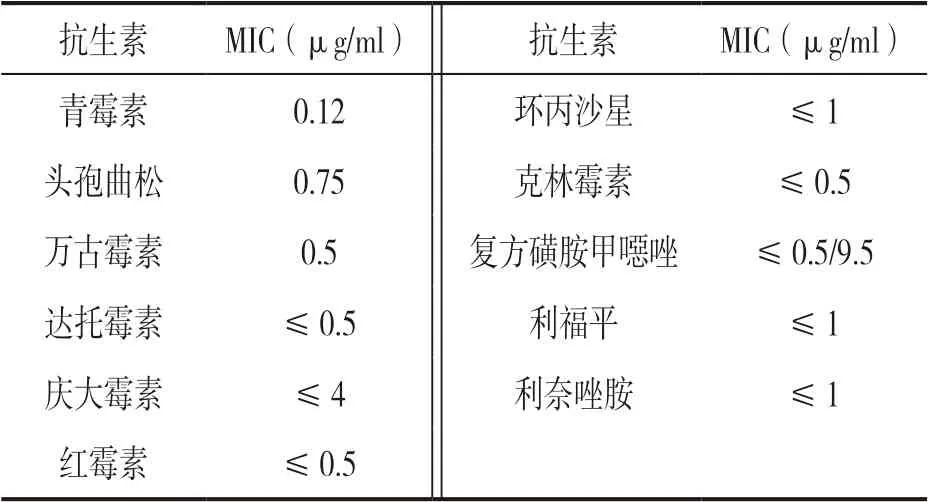
表1 白喉棒状杆菌药敏试验结果
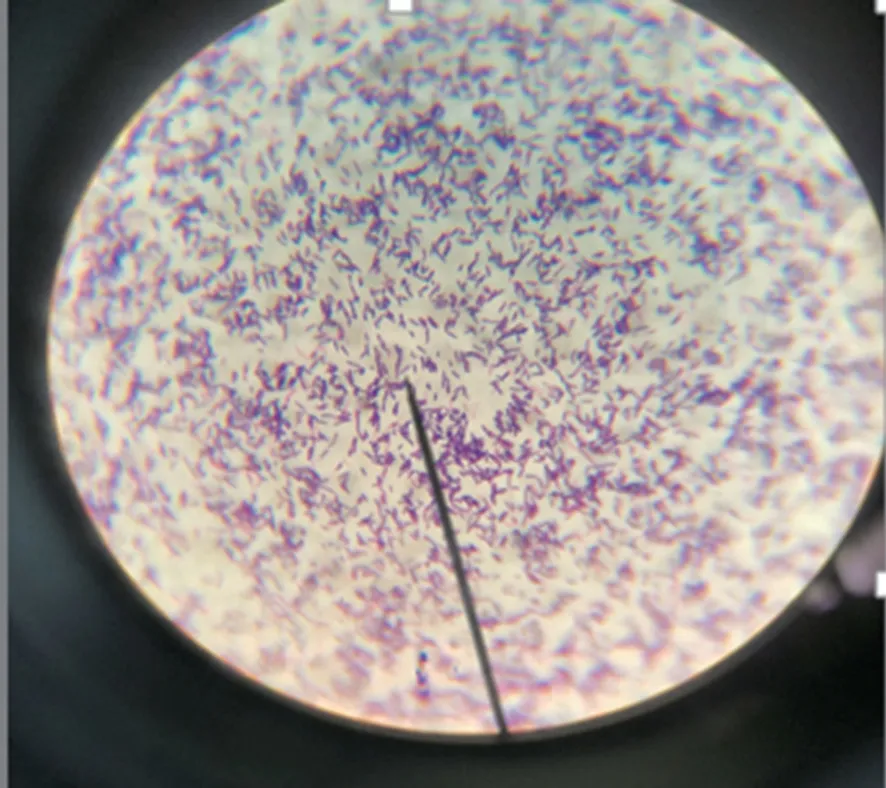
图2 革兰氏染色细菌形态
2.3 宏基因组测序结果 见图3。患者痰液送检mNGS 结果显示:高置信度指标包括人单纯疱疹病毒1 型、肺炎克雷伯菌、丙酸棒状杆菌、白喉棒状杆菌、溶血隐秘杆菌、46 种口腔/呼吸道定植菌。因为送检标本为痰液,本身存在大量口腔正常菌群,除了口腔正常菌群外,检测结果中显示肺炎克雷伯菌和白喉棒状杆菌存在较高的浓度、序列数及基因组覆盖度。同时检出耐药基因ErmX,提示大环内酯类、林可胺类及链阳霉素类耐药。

图3 宏基因组测序(mNGS)阳性病原体分布情况
2.4 16S rDNA 测序结果 该菌株经过DNA 提取、16S rDNA 区段扩增、二代测序及生物信息分析提示:该菌株99.8%物种分布为白喉棒状杆菌。
2.5 毒力基因结果 见图4。采用普通PCR 检测toxA 和toxB 毒力基因结果显示:该菌株toxA 和toxB 毒力基因均为阴性,阳性对照菌株toxA 和toxB 毒力基因均为阳性,结果提示该例菌株不含白喉棒状杆菌毒力基因。
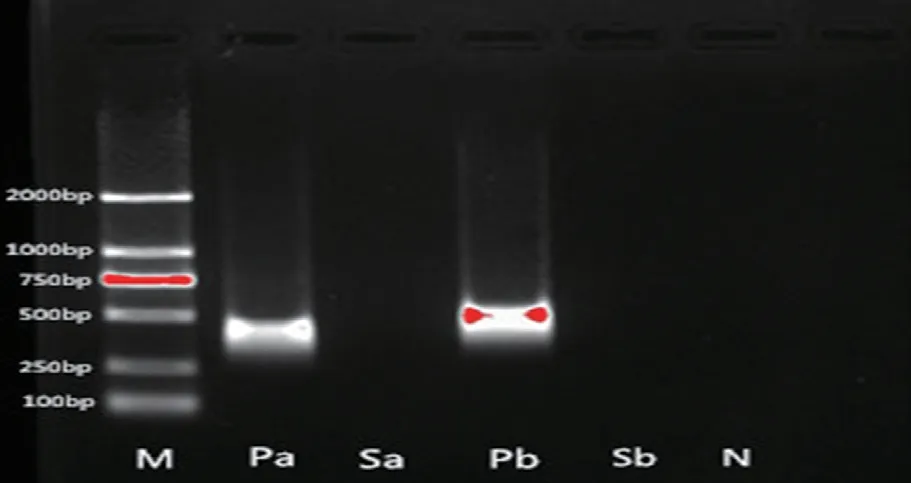
图4 普通PCR 检测毒力基因toxA 和toxB 结果
3 讨论
本例患者入院先后送检两份痰液标本,分别检出白喉棒状杆菌(1+)和肺炎克雷伯菌(4+),只在初次分离到白喉棒状杆菌,出现此种结果的原因可能为:患者入院后即开始使用头孢他啶联合左氧氟沙星抗感染,而白喉棒状杆菌药敏结果显示对绝大多数抗生素有着高度敏感性;由于患者病情较重入院即做了栓塞术、引流术及气管插管等有创性操作,增加了医院内感染风险;检出的肺炎克雷伯菌为耐碳青霉烯类菌株,属于广泛耐药菌株,除外替加环素和黏菌素均耐药。初次痰液标本中检出的白喉棒状杆菌,经质谱、mNGS 和16S rDNA 测序等鉴定均符合白喉棒状杆菌特性,毒力基因检测提示不产toxA 和toxB 毒力基因,但患者无上呼吸道感染症状,且查体未见白喉特征性白色假膜,根据白喉诊断标准[11],该患者为“无毒力白喉棒状杆菌携带者”。本例为上海近年来检出的首例无毒力白喉棒状杆菌携带者,文献报道[6-8]广州、浙江和福建2019年先后分别出现了无毒力白喉棒状杆菌携带者。随着白喉疫苗的计划免疫实施,全国范围内的白喉发病率已经得到了极大的控制,虽然本例为无毒力白喉棒状杆菌携带者,但仍应引起重视,结合此前报道的三例,有预防接种不详者,也有明确预防接种史者,出现这种人群中偶发现象到底是免疫接种不完全还是人群免疫力普遍降低造成的,目前尚不能明确。
从发展中国家到发达国家,由于全球化使人们能够从一个地方流动到另一个地方,白喉仍然是一个公共卫生问题[12]。虽然中国已经普遍控制白喉,但是一些发展中国家仍有白喉暴发,2017年印度尼西亚出现了白喉暴发[13],菲律宾马尼拉目前仍有大量白喉病例[14],尤其在幼儿中存在较高死亡率,提示可能与延迟入院或缺乏白喉抗毒素相关。一些发达国家也有相关白喉病例发生,2016年法国报道[15]从2000年开始出现白喉复燃的情况,主要集中发生在旅行者和难民,除了疫苗覆盖率不足还与国际旅行和日益增加的移民要求息息相关。
一直以来认为白喉棒状杆菌主要致病型为产毒菌株,近年来在包括波兰在内的许多国家发现,非产毒性白喉棒状杆菌也可引起感染,常表现为菌血症和心内膜炎等,死亡率很高[16]。本例患者由于其本身基础疾病较重可能掩盖了白喉棒状杆菌携带引起的感染症状,也正是由于患者入院接受治疗才会送检痰液标本检出白喉棒状杆菌,如果患者长期处于携带状态,当机体发生免疫功能低下时极有可能并发感染,引发相应的疾病。
上海作为国际贸易枢纽,存在极高的输入性病例风险,又有国内复燃的威胁,所以做好高质量的预防接种覆盖率和加强临床实验室诊断水平显得至关重要。尤其在临床症状不典型的情况下,实验室诊断对有效管理疑似病例及携带患者具有重要临床意义,可减少白喉的发病率及死亡率。目前绝大多数实验室已经具备白喉棒状杆菌的快速鉴定能力,近些年质谱技术的迅速发展更是大力推进了微生物的鉴定能力,相比传统的涂片镜检和生化反应鉴定,该技术不仅极大地缩短了鉴定所需时间,具有更多的细菌种属鉴定能力,近年来更是逐渐应用于耐药机制研究[17]。白喉是否携带毒力也是至关重要,因此除具备鉴定能力外,实验室应该提高检测毒力基因的能力,尽可能在短时间内向临床提供全面的实验室方面信息,以便临床第一时间作出应对措施,同时联合感控部门共同建立规范的应对制度。
近年来国内散发非产毒白喉棒状杆菌无症状携带者,目前尚不能排除其感染致病的可能性,所以对这类病例报道很重要,不仅可以加强实验室诊断水平,同时推动相关发病机制的研究,为白喉的感染控制提供更多的临床数据。

