盆膈上筋膜在腹腔镜括约肌间切除术中定位作用的临床效果分析*
李瑞奇,沈可欣,王泽铭,谢忠士
吉林大学中日联谊医院胃肠结直肠肛门外科 吉林长春 130031
直肠癌在我国所有恶性肿瘤中发病率较高,在男性中发病率位列第四,女性中发病率位列第三[1],近年来直肠癌发病率呈上升趋势,发病年龄趋于年轻化,男性患者占比越来越大[2]。随着新辅助放化疗、靶向治疗及免疫治疗等的推广应用,直肠癌的临床治疗有了更多元化的选择。有研究表明,对于病变局限于黏膜下层的早期直肠癌患者,新辅助放化疗联合经肛门内镜微创手术可取代全直肠系膜切除术[3]。但对于进展期中低位直肠癌患者,根治性手术切除仍然是最可靠的治疗手段[4]。而低位直肠癌手术中的保肛技术一直是外科医师重点关注的问题。在低位直肠癌中,可接受的远切缘从5 cm降至2 cm,甚至降至1 cm,这使得更多低位直肠癌患者可以通过保留括约肌获益[5]。括约肌间切除术(internal sphincter resection,ISR)适用于肿瘤下缘距齿状线距离短于5 cm的低位甚至超低位直肠癌,其以全直肠系膜切除为原则(total mesorectal excision,TME),在内外括约肌间进行分离,切除内括约肌、保留外括约肌及肛提肌,既保证了足够的远切缘,也在一定程度上保护了盆底结构与盆腔自主神经的功能,为患者保肛提供了可能性[6]。Park等[7]回顾性分析147例行ISR的局部晚期直肠癌患者的术后情况,中位随访时间为34个月,总体3年无病生存率达到64.9%,局部复发率为11.7%,说明ISR具有良好的肿瘤学治疗效果。然而,由于该手术难度较大及存在学习曲线,术后并发症如吻合口相关问题较为常见,其中吻合口漏发生率可达到4.8%~48%[8]。因此,ISR中对盆腔游离层面的准确辨识显得尤为重要,可以降低相关并发症发生率[9]。
盆膈上筋膜覆盖于肛提肌与尾骨肌的表面,是腹内筋膜的直接延续,支撑盆腔内脏器的出口,可在ISR中起到解剖定位的作用,降低进入错误平面的概率,减少相关并发症的发生。本文通过回顾性分析笔者团队开展ISR的中低位直肠癌患者的临床资料,探讨盆膈上筋膜在其中的解剖定位作用和临床应用效果,现报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2018年10月至2020年5月在吉林大学中日联谊医院胃肠结直肠肛门外科进行ISR的21例中低位直肠癌患者的临床资料。其中男性14例(66.7%),女性7例(33.3%);年龄(58.1±9.6)岁;BMI(24.1±2.9)kg/m2;肿瘤下缘距离肛缘距离3.0(2.2,4.1)cm;新辅助化疗3例(14.3%);术前MRI分期:T1期1例、T2期7例、T3期12例,1例患者无法评估;术前患者癌胚抗原4.9(2.0,10.1)ng/mL;ASA分级Ⅰ~Ⅱ级为7例(33.3%),Ⅲ~Ⅳ级为14例(66.7%)。所有患者术前肛门功能均良好。
1.2 纳入与排除标准
纳入标准:(1)术前肠镜定位为中低位(肿瘤下缘距肛缘距离≤7 cm),且病理学活检证实为直肠癌;(2)术前均接受胸、腹高分辨率CT及盆腔MRI检查;(3)肿瘤直径≤5 cm;(4)未发生肠梗阻或穿孔;(5) MRI或超声内镜诊断分期为T1~3NxM0,肿瘤未侵及肛提肌或外括约肌。排除标准:(1)既往腹部手术史;(2)术前已存在远处转移;(3)临床资料不完整。
1.3 手术方法
患者行静脉吸入复合麻醉,采用五孔法操作,以脐部穿刺孔作为观察孔,右下腹12 mm穿刺孔为主操作孔,手术操作严格遵循肿瘤手术探查原则以及TME原则。游离肠系膜下血管根部,离断并清扫D253组淋巴结,乙状结肠完全游离后束带牵引,继续向下分离直肠后间隙,注意保护腹下神经,切开该处直肠骶骨筋膜可以进入肛提肌上间隙,显露后侧壁盆膈上筋膜(见图1)。转向直肠前壁游离,于腹膜返折上方2~3 cm处切开腹膜,显露邓氏筋膜(Denonvilliers fascia),逐渐向尾侧游离至精囊腺下缘,切断邓氏筋膜并在其后方游离直肠前间隙,注意保护血管神经束(见图2)。女性患者选择在直肠生殖膈平面游离,注意保护阴道后壁,防止发生直肠阴道瘘。分离直肠两侧直至肛提肌裂孔边缘。从直肠侧后方5点、7点钟位置进入内外括约肌间隙,分离至齿状线水平(图3、图4)。直肠指诊确定肿瘤下缘与肛缘的距离,安装肛门牵开器,充分消毒后,在肿瘤下缘2 cm处全层切开直肠,显露内外括约肌间隙(图5),张力允许情况下荷包缝合关闭远端,从下往上进行游离,从后方往前方分离,直至与腹部会合,经肛门移除标本,采用器械吻合或者手工结肠肛管吻合。

图1 肛侧面辨识盆膈上筋膜
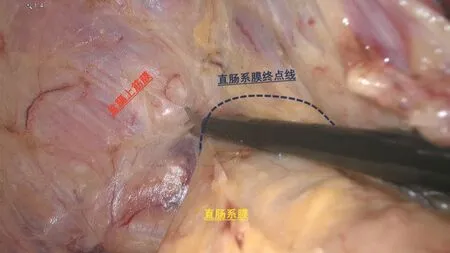
图2 腹侧面辨识盆膈上筋膜

图3 耻骨直肠肌平面

图4 痔血管平面

图5 内外括约肌间隙
1.4 观察指标
(1)手术相关指标及术后恢复指标:包括手术时间、术中出血量、术后首次进食时间、术后首次下床活动时间及住院时间。(2)手术标本及病理学指标:TNM分期、肿瘤直径、肿瘤下缘距远切缘距离、环周切缘阳性情况、淋巴结检出数、肿瘤分化程度等。(3)手术相关并发症:游离过深引起的术中损伤、术后并发症。(4)术后肛门功能评价指标:采用低位前切除综合征(low anterior resection syndrome,LARS)评分量表[10]进行评分,0~20分为无LARS,21~29分为轻度LARS,30~42分为重度LARS。
1.5 随访
所有患者术后均接受门诊和电话随访,根据LARS评分量表对患者进行肛门功能评定,同时查阅最近一次复查病历和影像学资料,评估患者生存时间和是否复发。随访时间截至2021年4月。
1.6 统计学方法
所有数据分析采用SPSS 24.0软件进行分析。符合正态分布的计量资料采用(±s)表示,偏态分布的计量资料采用M(QL,QU)表示,计数资料采用[n(%)]表示。
2 结果
2.1 手术相关指标及术后恢复指标
21例患者均顺利完成手术,无中转开腹病例,10例(47.6%)患者加行预防性造口术。平均手术时间 (242.9±66.4) min、术中出血量 30.5(23.6,65.5)mL、平均术后首次进食时间为(3.0±0.5)d、术后首次下床活动时间为(3.5±0.5)d,平均总住院时间为(15.2±3.8)d。
2.2 手术标本及病理学指标
术后病理大体标本长度为(22.3±3.3)cm,肿瘤下缘距远切缘距离为(2.9±1.4)cm。淋巴结检出数目(15.1±1.9)枚,所有病例标本系膜完整、切缘均为阴性。术后TNM分期:Ⅰ期5例(23.8%),Ⅱ期6例(28.6%),Ⅲ期10(47.6%)例。肿瘤分化程度:高分化2例(9.5%),中分化18例(85.7%),低分化1例(4.8%)。
2.3 手术相关并发症
术中出现输尿管损伤1例(4.8%)、阴道损伤1例(4.8%),术后1周内2例(9.5%)患者发生吻合口漏,经积极保守治疗后好转,顺利出院。其余患者均未出现术后并发症。
2.4 术后肛门功能情况
对未行预防性回肠造口的11例患者和10例行预防性回肠造口的患者分别在术后和还纳术后1个月、6个月使用LARS评分量表评估肛门功能。11例未行预防性回肠造口的患者术后1个月出现轻度LARS 4例,重度LARS 7例;术后6个月仅1例患者出现轻度LARS。10例行预防性回肠造口的患者在造口还纳术后1个月出现轻度LARS 8例,重度LARS 2例;造口还纳术后6个月,所有患者均无LARS。
2.5 随访结果
所有患者术后均接受门诊和电话随访7~30个月,中位随访时间23个月,随访至2021年4月无死亡病例,其中2例(9.5%)患者复发,其余19例(90.5%)患者均未出现局部复发及远处转移,恢复良好。
3 讨论
盆膈上筋膜是被覆肛提肌与尾骨肌的一层菲薄筋膜,TME手术应该将直肠系膜完整地从这层筋膜表面分离,然而由于盆腔空间狭小,许多情况下做到准确辨识的难度较大,易造成直肠系膜脂肪组织的残留,从而导致TME手术质量的下降,加之一些术者对TME观念理解存在偏差,往往在尚未显露这个层面时就进行了直肠系膜的裸化。但是对于超低位直肠癌行ISR时,假如不能暴露肛提肌裂孔,则无法通过正确的平面进入肛门内外括约肌间隙,而盆膈上筋膜可以提供良好的解剖定位作用。笔者团队在进行TME时发现,经直肠腔内切开时,依次切开黏膜、黏膜下层、固有肌层,全层切开后才能进入到正确的解剖层面,而这些组织层面的交界点需要一个明确的解剖标志去指引,并认为盆膈上筋膜在经肛全直肠系膜切除术(transanal total mesorectal excision,taTME)中可起到定位作用[11],在这个理念的引导下,复习手术录像并在后续的ISR实践中进行验证,发现盆膈上筋膜也可以很好地帮助手术医师寻找肛门内外括约肌间隙,提高TME的手术质量。
需要注意的是,由于盆腔空间狭小,在游离的过程中可能误切破盆膈上筋膜,直接暴露肛提肌,虽说这并不影响TME的手术质量,但是由此造成的游离平面混乱会增加后续寻找肛门内外括约肌间隙的难度。因此,在游离平面从直肠后间隙转到肛提肌上间隙时,要维持好牵引的张力,可以采用钝锐结合的方式仔细分离,避免过早切开6点钟方向的直肠尾骨韧带,应从5点、7点钟方向向前侧壁拓展。采用从后方推进的方式会造成侧壁系膜的残留,我们推荐的游离技巧是“先后再前再两侧”,前壁游离并非只是把握与直肠与前列腺(阴道)之间的层面,而要充分拓展前侧腔,与2点、10点钟方向紧贴直肠末端显露肛提肌裂孔“U”形顶端的盆膈上筋膜,而后再与5点、7点钟的拓展平面相连通。最佳的游离状态应在侧后壁看见肛提肌裂孔“U”形袢,可见覆盖其表面的盆膈上筋膜,然后沿此筋膜与直肠的交界点从5点、7点钟方向钝性分离进入肛门内外括约肌间隙。
膜解剖的意义在于保持手术范围在正确的解剖层面,随着对胚胎解剖学研究的深入,传统的解剖结构将被赋予更大的定位功能,有利于实现手术安全性和功能性的统一。在高清腹腔镜的可视化前提之下,术者精细的操作可以实现狭小区域膜间隙的寻找和分离,无论系膜还是筋膜都是手术必要的定位指引,探索和发现富有临床指导意义的术中解剖标志,有利于提高手术综合质量和治疗效果。

