雷公藤茎中的二萜类成分及生物活性研究
周晓琼,饶凯瑞,陈宣钦
昆明理工大学生命科学与技术学院,昆明 650500
雷公藤(TripterygiumwilfordiiHook.f.)是卫矛科雷公藤属植物,又名水莽草,断肠草等,多分布于长江流域以南及西南地区。雷公藤始载于《神农本草经》,其味苦、辛,性寒,归肝、肾二经,具有祛风除湿、杀虫解毒、消肿止痛和舒筋活络的功效[1]。雷公藤作为一种常用中药,多以根入药,已开发成多种雷公藤制剂,如雷公藤多苷片,雷公藤片,雷公藤总萜片和雷公藤双层片等[2],这些雷公藤制剂主要用于免疫和炎性疾病的治疗,如类风湿关节炎,红斑狼疮和溃疡性结肠炎等[3]。此外,现代药理学研究发现雷公藤还具有抗肿瘤活性,其在肿瘤治疗中具有很好的应用前景。
至今为止,国内外科研工作者已从雷公藤属中分离鉴定了500多个化合物,主要为二萜,三萜和倍半萜,其中二萜类成分骨架类型多样,包括松香烷型、海松烷型、对映贝壳杉烷型和其他类型。松香烷型三元环氧二萜内酯类化合物,如雷公藤甲素及其衍生物一直以来被认为是雷公藤二萜类成分中抗炎和抗肿瘤的主要活性成分[4]。然而,雷公藤甲素及其衍生物的含量低且多数具有较强的肝和肾毒性,这极大的限制了雷公藤的应用和开发。在雷公藤中,除雷公藤甲素及其衍生物外,是否存在其他低毒高效的抗炎和抗肿瘤活性二萜类成分,值得进一步研究。另一方面,有关雷公藤化学成分的研究主要集中在其主要药用部位根中,对其茎的化学成分研究不够深入,查阅文献发现从雷公藤茎或者茎和叶的混合提取物中分离到的化合物目前共24个,其中二萜类化合物有9个。鉴于此,本研究采用各种色谱和波谱技术对雷公藤茎中的二萜类成分进行了系统的分离和鉴定,并对分离得到的化合物进行了体外抗炎和抗肿瘤活性评价。
1 材料与方法
1.1 药材
干燥的雷公藤茎于2019年7月购自于昆明市新螺蛳湾药材市场,并由昆明理工大学陈宣钦副教授鉴定为雷公藤(Tripterygiumwilfordii),凭证标本(KUMST20190716)存放于昆明理工大学生命科学与技术学院资源药物化学重点实验室。
1.2 仪器与试剂
拌样硅胶(80~100目)、柱色谱用硅胶(200~300目)、十八烷基硅胶(ODS-C18,75 μmol,日本YMC公司)和羟丙基葡聚糖凝胶(Sephadex LH-20,20~100 μmol,Pharmacia公司);薄层色谱(TLC)用硅胶板(G和GF254,青岛海洋化工厂);色谱纯试剂甲醇和乙腈(Fisher公司);显色剂5% H2SO4-EtOH溶液(喷洒后适当加热);胎牛血清(FBS,Hyclone公司);基础培养基(DMEM,Thermofisher公司);二甲基亚砜(DMSO,Solarbio公司);小鼠巨噬细胞RAW 264.7(中国科学院昆明动物研究所)和脂多糖(LPS,sigma公司);Hela细胞株(中国科学院昆明动物研究所);4-羟乙基哌嗪乙磺酸(HEPES,Biosharp公司);青链霉素混合液(Solarbio公司);四甲基偶氮唑盐(MTT,Solarbio公司);一氧化氮合成酶抑制剂(L-NMMA,Beyo Time公司)。
Bruker DRX-500和Bruker AV Ⅲ-600核磁共振仪(德国,Bruker BioSpin Group);UV1102Ⅱ紫外分光光度计(Betop Scientific);高分辨质谱仪(Agilent 6530 LC/MSD);Jasco DIP-370数字偏振仪(日本,JASCO Corporation);Agilent 1200高效液相色谱仪(Agilent公司),配备ZORBAX SB-C18反相柱和二极管阵列检测器(Agilent公司);Spectra Max M2多功能读板机(美国,Moleccular Devices 公司)和CO2恒温培养箱(Thermofisher公司)。
1.3 方法
1.3.1 提取与分离
雷公藤茎50 kg粉碎,采用95%乙醇浸泡提取3次,每次60 L,每次24 h,浓缩后,加适量水溶解,并依次用石油醚,乙酸乙酯和正丁醇分别萃取3次。
乙酸乙酯部位(672 g)经硅胶柱层析(石油醚∶乙酸乙酯,5∶1和2∶1)进行划段,得到4个部分Fr.1~4。Fr.1(29 g)通过硅胶柱层析(石油醚∶乙酸乙酯,50∶1、30∶1和20∶1)划分为2个组分Fr.1.1~1.2。Fr.1.1(2.1 g)经过ODS-C18反相中压柱层析(甲醇∶水,70%→100%)分为2个组分Fr.1.1.1~1.1.2。Fr.1.1.1(90 mg)采用硅胶柱层析(石油醚∶乙酸乙酯,11∶1)进行纯化得到化合物4(10.7 mg)。Fr.1.2(18 g)经过ODS-C18反相中压柱层析(甲醇∶水,60%→100%)划分为Fr.1.2.1~1.2.4共4个组分。Fr.1.2.1(4.09 g)通过硅胶柱层析(石油醚∶乙酸乙酯,30∶1、20∶1和10∶1)得到Fr.1.2.1.1~1.2.1.4共4个组分,其中Fr.1.2.1.1(62.8 mg)经过硅胶柱层析(石油醚∶二氯甲烷,1∶1)分离纯化得到化合物2(34.3 mg)。Fr.1.2.1.2(45 mg)通过硅胶柱层析(石油醚∶二氯甲烷,1.5∶1和1∶1)分离纯化得到化合物5(6.7 mg)。Fr.1.2.1.3(420.1 mg)采用硅胶柱层析(石油醚∶二氯甲烷,1.5∶1和1∶1)得到2个部分Fr.1.2.1.3.1~1.2.1.3.2。Fr.1.2.1.3.1(63 mg)经过硅胶柱层析(石油醚∶乙酸乙酯,10∶1)分离纯化得化合物9(9.7 mg)。Fr.1.2.1.3.2(382.1 mg)采用硅胶柱层析(石油醚∶异丙醇,100∶1)分离纯化得化合物11(58.8 mg)。Fr.1.2.1.4(54.9 mg)通过硅胶柱层析(石油醚∶乙酸乙酯,12∶1)分离纯化得化合物12(5.0 mg)。Fr.1.2.2(548.9 mg)采用硅胶柱层析(石油醚∶氯仿,1∶10;氯仿∶乙酸乙酯,40∶1和30∶1)洗脱得到化合物19(26.4 mg)。Fr.1.2.3(618.2 mg)采用硅胶柱层析(二氯甲烷∶乙酸乙酯,10∶1)得到化合物16(121.9 mg)。Fr.1.2.4(2.45 g)经过硅胶柱层析(石油醚∶二氯甲烷,1∶1)洗脱得2个部分Fr.1.2.4.1~1.2.4.2。Fr.1.2.4.1(36.7 mg)采用硅胶柱层析(石油醚∶二氯甲烷,2∶1)得到化合物10(1.3 mg)。Fr.1.2.4.2(328.7 mg)经过硅胶柱层析(石油醚∶丙酮,35∶1)得到化合物17(23 mg)和化合物18(28.3 mg)。
Fr.2(49.48 g)经过ODS-C18反相中压柱层析(甲醇∶水,60%→100%)得到3个组分Fr.2.1~2.3。Fr.2.1(4.6 g)采用硅胶柱层析(石油醚∶乙酸乙酯,7∶1)洗脱得到2个组分Fr.2.1.1~2.1.2。Fr.2.1.1(288.8 mg)采用硅胶柱层析(石油醚∶乙酸乙酯,7∶1)分离纯化得化合物6(8.1 mg)和化合物7(12 mg)。Fr.2.1.2(943.8 mg)经过Sephadex LH-20(氯仿∶甲醇,1∶1)分离得到化合物20(29 mg)和2个组分Fr.2.1.2.1~2.1.2.2。Fr.2.1.2.1(100 mg)通过半制备HPLC(乙腈∶水,28%,tR= 9.2 min)得到化合物8(2.2 mg)。Fr.2.1.2.2(400 mg)采用硅胶柱层析(二氯甲烷∶乙酸乙酯,80∶1)得到化合物13(4.8 mg)。Fr.2.2(8.2 g)经过硅胶柱层析(二氯甲烷∶乙酸乙酯,120∶1和30∶1)分成2个部分 Fr.2.2.1~2.2.2。Fr.2.2.1(582.5 mg)采用硅胶柱层析(石油醚∶异丙醇,30∶1)分为2个部分Fr.2.2.1.1~2.2.1.2,其中Fr.2.2.1.1(124.2 mg)采用硅胶柱层析(石油醚∶二氯甲烷,1∶10)洗脱得到化合物1(2 mg),Fr.2.2.1.2(75 mg)采用硅胶柱层析(二氯甲烷∶乙酸乙酯,200∶1)分离纯化得到化合物14(24 mg)和化合物15(22.4 mg)。Fr.2.2.2(449.9 mg)经过硅胶柱层析(石油醚∶异丙醇,50∶1)划分为 Fr.2.2.2.1~2.2.2.2共2个部分。Fr.2.2.2.2(107 mg)采用硅胶柱层析(二氯甲烷∶乙酸乙酯,200∶1)分离,得到化合物3(15 mg)。
1.3.2 抗炎活性和毒性筛选
1.3.2.1 巨噬细胞RAW 264.7的培养
RAW 264.7细胞使用DMEM培养基(含有10%胎牛血清和1%青链霉素双抗溶液),于37 ℃、5% CO2培养箱中进行恒温培养,每日观察细胞生长的状态,同时DMEM培养液需要定期进行替换,直到细胞生长良好,覆盖率达90%以上对细胞进行传代。
1.3.2.2 Griess试剂的配制
Griess Ⅰ液:在1.0 g无水对氨基苯磺酸中加入6 mL的磷酸和适量的超纯水,进行水浴加热使其全部溶解,再定容至100 mL,进行除杂除菌后,于4 ℃的条件贮存备用。
Griess Ⅱ液:称取0.1 g的N-1-萘基乙二胺二盐酸盐同上述方法配制。
1.3.2.3 Griees法检测体外抗炎活性
把对数生长期的RAW 264.7细胞,按7×104浓度稀释,接种于96孔细胞培养板中(每孔加入100 μL细胞悬液),再置于37 ℃,5% CO2恒温培养箱中继续培养24 h后,把贴壁生长的细胞分别分为空白组、模型组(1 μg/mL脂多糖LPS)、实验组(待测物+1 μg/mL LPS)和阳性对照组(一氧化氮合成酶抑制剂L-NMMA+1 μg/mL LPS)等4个组,每组设3个复孔。其中,待测物的浓度分别为12.5、6.25、3.125、1.56 和0.78 μmol/L;继续培养24 h之后,吸取各孔细胞的上层清液加入50 μL的Griess Ⅰ溶液并用摇床振摇10 min,之后再加入50 μL的Griess Ⅱ溶液并在避光条件下振摇10 min,最后用酶标仪检测其在540 nm处的吸光值,使用IBM SPSS Statistics 20计算半数抑制浓度IC50值。
1.3.2.4 MTT法检测细胞毒性
把浓度为7×104的RAW 264.7细胞接种于96孔细胞培养板中,再置于37 ℃,5% CO2恒温培养箱中继续培养24 h,用不同浓度(50、25、12.5、6.25、3.125 μmol/L)的待测物处理RAW 264.7细胞。用MTT法检测化合物对RAW 264.7细胞的细胞毒性[5]。
1.3.2.5 MTT法检测抗肿瘤活性
把对数生长期的Hela细胞以每孔1×105的密度接种于96孔板中,恒温培养24 h后,以顺铂为阳性对照,以不同浓度50、25、12.5、6.25和3.12 μmol/L的样品作为实验组,作用48 h,用MTT比色法测定细胞存活率[6]。
2 实验结果
从雷公藤茎中分离得到了20个二萜类化合物(见图1),包括1个新二萜和19个已知二萜。
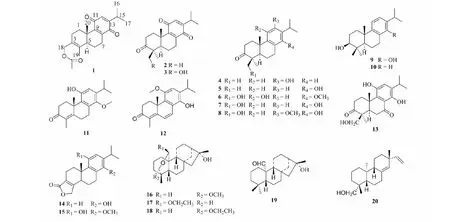
图1 化合物1~20的结构Fig.1 The structures of compounds 1~20
2.1 结构鉴定
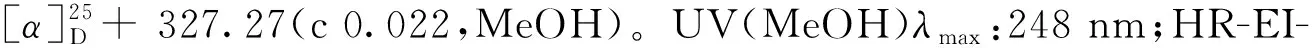
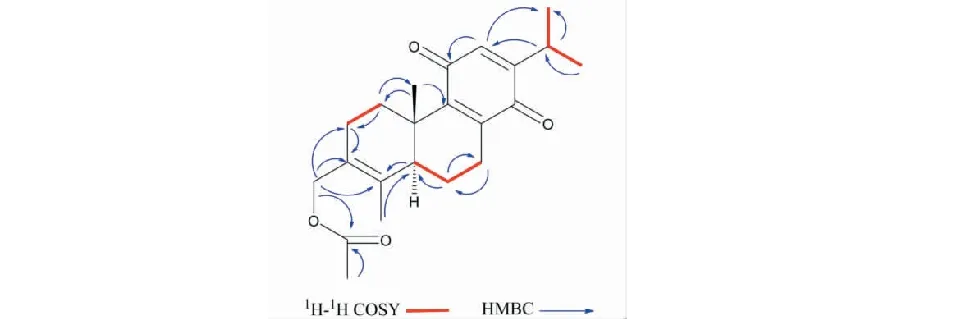
图2 化合物1的1H-1H COSY 和 HMBC相关Fig.2 1H-1H COSY and HMBC correlations of compound 1
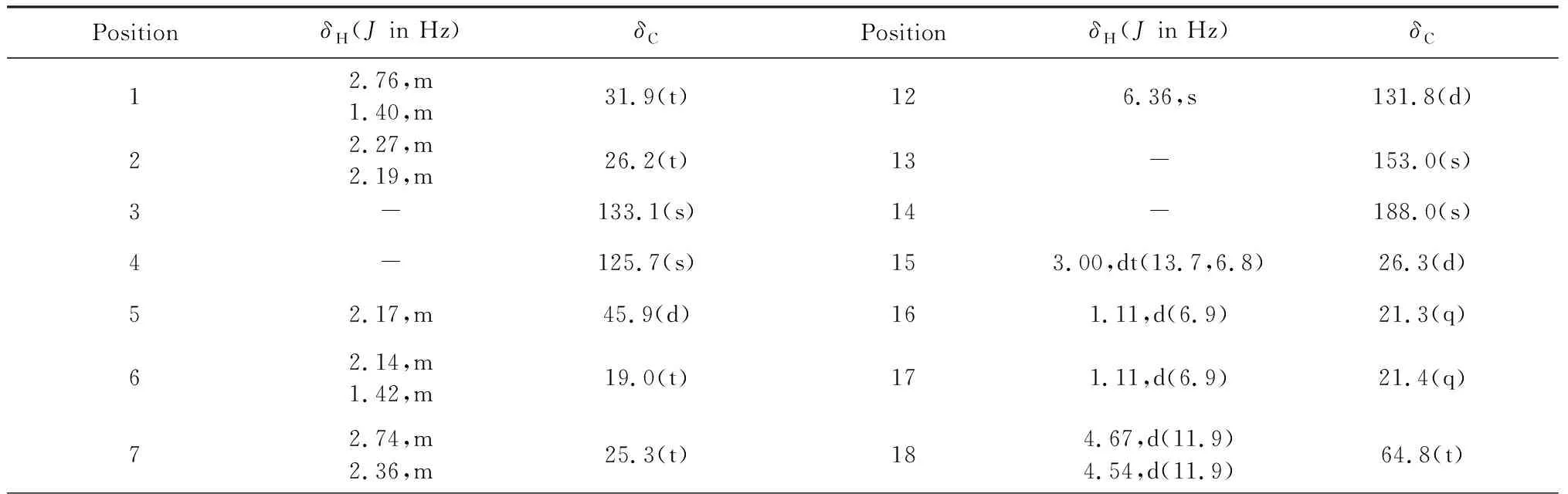
表1 化合物1的1H NMR(600 MHz,CDCl3)和13C NMR(150 MHz,CDCl3)谱数据
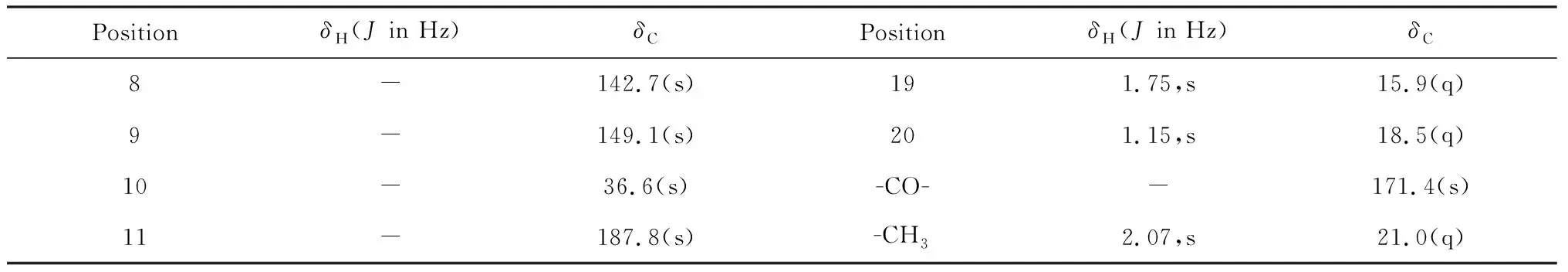
续表1
化合物2淡黄色油状物;分子式C20H26O3。1H NMR(600 MHz,CDCl3)δ:6.37(1H,s,H-12),3.00(1H,m,H-15),2.86(1H,m,H-2),2.82(1H,m,H-7),2.57(2H,m,H-1),2.32(1H,m,H-7),1.52(1H,m,H-6),1.30(3H,s,H-20),1.15(3H,s,H-19),1.12(3H,s,H-18),1.12(3H,d,J= 6.9 Hz,H-16),1.11(3H,d,J= 6.9 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:217.1(C-3),187.7(C-14),187.5(C-11),153.2(C-13),148.2(C-9),142.8(C-8),131.9(C-12),50.8(C-5),47.0(C-4),37.5(C-10),34.7(C-1),33.9(C-2),27.7(C-19),26.4(C-15),25.5(C-7),21.4(C-17),21.3(C-16),20.7(C-18),20.2(C-20),18.6(C-6)。以上波谱数据与文献[8,9]报道的数据一致,故鉴定化合物2为雷藤二萜醌H。
化合物3黄色无定形粉末;分子式C20H26O4。1H NMR(600 MHz,CDCl3)δ:6.38(1H,d,J= 1.2 Hz,H-12),4.06(1H,d,J= 11.4 Hz,H-19),3.46(1H,m,H-19),3.00(1H,m,H-15),2.84(1H,m,H-1),2.48(1H,ddd,J= 15.7,9.1,5.6 Hz,H-2),2.29(1H,ddd,J= 20.0,11.8,6.6 Hz,H-7),2.01(1H,dd,J= 13.0,2.2 Hz,H-5),1.85(2H,m,H-1,H-6),1.83(1H,m,H-1),1.43(1H,m,H-6),1.35(3H,s,H-18),1.28(3H,s,H-20),1.12(3H,d,J= 6.9 Hz,H-16),1.10(3H,d,J= 6.9 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:221.0(C-3),187.6(C-14),187.4(C-11),153.4(C-13),147.5(C-9), 142.5(C-8),131.9(C-12),65.6(C-19),51.6(C-5),50.2(C-4),37.1(C-10),34.4(C-1),34.2(C-2),26.4(C-15),25.5(C-7),22.6(C-18),21.4(C-17),21.3(C-16), 21.2(C-20),17.8(C-6)。以上波谱数据与文献[10]报道的数据一致,故鉴定化合物3为triptoquinone B。
化合物4无色油状物;分子式C20H28O2。1H NMR(600 MHz,CDCl3)δ:6.87(1H,s,H-11),6.63(1H,s,H-14),3.13(1H,m,H-15),1.27(3H,s,H-18),1.25(3H,d,J= 6.9 Hz,H-17),1.23(3H,d,J= 6.9 Hz,H-16),1.16(3H,s,H-19),1.13(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:217.9(C-3),151.1(C-12),145.6(C-9),132.3(C-13),126.8(C-8),126.6(C-14),111.8(C-11),50.5(C-5),47.4(C-4),37.5(C-1),37.0(C-10),34.6(C-2),30.1(C-7),26.9(C-18),26.8(C-15),24.6(C-20),22.7(C-17),22.5(C-16),21.0(C-19),20.4(C-6)。以上波谱数据与文献[11,12]报道的数据一致,故鉴定化合物4为hinokione。
化合物5无色油状物;分子式C20H28O2。1H NMR(600 MHz,CDCl3)δ:7.04(1H,d,J= 8.2 Hz,H-12),6.85(1H,d,J= 8.2 Hz,H-11),4.75(1H,s,14-OH),3.13(1H,m,H-15),2.92(1H,m,H-7),2.61(1H,m,H-7),2.56(1H,m,H-2),2.48(1H,m,H-2),1.93(1H,m,H-6),1.91(1H,m,H-1),1.88(1H,m,H-1),1.80(1H,m,H-6),1.33(3H,s,H-18),1.25(3H,d,J= 6.8 Hz,H-17),1.23(3H,d,J= 6.8 Hz,H-16),1.17(3H,s,H-19),1.14(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:217.3(C-3),150.1(C-14),146.4(C-9),130.4(C-13),123.6(C-12),120.8(C-8),117.3(C-11),50.0(C-5),47.4(C-4),37.6(C-1),37.1(C-10),34.8(C-2),26.9(C-15),26.6(C-19),24.7(C-7),24.4(C-18),22.8(C-17),22.5(C-16),21.2(C-20),19.5(C-6)。以上波谱数据与文献[10]报道的数据一致,故鉴定化合物5为雷酚萜。
化合物6白色粉末;分子式C21H30O4。1H NMR(600 MHz,CDCl3)δ:6.30(1H,s,H-12),4.40(1H,d,J= 11.4 Hz,H-19),3.67(3H,s,H-21),3.44(1H,d,J= 11.4 Hz,H-19),3.24(1H,m,H-15),3.08(1H,m,H-7),3.08(1H,m,H-1),2.77(1H,ddd,J= 15.1,11.2,6.7 Hz,H-2),2.55(1H,m,H-7),2.39(1H,m,H-2),2.22(1H,dd,J= 12.9,12.0 Hz,H-5),2.04(1H,m,H-1),1.85(1H,m,H-6),1.46(1H,m,H-6),1.42(3H,s,H-18),1.29(3H,s,H-20),1.18(3H,d,J= 6.9 Hz,H-16),1.17(3H,d,J= 6.9 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:223.8(C-3),150.5(C-11),148.4(C-14),139.7(C-13),130.7(C-9),130.6(C-8),111.8(C-12),66.1(C-19),60.8(C-21),52.6(C-5),49.9(C-4),37.6(C-10),35.4(C-1),34.6(C-2),26.5(C-7),26.1(C-15),23.8(C-17),23.8(C-16),22.8(C-18),21.1(C-20),19.1(C-6)。以上波谱数据与文献报道的数据一致[13],故鉴定化合物6为triptonediol。
化合物7黄色无定形粉末;分子式C20H28O3。1H NMR(600 MHz,CDCl3)δ:7.04(1H,d,J= 8.2 Hz,H-12),6.85(1H,d,J= 8.2 Hz,H-11),4.08(1H,d,J= 11.3 Hz,H-19),3.54(1H,d,J= 11.3 Hz,H-19),3.11(1H,m,H-15),2.92(1H,dd,J= 16.7,4.8 Hz,H-7),2.70(1H,ddd,J= 16.1,9.1,4.5 Hz,H-2),2.62(1H,dd,J= 16.8,8.1 Hz,H-2),2.48(1H,ddd,J= 13.0,8.2,4.5 Hz,H-1),2.10(1H,dd,J= 13.1,2.2 Hz,H-5),2.02(1H,m,H-1),1.97(1H,m,H-7),1.70(1H,m,H-6),1.35(3H,s,H-18),1.28(3H,s,H-20),1.25(3H,d,J= 6.8 Hz,H-16),1.24(3H,d,J= 6.8 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:220.4(C-3),150.0(C-14),145.6(C-9),130.4(C-13),123.7(C-12),120.7(C-8),117.7(C-11),65.7(C-19),51.0(C-4),50.7(C-5),37.3(C-1),36.8(C-10),35.0(C-2),26.9(C-15),25.5(C-20),24.8(C-7),22.7(C-17),22.5(C-16),22.1(C-18),19.0(C-6)。以上波谱数据与文献[10]报道的数据一致[14],故鉴定化合物7为triptobenzene A。
化合物8淡黄色无定形粉末;分子式C21H30O4。1H NMR(600 MHz,CDCl3)δ:6.36(1H,s,H-11),4.73(1H,s,14-OH),4.07(1H,d,J= 11.3 Hz,H-19),3.77(3H,s,H-21),3.49(1H,s,H-19),3.45(1H,m,H-15),2.99(1H,s,19-OH),2.80(1H,dd,J= 15.3,6.4 Hz,H-7),2.71(1H,ddd,J= 16.0,9.3,4.6 Hz,H-2),2.60(1H,dt,J= 16.1,8.1 Hz,H-2),2.50(1H,m,H-7),2.44(1H,ddd,J= 13.1,8.5,4.8 Hz,H-1),2.11(1H,dd,J= 13.0,2.2 Hz,H-5),2.06(1H,m,H-1),1.96(1H,m,H-6),1.68(1H,m,H-6),1.35(3H,s,H-18),1.32(3H,d,J= 7.2 Hz,H-16),1.31(3H,d,J= 7.2 Hz,H-17),1.29(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:220.4(C-3),156.8(C-12),151.5(C-14),145.2(C-9),119.2(C-13),113.8(C-8),100.8(C-11),65.6(C-19),55.7(C-21),50.9(C-4),50.8(C-5),37.2(C-1),37.0(C-10),34.9(C-2),25.4(C-20),24.3(C-7),24.3(C-15),22.2(C-18),20.9(C-16),20.8(C-17),19.1(C-6)。以上波谱数据与文献[15]报道的数据一致,故鉴定化合物8为wilforol F。
化合物9白色无定形粉末;分子式C20H30O2。1H NMR(600 MHz,CDCl3)δ:7.03(1H,d,J= 8.2 Hz,H-12),6.84(1H,d,J= 8.2 Hz,H-11),3.15(1H,m,H-15),2.85(1H,dd,J=16.5,6.5 Hz,H-7),1.25(3H,d,J= 6.9 Hz,H-16),1.22(3H,d,J= 6.9 Hz,H-17),1.20(3H,s,H-20),1.07(3H,s,H-18),0.90(3H,s,H-19);13C NMR(150 MHz,CDCl3)δ:150.2(C-14),148.3(C-9),130.2(C-13),123.4(C-12),120.6(C-8),116.5(C-11),78.7(C-3),49.2(C-5),38.9(C-4),37.3(C-10),37.1(C-1),28.2(C-19),28.0(C-2),26.8(C-15),24.9(C-20),24.7(C-7),22.8(C-17),22.5(C-16),18.2(C-6),15.4(C-18)。以上波谱数据与文献[14]报道的数据一致,故鉴定化合物9为triptobenzene B。
化合物10白色粉末;分子式C20H30O。1H NMR(600 MHz,CDCl3)δ:7.17(1H,d,J= 8.1 Hz,H-11),7.00(1H,m,H-12),6.90(1H,s,H-14),3.30(1H,m,H-3),2.95(1H,m,H-15),2.79-2.89(2H,m,H-15/H-7),1.23(3H,d,J= 7.3 Hz,H-17),1.21(3H,d,J= 7.3 Hz,H-16),1.19(3H,s,H-19),1.07(3H,s,H-18),0.89(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:146.8(C-9),145.7(C-13),134.7(C-8),126.8(C-14),124.4(C-11),123.9(C-12),78.8(C-3),49.8(C-5),39.0(C-4),37.3(C-10),36.9(C-1),33.4(C-15),30.7(C-7),28.2(C-18),28.0(C-2),24.9(C-20),24.0(C-17),24.0(C-16),18.9(C-6),15.4(C-19)。以上波谱数据与文献[16]报道的数据一致,故鉴定化合物10为abietatrien-3β-ol。
化合物11黄色油状物;分子式C20H26O3。1H NMR(600 MHz,CDCl3)δ:6.54(1H,s,H-12),3.66(3H, s,H-21),3.29(1H,s,H-15),3.24(1H,m,H-7),3.20(1H,m,H-1),2.96(1H,m,H-6),2.70(1H,m,H-2),2.49(1H,m,H-7),2.46(1H,m,H-2),2.28(1H,m,H-6),1.89(3H,s,H-18),1.84(1H,m,H-1),1.70(3H,s,H-20),1.18(3H,d,J= 6.9 Hz,H-17),1.16(3H,d,J= 6.9 Hz,H-16);13C NMR(150 MHz,CDCl3)δ:200.4(C-3),166.1(C-5),151.4(C-11),147.7(C-14),139.7(C-13),130.9(C-8),129.1(C-9),126.7(C-4),112.6(C-12),61.1(C-21),40.7(C-10),34.2(C-2),32.1(C-1),26.7(C-6),26.2(C-15),25.4(C-7),23.9(C-17),23.6(C-16),22.3(C-20),10.8(C-18)。以上波谱数据与文献[17]报道的数据一致,故鉴定化合物11为triptobenzene S。
化合物12黄色无定形粉末;分子式C20H24O3。1H NMR(600 MHz,CDCl3)δ:7.13(1H,d,J= 10.0 Hz,H-7),6.53(1H,s,H-12),6.53(1H,d,J= 10.0 Hz,H-6),3.83(3H,s,H-20),2.72(1H,m,H-1),2.64(1H,m,H-1),2.56(1H,m,H-2),2.24(1H,m,H-2),1.90(3H,s,H-18),1.39(3H,s,H-19),1.35(3H,d,J= 7.2 Hz,H-16),1.35(3H,d,J= 7.2 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:197.5(C-3),158.9(C-11),156.6(C-5),151.1(C-14),145.3(C-9),128.7(C-4),126.6(C-7),120.1(C-6),119.2(C-13),112.8(C-8),100.1(C-12),55.6(C-20),39.2(C-10),33.9(C-1),33.3(C-2),29.9(C-19),24.3(C-15),20.9(C-16),20.9(C-17),10.5(C-18)。以上波谱数据与文献[7]报道的数据一致,故鉴定化合物12为hypoglicin B。
化合物13黄色无定形粉末;分子式C20H26O5。1H NMR(600 MHz,CDCl3)δ:12.78(1H,s,14-OH),6.85(1H,s,H-12),5.04(1H,s,11-OH),4.07(1H,d,J= 11.3 Hz,H-19),3.53(1H,d,J= 11.3 Hz,H-19),3.32(1H,m,H-15),3.32(1H,m,H-1),3.12(1H,s,19-OH),2.76(1H,m,H-2),2.73(1H,m,H-6),2.65(1H,d,J= 2.5 Hz,H-5),2.64(1H,d,J= 2.5 Hz,H-6),2.54(1H,ddd,J= 15.6,8.7,6.7 Hz,H-2),2.07(1H,ddd,J= 14.1,9.7,6.7 Hz,H-1),1.42(3H,s,H-20),1.35(3H,s,H-18),1.20(3H,d,J= 6.6 Hz,H-16),1.29(3H,d,J= 6.6 Hz,H-17);13C NMR(150 MHz,CDCl3)δ:219.4(C-3),204.4(C-7),155.2(C-14),144.7(C-11),136.6(C-13),133.0(C-9),123.8(C-12),114.8(C-8),65.6(C-19),50.2(C-4),49.3(C-5),38.2(C-10),35.5(C-6),35.1(C-1),34.8(C-2),26.0(C-15),22.6(C-18),22.3(C-17),22.1(C-16),18.3(C-20)。以上波谱数据与文献[18]报道的数据一致,故鉴定化合物13为triregelin H。
化合物14黄色油状物;分子式C20H24O3。1H NMR(600 MHz,CDCl3)δ:7.08(1H,d,J= 8.2 Hz,H-12),6.96(1H,d,J= 8.2 Hz,H-11),4.89(1H,d,J= 3.4 Hz,14-OH),4.84(1H,m,H-19),4.77(1H,m,H-19),3.12(1H,m,H-15),2.92(1H,dd,J= 17.3,7.3 Hz,H-7),2.82(1H,m,H-7),2.51(2H,m,H-2),2.00(2H,m,H-6),1.70(2H,m,H-1),1.28(3H,d,J= 6.9 Hz,H-16),1.26(3H,d,J= 6.9 Hz,H-17),1.03(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:174.4(C-18),163.0(C-4),150.8(C-14),143.8(C-8),131.0(C-9),125.1(C-13),123.4(C-12),120.6(C-3),116.3(C-11),70.6(C-19),40.8(C-15),36.2(C-10),32.6(C-1),26.9(C-5),22.8(C-17),22.6(C-6),22.54(C-16),22.46(C-20),19.7(C-2),18.2(C-7)。以上波谱数据与文献[19,20]报道的数据一致,故鉴定化合物14为雷酚内酯。
化合物15黄色油状物;分子式C21H26O4。1H NMR(600 MHz,CDCl3)δ:6.48(1H,s,H-12),4.80(2H,m,H-19),3.69(3H,s,H-21),3.08(1H,m,H-15),2.40(2H,m,H-2),1.82(2H,m,H-1),1.18(6H,d,J= 6.9 Hz,H-16/H-17),1.16(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:174.6(C-18),163.4(C-4),150.8(C-14),149.1(C-11),139.9(C-13),130.8(C-9),129.2(C-8),125.2(C-3),111.9(C-12),70.7(C-19),60.7(C-21),44.0(C-15),37.2(C-10),31.0(C-1),26.0(C-5),25.5(C-2),23.8(C-17),23.8(C-16),19.5(C-6),18.6(C-7),17.3(C-20)。以上波谱数据与文献[19]报道的数据一致,故鉴定化合物15为雷酚新内酯。
化合物16无色油状物;分子式C21H34O3。1H NMR(600 MHz,CDCl3)δ:4.40(1H,dd,J= 11.1,2.7 Hz,H-20),4.14(1H,s,H-19),3.35(1H,d,J= 12.4 Hz,H-20),3.32(3H,s,H-21),2.24(1H,m,H-2),2.17(1H,m,H-5),1.87(1H,m,H-1),1.82(1H,m,H-6),1.73(1H,m,H-13),1.66(1H,m,H-14),1.37(3H,s,H-17),0.86(3H,s,H-18);13C NMR(150 MHz,CDCl3)δ:105.9(C-19),79.4(C-16),62.5(C-20),57.6(C-15),55.0(C-21),52.5(C-9),49.2(C-5),48.2(C-13),44.9(C-8),40.6(C-1),40.4(C-7),40.35(C-3),39.0(C-10),38.5(C-14),36.7(C-4),26.8(C-12),24.5(C-17),23.3(C-18),22.4(C-2),22.1(C-6),18.0(C-11)。以上波谱数据与文献[21]报道的数据一致,故鉴定化合物16为16α-hydroxy-19,20-epoxy-19R*-methoxy-kaurane。
化合物17无色油状物;分子式C22H36O3。1H NMR(600 MHz,CDCl3)δ:5.21(1H,s,H-20),3.97(1H,m,H-21),3.62(1H,dd,J= 11.3,2.7 Hz,H-19),3.49(1H,dd,J= 11.3,1.7 Hz,H-19),3.40(1H,m,H-21),2.52(1H,m,H-1),2.36(1H,m,H-2),1.99(1H,m,H-11),1.82(1H,s,H-13),1.38(3H,s,H-17),1.22(3H,t,J= 7.1 Hz,H-22),1.07(1H,m,H-5),0.68(3H,s,H-18);13C NMR(150 MHz,CDCl3)δ:101.7(C-20),79.5(C-16),71.7(C-19),64.1(C-21),58.0(C-15),54.2(C-9),52.1(C-5),49.0(C-13),44.9(C-8),41.7(C-10),41.2(C-3),40.6(C-7),38.7(C-14),35.7(C-1),33.3(C-4),25.6(C-12),24.4(C-17),23.3(C-18),22.4(C-2),19.8(C-6),18.6(C-11),15.1(C-22)。以上波谱数据与文献[22]报道的数据一致,故鉴定化合物17为16α-hydroxy-19,20-epoxy-20R*-ethoxy-kaurane。
化合物18白色粉末;分子式C22H36O3。1H NMR(600 MHz,CDCl3)δ:4.43(1H,dd,J= 11.0,2.8 Hz,H-20),4.25(1H,s,H-19),3.71(1H,m,H-21),3.36(1H,m,H-21),3.32(1H,d,J= 10.7 Hz,H-20),2.24(1H,m,H-2),2.16(1H,m,H-1),1.94(1H,m,H-6),1.81(1H,m,H-13),1.37(3H,s,H-17),1.20(3H,t,J= 7.1 Hz,H-22),0.85(3H,s,H-18);13C NMR(150 MHz,CDCl3)δ:104.2(C-19),79.5(C-16),62.7 (C-21),62.6(C-20),57.6(C-15),52.5(C-9),49.2(C-5),48.3(C-13),45.0(C-8),40.7(C-1),40.4(C-3),40.40(C-7),39.0(C-10),38.4(C-14),36.6(C-4),26.8(C-12),24.4(C-17),23.4(C-18),22.5(C-2),22.0(C-6),18.1(C-11),15.4(C-22)。以上波谱数据与文献[22]报道的数据一致,故鉴定化合物18为16α-hydroxy-19,20-epoxy-19R*-ethoxy-kaurane。
化合物19无色油状物;分子式C20H32O2。1H NMR(600 MHz,CDCl3)δ:10.41(1H,s,H-20),2.61(1H,d,J= 12.7 Hz,H-1),1.34(3H,s,H-17),0.92(3H,s,H-18),0.76(3H,s,H-19),0.58(1H,t,J= 13.0 Hz,H-1);13C NMR(150 MHz,CDCl3)δ:208.0(C-20),79.6(C-16),58.5(C-9),56.0(C-15),55.5(C-5),54.1(C-10),48.7(C-13),45.0(C-8),41.6(C-3),41.0(C-14),40.1(C-7),34.7(C-1),33.6(C-4),31.9(C-18),24.4(C-12),24.0(C-17),20.7(C-19),19.7(C-6),19.1(C-2),17.6(C-11)。以上波谱数据与文献[23]报道的数据一致,故鉴定化合物19为fischericin D。
化合物20白色无定形粉末;分子式C20H32O。1H NMR(600 MHz,CDCl3)δ:5.71(1H,dd,J= 17.4,10.4 Hz,H-15),5.13(1H,s,H-14),4.95(1H,dd,J= 10.4,2.0 Hz,H-16),4.90(1H,dd,J= 17.3,2.0 Hz,H-16),3.83(1H,d,J= 10.8 Hz,H-19),3.43(1H,d,J= 10.8 Hz,H-19),2.32(1H,ddd,J= 14.3,4.6,2.1 Hz,H-7),0.99(6H,s,H-17/H-18),0.70(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:147.3(C-15),138.1(C-8),128.0(C-14),112.8(C-16),65.2(C-19),55.7(C-5),51.4(C-9),39.1(C-1),38.6(C-13),38.5(C-10),38.3(C-4),36.1(C-7),35.7(C-12),35.3(C-3),29.4(C-17),27.0(C-18),22.4(C-6),19.2(C-11),18.6(C-2),15.8(C-20)。以上波谱数据与文献[24]报道的数据一致,故鉴定化合物20为ent-pimara-8(14),15-diene-19-ol。
2.2 抗炎活性评价
采用LPS诱导小鼠单核巨噬细胞的体外炎症模型,以L-NMMA作为阳性对照,对从雷公藤中分离得到的20个单体化合物进行体外抗炎活性研究,结果表明化合物2、3和20对LPS诱导NO的产生有显著的抑制作用,IC50分别为2.01、1.70和1.77 μmol/L,活性远强于L-NMMA(IC50= 24.89 μmol/L,表2),其他化合物IC50值大于50,没有显示出明显的抗炎活性。

表2 化合物2、3和20的体外抗炎活性
2.3 抗肿瘤活性评价
采用MTT法评价了化合物1~20对Hela细胞增殖的影响,结果表明只有化合物11具微弱的抗肿瘤活性,IC50值为18.41 μmol/L,其他化合物没有明显的活性(IC50>40 μmol/L)。
3 讨论与结论
本实验从雷公藤茎的乙醇提取物的乙酸乙酯萃取相中分离鉴定了20个二萜类化合物,骨架类型包括二萜醌类、松香烷型、海松烷型和对映贝壳杉烷型,其中1为新的二萜醌类化合物,化合物10、19和20为首次从雷公藤中分离得到,在以往的研究基础上,进一步丰富了雷公藤化学成分的研究内容。我们并没有分离得到具有三元环氧结构的松香烷型二萜内酯,可能是因为这类化合物主要分布在根部,其在茎中含量较低的缘故。对化合物1~20进行了体外抗炎活性和抗肿瘤活性筛选,化合物2、3和20具有显著的抗炎活性。2为C环具有对醌结构的松香烷型二萜,C环的对醌结构可能是松香烷型二萜抗炎的关键活性基团。前人的研究表明具有三元环氧结构的松香烷型二萜内酯(雷公藤甲素及其衍生物)是雷公藤中二萜类成分抗炎的主要活性成分,而本研究表明,除雷公藤甲素及其衍生物外,具有C环对醌结构的松香烷型二萜可能也是雷公藤二萜类抗炎的活性成分之一[25]。本研究的发现为我们对雷公藤抗炎物质基础的认识提供了新线索,也为以松香烷型二萜作为抗炎先导化合物的结构改造提供了思路。此外,所有的化合物均没有显示显著的抗肿瘤活性,与文献报道一致,具有三元环氧结构的松香烷型二萜内酯可能才是雷公藤抗肿瘤的关键活性成分[4]。

