芒针透刺督脉治疗卒中后中枢性疼痛疗效研究∗
贾泽坤 朋源凤 周 婷 燕练钢 江 娜 李 静 曹 奕
(安徽中医药大学第二附属医院,安徽 合肥 230061)
卒中后中枢性疼痛(CPSP)是一种严重影响脑血管疾病患者康复、生活质量的衰弱性、慢性疾病[1],可单独表现为疼痛症状或合并于肩手综合征、偏身感觉障碍、卒中后抑郁等相关疾病中。由于该病诊疗机制尚未明确,临床各种治疗方法尚处于探索阶段。有研究提示[2],卒中后损伤半球的活动可能因协同作用被破坏而受到健侧半球抑制,病变区域和大多数个体CPSP病变在功能上与前/中扣带皮层、脑岛、丘脑和下顶叶相连。一定程度上,认为不同形式的皮层刺激可能是解决半球间功能抑制的有效途径。研究显示orexin-A/OX1R信号可能通过激活下行疼痛控制系统在小鼠CPSP中发挥重要作用[3]。三环类抗抑郁药、阿片类、麻醉药、抗癫痫药物等均被报道有助于脑卒中患者的康复过程,但是多存在适用范围缺陷,运动皮质电刺激、扣带回切除、硬膜外电极植入等外科操作侵入性及并发症多等特点决定了使用受限。长期以来,中医学对于中风病临证经验丰富,针灸疗法在卒中性疾病中的作用日益显著。本文旨在采用芒针透刺督脉治疗CPSP,为临床辨治提供借鉴。
1 资料与方法
1.1 病例选择 1)诊断标准:西医诊断标准参照2009年Klit等推荐的CPSP标准[4];中医诊断依据《中风病诊断与疗效评定标准(试行)》[5];急性起病,以偏瘫、失语、偏身感觉异常甚至昏迷为主症,可有头疼、躯体痛、眩晕、饮水呛咳等兼症。2)纳入标准:符合上述诊断标准;CPSP症状疼痛部位符合神经生理学分布,与病灶契合;性别不限,年龄35~80岁;病程不限,认知功能正常,能配合芒针治疗,完成疼痛评估和相关功能评估;签署知情同意书。3)排除标准:不符合纳入标准者;排除其他原因导致的疼痛者;有严重原发性疾病或癫痫、精神病者;不能配合芒针治疗,畏针者;普瑞巴林胶囊禁忌证者;妇女妊娠、哺乳期。4)剔除标准:诊疗过程中发生严重不良事件或出现严重并发症、未及时复诊,无法完成评估、病例资料难以统计患者。
1.2 临床资料 选择2018年6月至2020年6月间安徽中医药大学第二附属医院脑病四科CPSP患者60例。按随机数字表法分为针刺组、药物组各30例。两组患者临床资料(性别、年龄、卒中类型、病程)差异无统计学意义(P>0.05)。见表1。
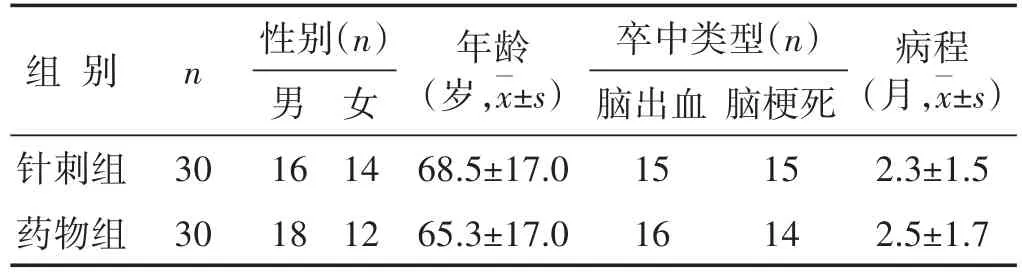
表1 两组临床资料比较
1.3 治疗方法 1)药物组:参照《中国脑卒中康复治疗指南》[6]脑卒中功能障碍和康复范畴,予卒中患者降压、控糖、调脂等基础治疗,并选择营养神经药物防治并发症及脑血管病再发。康复诊疗按照《作业治疗学》《运动疗法技术学》进行康复治疗和评定。治疗药物选用普瑞巴林胶囊[7](重庆赛维药业有限公司,国药准字H20130073,75 mg/粒)每天早1粒,口服。2)针刺组:常规诊疗基础上施以芒针疗法[8]。(1)针具:华佗牌针灸针(苏州医疗用品有限公司),直径0.16~0.45 mm、长度100~150 mm。(2)芒针取穴:取患侧百会透刺脑户、大椎透刺至阳、筋缩透刺悬枢、腰阳关透刺长强。加减选穴:患侧上肢痹痛肩髃透刺曲池、曲池透刺外关、指端麻木挛痛合谷透刺后溪。下肢痹痛血海透刺箕门、梁丘透刺伏兔、足三里透刺三阴交、丘墟透刺照海。(3)针刺操作:骨度分寸法选用芒针针具,督脉经穴选用4寸,躯干经穴穴距较大时选用5寸、6寸;患者俯卧位,施术皮肤、医者指端75%乙醇消毒,无菌操作;局部皮肤浅薄处提捏进针,皮肤厚重者舒张进针,透皮后节律进针法进针,以押手感知、辅助针刺方向,进针7~8分,可行小幅度弹、刮、捻运针手法,得气后以出现局部皮肤潮红、汗出,肌肉收缩、关节运动为度,并以患者能耐受为宜。14 d为1个疗程,共治疗2个疗程,疗程间隔1 d。
1.4 观察指标 患者治疗前后采用疼痛视觉模拟量表(VAS)评估疼痛程度,改进的Fugl-Meyer评分法评估感觉、运动功能、感觉阈值(CPT)评估疼痛感觉和疼痛阈值,日常生活能力(MRS)评价生活质量。由同一位医师在舒适、安静环境(温度25~28℃)下进行,具体方法如下。(1)VAS:评估疼痛及异常感觉(麻木、缺失、刺痛等)程度,0~10分制,分数与疼痛程度呈正比[9]。(2)改进的Fugl-Meyer评分法:感觉评定表满分42分,含浅感觉20分、本体觉16分、皮层觉6分,分数越高感觉障碍越轻。运动评定表满分100分,含运动模式、反射活动与抗拒、速度、协调等方面,分数越高运动功能越好。(3)CPT:使用北京迪美德尔科技有限公司电流阈值检测仪,手动模式进行检测,首先判断参与者是否存在刺激反应,再将电极片放置在患侧食指远端关节的内外侧,确定3个初始试探阈值(5、250、2 000 Hz),在初始阈值附近进行正弦波刺激,3个频率检测共约10 min,记录数据,定量评估感觉纤维阈值,确定在特定阈值刺激下操作及数据一致性和可重复性[10]。(4)MRS:评价卒中患者活动功能恢复程度、生活能力[11]。1.5 统计学处理 应用SPSS20.0统计软件。计量资料以()表示,在满足参数检验法基础上,两组独立样本使用t检验,率表示计数资料,比较分析选用χ2检验。P<0.05为差异有统计学意义。
2 结 果
2.1 两组治疗前后VAS、MRS评分比较 见表2。相比于治疗前,治疗后两组VAS疼痛评分均显著减少,针刺组优于药物组(P<0.05)。治疗后两组MRS评分较前均有改善,生活能力优于治疗前(P<0.05),且针刺组优于药物组(P<0.05)。
表2 两组治疗前后VAS、MRS评分比较(分±s)

表2 两组治疗前后VAS、MRS评分比较(分±s)
注:与本组治疗前比较,∗P<0.05;与药物组同时期比较,△P<0.05。下同。
组别针刺组(n=30)药物组(n=30)时间治疗前治疗后治疗前治疗后VAS积分6.48±1.39 4.35±1.41*△6.35±1.41 4.68±1.52*MRS积分3.81±1.01 2.29±0.49*△3.79±1.14 2.91±0.67*
2.2 两组治疗前后Fugl-Meyer感觉、运动障碍评分比较 见表3。治疗后两组患者Fugl-Meyer感觉、运动障碍评分均较前增加(P<0.05),针刺组显著高于药物组(P<0.05)。
表3 两组治疗前后Fugl-Meyer感觉、运动障碍评分比较(分±s)
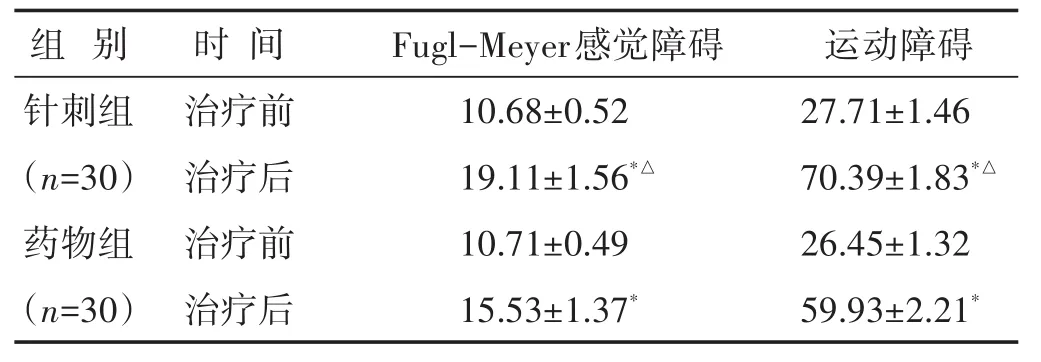
表3 两组治疗前后Fugl-Meyer感觉、运动障碍评分比较(分±s)
组别针刺组(n=30)药物组(n=30)时间治疗前治疗后治疗前治疗后Fugl-Meyer感觉障碍10.68±0.52 19.11±1.56*△10.71±0.49 15.53±1.37*运动障碍27.71±1.46 70.39±1.83*△26.45±1.32 59.93±2.21*
2.3 两组治疗前后CPT评分比较 见表4。与治疗前相比,针刺组CPT数据下降明显(P<0.05),药物组与治疗前相比无显著性差异(P>0.05),针刺组CPT各初始阈值频率数据均显著低于药物组(P<0.05)。
表4 两组治疗前后CPT评分比较(分±s)
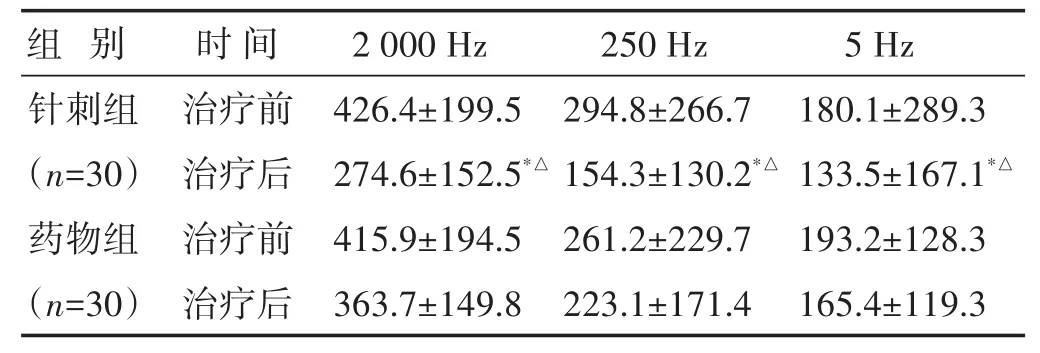
表4 两组治疗前后CPT评分比较(分±s)
组别针刺组(n=30)药物组(n=30)时间治疗前治疗后治疗前治疗后2 000 Hz 426.4±199.5 274.6±152.5*△415.9±194.5 363.7±149.8 250 Hz 294.8±266.7 154.3±130.2*△261.2±229.7 223.1±171.4 5 Hz 180.1±289.3 133.5±167.1*△193.2±128.3 165.4±119.3
3 讨 论
CPSP继发于卒中后躯体感觉通路障碍,神经病变疼痛区域可能涉及前额皮质、腹膜前结节皮层、杏仁核、海马、腹膜灰色、腹膜、神经基质及其连接等区域。触觉痛作为无害的触觉刺激被认为是痛苦的,却未得到足够的重视,往往被忽视在卒中后其他疾病诊断中,延后了对本病的诊断和治疗研究进展。日本学者长板和明在一项基于丘脑病变的非人类灵长类动物(猕猴)CPSP模型研究中发现,动物行为变化与触觉痛觉发生一致[12]。丘脑损伤后观察到行为改变时,刺激显著激活疼痛相关脑区,包括后岛叶皮层、前扣带皮层、次级躯体感觉皮层和杏仁核,其结果表明皮质活动的增加在CPSP诱导的异位痛中发挥了作用。硬膜外脑刺激(EBS)、颅磁刺激(TMS)和颅内直流刺激(tDCS)的初级运动皮层(M1)脑刺激已被探索为CPP的潜在疗法,这些技术已经证明了可变的临床疗效。美国波士顿大学医学院脑动力学实验室生成了MRI引导的有限元模型,研究了不同模型之间刺激电流密度分布的幅度、方向和最大位置的变化,结果提示中风区域组织特性改变可能会影响刺激诱导镇痛作用和(或)导致在CPSP脑刺激治疗期间发生高度可变的结果,这种脑组织电导率差异限制了这些技术的功效。在规划刺激治疗时,应考虑相对电流-神经元结构,尤其是使用TMS预测EBS响应等跨技术的使用[13]。由大脑中异常或过度的神经元活动引起的疼痛研究中发现神经病理性疼痛和癫痫的实验模型存在许多相似的病理生理现象[14]。临床上,针对神经病理性疼痛,普瑞巴林和加巴喷丁被指南推荐为治疗的一线药物[15]。药物机制在于抑制依赖性钙通道的α2-σ亚基蛋白,减少兴奋性神经递质的释放,降低神经元兴奋性,增加膜稳定性,从而减少神经元异常放电。临床病例也曾报道一例难治性CPSP患者在超声波指导下每天接受2 mL 2%利多卡因的注射,以阻止硬质结节,疼痛在强度和频率上迅速消退[16]。然而在复杂通路调节失常以及多途径损伤干扰下,针对性疗法和药物使用尚存在局限性和不确定性。
本病属中医学“偏枯”“麻痹”“顽厚”范畴,病机关键为不荣或不通致气血无法正常运达肌表,肌肤失于煦濡。督脉为阳脉之海,起于下极俞,沿脊背至风府,入脑上巅,调节一身阳气,联络机体气机的上下运动。督脉与中枢神经系统皮质脊髓束走行上同向同行,皮质脊髓束约束、支配躯干,接受刺激、传导运动功能,施针于督脉可接受全身各处的传入信息,反馈于脑,通过与皮质脊髓束的特殊对应关系来恢复机体机能,促进、协调运动性传出,或储存于中枢神经系统内,有助于学习、记忆神经基础的形成[17]。谷诗浓等[18]从细胞自噬角度探讨针刺干预缺血再灌注大鼠模型蛋白Beclin-1表达对神经功能缺失的影响,实验结果显示“通督调神”针刺可通过干预自噬蛋白复合体的合成影响自噬体膜的结合形成过程,实现对脑组织自噬水平的调控,减少细胞坏死范围,保护神经功能。从督脉经、穴论证、治疗卒中及其后遗症的临床疗效得到了确切而广泛的认可。
芒针源于古九针之长针,针长刺深,一针多透,刺激性强,尤其适用人体局部平坦、肌肉丰厚之处,透刺督脉可激发六阳经经气,又可振奋腰脊肾府元阳,络诸经摄御一身阳气、卫外邪于体表;亦可转输阴精于脏腑,协调一身阴阳,使机体得温煦而濡养,官窍通而痛止。有研究表明芒针透刺背部腧穴可刺激位于脊柱两侧的竖脊肌,维持躯干的稳定性,强化躯干肌来恢复平衡[19]。竖脊肌位于脊柱两侧,为督脉之别,包含浅层和深层肌群,为胚胎层向背侧卷曲发育形成。芒针透刺督脉经别夹脊穴及背腧穴,贯通脊、腰、项阴阳,扶阳补虚以壮腰脊,调阴泄实可止挛痛。芒针针法作为中医针灸学特种针法,虽难于操作,但适用性广,尤其善于深留久痹。本文通信作者曹奕为安徽省名中医,长期致力于针刺防治脑血管疾病,基于督脉“督一身阳气”“从巅入脑”理论基础,在临床和实验上不断深耕督脉论治在卒中性疾病中的应用[20-21]。本研究发挥芒针特点,结合现代医学神经生理学、解剖学理论,研究芒针透刺督脉可通过局部通络止痛作用和调节脊神经神经刺激感传,协调大脑功能,对于中枢神经系统起到反馈、调节作用,以改善卒中后中枢性神经痛临床症状。
目前,CPSP是脑卒中最未得到承认的后果之一,包括中风后中枢性疼痛、复杂的区域疼痛综合征,兼有神经激惹、缺失两种模式,制定有效的治疗策略具有紧迫性。本研究采用VAS评估疼痛程度,改进的Fugl-Meyer评分法评估感觉、运动功能、CPT评估疼痛感觉和疼痛阈值,MRS评价生活质量,旨在多角度评估芒针透刺督脉穴位对CPSP的综合疗效,较一般检测评价全面而准确度高,能够为进一步临床研究论治提供基础。

