MR FLAIR与1H-MRS对颞叶癫痫致痫灶定侧的价值
付丽媛,梁永刚,王晓阳,陈佳敏,李丹菲,肖慧,许尚文,陈自谦
联勤保障部队第900医院 放射诊断科,福建 福州 350025
引言
癫痫是一种难治性中枢神经系统疾病,在全球有超过5000万癫痫患者,在我国有超过900万患者。在这些患者中,约70%为颞叶癫痫(Temporal Lobe Epilepsy,TLE),大多数为药物难治性癫痫[1]。手术切除癫痫灶能够使一半以上的患者癫痫发作得到更好的控制或治愈,可以显著改善患者的预后,但是如何科学、准确、合理的定位TLE致痫灶是手术成功与否的关键。目前,有多种技术用于TLE致痫灶定侧定位诊断[2‐5]。磁共振成像(Magnetic Resonance Imaging,MRI)由于其多参数成像、组织分辨率高、无电离辐射等优点成为TLE患者术前致痫灶定侧常用的检查方法之一,它不仅能够显示结构变化,同时其磁共振波谱成像可以从生化代谢方面做出病变诊断[6]。液体衰减反转恢复序列(Fluid Attenuated Inversion Recovery,FLAIR)能基本满足诊断需要,是一个应用于海马硬化诊断的传统序列[7‐8]。如果要提高诊断效能就需要使用其他方法进行弥补。MR波谱成像技术(Magnetic Resonance Spectroscopy,1H‐MRS)是目前唯一无创活体显示组织代谢的影像学检查方法,能早期从分子水平反映癫痫灶细胞生化和代谢状态的改变。因此,本研究主要采用MRI FLAIR及1H‐MRS对TLE致痫灶进行定侧,评价它们在TLE患者致痫灶定侧中的效能与应用价值。
1 材料与方法
1.1 研究对象
选取2017年12月至2020年6月经我院癫痫中心确诊的难治性颞叶癫痫且接受手术治疗患者20例,其中男10例,女10例;年龄16~51岁,平均年龄(33.05±10.16)岁;病程3~40年,平均病程12.25年。所有患者临床资料完整,术前均进行常规MRI平扫及1H‐MRS扫描,所有患者无其他系统疾病且能耐受MR检查。纳入标准:① 患者临床资料完整且确诊为难治性颞叶癫痫的患者;② 患者及家属同意并能配合完成检查;③ 术后随访疗效显著,且均有病理结果证实。排除标准:① 非药物难治性颞叶癫痫;② 患者不能耐受MRI检查;③ 继发性癫痫;④ 有严重的神经内、外科及精神类疾病;⑤ 有严重的其他系统疾病。
同时,选取正常健康志愿者19例为正常对照组,其中男9例,女10例,年龄20~52岁,平均年龄(34.79±11.03)岁,均行MRI平扫及1H‐MRS检查。所有被试者均对检查知情同意,且经医院伦理委员会批准。
1.2 检查方法
(1)MRI平扫:采用西门子Trio 3.0 T MR,12通道颅脑相控阵线圈。所有受试者均行常规头颅轴位T1WI、T2WI、FLAIR序列,以排除受试者患有脑梗塞、脑萎缩、脑肿瘤等其他脑部疾病。海马扫描采用平行与垂直于海马长轴的斜轴与斜冠状位FLAIR序列,FLAIR序列参数为:TR=8000 ms,TE=90 ms,TI=2000 ms,层厚=2 mm,层间距=0.2 mm。
(2)1H‐MRS扫描:首先进行全脑矢状面三维磁化准备快速梯度回波(3D Magnetization Prepared Rapid gradient Echo imaging,MP‐RAGE)T1加权成像扫描,序列参数:TR=1900 ms,TE=2.5 ms,FOV=240 mm×240 mm,层厚=1.0 mm,层间距=0,扫描层数176层,翻转角=9°,矩阵=256×256。扫描完毕后以海马为目标,重建出轴位及斜冠状位,用于1H‐MRS扫描定位。感兴趣区应包含双侧海马,视野一般设定为感兴趣区的2倍,添加预饱和带,扫描前手动匀场,待半高宽≤25 Hz进行1H‐MRS扫描。MRS采用多体素3D化学位移成像技术,扫描参数为TR=1700 ms,TE=30 ms,激励采集次数为3次,接收带宽1200 Hz/Pixel,体素大小约8 mm×8 mm×8 mm。
1.3 图像处理及数据分析
(1)FLAIR图像分析:由两位主治以上影像科医师在工作站分析平行与垂直于海马长轴的斜轴与斜冠状位FLAIR图像,主要观察双侧海马大小、形态、信号等,如果发现海马信号比对侧增高,海马体积比对侧缩小、海马头部浅沟消失、侧脑室颞角比对侧增大等异常改变中的两条及两条以上异常改变,则判定为患侧[9]。
(2)1H‐MRS处理与分析:将扫描得到的数据发送到工作站后采用MRS专用后处理软件对其进行规范化后处理,以谷氨酸(Glutamate,Glu)和肌酸(Creatine,Cr)为研究目标,测量所有被试的双侧海马Glu/Cr比值,绘制受试者工作特性曲线(Receiver Operating Characteristic Curve,ROC)得出诊断临界值,将Glu/Cr值较大且高于临界值的一侧定义为患侧,双侧Glu/Cr比值均低于临界值则为阴性患者[10‐11]。
1.4 统计学分析
采用SPSS 21.0软件进行统计学分析,以病理结果为参考,分别计算出FLAIR、MRS、FLAIR联合MRS对TLE致痫灶定侧定位的敏感性、特异性、准确性及诊断效能。
2 结果
2.1 FLAIR图像信号特征及诊断效能
19名正常对照组常规MRI及FLAIR表现为双侧海马信号均匀一致,结构完整,大小均一致,未见明显的萎缩,在FLAIR序列上双侧海马信号均未见明显增高。20例患者均进行了手术治疗,术后临床症状明显缓解或者消失,术后病理显示海马硬化伴胶质增生,神经元细胞有不同程度的变性、减少或缺失。本组患者中有17例患者MRI FLAIR表现为海马体积较对侧缩小、信号增高、海马头部浅沟消失、侧脑室颞角较对侧扩大等异常改变中的两条及两条以上异常改变,可准确进行定侧定位,另有3例患者FLAIR图像上未见明显异常,采用其他技术定侧后,术后最终病理均为海马硬化。FLAIR序列定侧诊断的灵敏度、特异度、准确度分别为85%、94.7%、89.7%。对其诊断效能行ROC曲线评价,曲线下面积为0.899。
2.2 MRS诊断效能
通过ROC曲线所获得的MRS Glu/Cr的临界值为2.12,将Glu/Cr比值高于2.12认为其为患侧,20例TLE患者中,15例患者定侧结果与病理诊断符合,5例患者出现两侧海马Glu/Cr比值均小于2.12,经其他技术定侧后手术,术后支持海马硬化。MRS Glu/Cr定侧诊断的灵敏度、特异度、准确度分别为75%、94.7%、84.6%。对其诊断效能行ROC曲线评价,曲线下面积为0.871。
2.3 FLAIR联合MRS诊断效能
将FLAIR与MRS联合对TLE患者致痫灶进行综合定位,以两者中任意一个为阳性则定义为阳性,当两种方法定侧结果相反时以FLAIR为准。20例患者中,19例患者定侧结果与病理诊断相符合(图1),有1例患者FLAIR及MRS均为阴性,经过其他技术定侧后手术,术后支持海马硬化。两者联合定侧诊断灵敏度、特异度、准确度分别为95%、94.7%、94.87%。对其诊断效能行ROC曲线评价,曲线下面积为0.949(表1,图2)。
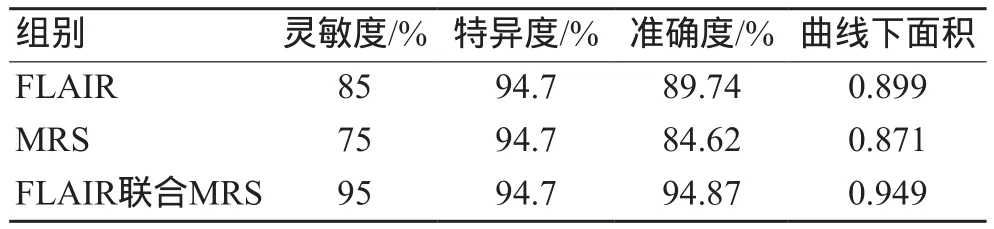
表1 FLAIR、MRS及两者联合诊断效能评价
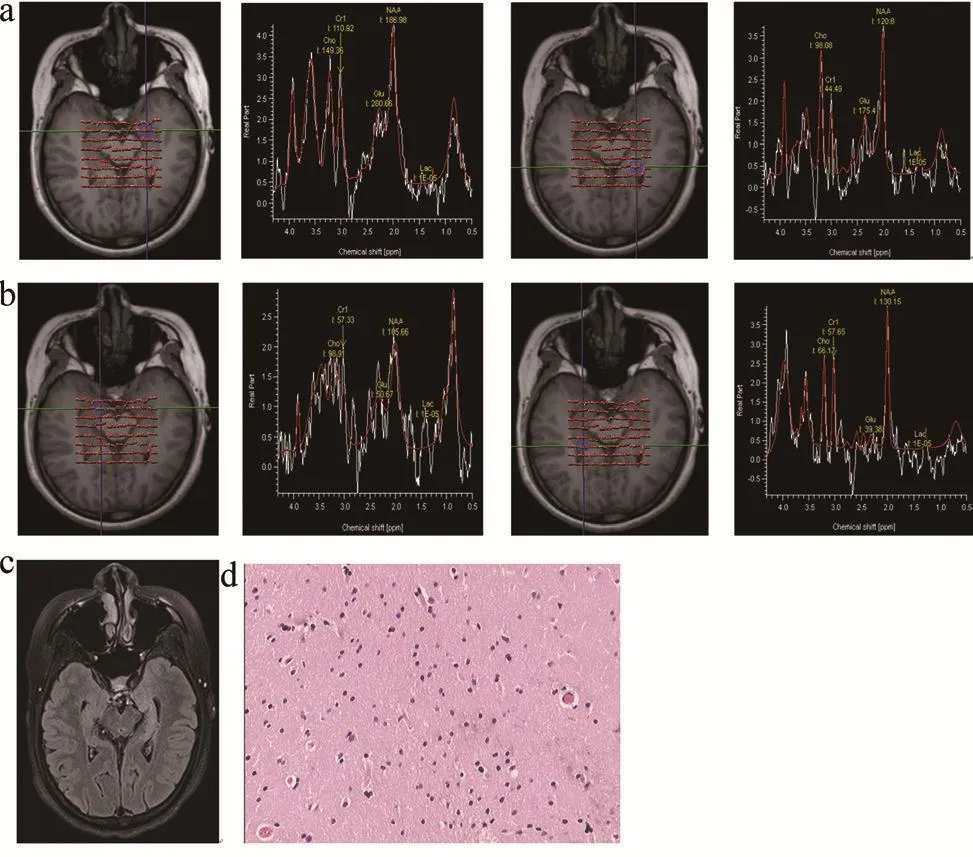
图1 左侧颞叶癫痫患者MRS、FLAIR及病理图像
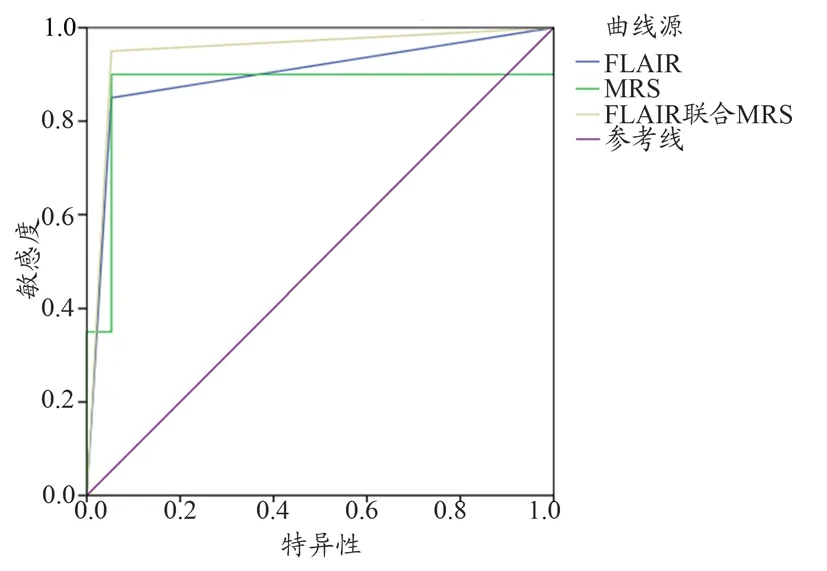
图2 FLAIR、MRS及两者联合诊断ROC曲线
3 讨论
癫痫是一种常见的神经系统疾病,它具有反复发作,高致残率和治愈困难的特点,且需要终生服药,给患者及其家人带来沉重的经济负担和身心痛苦[12‐15]。大多数癫痫可以通过药物控制,但仍有约1/3的患者药物治疗无效,对于此部分患者,如若通过影像学技术精准定位,早期手术可显著改善患者预后[1]。MRI是TLE患者致痫灶定侧的常用方法之一,MRI不但可以提供结构变化的依据,同时其功能成像能对其生化代谢进行测量,从而为定侧提供依据。
FLAIR序列是目前应用较多的用于TLE患者致痫灶定侧的方法之一,该序列具有信噪比高、扫描时间合理、病人可耐受及图像质量好的优点,可以显示患者海马体积、结构、信号等特征性的改变[16]。该序列抑制了表现为高信号的脑脊液信号,而其他脑组织仍保持T2WI的特点,这样就增加了病灶与背景的对比度,更有利于发现病灶[17]。本组20名患者中,17例患者存在海马体积较对侧不同程度缩小、侧脑室颞角较对侧扩大、信号增高、结构改变等特征,且术后得到了证实。另外3例经病理证实为海马硬化,但在FLAIR序列上没有明显变化,这是因为肉眼观察有所限制所导致的。研究结果表明,FLAIR序列有较好地诊断效能,基本满足诊断需要,如果要提高诊断的准确度就需要提高图像分辨率或者使用其他方法进行弥补。
MRS也被越来越多的应用于TLE患者致痫灶定侧。在过去的研究中,主要代谢物为N‐乙酰天门冬氨酸、Cr和胆碱,通过测定其含量或者比值,从而为致痫灶的定侧定位诊断提供有价值的信息[18]。除了以上常用代谢产物,其他一些代谢物目前也慢慢成为研究的热点,比如Glu。Glu是一种兴奋性神经递质,它在大脑中的代谢转化主要依靠星形胶质细胞,海马硬化后,星形胶质细胞增殖,增殖细胞不能发挥正常的细胞功能,它表达谷氨酸合成酶和谷氨酸脱氢酶的活性显著降低,这导致细胞外Glu的清除率显著降低,从而导致Glu聚集。有研究发现,癫痫患者的Glu含量是正常人水平的5倍[19‐21]。MRS可对Glu的浓度进行检测,从而用于TLE患者致痫灶的定侧研究。本研究20例患者中,有15例患者一侧海马Glu峰升高,术后病理证实为海马硬化。5例Glu阴性患者术后病理证实均为海马硬化,误诊的原因可能与MRS后处理时感兴趣区的选择有关,从而造成假阴性。将FLAIR与MRS两者联合进行诊断,有助于提高其诊断灵敏度、准确度及诊断效能。这说明MR成像技术单一使用,是有其局限性的,在这种情况下,联合两种成像技术对颞叶癫痫致痫灶进行综合定侧定位,可充分发挥各种影像技术的优越性,实现优势互补[22‐24]。
本研究的局限性在于:① 样本量较小,可能会对结果造成偏倚,在后续研究中需要加大样本量;② 1H‐MRS检查容易受到多种因素的影响,可能会对结果也有影响,需要在检查中做好质控。

