牙源性钙化上皮瘤1例临床病理分析及文献复习
张艳宁 侯亚丽 于美清 宋鹏 郝亚丽 李荷香
050017石家庄,河北医科大学口腔医学院·口腔医院1.病理科,2.放射科,河北省口腔医学重点实验室,河北省口腔疾病临床医学研究中心
牙源性钙化上皮瘤(calcifying epithelial odontogenic tumor,CEOT)又称Pindborg瘤,为少见的良性牙源性上皮性肿瘤[1],有局部浸润性。术后复发率约12.6%[2],有恶变报道[3]。其独特的组织学表现可能将其误诊为低分化癌,因而备受重视。
1 资料与方法
1.1 基本资料
患者,女,45岁,因上颌骨肿物5个月入院。
1.2 临床检查
面部基本对称,张口度、开口型未见异常。12~14区腭侧可见坑状凹陷,15~16区腭侧可见膨隆,14~16区牙龈红肿,压痛明显。曲面断层片可见15~22区不规则骨质破坏区,界清,牙根均有吸收(图1)。CBCT显示唇(颊)、腭侧骨壁部分破坏(图1)。

图1 曲面断层及CBCT
1.3 检查结果
囊/实性肿物,质脆,易出血,与腭侧软组织粘连。
1.4 病理检查
灰白色不规则软组织3块,最大者约2.0 cm×2.0 cm×0.5 cm。镜下检查:肿瘤上皮细胞胞浆红染或透明,排列成团块或小条索,分布于疏松纤维结缔组织中。可见大量圆形、均质红染的淀粉样物质(图2),刚果红染色呈砖红色阳性(图3)。间质有少量炎细胞。免疫组化显示:CK14、CK17均表达阳性(图 4~5)。

图2 HE染色
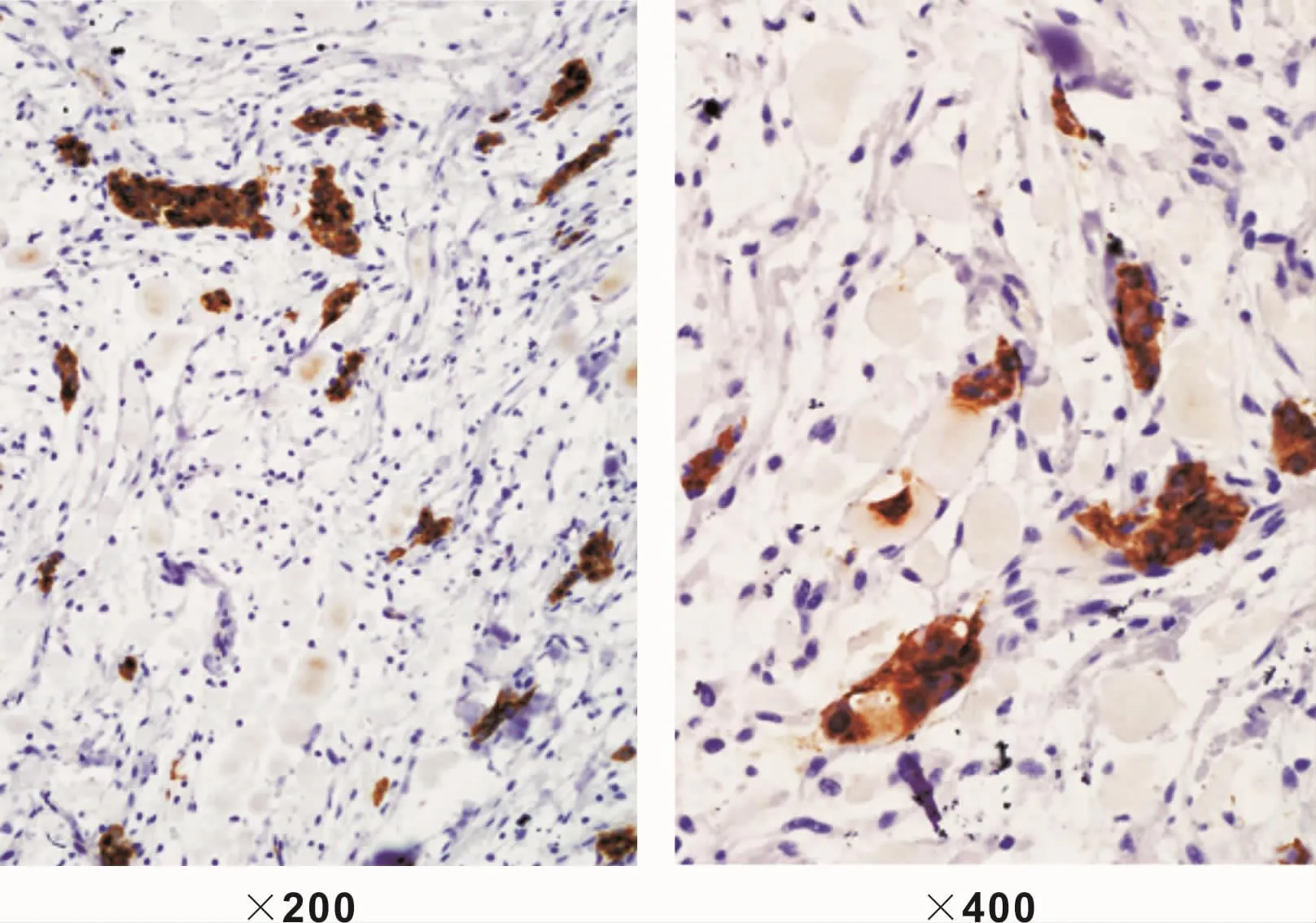
图4 抗CK14免疫组织化学染色CK14表达阳性
1.5 病理诊断
牙源性钙化上皮瘤。
2 讨 论
2.1 CEOT的病理表现
典型病理表现:镜下肿瘤由多边形上皮细胞组成,并见清晰的细胞间桥。纤维性间质常见退变。上皮细胞排列呈片状或岛状,偶成筛孔状。瘤细胞与胞核多形性明显,有淀粉样物质,常发生钙化[4],呈同心圆沉积。
Liu等[5]将CEOT分为四种类型:第一型,由片状或巢状多面体上皮细胞和纤维间质组成,细胞轮廓和细胞间桥明显。细胞有异形性,但没有分裂像。间质可退变,可见钙化;第二型,肿瘤上皮细胞排列成筛孔状,筛孔内可见红染均质物;第三型,肿瘤上皮细胞散在或密集分布,细胞多形性、胞核异形性明显。间质内含黏液,富含血管、红染均质钙化物;第四型,肿瘤上皮细胞排列成巢状或条索状,部分胞浆红染,部分胞浆透明。间质由致密纤维组成,可见红染均质物质。
2.2 CEOT的组织病理学变异型
CEOT有较多的组织学变异型,如无钙化型、透明细胞型、朗格汉斯细胞型、色素型、恶性型及囊性变异等。
其中报道较多的有:透明细胞型牙源性钙化上皮瘤(Clear-cell variant of calcifying epithelial odontogenic tumor):在典型的CEOT组织学背景上,间杂有胞浆透明或空泡状、边界清楚的上皮细胞。胞核大小变化不大,少数呈空泡状,胞浆含有糖原。朗格汉斯细胞型牙源性钙化上皮瘤(Langerhans cell-containing calcifying epithelial odontogenic tumor):以小条索或巢状结构为主,可见较多透明细胞,胞浆含有 Birbeck颗粒[6],极少发生钙化。CDla、CD68、HLA-DR、S-100等在瘤细胞中均有表达。牙源性上皮性联合瘤(combined epithelialod ontogenic tumor):由牙源性腺样瘤和CEOT共同构成[7],但有学者并不认为这是两种肿瘤的复合或两个不同/独立的疾病,亦或是牙源性腺样瘤的病变之一[8]。
2.3 鉴别诊断
2.3.1 颌骨原发性或转移性鳞状细胞癌 其具有鳞状细胞癌的一般特点,肿瘤细胞有多形性,细胞间桥明显。但CEOT核分裂像少见,且有特征性的淀粉样物质。
2.3.2 牙源性透明细胞癌 此瘤不含有钙化物。
2.3.3 唾液腺恶性肿瘤 尤其是透明细胞型牙源性钙化上皮瘤需要与含透明细胞的唾液腺恶性肿瘤相鉴别。后者免疫组化Actin、S-100阳性,而前者细胞缺乏异型性,并有淀粉样物质。
综上所述,CEOT病理表现多样,但又较为少见,目前还需要更多的临床病理资料来完善对其认识。

