2型糖尿病患者尿微量白蛋白与外周动脉疾病的相关性
谢沂均
广州市第一人民医院内分泌内科,广东广州 510080
目前全球有4.63亿成年人患有糖尿病,其中1/2的糖尿病患者未被诊断[1]。2型糖尿病(type 2 diabetes mellitus,T2DM)发病的确切时间通常无法确定,在初次诊断2型糖尿病时,即可能合并糖尿病肾病(diabetic kidney disease,DKD),而也有部分糖尿病患者因无法愈合的下肢溃疡来医院就诊,提示糖尿病合并外周动脉病变(peripheral arterial disease,PAD)。近年来,一些非传统的危险因素,如肾功能损害成为动脉粥样硬化临床研究的热点。糖尿病患者合并DKD后,心血管风险显著升高[2]。研究表明,慢性肾脏病(chronic kidney disease,CKD)对PAD患者的发病率、病死率及医疗费用有极大影响[3]。该研究选取广州市第一人民医院内分泌内科2018年9月—2020年7月的T2DM患者468例,通过评估T2DM合并PAD患者糖尿病肾病进展,检测尿微量白蛋白水平,分析尿微量白蛋白与PAD的相关性,旨在更深入地了解糖尿病患者微血管病变与大血管病变的关系,为T2DM患者早期诊断及预测PAD提供理论依据,现报道如下。
1 对象与方法
1.1 研究对象
回顾性选取于广州市第一人民医院内分泌内科住院治疗的T2DM患者468例,其中男248例,女220例。纳入标准:①年龄在18~80岁;②2型糖尿病符合《中国2型糖尿病防治指南》中的相关诊断标准;③无足溃疡、坏疽及足部感染。排除标准:①其他类型糖尿病;②既往接受下肢手术;③有糖尿病急性并发症;④严重心、脑血管疾病;⑤严重肝、肾功能不全。根据尿微量白蛋白排泄率分为无蛋白尿组(normal albuminuria,N组,165例)、微量白蛋白尿组(microalbuminuria,MICRO组,139例)、大量蛋白尿组(macro albuminuria,MACRO组,164例)。该研究经医院伦理委员会审核批准,伦理号K-2020-109-01。
1.2 方法
收集患者的年龄、性别、病程、收缩压(systolic blood pressure,SBP)、舒 张 压(diastolic blood pressure,DBP)、合并视网膜病变(diabetic retinopathy,DR),体质量指数(body mass index,BMI)。禁食10~12 h,于次日晨空腹抽取肘静脉血5 mL,室温静置约30 min,3 000 r离心10 min,提取血清,-80℃保存。采用OLYMPUS AU-5400全自动生化分析仪检测空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(postprandial plasma glucose,PPG)、空腹C肽(C-peptide,Cpep)、餐后2 hC肽(2 hCpep)、血肌酐(creatinine,CR)、糖化血红蛋白(glycosylated hemoglobin,HbA1c)、谷 丙 转 氨 酶(alanine aminotransferase,ALT)、三 酰 甘 油(triglyceride,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、白蛋白(albumin,ALB)等,计算肾小球滤过率(estimated glomerular filtration rate,eGFR)。固定专人操作,美国GE LOGIQ E9型彩色超声诊断仪检查下肢血管,观察管腔内膜中层厚度有无增厚、斑块、狭窄形成,检测部位为双侧股总动脉、股浅动脉、胫(前)后动脉、足背动脉。根据下肢动脉彩超进行外周动脉疾病的动脉硬化闭塞分级[4]。见表1。

表1 外周动脉硬化闭塞分级标准
1.3 统计方法
采用SPSS 26.0统计学软件进行数据分析。正态分布计量资料以(±s)表示,两组间比较采用t检验,多组间比较采用单因素方差分析,计数资料以[n(%)]表示,采用χ2检验。偏相关分析T2DM患者下肢血管病变分级与各指标的相关性。以P<0.05或P<0.01为差异有统计学意义。
2 结果
2.1 研究对象的一般资料
结果显示,MACRO组、MICRO组与N组3组间的性 别、DBP、BMI、PPG、2 hCpep、ALT、TG、TC、LDL-C、HbA1c的差异无统计学意义(P>0.05)。与另两组相比,MACRO组的年龄更大、糖尿病病程更长、SBP、FPG、空腹Cpep均较高,同时伴有明显的肾脏损伤,eGFR较低,24 h尿蛋白定量及CR均较高。MACRO组的ALB均显著低于N组及MICRO组(P<0.05),而DR率则高于N组及MICRO组。而MICRO组的年龄、糖尿病病程、SBP、FPG、空腹Cpep、24 h尿蛋白定量及CR处于中等水平,N组的则最小。患者的基本资料见表2。
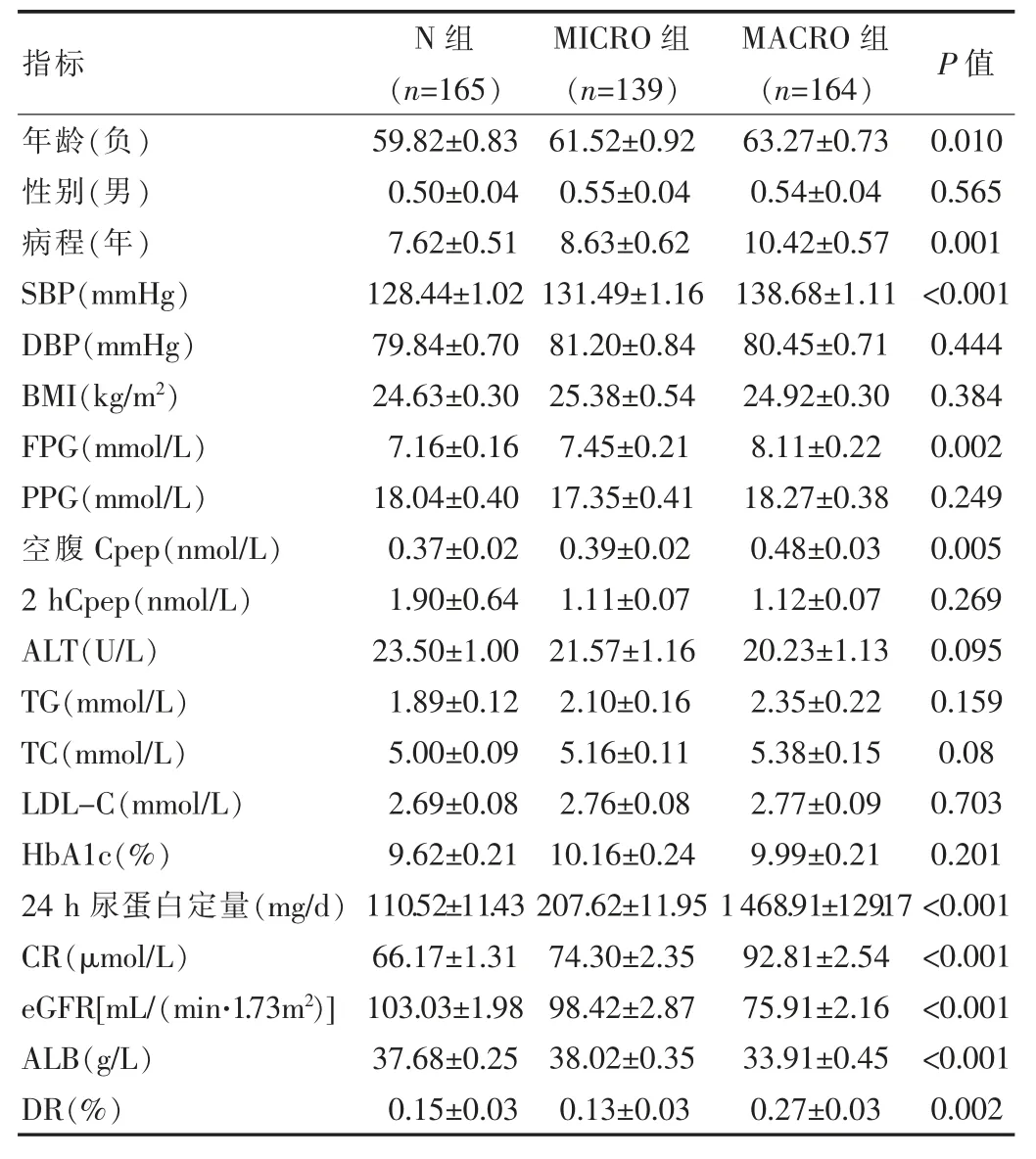
表2 研究对象的一般资料
2.2 尿微量白蛋白水平与PAD分级的关系
MACRO组的PAD分级高于MICRO组及N组,MICRO组的PAD分级高于N组,3组间差异有统计学意义(P<0.05),见表3。

表3 尿微量白蛋白与PAD分级
2.3 相关性分析
在校正其余混杂因素后,通过相关性分析显示,尿微量白蛋白排泄率与24 h尿蛋白定量、PAD分级相关关系显著,相关性密切,呈正相关(P<0.05),与TG、LDLC、TC关系较密切(P<0.05),与TG、LDL-C呈正相关,与TC呈负相关。见表4。
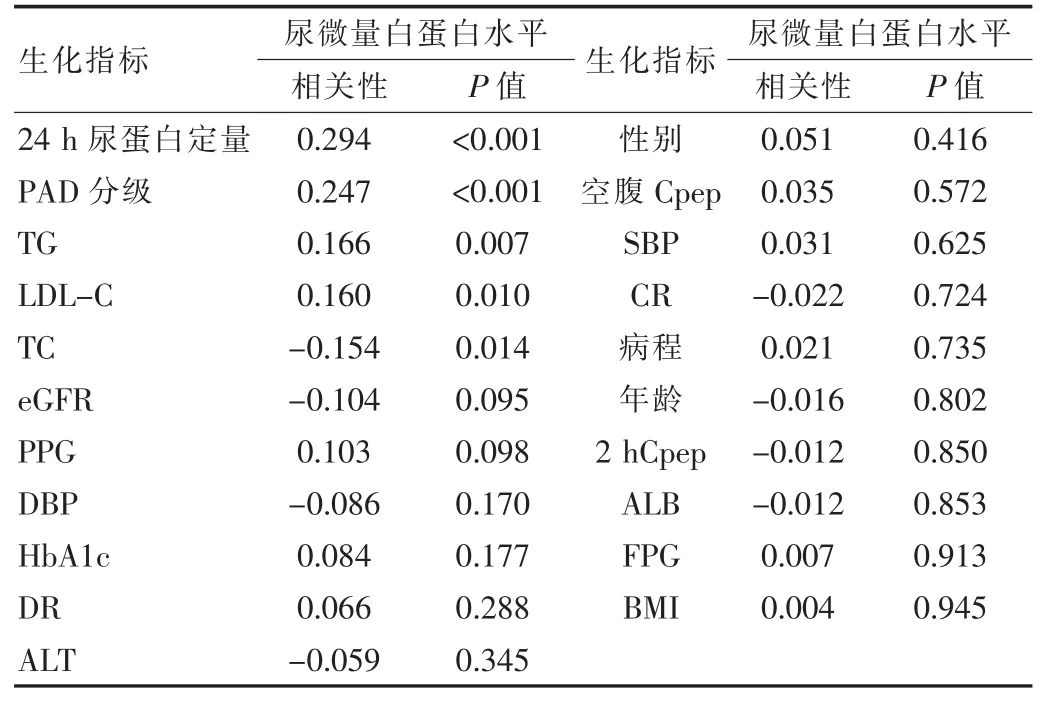
表4 相关性分析
3 讨论
在长期研究中,确诊为糖尿病20年以上的患者肾脏病变的累积发生率约为27%~60%,出现蛋白尿后10年终末期肾脏病(end stage renal disease,ESRD)的发生率约为10%~35%,伴有糖尿病的ESRD患者心血管疾病病死率更高,这可能是由于糖尿病加剧了患者动脉硬化的程度。事实上,大多数糖尿病肾病患者都合并心血管疾病。血糖升高以及糖尿病本身,通过多种机制,包括胰岛素抵抗、炎症、内皮功能障碍,以及葡萄糖对微血管的毒性作用,导致心血管疾病(cardiovascular disease,CVD)的风险增加[5]。糖尿病和慢性肾脏疾病都与CVD密切相关,控制血糖和血压可以降低相关风险。值得注意的是,多数糖尿病患者死于CVD,并非CKD[6]。与糖尿病相关的,最常见和最典型的CVD是冠心病、脑血管病、外周动脉疾病和充血性心力衰竭。外周动脉疾病(peripheral arterial disease,PAD)好发于2型糖尿病患者,并与心血管疾病密切相关,是临床上常见的糖尿病大血管并发症之一,是下肢截肢的一个重要原因。一旦出现缺血性坏疽、间歇性跛行,其治疗难度较大,不仅使患者感到生理上的痛苦,还会使患者经济负担逐渐增加。与1型糖尿病患者相比,2型糖尿病患者糖尿病足并发症的患病率更高[7]。对于糖尿病患者来讲,即使存在PAD,症状往往不典型,如缺乏间隙性跛行,静息痛;另外一方面,足溃疡的患者往往同时存在动脉钙化,足部感染,水肿和周围神经病。这些因素均导致PAD诊断比没有糖尿病的患者更具有挑战性。不到1/3的医生认识到糖尿病相关的周围神经病变的表现,即使患者有症状,而且,医疗专业人员对糖尿病足并发症的综合管理和治疗缺乏了解[1]。糖尿病合并PAD预后较差,比多数恶性肿瘤的5年病死率还要高,接近于50%,进一步,糖尿病合并PAD的截肢患者2年内病死率即达50%。显而易见,全面诊治合并糖尿病的PAD患者至关重要。
如今,有关PAD的大多数研究都将踝肱指数(ankle brachial index,ABI)评估作为筛选测试。该测量是简单、无创、无风险且廉价,正常ABI介于1~1.3[8]之间,0.91~0.99可接受,ABI低于0.9表示存在PAD。ABI具有较高的敏感性和特异性,但不能对所有类型的患者都达到如此高的准确率。老年人、糖尿病患者或肾病患者的动脉通常钙化,且大部分存在血管硬化,导致此类病例的敏感性较差[9],对于一组患有PAD的患者,ABI似乎正常(1~1.3)甚至是超常(高于1.3)[9]。同时ABI仅在存在能够降低踝部收缩压的晚期动脉病变的情况下才导致异常,因此下肢的早期动脉粥样硬化病变不能通过ABI测量来检测[10]。该研究拟评估合并或不合并尿蛋白的糖尿病患者中发生PAD的风险,考虑在糖尿病患者或动脉钙化的老年人中,ABI敏感性较低,容易出现假阴性,故对于PAD的早期识别,使用超声作为无创影像学评估。血管彩超可以很好测量内中膜厚度、斑块大小、明确斑块性质,结合彩色多普勒成像及频谱多普勒可以诊断动脉狭窄或闭塞的部位和程度。超声检查目前在临床上作为筛查首选的检查方法,可准确诊断病变部位及程度。一项研究比较了彩色多普勒成像和血管造影在51例患者的100条腿上的闭塞和狭窄,闭塞检测的敏感性为95%,特异性为99%;狭窄检测的敏感性为92%,特异性为97%[9]。总体来说,虽然ABI作为辅助诊断的初始临床试验是有用的,但ABI无法确定动脉狭窄或闭塞的位置。而血管超声用于确定解剖、血流动力学和病变形态,被认为是诊断外周动脉疾病、揭示动脉闭塞和狭窄的金标准和非常有力的工具[10]。
CKD患者发生心血管事件的绝对风险与已有冠心病患者相似,而ESKD患者透析时发生心血管事件和死亡的风险是普通人群的40~50倍[11]。慢性肾脏疾病导致截肢率高1.8倍,且随着慢性肾脏疾病阶段的增加而逐步增加。慢性肾脏病使外周血管疾病患者的院内病死率增加,随着慢性肾脏病分期升高,风险逐步增加。 慢性肾脏病4期和Fontaine IV期并存的患者的院内病死率最高。与整个PAD队列相比,慢性肾脏疾病导致费用增加15%,住院时间增加21%。提示CKD对PAD住院患者的发病率、院内病死率、截肢、住院时间长短和报销费用的阶段性影响[12]。
糖尿病肾病的发生对糖尿病下肢血管病变有早期预警作用,风险的增加是多因素的,包括晚期肾功能衰竭与胰岛素抵抗、高血压、血脂异常[13]、血管钙化[14]、慢性炎症、蛋白质能量消耗和缺乏规律运动[15]等,有研究表明[16],大量蛋白尿可能是动脉硬化的早期指标。微量白蛋白尿作为糖尿病肾损害最早期、最敏感的指标之一,已被证实其出现可能提示T2DM患者存在全身广泛的内皮细胞功能紊乱,包括全身的大动脉。既往研究证实[17],在糖尿病受试者中,合并白蛋白尿的患者患PAD风险是没有蛋白尿的1.90倍,但并没有对蛋白尿的程度进一步研究,同时,对于非糖尿病受试者,白蛋白尿的程度与PAD无关。一项研究表明[18],大量蛋白尿的患者空腹血糖、尿素氮、肌酐、收缩压均大于无蛋白尿及微量蛋白尿的患者,下肢动脉病变发生率也明显较高,但该研究针对下肢病变的调查主要采用问卷法,客观性不足。中国台湾的一项研究发现,在年龄超过50岁的2型糖尿病人群中,蛋白尿比eGFR<60 mL/min/1.73 m2更能说明周围动脉疾病[19]。该研究中共采集了468例2型糖尿病患者的生化指标,其中分为无蛋白尿组、微量白蛋白尿急大量蛋白尿组,通过下肢动脉彩超评估下肢动脉硬化的程度,在调整了潜在的混杂因素后,发现2型糖尿病合并大量蛋白尿的患者动脉硬化闭塞程度更高,印证了大量蛋白尿的2型糖尿病患者下肢动脉病变率更高这一观点。
作为糖尿病微血管和大血管并发症之一,糖尿病性肾病和周围动脉疾病均被认为是一种广泛性的内皮功能障碍,由一氧化氮的生物利用度降低引起,实际上是在微量白蛋白尿发生之前[20]。肾小球内压力升高会导致肾小球毛细血管脱落,一方面肾小球内压力进一步升高,白蛋白通过肾小球毛细血管的渗透更大另一方面。确实,在2型糖尿病患者中,存在白蛋白尿时肾小球内压较高。此外,在肾脏质量大量减少的患者,剩余的肾脏质量与尿白蛋白排泄成反比[21]。动物实验也证明蛋白尿与动脉僵硬有关,蛋白尿抑制大鼠血管的扩张性、壁应力,表现为肠系膜阻力动脉横截面积、内径和外径的减小[22]。实际上蛋白尿增多和心血管损害之间的潜在机制仍需进一步阐明。
该研究的局限性,研究对象仅源于该院内分泌内科的住院患者,可能存在一定的选择偏移。该研究采用横断面设计,不能得出确定明确的因果关系。超声检查的准确性依赖仪器及操作者的水平,因此尚有一定的局限性。期待未来更多不同人群的大样本、前瞻性研究来验证这一观点。
综上所述,尿微量白蛋白较高的2型糖尿病患者下肢动脉硬化的风险相对增加,在今后的临床随访中,通过检测尿微量白蛋白的水平,可为2型糖尿病外周动脉疾病的早期诊断提供依据。

