单侧双通道内镜技术对腰椎间盘突出合并腰椎管狭窄症患者腰椎功能的改善作用
张 腾
(徐州市贾汪区人民医院骨科,江苏 徐州 221011)
腰椎间盘突出症是指机体椎间盘向后突出而压迫神经;腰椎管狭窄症是由于腰椎管组织异常,使腰椎管的容量降低,导致椎管神经受挤压或刺激而引起的腰椎退行性疾病,其临床症状为腰部疼痛、下肢乏力、麻木、行走困难等[1]。腰椎间盘突出症与腰椎管狭窄症常合并出现,两种疾病之间相互作用、相互影响,增加疾病的复杂程度,增加临床治疗难度。传统全椎板切除术虽可以减轻患者的临床并发症状,但对患者的伤害较大,易出现腰椎不稳的并发症。单侧双通道内镜技术(UBE)是目前临床新兴的治疗手段,具有操作方便、手术视野广阔等优点,可经椎板间入路或椎间孔入路实施,成功应用于多种脊柱外科疾病的治疗[2]。本文旨在探讨UBE对腰椎间盘突出合并腰椎管狭窄症患者腰椎功能与炎症反应的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2019年6月至2020年8月徐州市贾汪区人民医院收治的50例腰椎间盘突出合并腰椎椎管狭窄症患者,根据随机数字表法分为对照组与研究组,各25例。对照组患者中男性14例,女性11例;年龄54~72岁,平均(63.47±3.25)岁。研究组患者中男性13例,女性12例;年龄53~73岁,平均(63.27±3.26)岁。两组患者一般资料对比,差异无统计学意义(P> 0.05),组间可比。诊断标准:腰椎间盘突出症符合《腰椎间盘突出症》[3]中的诊断标准,腰椎管狭窄症符合《实用骨科学》[4]中的相关标准。纳入标准:符合上述诊断标准者;存在不同程度的腰痛或下肢放射性疼痛症状者;手术前3个月经正规非手术治疗无效者;能耐受手术者等。排除标准:患有椎体滑脱或椎体骨折等其他腰椎疾病者;并发脊柱结核或腰椎肿瘤者;存在意识障碍或精神疾病者等。本研究经徐州市贾汪区人民医院医学伦理委员会审核批准,患者或家属对本研究知情同意。
1.2 方法 给予对照组患者传统全椎板切除术,患者取俯卧位,麻醉消毒后,在C型臂下透视,沿着棘突后正中线作一个长度为5~7 cm的切口,充分暴露椎板后依次清理外部组织、椎板、髓核病变组织等,摘除侧隐窝和神经根管狭窄部位,最后在C型臂下观察患者的神经根情况,若发现有松弛症状,需要压迫解除硬膜囊,完成上述操作后,留置引流管,缝合手术切口,结束手术。给予研究组患者UBE治疗,患者取俯卧位,双侧上肢向外伸展和向上举,并将双臂放在支壁板上,在腋下放入腋垫,做好全身麻醉后,C型臂透视,以责任椎间隙为中心,在左侧距中线1 cm、上下距中线10~15 cm处各作一个切口标记,在头端作一个长度为8 mm的切口作为观察通道,在尾端作一个长度为12 mm的切口作为工作通道,并且在两个通道分别置入关节镜和减压器械;沿着标记处依次切开皮肤组织,钝性分离椎板表面的软组织,置入关节镜,并调整关节镜的方向,暴露病灶部位,然后采用等离子射频刀钝性分离骨性椎板和黄韧带表面的组织,暴露关节突关节内缘;在内镜下,打开硬膜囊,暴露椎间盘,切除髓核组织,必要时可进行椎管加压处理,之后留置引流管,缝合切口。两组患者均于术后随访3个月。
1.3 观察指标 ①手术指标。记录并比较两组患者的手术时间、术中出血量和出院时间。②腰椎功能与疼痛程度。依据Oswestry功能障碍指数(ODI)[5]评价两组患者术前、术后3个月的腰椎功能,内容包括疼痛强度、坐位、步行、站立以及社会生活等项目,总分50分,分数越高,提示患者功能障碍越严重;依据腰痛评分量表(JOA)[6]评价两组患者术前、术后3个月的腰痛程度,包括主观症状(下腰痛、腿痛、步态)、临床体征(直腿抬高、感觉障碍、运动障碍)、日常活动受限度和膀胱功能4个部分,总分29分,分数越高,提示患者腰椎功能越良好;依据视觉模拟疼痛量表(VAS)[7]评价两组患者术前、术后3个月的疼痛程度,总分10分,分数越高,提示患者疼痛越剧烈。③炎性因子指标。分别采集两组患者术后即刻、 48 h的空腹静脉血约5 mL,3 000 r/min的转速离心10 min取血清,使用酶联免疫吸附法检测血清白介素-4(IL-4)、白介素-17(IL-17)及肿瘤坏死因子-α(TNF-α)水平。
1.4 统计学方法 采用SPSS 23.0统计软件分析数据,计量资料用(±s)表示,采用t检验。以P< 0.05为差异有统计学意义。
2 结果
2.1 手术指标 经比较研究组患者手术时间、住院时间均较对照组缩短,术中出血量较对照组减少,差异均具有统计学意义(均P< 0.05),见表1。
表1 两组患者手术指标比较(±s)
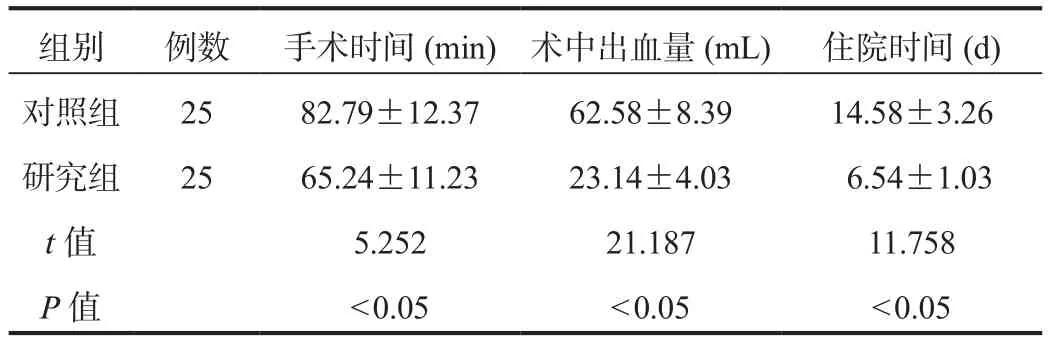
表1 两组患者手术指标比较(±s)
组别 例数 手术时间(min)术中出血量(mL) 住院时间(d)对照组 25 82.79±12.37 62.58±8.39 14.58±3.26研究组 25 65.24±11.23 23.14±4.03 6.54±1.03 t值 5.252 21.187 11.758 P值 < 0.05 < 0.05 < 0.05
2.2 腰椎功能与疼痛程度 与术前相比,术后3个月两组患者的ODI、VAS评分均下降,且研究组低于对照组;但两组患者的JOA评分均上升,且研究组高于对照组,差异均具有统计学意义(均P< 0.05),见表2。
表2 两组患者腰椎功能与疼痛程度比较(±s, 分)
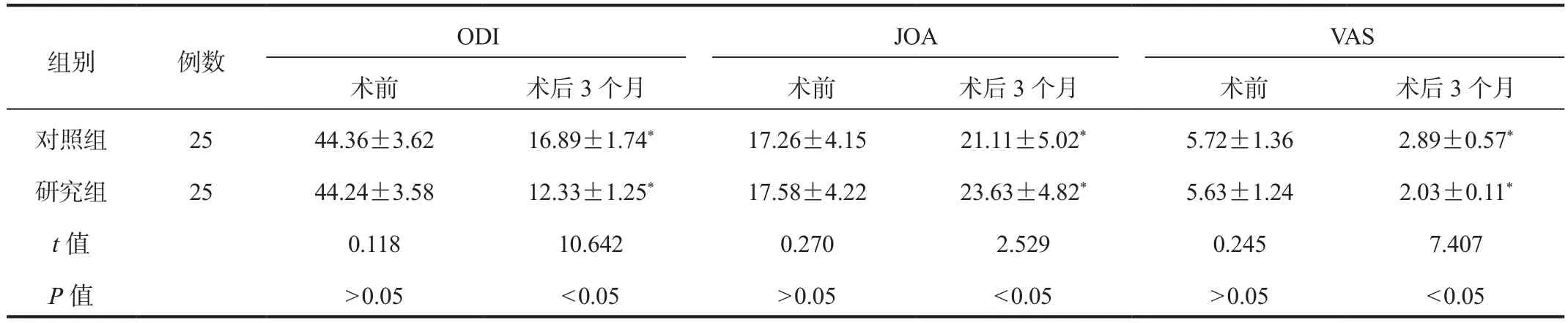
表2 两组患者腰椎功能与疼痛程度比较(±s, 分)
注:与术前比,*P < 0.05。ODI:Oswestry功能障碍指数;JOA:腰痛评分量表;VAS:视觉模拟疼痛量表。
组别 例数ODI JOA VAS术前 术后3个月 术前 术后3个月 术前 术后3个月对照组 25 44.36±3.62 16.89±1.74* 17.26±4.15 21.11±5.02* 5.72±1.36 2.89±0.57*研究组 25 44.24±3.58 12.33±1.25* 17.58±4.22 23.63±4.82* 5.63±1.24 2.03±0.11*t值 0.118 10.642 0.270 2.529 0.245 7.407 P值 > 0.05 < 0.05 > 0.05 < 0.05 > 0.05 < 0.05
2.3 炎症反应 与术后即刻相比,术后48 h两组患者血清IL-17、TNF-α均下降,且研究组低于对照组;但两组患者的血清IL-4水平均上升,且研究组高于对照组,差异均具有统计学意义(均P< 0.05),见表3。
表3 两组患者炎症因子指标比较(±s, pg/mL)
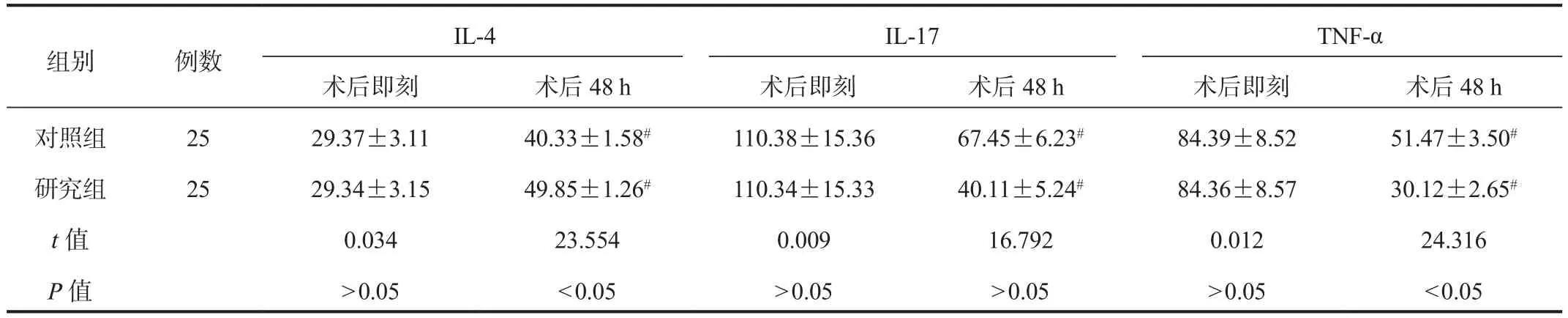
表3 两组患者炎症因子指标比较(±s, pg/mL)
注:与术后即刻比,#P < 0.05。IL-4:白介素-4;IL-17:白介素-17;TNF-α:肿瘤坏死因子-α。
组别 例数IL-4 IL-17 TNF-α术后即刻 术后48 h 术后即刻 术后48 h 术后即刻 术后48 h对照组 25 29.37±3.11 40.33±1.58# 110.38±15.36 67.45±6.23# 84.39±8.52 51.47±3.50#研究组 25 29.34±3.15 49.85±1.26# 110.34±15.33 40.11±5.24# 84.36±8.57 30.12±2.65#t值 0.034 23.554 0.009 16.792 0.012 24.316 P值 > 0.05 < 0.05 > 0.05 > 0.05 > 0.05 < 0.05
3 讨论
腰椎间盘突出症主要是由损伤、腰椎间盘退行性变等所致,好发于中老年人群,在临床上表现为腰背痛、坐骨神经痛等症状,多与腰椎管狭窄合并出现,给患者的日常生活带来不良影响。患者发生合并症后,其治疗难度大,风险较高,因此选择合适的手术方法对于保障患者生命安全具有重大的临床意义。传统全椎板切除术是治疗腰椎间盘突出症合并腰椎椎管狭窄症的常规术式,能够清除病变组织,降低椎管内压,改善患者的预后,但是给患者造成的伤害较大,且手术操作比较复杂,手术耗时长,影响患者的术后恢复。
近年来,随着微创技术的发展与完善,UBE已逐渐被用于腰椎间盘突出症和腰椎椎管狭窄症的治疗中,对患者的预后起着重要的作用。田大胜等[8]研究表明,UBE可以提高腰椎间盘突出合并腰椎管狭窄症患者的临床疗效,改善患者的腰椎功能,减少患者的腰痛、下肢痛的疼痛程度,减少患者不良反应的发生。本次研究中,术后3个月研究组患者ODI、VAS评分均较对照组下降,但研究组患者JOA评分较对照组升高;研究组患者的手术时间、住院时间均较对照组缩短,且术中出血量较对照组降低,提示UBE可以缩短腰椎间盘突出合并腰椎管狭窄症患者的手术和住院时间,减少患者术中出血量,改善患者的腰椎功能,降低患者的疼痛程度。
研究证实,血清炎性因子在腰椎间盘退变的发生发展中具有至关重要的作用,TNF-α可以促使患者机体内血管内皮生长因子、神经营养因子、神经生长因子及脑源性神经营养因子的表达,促进椎间盘血管的生成及神经支配,诱导炎症反应,促使病情加重;IL-17为促炎因子,其水平升高,提示患者炎症反应加重,患者病情进展;IL-4为抗炎因子,其水平降低,提示患者炎症反应加重,患者病情进展[9]。UBE可以通过摘除腰椎间盘突出合并腰椎管狭窄症患者病变的腰间盘突出组织,切除患者狭窄区域组织,降低患者体内的炎性因子水平,减轻患者机体内的炎症反应。本次研究中,术后48 h研究组患者血清IL-17、TNF-α低于对照组,但研究组患者的血清IL-4水平高于对照组,提示UBE可以降低腰椎间盘突出合并腰椎管狭窄症患者体内的炎性因子水平,减轻炎症反应。
综上,UBE可以缩短腰椎间盘突出合并腰椎管狭窄症患者的手术时间和住院时间,减少患者术中出血量,改善患者的腰椎功能,降低患者的疼痛程度,减轻患者的炎症反应,值得临床应用和推广。

