牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗免疫持续期研究
郝雪斌 牛秀岭 张海成 邵小秦 张春霞 王英/金宇保灵生物药品有限公司 010100
弓艳春/内蒙古自治区动物卫生监督所 010051
BVD 和IBR 均为OIE 法定报告的动物疫病,在我国分别为三类和二类动物疫病,严重威胁养牛业的安全。该病的根治方法是阳性牛检出与捕杀,而预防的主要措施是接种疫苗。国外已有大量BVD 和IBR 的商品化单苗或联苗,但国内由于起步较晚,对该两种疾病未引起足够重视,中国兽医药品监察所与金宇保灵生物药品有限公司联合研制的牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗实现了两种病同时预防接种技术,解决目前国内无疫苗的现实难题。针对目前BVD 和IBR 较为严重的流行形势,采用流行优势毒株制备安全高效的灭活疫苗应为防控这两种疾病的首选。对其免疫效果进行评价,从而确定免疫评价方法,指导疫苗使用。
1 材料与方法
1.1 试验材料
1.1.1 疫苗牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗(BVDV/NMG 株+IBRV/LY 株)3 批(批号:S19001、S19002、S19003)。由金宇保灵生物药品有限公司提供。
1.1.2 试验动物2~6月龄健康易感牛(BVDV 血清中和抗体效价不高于1∶2 或ELISA 抗体阴性、IBRV 血清中和抗体效价不高于1∶2 或ELISA 抗体阴性、BVDV 抗原阴性、IBRV 抗原阴性)100 头,购于锡林郭勒盟正蓝旗和包头市达茂旗。
1.1.3 检测试剂盒、试剂BVDV 间接免疫荧光试剂盒购至中国兽医药品监察所。
BVDV PCR 引物由北京六合华大基因科技股份有限公司合成,预期扩增片段大小为288bp。
1.1.4 细胞中和试验用细胞和抗原MDBK 传代细胞,由金宇保灵生物药品有限公司提供。
BVDV 中和试验用病毒,为NMG 株:病毒含量为107.5TCID50/ml。由金宇保灵生物药品有限公司提供。
IBRV 中和试验用病毒,为LY 株中和毒:病毒含量为108.0TCID50/mL。由金宇保灵生物药品有限公司提供。
1.1.5 试验器材96 孔细胞培养板、移液器及配套尖头、二氧化碳培养箱、1.5~2mL 离心管及架子、倒置显微镜、生物安全柜,旋涡混合器、德国BiometraPCR 扩增仪、Tanon-1600 凝胶成像系统、DYY-6C 电泳仪等均由金宇保灵生物药品有限公司检测中心提供。
1.2 方法
1.2.1 免疫每批试验疫苗免疫30 头2~6 月龄健康易感牛(BVDV 血清中和抗体效价不高于1 ∶2 或ELISA 抗体阴性、IBRV 血清中和抗体效价不高于1 ∶2 或ELISA 抗体阴性、BVDV 抗原阴性、IBRV 抗原阴性),每头牛颈部肌肉注射2mL 疫苗。3 批疫苗共免疫90 头牛,并同条件饲养阴性对照试验牛10 头。初免后21d,以相同免疫剂量和免疫途径进行二免。
1.2.2 采血及抗体检测各批次免疫牛分别在一免14 日、21 日和二免后14 日、21 日、60 日、90 日、120 日、150 日、180 日分别采血分离血清检测中和抗体。
1.2.3 BVDV、IBRV 血清中和抗体测定
(1)材料待检血清、标准阳性对照血清、标准阴性对照血清、病毒液、含2%新生牛血清的DMEM 细胞维持液、胰酶-EDTA 消化液、96 孔细胞培养板、移液器及配套尖头、二氧化碳培养箱、1.5~2mL 离心管及架子、倒置显微镜、生物安全柜,旋涡混合器等。
(2)操作程序
1)血清灭活用前将待检血清、阳性对照血清和阴性对照血清经56℃热灭活30min。
2)血清稀释用含2%新生牛血清的DMEM 培养基对灭活后的待检样品在96 孔细胞培养版中进行2 倍系列稀释,每份血清加4 孔,每孔50μL。标准阴、阳性对照血清根据实际效价进行适当稀释(一般作1 ∶2 稀释)。
3)中和用病毒稀释用含2%新生牛血清的DMEM 培养基将中和用病毒稀释到200TCID50/0.1mL。
4)中和向每份血清样品的每个稀释度中加入50μL 中和病毒工作液,振摇混匀后,置37℃中和1h,期间振摇2~3 次。
5)加细胞悬液将生长成良好单层的MDBK 细胞用胰酶-EDTA 消化液消化分散后,用生长液配制成含20 万/mL 的细胞悬液同步加到血清-病毒中和孔中,每孔100μL。加样完成后做好标记,然后置37℃、5%CO2培养箱中继续培养2~3日。
6)试验需做下列对照:
阳性血清对照:2 倍稀释血清50μL +中和病毒工作液50μL +细胞悬液100μL。
阴性血清对照:2 倍稀释血清5L0μL+中和病毒工作液50μL +细胞悬液100μL。
正常细胞对照:细胞悬液100μL+维持液100μL。
血清毒性对照:2 倍稀释血清50μL+维持液50μLl +细胞悬液100μL。
中和病毒对照:中和病毒工作液50μL+稀释液50μL +细胞悬液100μL。
7)结果判定
每天用倒置显微镜观察细胞孔是否出现CPE,统计待检血清病变孔数,按Reed-Muench 法计算血清中和抗体效价。试验成立条件为:中和病毒对照、阴性血清对照应出现CPE,血清毒性对照应无血清毒性,阳性血清对照和正常细胞对照应不出现CPE。
2 结果
2.1 免疫后牛不同时间BVDV 中和抗体滴度测定结果由表1、2 和图1 可知,3 批疫苗二免后21日BVDV 和IBRV 抗体滴度达到最高峰并维持至90 日,比二免后其他时间段抗体滴度高,二免后180 日(6 个月)时BVDV 中和抗体滴度大于1:128在50%以上,显示二联灭活疫苗BVD 部分免疫原性良好。
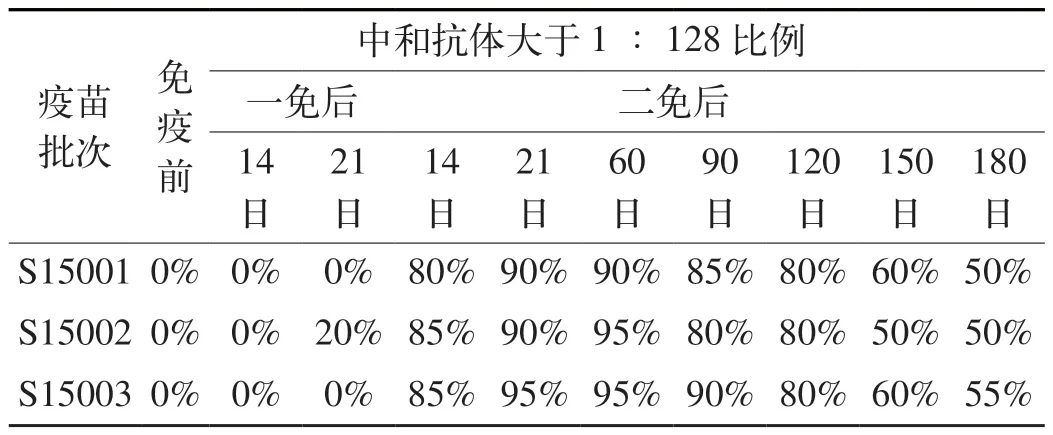
表1 二免后牛不同时间BVDV 中和抗体滴度大于1 ∶128 比例
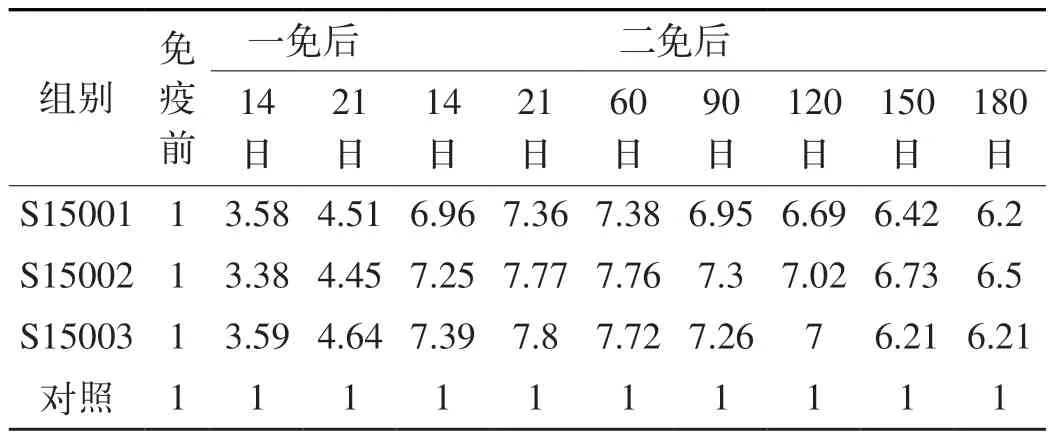
表2 二免后牛不同时间BVDV 中和抗体效价平均值(log2)
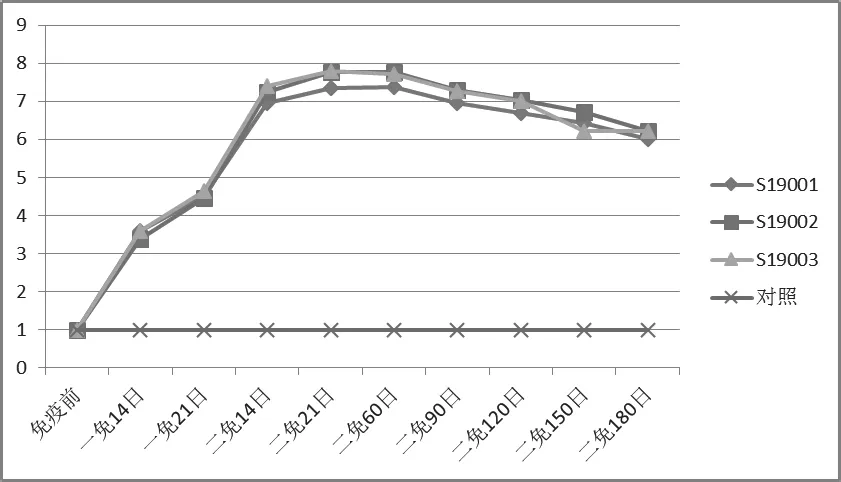
图1 二免后牛不同时间BVDV 中和抗体效价消长规律
2.2 免疫后牛不同时间IBRV 中和抗体滴度测定结果由表3、4 和图2 可知,3 批疫苗二免后21 日IBRV 抗体滴度达到最高峰并维持至90 日,比二免后其他时间段抗体滴度高,二免后180 日(6 个月)时IBRV 抗体中和抗体滴度大于1:64在55%以上,也显示二联灭活疫苗IBR 免疫原性良好。
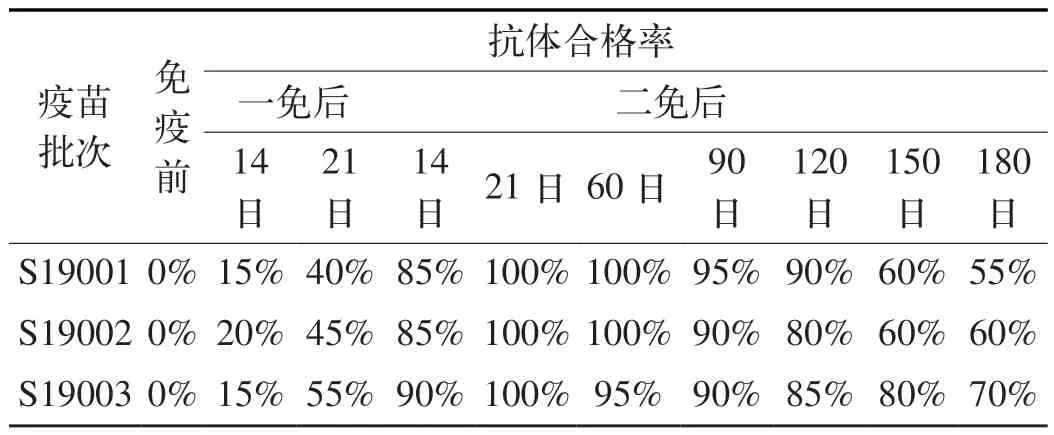
表3 二免后不同时间IBRV 中和抗体滴度大于1 ∶64 比例
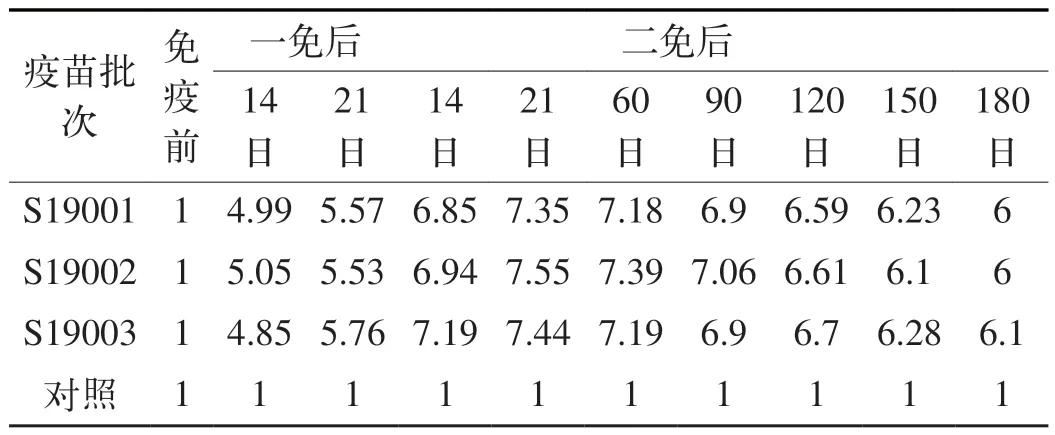
表4 二免后牛不同时间IBRV 中和抗体效价平均值(log2)
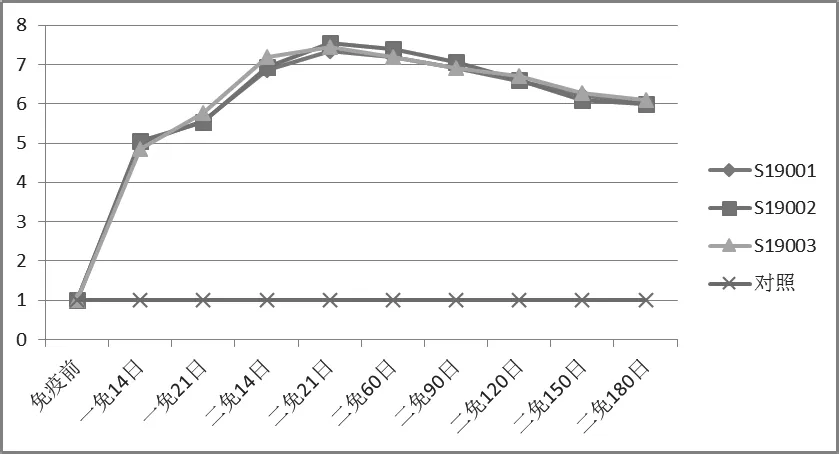
图2 二免后牛不同时间IBRV 中和抗体效价消长规律
3 讨论
试验牛在免疫以后未出现精神食欲异常和其他不良反应,说明疫苗使用安全,也反映出疫苗制备工艺中抗原纯化彻底和热源物质控制严格。
通过牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗免疫后不同时间BVD 和IBR 中和抗体检测表明,BVD 和IBR中和抗体在一免后14 日和21 日均不能达到较高的中和抗体滴度,只有进行二免才可以达到较高中和抗体滴度。从中和抗体达到高峰的时间分析,BVD 和IBR 两种抗原在牛体免疫应答并未互相拮抗,均在二免后21 日出现中和抗体高峰,与赵月兰等2009 年制备牛病毒性腹泻油乳剂灭活苗免疫效果评价和冷雪等2010 年评价牛传染性鼻气管炎灭活疫苗效力时抗体达到高滴度时间是一致的。并且高抗体滴度持续6月以上,此结论与1982 年Joseph R.Kolar 等完成的实验结论也是一致的。表明该二联灭活苗二免后维持6 月以上的高中和抗体水平是有保障的。
通过牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗免疫后不同时间BVD 和IBR 中和抗体滴度消长分析,从一次免疫后14 日中和抗体检测表明IBR 产生中和抗体比BVD产生中和抗体要高,且中和抗体滴度IBR 比BVD 高一个滴度。二次免疫后21 日检测表明BVD 和IBR 中和抗体滴度均达到1:128 以上,并维持90d 左右逐渐下降,值得注意的是在中和抗体滴度下降过程中发现IBR 中和抗体下降速度快于BVD 中和抗体下降速度。说明免疫牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗后产生抵御IBR 感染的中和抗体比抵御BVD 感染的中和的抗体产生更快,但BVD 中和抗体高滴度持续时间比IBR 长。
4 结论
牛病毒性腹泻、牛传染性鼻气管炎二联灭活疫苗(BVDV/NMG 株+IBRV/LY 株)免疫牛后,一免后14 日产生抗体,二免后21 日平均抗体滴度达到最高值并维持至少90 日,随时间延续抗体滴度逐步下降,到120 日时BVDV 中和抗体不低于1 ∶128 和IBRV 中和抗体不低于1 ∶64 在80%以上,180 日时BVDV 中和抗体不低于1 ∶128 在50%以上,IBRV 中和抗体不低于1 ∶64 在55%以上。说明该疫苗两次免疫后牛维持较高BVDV 和IBRV 中和抗体至少6 个月,可以指导牛场免疫程序的制定,保护牛免受BVDV 和IBRV感染,提高牛场经营效益。

